文档内容
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
2023—2024 学年度第二学期第五次测试
九年级化学
1.本试卷共9页,共两部分,共39题,满分70分。考试时间70分
钟。
注
2.在试卷和答题卡上准确填写学校、班级、姓名和学号。
意
事
3.试题答案一律填涂或书写在答题卡上,在试卷上作答无效。
项
4.在答题卡上,选择题用2B铅笔作答,其他试题用黑色字迹签字笔
作答。
能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32
第一部分
本部分共25题,每题1分。在每题列出的四个选项中,只有1个选项符合题意。
1. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气体
2. 下列氧气的性质中,属于化学性质的是
A. 无色无味 B. 密度大于空气 C. 能支持燃烧 D. 沸点低
3. 化肥对提高农作物的产量具有重要作用。下列物质能用作钾肥的是
A. KSO B. CO(NH) C. NH Cl D. Ca(HPO )
2 4 2 2 4 2 4 2
4. 下列物质的俗称与化学式对应正确的是
A. 火碱——NaHCO B. 石灰石——Ca(OH)
3 2
C. 纯碱——NaCO D. 消石灰——CaO
2 3
5. 碳元素与氧元素的本质区别是
A. 质子数不同 B. 电子数不同
C. 中子数不同 D. 最外层电子数不同
6. 下图所示的图标表示
A. 禁止烟火 B. 禁止燃放鞭炮 C. 禁止吸烟 D. 禁止堆放易燃物
的
7. 下列化学用语 含义正确的是
A. H — 1个氢元素 B. H — 1个氢分子
2
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
.
C H+ — 1个氢原子 D. — 1个氢离子
8. 浓硫酸暴露在空气中,质量会增加,是因为浓硫酸具有
A. 酸性 B. 碱性 C. 吸水性 D. 腐蚀性
9. 下列物质的化学式中,书写正确的是
A. 氯化铁FeCl B. 碳酸钾KCO
3 3
C. 氧化镁MgO D. 氯化锌ZnCl
2
10. 下列物质的用途主要利用其化学性质的是
A. 干冰用于人工降雨 B. 氢氧化钠用作实验室干燥剂
C. 熟石灰用于改良酸性土壤 D. 稀有气体用作电光源
11. 人体内一些液体的正常pH范围如下,其中酸性最强的是
A. 胰液 7.5~8.0 B. 胆汁 7.1~7.3 C. 血浆 7.35~7.45 D. 胃液 0.9~1.5
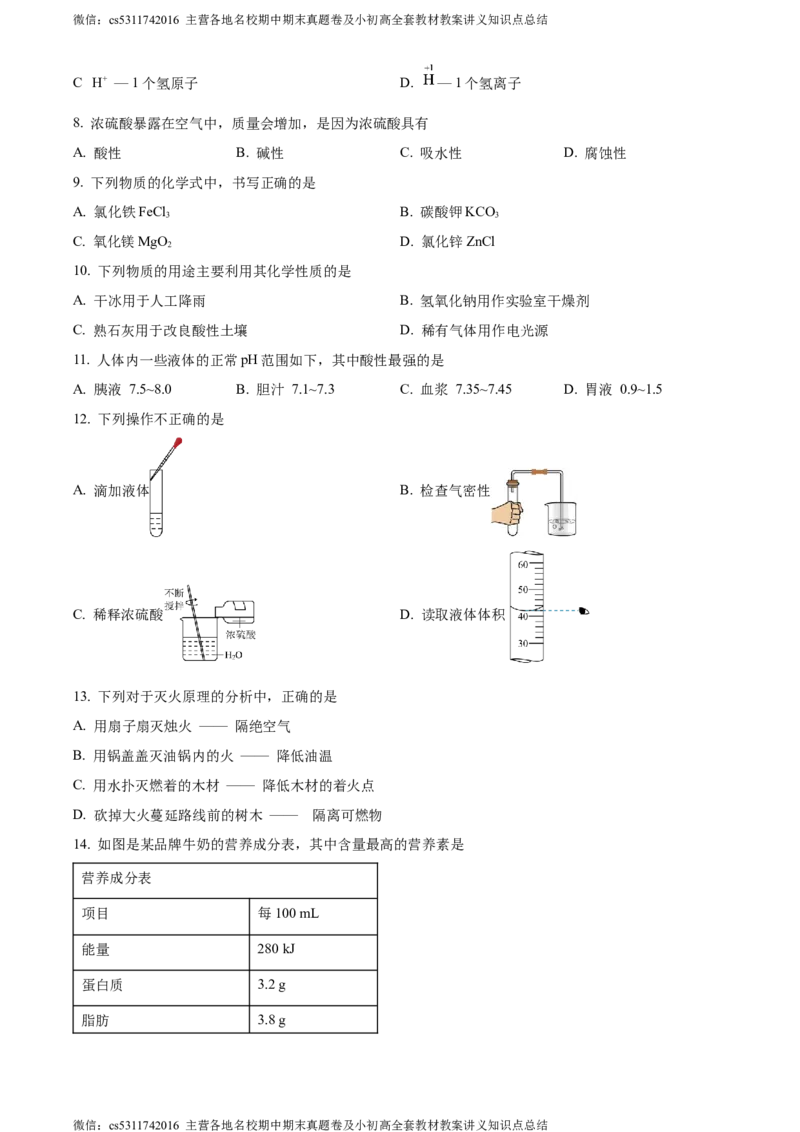
12. 下列操作不正确的是
A. 滴加液体 B. 检查气密性
C. 稀释浓硫酸 D. 读取液体体积
13. 下列对于灭火原理的分析中,正确的是
A. 用扇子扇灭烛火 —— 隔绝空气
B. 用锅盖盖灭油锅内的火 —— 降低油温
C. 用水扑灭燃着的木材 —— 降低木材的着火点
D. 砍掉大火蔓延路线前的树木 —— 隔离可燃物
14. 如图是某品牌牛奶的营养成分表,其中含量最高的营养素是
营养成分表
项目 每100 mL
能量 280 kJ
蛋白质 3.2 g
脂肪 3.8 g
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
碳水化合物 5.0 g
钠 53 mg
钙 100 mg
A. 蛋白质 B. 油脂 C. 糖类 D. 无机盐
“点击化学”和“生物正交化学”是2022年诺贝尔化学奖的成果。北京大学课题组开发的铜基催化生物
正交断键反应在医药研究中发挥着重要作用。回答下列小题。
15. 铜元素在元素周期表中的信息如图。下列有关铜元素的说法不正确的是
A. 元素符号是Cu B. 质子数是29
C. 相对原子质量63.55 g D. 属于金属元素
16. 白癜风患者在治疗过程中需要补铜,这里的“铜”指的是
A. 单质 B. 元素 C. 分子 D. 原子
17. 几种矿石的主要成分如下,可用于冶炼铜的矿石是
A. 菱铁矿(FeCO) B. 软锰矿(MnO )
3 2
C. 方铅矿(PbS) D. 孔雀石[Cu (OH) CO]
2 2 3
18. BTTAA(C H N O)是铜基催化剂的重要组成物质,下列关于BTTAA说法不正确的是
19 30 10 2
A. 由4种元素组成
B. 由61个原子构成
C. 氢、氧元素质量比为15:16
D. 氮元素的质量分数计算式为
19. 依据下列20℃时的实验,回答下列小题。
已知:20℃和40℃时NH Cl固体的溶解度分别为37.2g和45.8g。
4
序号 ① ② ③
加入NH Cl的质量/g 20 35 40
4
水的质量/g 100 100 100
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
1. ①~③所得溶液属于饱和溶液的是________
A ① B ② C ③ D ②③
2. 下列关于①~③所得溶液说法不正确的是________
A 溶液质量:①<②
B ①中溶质与溶剂的质量比为1:5
C ②中溶质的质量分数为35%
D 将③升温到40℃,溶质的质量分数增大
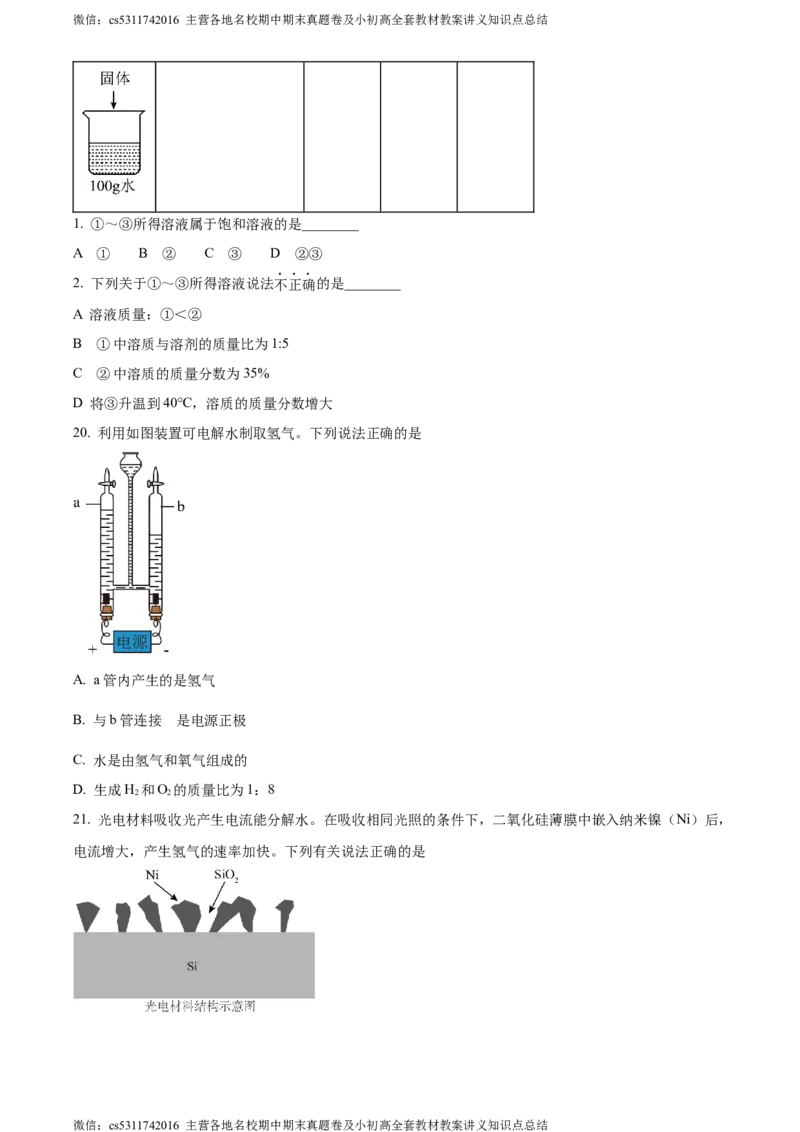
20. 利用如图装置可电解水制取氢气。下列说法正确的是
A. a管内产生的是氢气
的
B. 与b管连接 是电源正极
C. 水是由氢气和氧气组成的
D. 生成H 和O 的质量比为1:8
2 2
21. 光电材料吸收光产生电流能分解水。在吸收相同光照的条件下,二氧化硅薄膜中嵌入纳米镍(Ni)后,
电流增大,产生氢气的速率加快。下列有关说法正确的是
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
A. 二氧化硅属于混合物
B. 该材料可将电能转化为光能
C. 纳米镍可提高二氧化硅薄膜的电阻
D. 硅元素在地壳中的含量优势是其能用于光电材料的原因之一
22. 氨催化氧化是制硝酸的主要反应之一。该反应前后分子种类变化的微观示意图如下。下列说法正确的
是
A. 属于氧化物的物质有一种 B. 丁由三种原子构成
C. 生成的丙与丁的质量比为10:9 D. 该反应前后分子和原子的数目均改变
23. 氢氧化钴[CO (OH) ]受热易分解,能与酸性溶液反应, 可作涂料和清漆的干燥剂, 制备方法为:①
2
Co+2HCl=COCl +H ↑②COCl +2NaOH=Co(OH) ↓+2NaCl下列判断正确的是
2 2 2 2
A. 钴的金属活动性比铜的弱 B. 可以利用氢氧化钴干燥氯化氢气体
C. 氢氧化钴的化学性质稳定 D. ①为置换反应,②为复分解反应
24. 下列实验方法不能达到实验目的的是
选项 实验目的 操作
A 鉴别稀盐酸和NaCl溶液 滴加紫色石蕊溶液
B 检验某固体中是否含有碳酸盐 加入足量稀盐酸
C 鉴别CO和CO 将气体通入澄清石灰水
2
D 除去Cu(NO ) 溶液中少量AgNO 加入过量铜粉,一段时间后过滤
3 2 3
A. A B. B C. C D. D
第二部分 非选择题(共45分)
〖生活现象解释〗
25. 共享单车以绿色、节能、便捷等优势受到大家的青睐。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
(1)图中所示自行车部件中,属于金属材料的是 (填字母序号)。
A. 钢铁骨架 B. 塑料外壳 C. 合成橡胶轮胎
(2)制造车体需要大量的钢铁,写出用CO和Fe O 反应炼铁的化学方程式________。
2 3
(3)大力发展共享单车、提倡绿色出行,可以减少温室气体________的排放。
的
26. 人类 生产生活离不开能源。
的
(1)目前使用 燃料大多来自化石燃料,包括______、石油和天然气。
(2)天然气完全燃烧的化学方程式为______。
27. 氢气是理想的清洁能源,中国科学家研究出镁基固态储氢技术。
(1)金属镁和氢气在300°C和高压条件下发生化合反应,生成氢化镁(MgH ),实现了固态储氢。该反应
2
的化学方程式为_________。
(2)为调控该材料释放氢气的性能,加入钛作催化剂。对钛的作用认识正确的是_______(填序号)。
A. 可改变释放氢气的反应速率
B. 可增加释放出的氢气的总质量
C. 钛的化学性质在反应前后不发生改变
〖科普阅读理解〗
28. 阅读下面科普短文。
酱油是我国传统调味品之一,是以大豆、小麦等原料,经过原料预处理、制曲、发酵、浸出淋油及加热配
制等工艺生产出来的调味品,营养极其丰富,主要营养成份包括氨基酸、可溶性蛋白质、糖类、酸类等。
制曲是酱油酿造的重要工序,制曲工艺的主要流程为:主辅料→混合→润水→蒸煮→冷却→接种→通风培
养→成曲。成曲的蛋白酶活力值越高,成曲质量越好。
选择适合的菌种,温度控制在米曲霉最适合生长的32~33℃。主料大豆为蛋白质源,辅料米糠为淀粉源。
选取不同的主辅料配比,在润水量120%,蒸料时间30min,制曲时间36h的条件下制曲,所得蛋白酶活力
值如下表。
表 主辅料配比与蛋白酶活力值
实验序 主辅料 配比 蛋白酶活力值(单位
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
号 U/g)
大豆,米 1:
1-1 743.66
糠 1.2
大豆,米
1-2 1:1 957.28
糠
大豆,米 1:
1-3 1003.53
糠 0.8
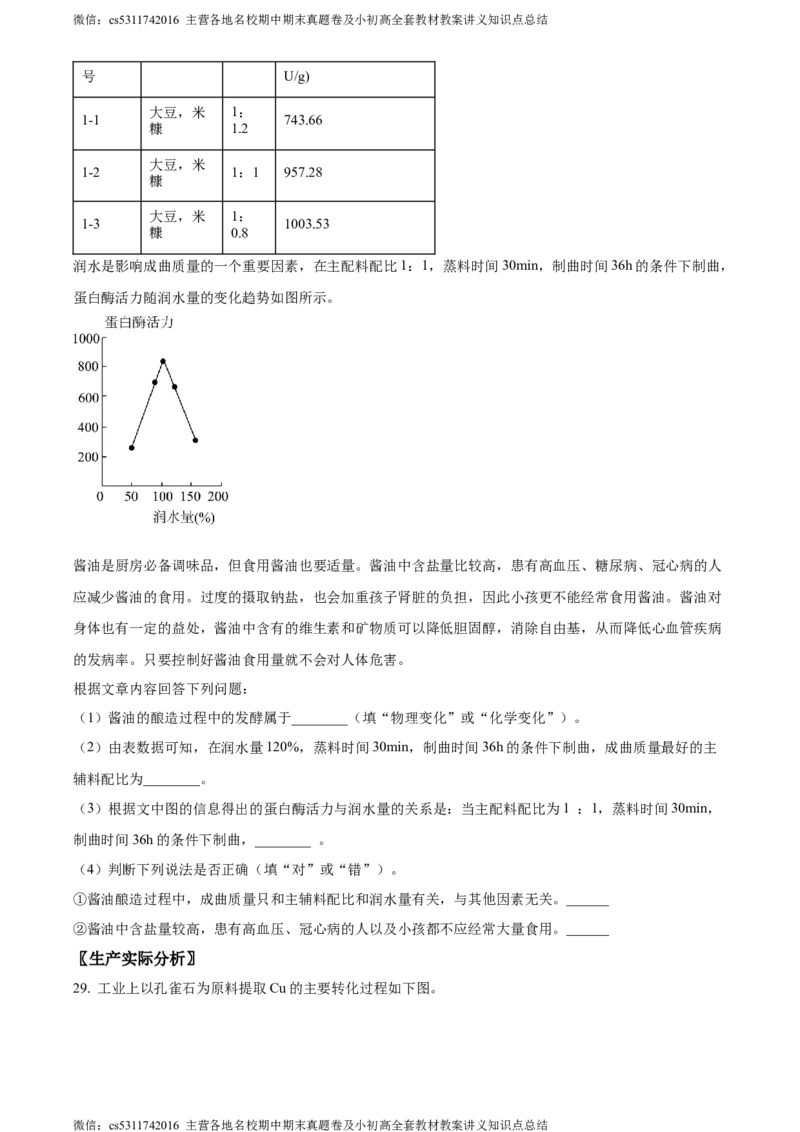
润水是影响成曲质量的一个重要因素,在主配料配比1:1,蒸料时间30min,制曲时间36h的条件下制曲,
蛋白酶活力随润水量的变化趋势如图所示。
酱油是厨房必备调味品,但食用酱油也要适量。酱油中含盐量比较高,患有高血压、糖尿病、冠心病的人
应减少酱油的食用。过度的摄取钠盐,也会加重孩子肾脏的负担,因此小孩更不能经常食用酱油。酱油对
身体也有一定的益处,酱油中含有的维生素和矿物质可以降低胆固醇,消除自由基,从而降低心血管疾病
的发病率。只要控制好酱油食用量就不会对人体危害。
根据文章内容回答下列问题:
(1)酱油的酿造过程中的发酵属于________(填“物理变化”或“化学变化”)。
(2)由表数据可知,在润水量120%,蒸料时间30min,制曲时间36h的条件下制曲,成曲质量最好的主
辅料配比为________。
(3)根据文中图的信息得出的蛋白酶活力与润水量的关系是:当主配料配比为1 :1,蒸料时间30min,
制曲时间36h的条件下制曲,________ 。
(4)判断下列说法是否正确(填“对”或“错”)。
①酱油酿造过程中,成曲质量只和主辅料配比和润水量有关,与其他因素无关。______
②酱油中含盐量较高,患有高血压、冠心病的人以及小孩都不应经常大量食用。______
〖生产实际分析〗
29. 工业上以孔雀石为原料提取Cu的主要转化过程如下图。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
(1)可将Cu (OH) CO 固体从碱浸液中分离出来的操作Ⅰ为___________。
2 2 3
(2)酸浸步骤中使用的是___________(填“稀盐酸”或“稀硫酸”)。
(3)电解CuSO 溶液可制得Cu。补全该反应的化学方程式:2CuSO +2H O
4 4 2
2HSO +2Cu+___________↑。
2 4
30. 烟气脱硫是煤炭清洁利用的关键一环,钠—钙双碱烟气脱硫工艺流程如下图。
试剂 Ca(OH) NaOH
2
价格(元/
0.36 2.90
kg)
资料:①部分原料的价格如表;
②CaSO 可用于造纸和制糖等;
3
③石灰浆的主要成分是Ca(OH) 。
2
(1)吸收塔中,“喷淋和使用小球”的目的是________。
(2)再生池中,发生的复分解反应的化学方程式为________。
(3)清液池中,试剂X可除去Ca(OH) ,防止其混入吸收塔。试剂X是________。
2
(4)下列关于钠—钙双碱脱硫工艺的说法正确的是 (填序号)。
A. 污染物SO 最终转化为CaSO,可实现“变废为宝”
2 3
B. 利用石灰浆使NaOH再生,可降低生产成本
〖基本实验及其原理分析〗
31. 从A或B两题中任选一个作答(图中夹持仪器略去),若两题均作答,按A计分。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
A、用甲装置进行实验 B、用乙装置制取CO
2
(1)加热KMnO 制取氧气的化学方程式为______ (1)反应的化学方程式为______。
4
(2)木炭遇O 燃烧时,现象为______。 (2)用向上排空气法收集CO 的原因是______
2 2
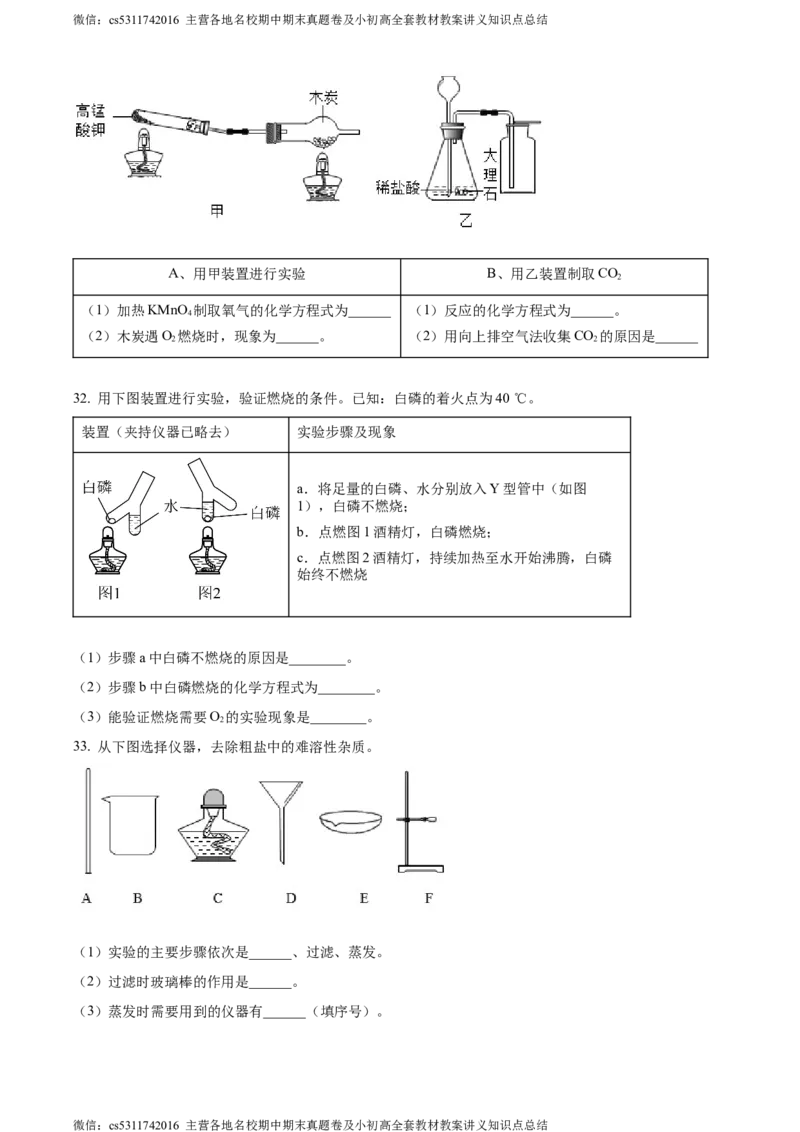
32. 用下图装置进行实验,验证燃烧的条件。已知:白磷的着火点为40℃。
装置(夹持仪器已略去) 实验步骤及现象
a.将足量的白磷、水分别放入Y型管中(如图
1),白磷不燃烧;
b.点燃图1酒精灯,白磷燃烧;
c.点燃图2酒精灯,持续加热至水开始沸腾,白磷
始终不燃烧
(1)步骤a中白磷不燃烧的原因是________。
(2)步骤b中白磷燃烧的化学方程式为________。
(3)能验证燃烧需要O 的实验现象是________。
2
33. 从下图选择仪器,去除粗盐中的难溶性杂质。
(1)实验的主要步骤依次是______、过滤、蒸发。
(2)过滤时玻璃棒的作用是______。
(3)蒸发时需要用到的仪器有______(填序号)。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
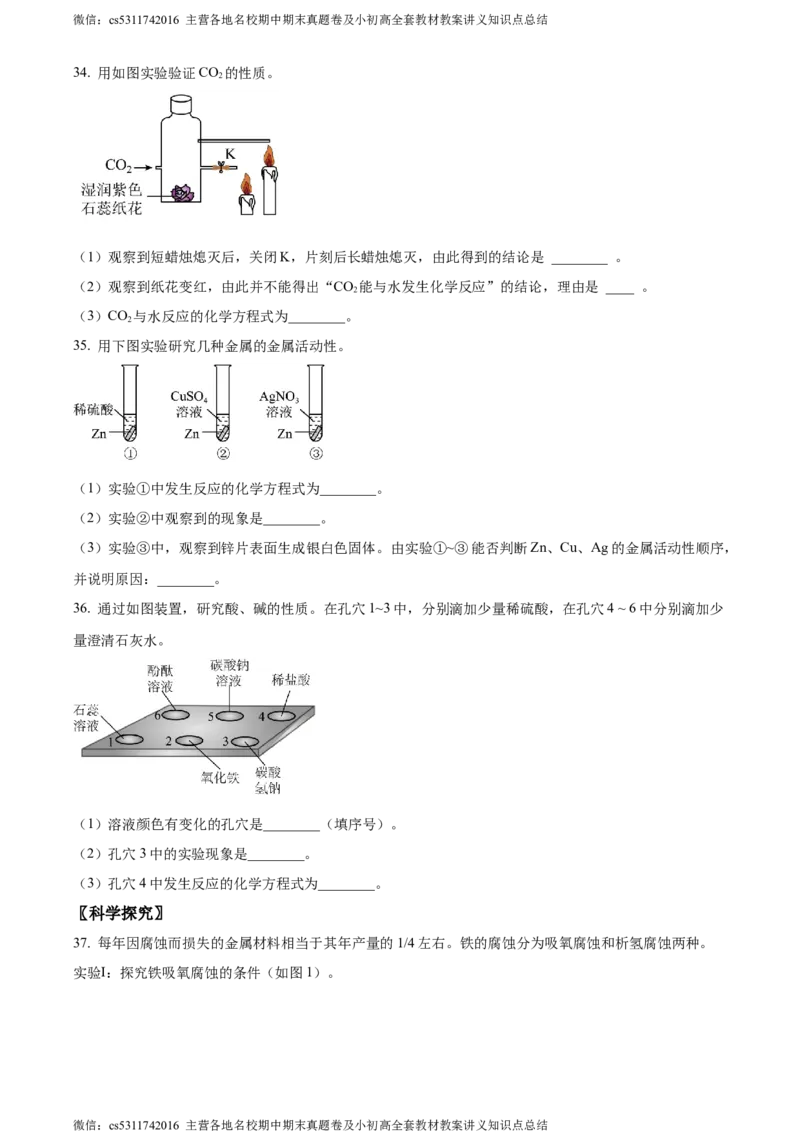
34. 用如图实验验证CO 的性质。
2
(1)观察到短蜡烛熄灭后,关闭K,片刻后长蜡烛熄灭,由此得到的结论是 ________ 。
(2)观察到纸花变红,由此并不能得出“CO 能与水发生化学反应”的结论,理由是 ____ 。
2
(3)CO 与水反应的化学方程式为________。
2
35. 用下图实验研究几种金属的金属活动性。
(1)实验①中发生反应的化学方程式为________。
(2)实验②中观察到的现象是________。
(3)实验③中,观察到锌片表面生成银白色固体。由实验①~③能否判断Zn、Cu、Ag的金属活动性顺序,
并说明原因:________。
36. 通过如图装置,研究酸、碱的性质。在孔穴1~3中,分别滴加少量稀硫酸,在孔穴4 ~ 6中分别滴加少
量澄清石灰水。
(1)溶液颜色有变化的孔穴是________(填序号)。
(2)孔穴3中的实验现象是________。
(3)孔穴4中发生反应的化学方程式为________。
〖科学探究〗
37. 每年因腐蚀而损失的金属材料相当于其年产量的1/4左右。铁的腐蚀分为吸氧腐蚀和析氢腐蚀两种。
实验Ⅰ:探究铁吸氧腐蚀的条件(如图1)。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
实验Ⅱ:探究影响析氢腐蚀速率的因素。
【查阅资料】铁在强酸性条件下发生析氢腐蚀。
【设计实验】小组同学用图2所示装置进行实验。
【实验记录】20℃时,每组实验加入铁炭总质量为36g,酸的体积为10mL,30秒后读出U形管右液柱上
升的高度值。(温馨提示:mol/L是一种浓度单位)。
酸的浓度
铁碳质量比 酸的种类 反应时间/s 高度值/cm
(mol/L)
① 6:1 稀盐酸 2.0 30 8.5
② 8:1 稀盐酸 2.0 30 13.0
③ 10:1 稀盐酸 2.0 <30 14.0
④ 8:1 稀醋酸 2.0 30 3.0
⑤ 8:1 稀硫酸 2.0 <30 14.5
⑥ 8:1 稀盐酸 1.0 30 6.5
⑦ 8:1 稀盐酸 4.0 <30 15.5
【解释与结论】
(1)探究铁吸氧腐蚀的条件(如图1)实验中,证明铁生锈与氧气有关的实验现象为___。
(2)铁与盐酸反应的化学方程式为________。
(3)本实验探究了________种可能影响反应速率的因素。
(4)对比实验①②③,得出的结论是________。
(5)分析酸的浓度对铁析氢腐蚀速率的影响应对比实验______(填序号)。
【反思与评价】
(6)在实验Ⅱ的基础上继续研究,设计实验,证明当其他条件相同时,温度对铁的析氢腐蚀速率有影响,
实验方案为 :铁碳总质量36g,质量比8:1,使用2.0 mol/L稀盐酸10 mL,________。
〖实际应用定量分析〗
38. 工业生产浓硫酸时会产生有毒的二氧化硫(SO )气体,用氢氧化钠溶液吸收二氧化硫防止空气污染,
2
化学方程式为SO + 2NaOH = Na SO + H O。现有40 kg氢氧化钠,配成溶液后,理论上可吸收二氧化硫
2 2 3 2
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
气体的质量是多少?
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结