文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题二 物质的性质与应用
金属与金属矿物
(试题分值:80分 测试时间:50分钟)
一、选择题(本题包括20小题,每小题2分,共40分.每小题只有一个正确答案)
1.【新情境】(2024·吉林长春·中考真题)2024年5月,武王墩墓出土了迄今为止东周时期最大的青铜
圆鼎。青铜是以铜和锡为主要成分的合金,青铜属于
A.非金属材料 B.金属材料 C.合成材料 D.复合材料
2.【新考向】(24-25九年级上·黑龙江哈尔滨·期中)第九届亚冬会将于2025年2月7日至2月14日在
哈尔滨举行,哈尔滨是历史文化名城、中国冰雪文化之都,有很多标志性建筑。下列说法错误的是
A.铁制围栏刷油漆主要 B.铝合金制成的外壳具有很好 C.钢筋属于金 D.教堂门窗用纯金
为了防锈 的抗腐蚀性 属材料 属制成
A.A B.B C.C D.D
3.【联系生活】——垃圾分类
(2023·甘肃金昌·中考真题)垃圾分类的意义在于提升资源的利用率。从垃圾分类角度,易拉罐属于
A.有害垃圾 B.可回收垃圾
C.其他垃圾 D.厨余垃圾
4.【传统文化】——文物“越王勾践剑”
(2024·山西晋城·三模)国家一级文物“越王勾践剑”被誉为“天下第一剑”,是青铜武器中的珍品,埋
藏在地下两千多年出土时依然光彩夺目,没有锈蚀。这体现出铸剑材料的最大优点是
A.颜色漂亮 B.熔点较高 C.硬度较大 D.抗腐蚀性好
5.【传统文化】——鎏金技术和铜镜
(23-24九年级下·湖北襄阳·自主招生)材料 1:鎏金技术,汉代以前人们就掌握,人们以7 比 1 的金
汞比例调成液态“金汞齐”,涂在器物表面,炭火烘烤,使其中汞成分挥发掉,金成分留在器物上,大约
重复涂烤三次即可。
材料2:铜镜是古代我国人民的伟大创造,清代科学家郑复光所撰《镜镜冷痴》载有“铜色本黄,杂锡则
青,青近白,故宜于镜”;《吕氏春秋》载有“金柔锡柔,合两柔则为刚”。下列相关叙述不正确的是
A.制作铜镜的材料为铜锡合金(青铜)
B.金柔锡柔,合两柔则为刚说明青铜硬度大于各成分金属
C.鎏金工艺过程中,使用了类似溶解、蒸发的操作
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D.铝露置在空气中很容易与氧气反应生成氧化铝。将铝溶于汞形成液态“铝汞齐”,其中的铝很难与氧
气反应
6.(2023·四川攀枝花·中考真题)根据铁锈蚀的条件判断,下列情况中,铁钉最容易生锈的是
A. B.
C. D.
7.【新情境】(24-25九年级上·黑龙江哈尔滨·阶段练习)2025年2月7日至2月14日亚洲冬季运动会
将在哈尔滨盛大举行,哈尔滨火车站是全国第二大欧式风格的火车站,是“尔滨”一张美丽的名片!下列
有关说法错误的是
A.铺设地面的大理石的主要成分是碳酸钙
B.火车站修建时使用到的金属材料均为纯铁
C.火车站内的钢轨采用的是硬度大、韧性好的锰钢
D.火车站室外铁围栏采用了在表面刷漆的方法来防锈
8.(2023·山东菏泽·中考真题)碲化镉薄膜电池是一种重要的太阳能电池,其材料之一镉(Cd)的制备是
在铜镉渣(主要含有Cd、Zn、Cu、Fe单质)中加入足量的稀硫酸充分反应,过滤出铜渣,然后对滤液进行
除铁净化,再加入锌粉置换出镉,下列金属的活动性顺序正确的是
A.Zn>Cu>Cd B.Zn>Cd>Cu C.Cu>Zn>Cd D.Cd>Zn>Cu
9.(2024·湖北襄阳·模拟预测)生产生活中所说的“五金”指的是金、银、铜、铁、锡五种金属,经人
工加工可以制成艺术品、金属器件和装饰品等。下列有关说法正确的是
A.上述“五金”都具有银白色金属光泽
B.上述“五金”分别投入稀盐酸中,其表面都会冒出气泡
C.将上述“五金”中的铁的位置移到最后,刚好符合金属活动性由弱到强的顺序
D.上述“五金”在自然界都主要以单质形式存在
10.(2024·西藏·中考真题)青藏高原有丰富的金属矿产资源。下列有关金属资源的利用和保护不正确的
是
A.将铁制品放在潮湿的空气里
B.在钢铁表面涂油、刷漆都能防止生锈
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C.废旧金属回收利用可以节约金属资源
D.有计划、合理地开采矿物是保护金属资源的有效途径
11.(2024·甘肃嘉峪关·模拟预测)下列化学方程式中,完全正确的是
A.2Fe + 6HCl = 2FCl + 3H ↑ B.Cu + H SO =CuSO + H ↑
e 3 2 2 4 4 2
C.Zn+CuSO =ZnSO +Cu D.H↑+ CuO =Cu + H O
4 4 2 2
12.(2024·山东临沂·二模)已知金属M、Fe和H活动性强弱关系为: ,下列说法中不正确
的是
A.金属M可以是Mg或Sn
B.将金属M放入稀硫酸中,会有气泡冒出
C.将金属M放入 溶液中,金属表面有红色固体析出
D.若金属铁(足量)放入 溶液中,溶液变为浅绿色
12.(2024·山东聊城·一模)为验证锌、锡、铜三种金属的活动性及它们和氢元素的位置关系,小丽设计
了如下实验:
下列组合中可以达到实验目的是
A.②③④ B.①②③ C.①②④ D.①③④
14.【传统文化】——古籍记载
(2024·重庆·二模)《清波杂志》卷十二有书:“信州铅山胆水自山下注,势若瀑布,用以浸铜,铸冶是
赖,虽干溢系夫旱涝,大抵盛于春夏,微于秋冬。古传人至水滨,遗匙钥,翌日得之,已成铜矣。”这里
的“胆水”指的是CuSO 溶液,下列说法不正确的是
4
A.上文描述的是CuSO 溶液与Fe的反应
4
B.“胆水”通常不用铁制容器盛装
C.Cu无法直接与稀硫酸反应制得CuSO
4
D.“胆水”中存在的微粒只有2种
15.(2024·辽宁丹东·模拟预测)向含有 、 的混合溶液中加入一定量锌粉,充分反应后
过滤,得到滤渣和滤液。关于滤渣和滤液的成分有如下描述:
①滤液中一定含有
②滤渣中一定含有Ag,可能含有Cu和Zn
③若滤液呈蓝色,则向滤渣中滴加稀盐酸无明显现象
④若向滤渣中滴加稀盐酸有气泡产生,则滤液中一定没有 和 ,
以上四种描述中正确的是
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.①②③ B.②③④ C.②④ D.①②③④
16.【结合生产】——废旧金属回收
(2024·山东青岛·一模)废旧手机中含有贵金属金(Au),图是回收Au的简略流程图,下列说法错误的
是
A.粉碎可以增大反应物的接触面积,加快反应速率
B.滤液a中的阳离子是Fe2+和Zn2+
C.在滤液b中加入过量的氢氧化钠溶液,会产生蓝色沉淀
D.由上述过程可知,Zn、Au、Cu三种金属的活动性顺序为Zn>Cu>Au
17.(2024·山东青岛·一模)某研究性学习小组用以下实验比较银、铜、锌的活动性顺序,实验结束后将
两试管剩余物倾倒至一个烧杯中,烧杯内溶液质量变化情况如图所示,下列说法不正确的是
A.通过该实验可以判断三种金属的活动性顺序为锌>铜>银
B.试管乙中反应后锌一定过量
C.a点处烧杯内只有一种固体
D.取b~c段溶液滴加稀盐酸无沉淀产生
18.(2024·广西南宁·模拟预测)将一定量的锌粉加入到硝酸铜、硝酸银的混合溶液中,溶液最终变为无
色,下列图像能表示对应变化关系的是
A.①③ B.②④ C.②⑤ D.①④
19.(2024·广西·中考真题)广西铝土矿资源丰富.铝土矿的主要成分是
A.二氧化硅 B.氧化铝 C.四氧化三铁 D.碳酸钙
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
20.(2024·山东滨州·中考真题)下列做法不能减缓或防止钢铁锈蚀的是
A.经常用食盐水清洗铁制品 B.保持铁制品表面清洁干燥
C.在铁制品表面涂油漆 D.在钢铁的表面镀一层不易锈蚀的金属
二、填空题(本题4小题,每空1分,共16分)
21.(4分)(2024·辽宁丹东·模拟预测)金属材料已得到越来越广泛的应用,请依据所学知识回答下列
问题, 钢铁是最常用的金属材料。
(1)钢属于 (填“纯净物”或“混合物”);
(2)将钢片和纯铁片相互刻画,纯铁片上留下划痕,说明 。
(3)向硝酸镁和硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,观察到滤液为无色,则该滤液中的
溶质一定有 ,滤渣中一定有 。
22.(8分)(2023·山东德州·中考真题)金属材料在生产、生活中有着广泛的用途,金属资源应得到有
效的利用和保护。
(1)利用金属矿产冶炼金属是获得金属材料的主要途径。工业上炼铁常用的原料有赤铁矿(主要成分为
Fe O)。焦炭(主要成分为碳)、石灰石和空气。其主要反应过程如下:
2 3
①上述流程中X的化学式是 。写出反应Ⅱ的化学方程式: 。
②反应Ⅲ为炼铁的主要反应,其反应的化学方程式为 。
(2)为了从某废旧电子产品中提炼贵重金属,并得到硫酸铜溶液。有如下流程:
①“步骤二”中能与稀硫酸反应的是粗铜中的 (填化学式,下同),“步骤三”是滤渣Ⅰ中的
与空气中的氧气发生反应。
②写出“步骤四”中发生反应的化学方程式: 。。
三、实验题
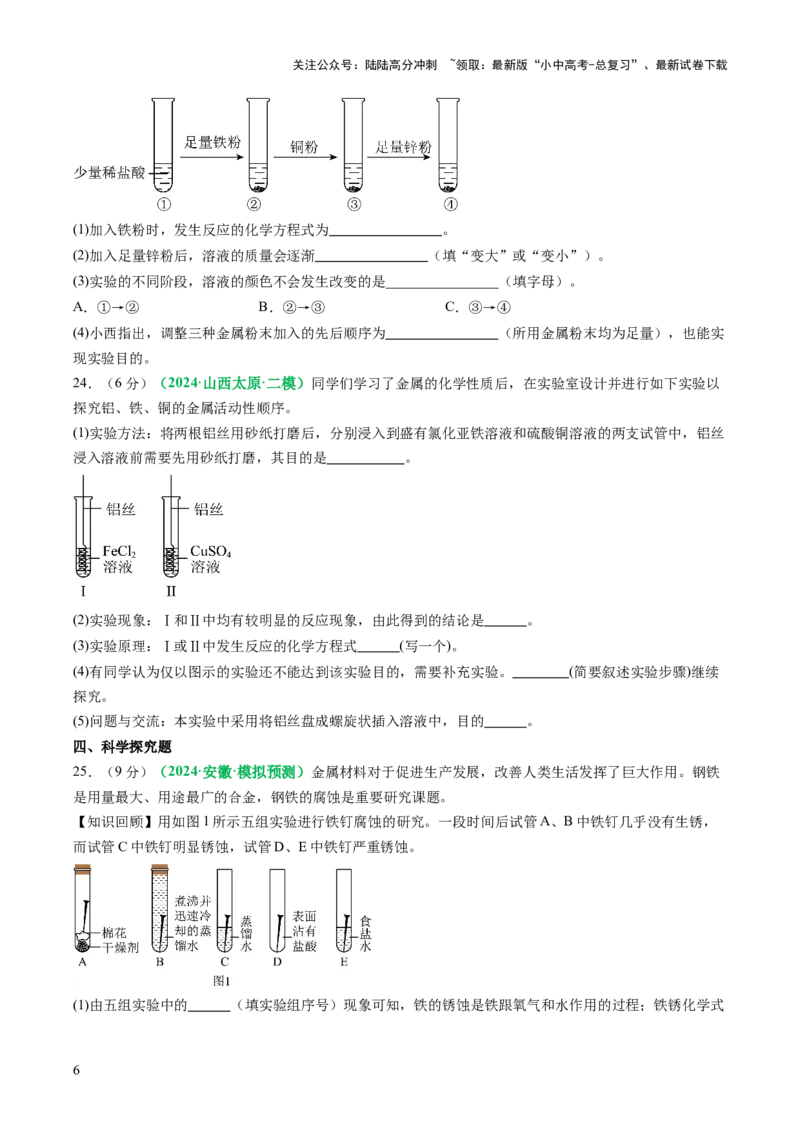
23.(4分)(2024·陕西咸阳·二模)为验证铁、锌、铜三种金属的活动性强弱,小安只用一支试管和少
量稀盐酸就达到了目的。实验流程如图所示:
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)加入铁粉时,发生反应的化学方程式为 。
(2)加入足量锌粉后,溶液的质量会逐渐 (填“变大”或“变小”)。
(3)实验的不同阶段,溶液的颜色不会发生改变的是________________(填字母)。
A.①→② B.②→③ C.③→④
(4)小西指出,调整三种金属粉末加入的先后顺序为 (所用金属粉末均为足量),也能实
现实验目的。
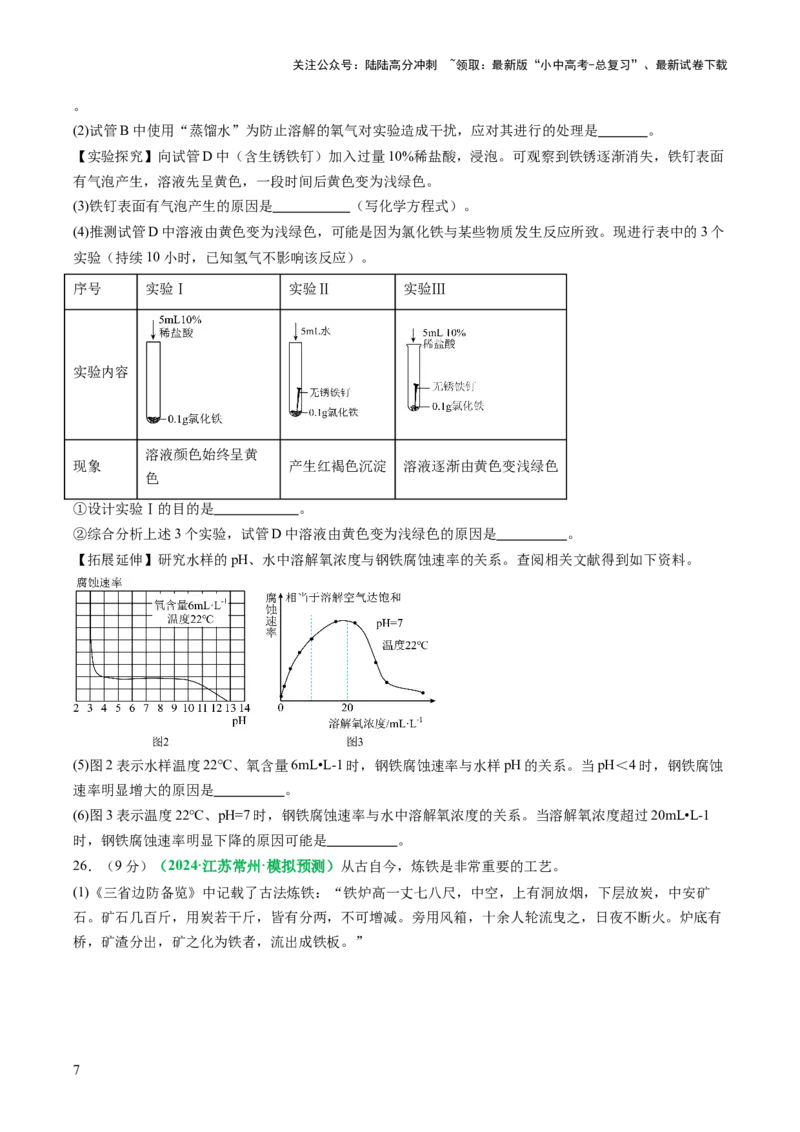
24.(6分)(2024·山西太原·二模)同学们学习了金属的化学性质后,在实验室设计并进行如下实验以
探究铝、铁、铜的金属活动性顺序。
(1)实验方法:将两根铝丝用砂纸打磨后,分别浸入到盛有氯化亚铁溶液和硫酸铜溶液的两支试管中,铝丝
浸入溶液前需要先用砂纸打磨,其目的是 。
(2)实验现象:Ⅰ和Ⅱ中均有较明显的反应现象,由此得到的结论是 。
(3)实验原理:Ⅰ或Ⅱ中发生反应的化学方程式 (写一个)。
(4)有同学认为仅以图示的实验还不能达到该实验目的,需要补充实验。 (简要叙述实验步骤)继续
探究。
(5)问题与交流:本实验中采用将铝丝盘成螺旋状插入溶液中,目的 。
四、科学探究题
25.(9分)(2024·安徽·模拟预测)金属材料对于促进生产发展,改善人类生活发挥了巨大作用。钢铁
是用量最大、用途最广的合金,钢铁的腐蚀是重要研究课题。
【知识回顾】用如图1所示五组实验进行铁钉腐蚀的研究。一段时间后试管A、B中铁钉几乎没有生锈,
而试管C中铁钉明显锈蚀,试管D、E中铁钉严重锈蚀。
(1)由五组实验中的 (填实验组序号)现象可知,铁的锈蚀是铁跟氧气和水作用的过程;铁锈化学式
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
。
(2)试管B中使用“蒸馏水”为防止溶解的氧气对实验造成干扰,应对其进行的处理是 。
【实验探究】向试管D中(含生锈铁钉)加入过量10%稀盐酸,浸泡。可观察到铁锈逐渐消失,铁钉表面
有气泡产生,溶液先呈黄色,一段时间后黄色变为浅绿色。
(3)铁钉表面有气泡产生的原因是 (写化学方程式)。
(4)推测试管D中溶液由黄色变为浅绿色,可能是因为氯化铁与某些物质发生反应所致。现进行表中的3个
实验(持续10小时,已知氢气不影响该反应)。
序号 实验Ⅰ 实验Ⅱ 实验Ⅲ
实验内容
溶液颜色始终呈黄
现象 产生红褐色沉淀 溶液逐渐由黄色变浅绿色
色
①设计实验Ⅰ的目的是 。
②综合分析上述3个实验,试管D中溶液由黄色变为浅绿色的原因是 。
【拓展延伸】研究水样的pH、水中溶解氧浓度与钢铁腐蚀速率的关系。查阅相关文献得到如下资料。
(5)图2表示水样温度22℃、氧含量6mL•L-1时,钢铁腐蚀速率与水样pH的关系。当pH<4时,钢铁腐蚀
速率明显增大的原因是 。
(6)图3表示温度22℃、pH=7时,钢铁腐蚀速率与水中溶解氧浓度的关系。当溶解氧浓度超过20mL•L-1
时,钢铁腐蚀速率明显下降的原因可能是 。
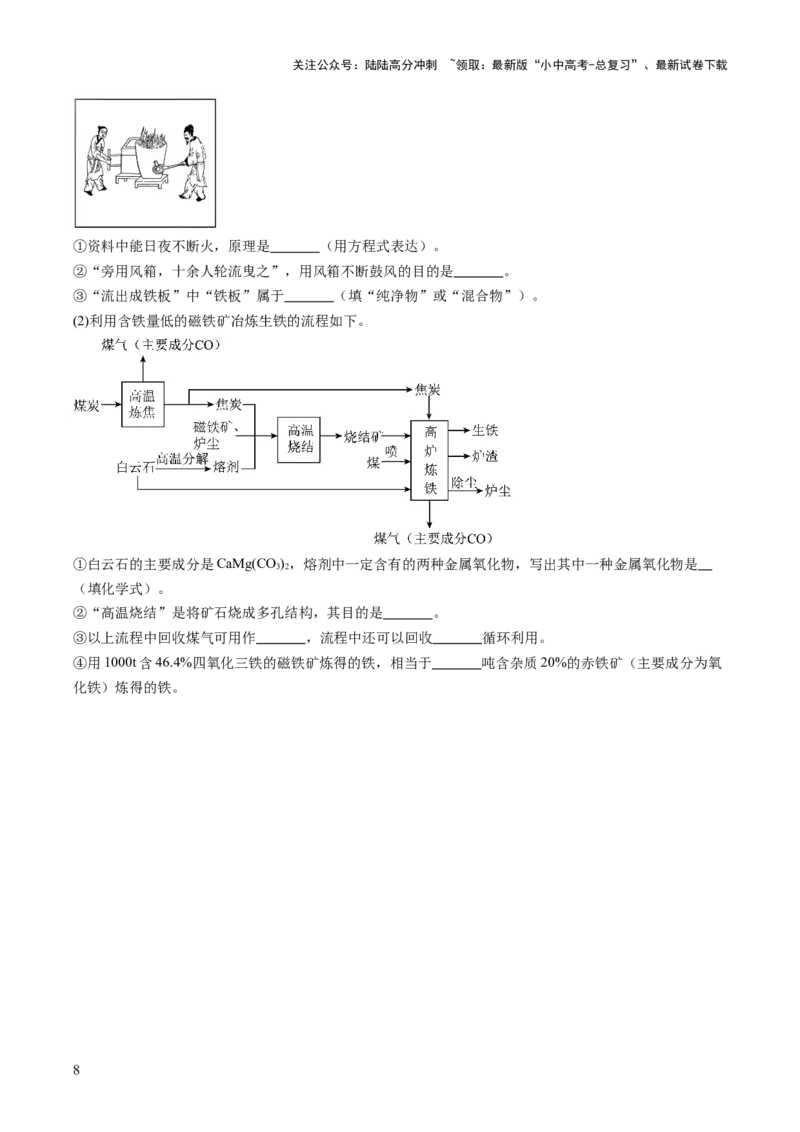
26.(9分)(2024·江苏常州·模拟预测)从古自今,炼铁是非常重要的工艺。
(1)《三省边防备览》中记载了古法炼铁:“铁炉高一丈七八尺,中空,上有洞放烟,下层放炭,中安矿
石。矿石几百斤,用炭若干斤,皆有分两,不可增减。旁用风箱,十余人轮流曳之,日夜不断火。炉底有
桥,矿渣分出,矿之化为铁者,流出成铁板。”
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①资料中能日夜不断火,原理是 (用方程式表达)。
②“旁用风箱,十余人轮流曳之”,用风箱不断鼓风的目的是 。
③“流出成铁板”中“铁板”属于 (填“纯净物”或“混合物”)。
(2)利用含铁量低的磁铁矿冶炼生铁的流程如下。
①白云石的主要成分是CaMg(CO ),熔剂中一定含有的两种金属氧化物,写出其中一种金属氧化物是
3 2
(填化学式)。
②“高温烧结”是将矿石烧成多孔结构,其目的是 。
③以上流程中回收煤气可用作 ,流程中还可以回收 循环利用。
④用1000t含46.4%四氧化三铁的磁铁矿炼得的铁,相当于 吨含杂质20%的赤铁矿(主要成分为氧
化铁)炼得的铁。
8