文档内容
2024年高三上学期化学期中考试试卷
一、单选题
1.下列物质属于电解质的是( )
A.饱和食盐水 B.二氧化碳
C.石墨 D.硫酸钡
2.设 为阿伏加德罗常数的值,下列叙述不正确的是
A. 晶体中含有 个阳离子
B.100g质量分数为46%的 水溶液中O原子数为
C.标准状况下,2.24L一氯甲烷中含 型σ键数目为
D.常温下, 的 溶液中,水电离出的OH-数目为
3.下列关于纯净物、混合物、强电解质、弱电解质和非电解质的组合正确的是
强电解
纯净物 混合物 弱电解质 非电解质
质
A 氨 水 氯 水 硫 酸 醋 酸 干 冰
B 氧化铁 盐 酸 硫酸钡 亚硫酸 二氧化硫
C 胆 矾 碘 酒 苛性钾 氢硫酸 碳酸钙
D 氯化氢 氢氧化钠溶液 氯化钠 磷 酸 氯 气
A.A B.B C.C D.D
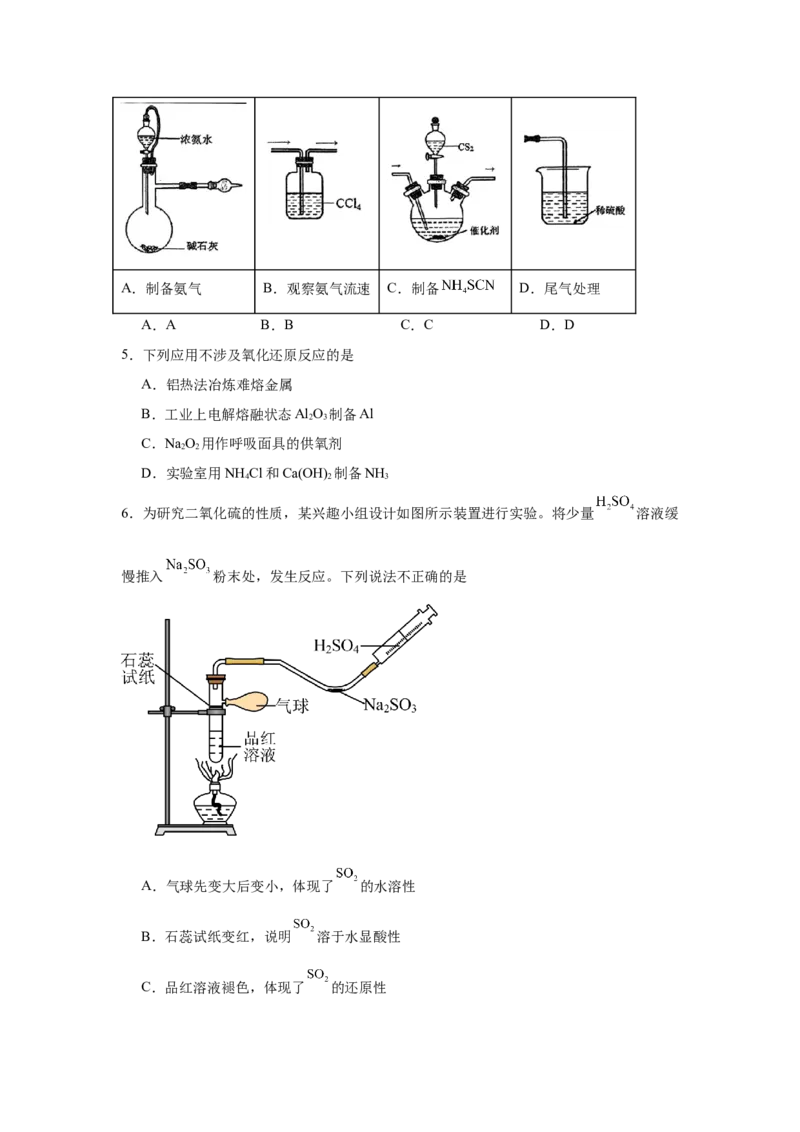
4.某小组模拟工业制备 ,其原理是: ,其
中不合理的是A.制备氨气 B.观察氨气流速 C.制备 D.尾气处理
A.A B.B C.C D.D
5.下列应用不涉及氧化还原反应的是
A.铝热法冶炼难熔金属
B.工业上电解熔融状态Al O 制备Al
2 3
C.NaO 用作呼吸面具的供氧剂
2 2
D.实验室用NH Cl和Ca(OH) 制备NH
4 2 3
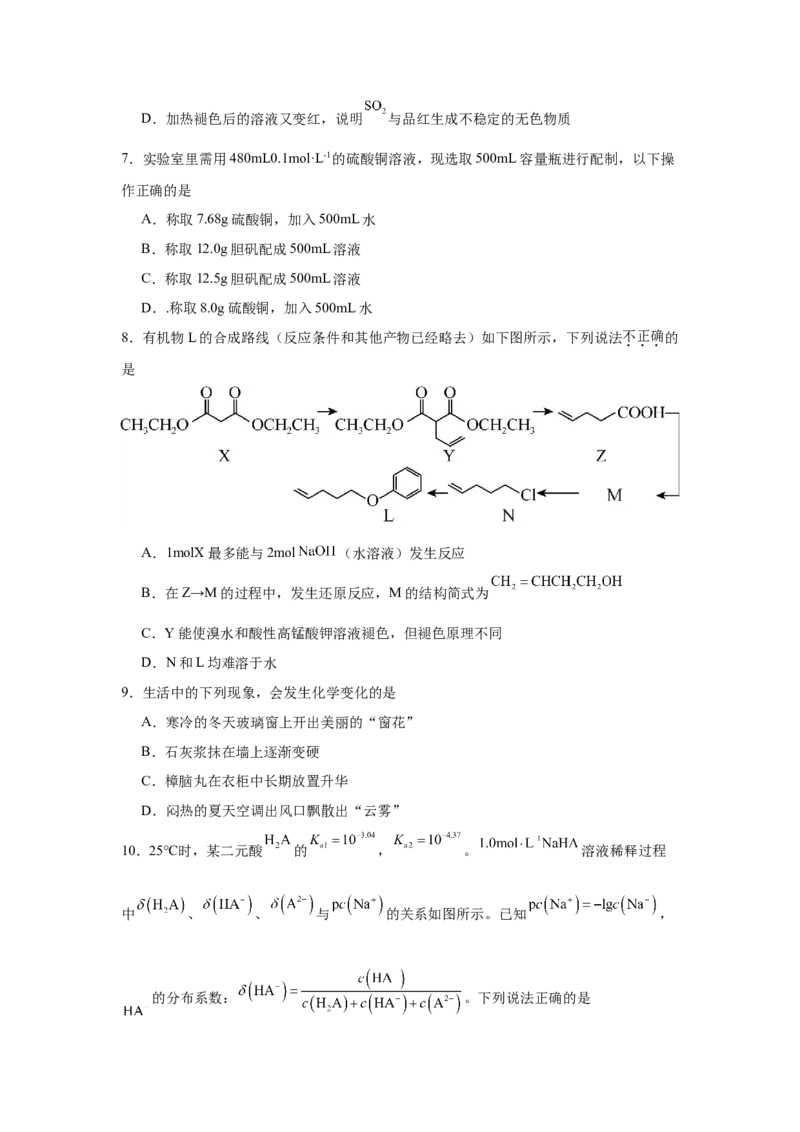
6.为研究二氧化硫的性质,某兴趣小组设计如图所示装置进行实验。将少量 溶液缓
慢推入 粉末处,发生反应。下列说法不正确的是
A.气球先变大后变小,体现了 的水溶性
B.石蕊试纸变红,说明 溶于水显酸性
C.品红溶液褪色,体现了 的还原性D.加热褪色后的溶液又变红,说明 与品红生成不稳定的无色物质
7.实验室里需用480mL0.1mol·L-1的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操
作正确的是
A.称取7.68g硫酸铜,加入500mL水
B.称取12.0g胆矾配成500mL溶液
C.称取12.5g胆矾配成500mL溶液
D..称取8.0g硫酸铜,加入500mL水
8.有机物L的合成路线(反应条件和其他产物已经略去)如下图所示,下列说法不正确的
是
A.1molX最多能与2mol (水溶液)发生反应
B.在Z→M的过程中,发生还原反应,M的结构简式为
C.Y能使溴水和酸性高锰酸钾溶液褪色,但褪色原理不同
D.N和L均难溶于水
9.生活中的下列现象,会发生化学变化的是
A.寒冷的冬天玻璃窗上开出美丽的“窗花”
B.石灰浆抹在墙上逐渐变硬
C.樟脑丸在衣柜中长期放置升华
D.闷热的夏天空调出风口飘散出“云雾”
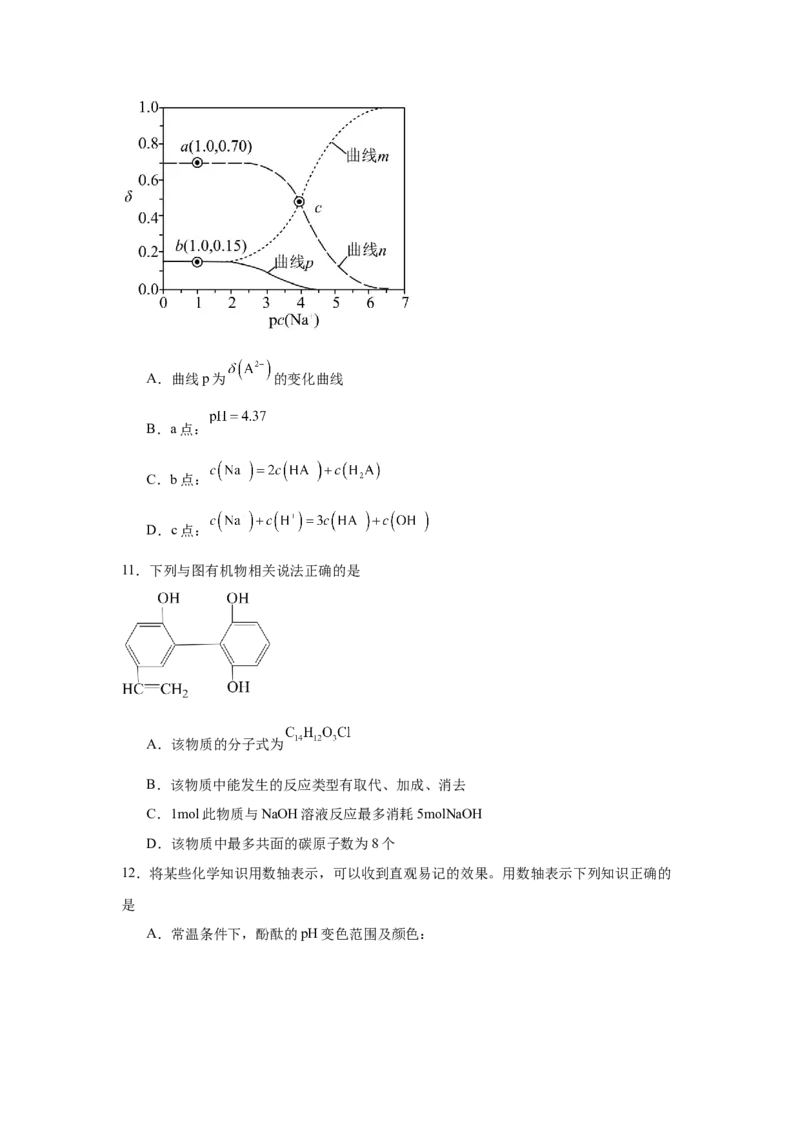
10.25℃时,某二元酸 的 , 。 溶液稀释过程
中 、 、 与 的关系如图所示。已知 ,
的分布系数: 。下列说法正确的是A.曲线p为 的变化曲线
B.a点:
C.b点:
D.c点:
11.下列与图有机物相关说法正确的是
A.该物质的分子式为
B.该物质中能发生的反应类型有取代、加成、消去
C.1mol此物质与NaOH溶液反应最多消耗5molNaOH
D.该物质中最多共面的碳原子数为8个
12.将某些化学知识用数轴表示,可以收到直观易记的效果。用数轴表示下列知识正确的
是
A.常温条件下,酚酞的pH变色范围及颜色:B.常温条件下,甲基橙的pH变色范围及颜色:
C.AlCl 溶液与NaOH溶液混合铝元素的形式:
3
D.CO 和NaOH溶液反应后的产物:
2
13.下列实验装置或标识及对应叙述正确的是
D.此图标是提示实验中
C.图甲装置中将C管
B.收集 并验 会用到电器,可以直接湿
A.保存液溴 位置提高可用于检验
满 手操作,但实验结束应及
装置气密性
时切断电源
A.A B.B C.C D.D
14.下列物质除杂的操作正确的是
选项 物质(杂质) 操作
A N(H ) 气体依次通过灼热的CuO、浓硫酸
2 2
B NaCl溶液( ) 加入稀硫酸至不再产生气泡
C Mg粉(Al) 加入足量稀盐酸,过滤、洗涤、干燥D 溶液( ) 加入足量锌粉,过滤
A.A B.B C.C D.D
二、解答题
15.某溶液仅含如表离子中的5种(不考虑水的电离及离子的水解)且各种离子物质的量均
为1 mol。
阳离子 Na+ 、Mg2+ 、Fe3+ 、Al3+ 、Fe2+
OH- 、 、Cl- 、 、
阴离子
①若向溶液中加入KSCN溶液无明显变化;
②若向原溶液中加入稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,且溶液中
阴离子种类不变。
请推断:
(1)原溶液中含有的阳离子是 ; 含有的阴离子是 。
(2)向原溶液中加入足量稀盐酸发生反应的离子方程式为 。
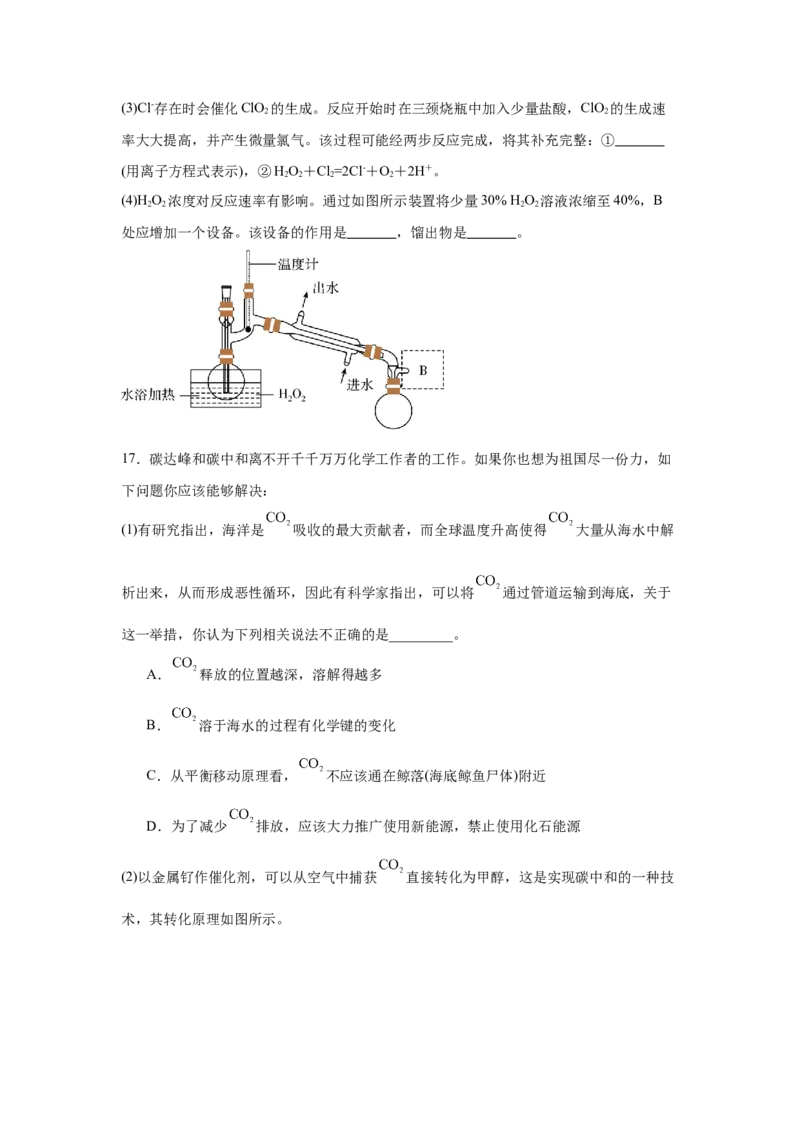
16.ClO 是一种优良的消毒剂,浓度过高时易发生分解,常将其制成NaClO 固体,以便运
2 2
输和贮存。过氧化氢法制备NaClO 固体的实验装置如图所示。
2
已知:
2NaClO+HO+HSO =2ClO ↑+O↑+NaSO +2HO
3 2 2 2 4 2 2 2 4 2
2ClO +HO+2NaOH=2NaClO +O↑+2HO
2 2 2 2 2 2
ClO 熔点-59 ℃、沸点11 ℃;HO 沸点150 ℃
2 2 2
请回答:
(1)仪器A的作用是 ;冰水浴冷却的目的是 , (写两种)。
(2)空气流速过快或过慢,均降低NaClO 产率,试解释其原因 。
2(3)Cl-存在时会催化ClO 的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO 的生成速
2 2
率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完整:①
(用离子方程式表示),②HO+Cl=2Cl-+O+2H+。
2 2 2 2
(4)H O 浓度对反应速率有影响。通过如图所示装置将少量30% H O 溶液浓缩至40%,B
2 2 2 2
处应增加一个设备。该设备的作用是 ,馏出物是 。
17.碳达峰和碳中和离不开千千万万化学工作者的工作。如果你也想为祖国尽一份力,如
下问题你应该能够解决:
(1)有研究指出,海洋是 吸收的最大贡献者,而全球温度升高使得 大量从海水中解
析出来,从而形成恶性循环,因此有科学家指出,可以将 通过管道运输到海底,关于
这一举措,你认为下列相关说法不正确的是_________。
A. 释放的位置越深,溶解得越多
B. 溶于海水的过程有化学键的变化
C.从平衡移动原理看, 不应该通在鲸落(海底鲸鱼尸体)附近
D.为了减少 排放,应该大力推广使用新能源,禁止使用化石能源
(2)以金属钌作催化剂,可以从空气中捕获 直接转化为甲醇,这是实现碳中和的一种技
术,其转化原理如图所示。根据流程图,在该反应中,高分子物质 的作用是 。若
在实验室一个5L的容器中通过该反应一小时捕获 的质量为22kg,则这一小时内该反
应用另一反应物H 表示的反应速率为 。
2
催化重整对温室气体的减排具有重要意义,某温度下在体积为2L的容器中加
入3mol 、3mol 以及催化剂,同时进行反应:
①
②
(3)写出该温度下CO和 生成 的热化学方程式 。
(4)若达到平衡时测得有水蒸气0.5mol、CO1.5mol、 2mol,若在同一温度下某时刻测得
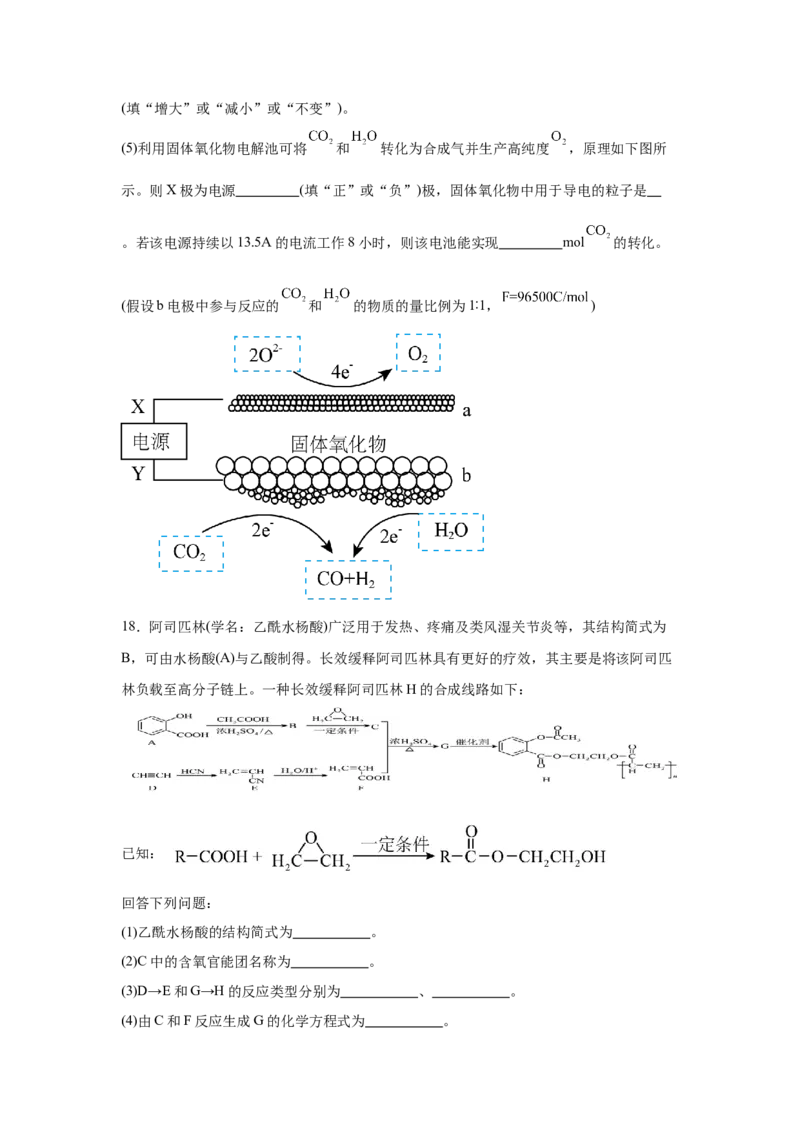
体系中CO、 、 、 的物质的量均为2mol,则此后一段时间内, 将(填“增大”或“减小”或“不变”)。
(5)利用固体氧化物电解池可将 和 转化为合成气并生产高纯度 ,原理如下图所
示。则X极为电源 (填“正”或“负”)极,固体氧化物中用于导电的粒子是
。若该电源持续以13.5A的电流工作8小时,则该电池能实现 mol 的转化。
(假设b电极中参与反应的 和 的物质的量比例为1∶1, )
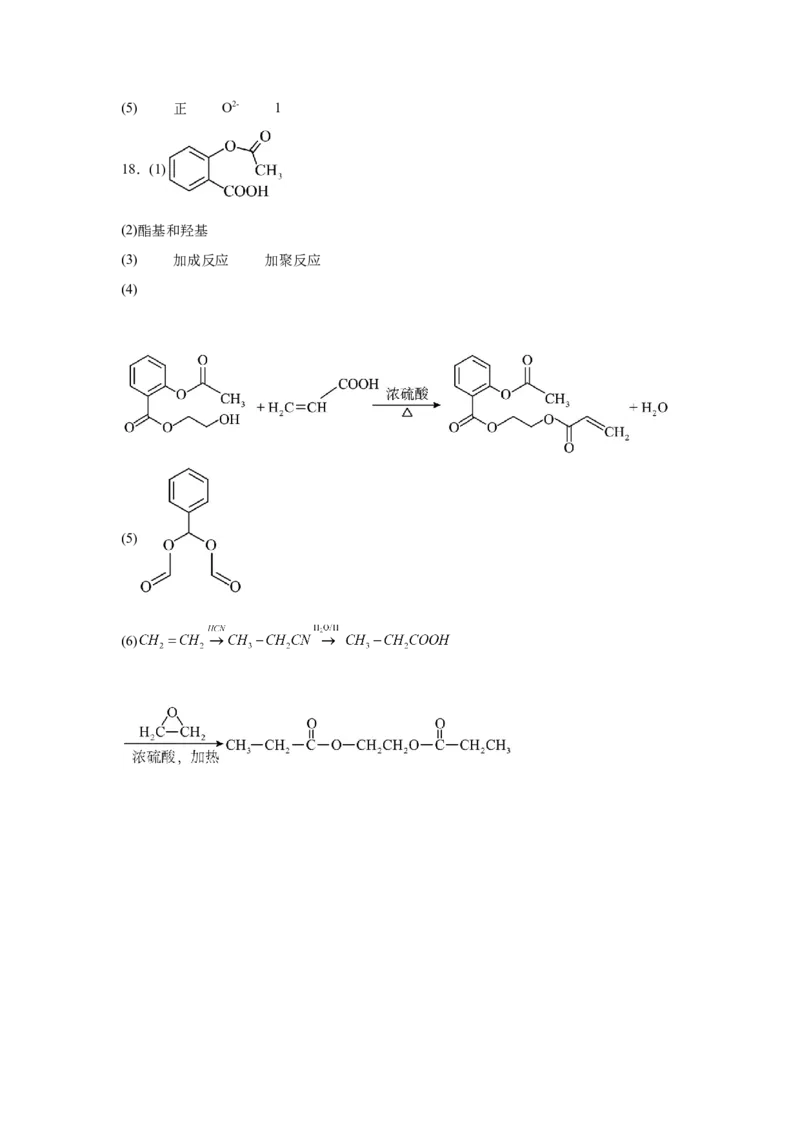
18.阿司匹林(学名:乙酰水杨酸)广泛用于发热、疼痛及类风湿关节炎等,其结构简式为
B,可由水杨酸(A)与乙酸制得。长效缓释阿司匹林具有更好的疗效,其主要是将该阿司匹
林负载至高分子链上。一种长效缓释阿司匹林H的合成线路如下:
已知:
回答下列问题:
(1)乙酰水杨酸的结构简式为 。
(2)C中的含氧官能团名称为 。
(3)D→E和G→H的反应类型分别为 、 。
(4)由C和F反应生成G的化学方程式为 。(5)有机物M是阿司匹林的同分异构体,具有以下特征,写出M的结构简式 。
①只含1中官能团,且能够发生银镜反应;
②核磁共振氢谱为五组峰,峰面积比为2:2:2:1:1;
③能够发生水解反应,且水解产物只有两种;
(6)设计以乙烯和 为原料制备
的合成路线 (无机试剂任选)。参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 D C B D D C C B B D
题号 11 12 13 14
答案 C D C A
1.D
2.C
3.B
4.D
5.D
6.C
7.C
8.B
9.B
10.D
11.C
12.D
13.C
14.A
15. Fe2+、Mg2+ Cl-、NO 、SO 3Fe2++NO +4H+===3Fe3++NO↑+
2HO
2
16.(1) 防止倒吸 降低NaClO 的溶解度;减少HO 的分解; 增加ClO 的
2 2 2 2
溶解度;减少ClO 的分解(任写两种)
2
(2)空气流速过慢时,ClO 不能及时被移走,浓度过高导致分解;空气流速过快时,ClO 不
2 2
能被充分吸收
(3)2 +2Cl-+4H+=2ClO ↑+Cl↑+2HO
2 2 2
(4) 减压 HO
2
17.(1)D
(2) 催化剂 5
(3)CO(g)+H O(g) =CO (g)+ H (g) ΔH=-41.2kJ/mol
2 2 2
(4)减小(5) 正 O2- 1
18.(1)
(2)酯基和羟基
(3) 加成反应 加聚反应
(4)
(5)
(6)