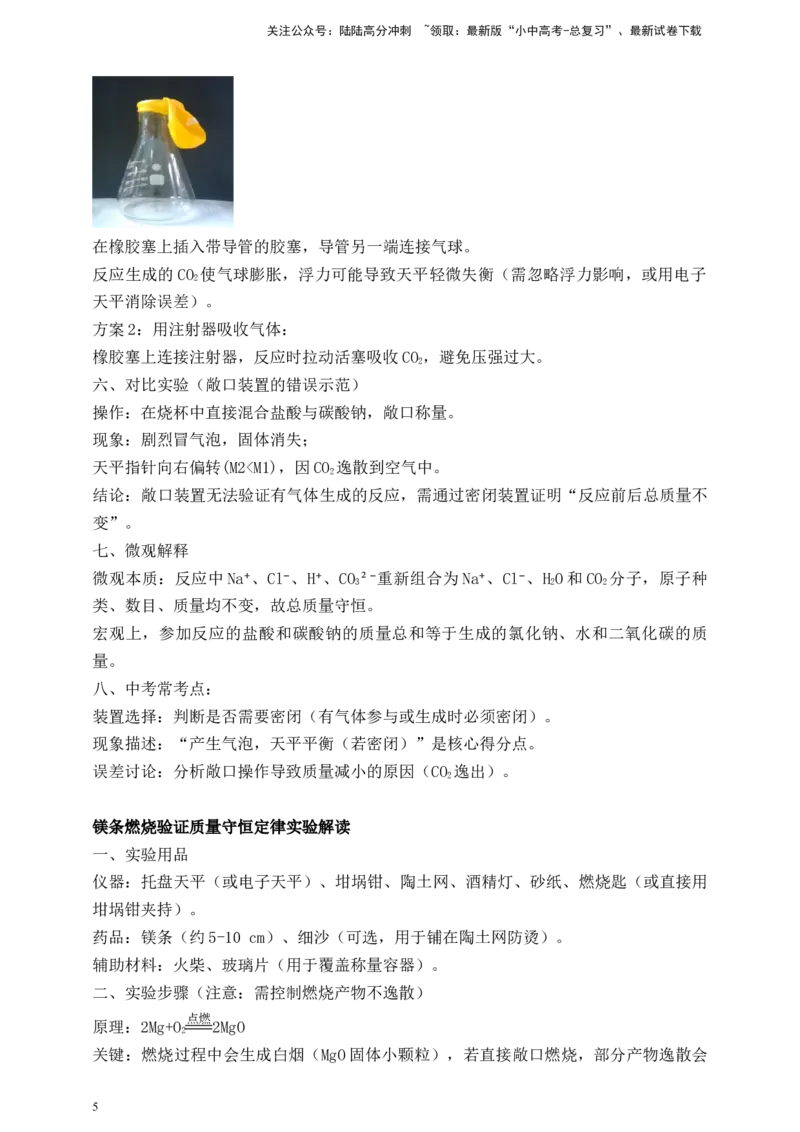
文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(七)质量守恒定律
实验深度突破:
铜与氧气反应验证质量守恒定律
一、实验原理
△
化学方程式:2Cu+O 2CuO
2
核心逻辑:通过称量反应前后锥形瓶内物质的总质量,验证化学反应遵循质量守恒定律
(反应前后总质量相等)。
二、实验装置与药品
实验仪器:锥形瓶、带导管的橡胶塞(导管一端系气球)、酒精灯、托盘天平、坩埚
钳。
药品:铜粉(或铜片)、细沙。
三、实验步骤
1、称量反应前总质量:
2、在锥形瓶底部铺少量细沙(防止加热时瓶底炸裂),放入铜粉,塞上带气球的橡胶
塞。
3、用托盘天平称量锥形瓶+药品+橡胶塞的总质量,记为M1。
4、加热反应:用酒精灯给锥形瓶均匀加热,观察到铜粉由红色逐渐变为黑色(生成
CuO)。
注意:加热时气球会因气体膨胀而鼓起,冷却后逐渐变瘪(氧气被消耗)。
称量反应后总质量:
5、冷却至室温后,再次称量锥形瓶+药品+橡胶塞的总质量,记为M2。
四、实验现象与结论
现象:铜粉变黑,气球先膨胀后变瘪。
M1=M2(或误差在允许范围内)。
结论:化学反应前后物质的总质量相等,验证质量守恒定律成立。
五、关键注意事项
1、气球的作用:平衡气压(防止瓶内气体膨胀冲开瓶塞),同时密封体系,避免空气
逸出或进入。
2、冷却后称量:避免热胀冷缩对质量测量产生干扰。
3、药品铺细沙:防止加热时锥形瓶局部过热炸裂。
实验误差分析:
若M2M1,可能是未冷却时空气进入瓶内。
微观解释:
铜原子与氧分子反应生成氧化铜分子,原子种类(Cu、O)、数目、质量均不变,故总
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
质量守恒。
宏观上,参加反应的铜和氧气的质量总和等于生成的氧化铜的质量。
铁与硫酸铜反应验证质量守恒定律
一、实验用品
仪器:托盘天平(带砝码或电子天平)、锥形瓶(或烧杯)、橡胶塞(或封口膜)、量
筒、镊子。
药品:铁钉(或铁粉)、硫酸铜溶液(蓝色)。
辅助材料:砂纸、细线(可选)。
二、实验步骤(密闭体系)
原理:Fe+CuSO =Cu+FeSO
4 4
步骤:
1、药品准备:
2、用砂纸打磨铁钉表面铁锈和氧化膜,至光亮(确保反应充分)。
3、用量筒量取约50 mL硫酸铜溶液,倒入锥形瓶中。
4、组装装置并称量:
5、将铁钉用细线系住,悬挂于锥形瓶内(不接触溶液,避免提前反应),立即用橡胶
塞密封瓶口。
6、将整个装置放在托盘天平上,称量总质量(M1)(需调平天平,记录数据)。
7、引发反应:倾斜锥形瓶,使铁钉浸入硫酸铜溶液中,轻轻摇晃瓶身(加速反应)。
观察现象,同时保持装置密闭。
8、静置与二次称量:
待溶液颜色不再变化,再次称量装置总质量(M2)。
三、实验现象
反应过程中:
1、铁钉表面:逐渐附着一层红色固体(生成的铜)。
2、溶液颜色:由蓝色逐渐变为浅绿色。
3、无气泡产生(排除气体参与反应的干扰)。
称量结果:天平保持平衡,即(M1=M2),验证质量守恒定律。
四、关键注意事项
1、装置密封性:必须使用密闭容器(如带塞子的锥形瓶),防止液体溅出或空气影响
(虽无气体参与,但敞口可能因蒸发导致误差)。
若用烧杯,可用封口膜覆盖瓶口,并用橡皮筋扎紧。
2、铁钉处理:铁锈(主要成分为Fe O ))会阻碍反应,需彻底打磨至光亮;
2 3
铁粉反应速率更快,但需用滤纸包裹防止散落。
3、溶液浓度与用量:
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)硫酸铜溶液浓度不宜过低,否则反应现象不明显;
(2)铁钉需过量,确保硫酸铜完全反应(若铁钉不足,溶液可能残留蓝色)。
称量时机:
(3)反应放热较少,可无需冷却直接称量,但需待固体完全沉降后再操作(避免晃动
导致质量误差)。
五、误差分析与改进
1、天平不平衡的可能原因:
(1)左盘偏轻:装置未密封,液体蒸发或倾倒时少量溶液溅出;
(2)右盘偏轻:铁钉未打磨,表面氧化物参与反应导致实际铁质量偏小。
改进方案:
(1)用电子天平实时称量,观察反应过程中质量是否恒定;
(2)若用铁粉,可将铁粉装入小试管中,倾斜试管使铁粉倒入硫酸铜溶液(避免粉末
洒出)。
六、微观解释
微观解释:反应中Fe原子置换出Cu² ,原子种类(Fe、Cu、S、O)和数目均不变,离
⁺
子重新组合后总质量守恒。
宏观上,参加反应的铁和硫酸铜的质量总和等于生成的铜和硫酸亚铁的质量。
七、中考常考点
装置选择:判断是否需要密闭(无气体参与时敞口可简化,但教材推荐密闭)。
现象描述:“铁钉变红,溶液变浅绿”是核心得分点。
方程式书写:注意产物为硫酸亚铁,非硫酸铁。
误差讨论:分析敞口操作是否影响结论(通常不影响,但需强调理论上应密闭)。
盐酸与碳酸钠反应验证质量守恒定律
一、实验用品
仪器:托盘天平(或电子天平)、锥形瓶(带橡胶塞)、小试管、镊子、量筒。
药品:稀盐酸(约3-5%浓度)、碳酸钠粉末(或颗粒)。
辅助材料:砂纸(若使用金属仪器需打磨)、细线(可选)。
二、实验步骤(密闭体系,防止气体逸出)
原理:Na CO +2HCl=2NaCl+H O+CO ↑
2 3 2 2
关键:因有气体生成,必须用密闭装置防止质量损失。
步骤:
1、药品分装:
2、用量筒量取10-15mL稀盐酸,倒入锥形瓶中。
3、用镊子取少量碳酸钠粉末(约2-3g),放入小试管中(避免直接接触盐酸)。
4、组装装置并称量:
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
5、将小试管用细线悬挂于锥形瓶内(确保不接触盐酸),迅速用橡胶塞密封瓶口。
6、将整个装置放在托盘天平上,称量总质量(M1)(调平天平,记录数据)。
7、引发反应:倾斜锥形瓶,使稀盐酸流入小试管中与碳酸钠接触,轻轻摇晃锥形瓶
(加速反应)。
8、观察现象的同时保持装置密闭。
9、静置与二次称量:待反应停止(不再有气泡产生),再次称量装置总质量(M2)。
三、实验现象
反应过程中:
1、剧烈反应,气泡产生(生成的CO 气体)。
2
2、碳酸钠粉末逐渐溶解消失。
3、溶液仍为无色透明(产物NaCl溶液为无色)。
称量结果:
1、若装置完全密闭:天平保持平衡,(M1=M2),验证质量守恒定律。
2、若装置漏气:天平指针向右偏转((M2M1)(因反应物包含氧气质量)。
若白烟部分逸散:(M2)可能接近(M1)或略大(实际操作中难以完全收集,易导致误
差)。
方案2(密闭):
天平平衡,(M1=M2)(氧气参与反应但未逸出,总质量守恒)。
四、关键注意事项
安全操作:
1、燃烧时不可直视火焰(强光可能损伤眼睛),需佩戴护目镜或用滤光片遮挡。夹持
镁条的坩埚钳需干燥,避免接触水导致烫伤。
2、减少产物逸散:敞口实验时,可在陶土网上方倒扣烧杯(留缝隙通气),减少白烟
飘落损失。
3、称量动作要迅速,避免燃烧后的高温固体与空气进一步反应(如吸收 CO 生成
2
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
MgCO )。
3
装置选择:
最佳方案:使用带玻璃导管的锥形瓶(导管末端套气球),既能平衡气压,又能收集白
烟(气球膨胀后冷却会收缩,吸入部分白烟)。
五、误差分析与改进
天平不平衡的常见原因:
1、白烟(MgO)逸散到空气中,导致M2MO )。
2
3、装置评价:对比敞口与密闭装置的科学性,强调气体参与反应需用密闭体系。
化学反应中原子的种类、数目、质量均守恒,因此宏观上反应前后物质总质量不变,符
合质量守恒定律。密闭条件下:反应前后总质量相等,验证质量守恒定律;敞口条件
下:需考虑气体参与或生成的质量,不能直接通过天平称量判断守恒,需结合理论分
析。
中考命题探秘
一、考情分析
质量守恒定律作为初中化学的核心内容之一,在中考里占据着重要位置,尤其是与之相
关的实验,更是中考考查的重点,它全面检验学生对化学知识的理解与运用能力。回顾
近几年各地中考真题,质量守恒定律实验的考查频率相当高。几乎每年都会涉及这一考
点。从考查内容来看,不仅关注学生对质量守恒定律基本概念的理解,像“参加化学反
应的各物质的质量总和等于反应后生成的各物质的质量总和”这一核心内容,还着重考
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
查学生对实验细节、实验误差分析以及运用定律解决实际问题的能力。并且该知识点常
与化学方程式书写、化学反应类型判断等知识相互关联,综合考查学生的知识体系构
建。
二、考查形式
1.选择题:常考查对质量守恒定律基本概念的理解,如判断化学反应前后物质质量的变
化情况,根据实验现象判断是否遵循质量守恒定律,比较反应前后各物质质量的大小关
系,分析化学反应中元素化合价的变化是否符合质量守恒定律等。
2.填空题:常利用质量守恒定律推断物质的组成元素,给定化学反应的部分信息,确定
未知物质的化学式,根据质量守恒定律配平化学方程式,填写反应前后物质的质量、元
素质量等相关数据。
3.实验探究题:主要围绕质量守恒定律的实验验证展开。包括实验装置的选择与评价,
判断给定的实验装置能否用于验证质量守恒定律并说明理由;实验操作步骤的考查,如
实验前的准备工作、实验过程中的正确操作方法、实验结束后的处理等;实验现象的描
述与分析,准确描述实验中观察到的现象,并依据质量守恒定律对现象进行解释;实验
误差分析,找出实验过程中可能导致误差的因素,并提出改进措施。
4.计算题:通常将质量守恒定律与化学反应中物质质量的计算紧密结合。例如,根据反
应前后物质质量的变化,计算反应物或生成物的质量;结合化学方程式,利用质量守恒
定律确定混合物中某一物质的质量分数;通过质量守恒定律计算化学反应中各物质的质
量比等。
三、中考所占分值或比例
在各地中考化学试卷中,质量守恒定律实验及相关内容所占分值和比例各有不同。在满
分100分的化学试卷里,这部分内容分值大概在8-15分,约占总分的8%-15%。在一些
将化学与物理等科目合卷的地区,若试卷总分 200分,化学部分占100分左右,那么质
量守恒定律相关内容分值大概在6-12分,约占化学总分的6%-12%。不过,不管具体分
值和比例如何变化,它始终是中考化学考查的重点知识模块。
四、中考预测
1.考查内容创新:未来中考可能会结合前沿科技或生活实际,创设新颖的问题情境来考
查质量守恒定律实验。比如以新型材料的合成、环境保护中的化学反应等为背景,让学
生运用质量守恒定律去分析和解决问题。
2.实验探究深化:实验探究题的难度或许会有所增加,对实验设计的创新性、科学性以
及学生的批判性思维能力提出更高要求。例如,要求学生自主设计实验方案来验证质量
守恒定律,并且要考虑到实验过程中的各种干扰因素,同时还可能会涉及不同实验方案
的对比与评价。
3.跨学科融合趋势:随着教育对学生综合素养的重视,质量守恒定律的考查可能会与物
理学科中的能量守恒、物质的状态变化等知识进行融合,考查学生跨学科解决问题的能
力。
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
五、备考建议
1.夯实基础概念:深入理解质量守恒定律的内涵和外延,通过举例、对比等方式,明确
“参加反应”“质量总和”等关键词的含义,能够从微观角度(原子的种类、数目和质
量不变)解释质量守恒定律。
2.重视实验细节:仔细梳理教材中的质量守恒定律实验,掌握实验的原理、装置、步
骤、现象和结论。对实验中的关键操作,如称量的准确性、装置的气密性检查、药品的
取用等,要反复琢磨;同时,要学会分析实验误差产生的原因,并思考改进方法。
3.强化练习巩固:通过有针对性的练习题,加深对质量守恒定律的应用能力。在练习过
程中,注重总结解题方法和技巧,比如如何利用质量守恒定律进行物质化学式的推导、
质量的计算等。对于做错的题目,要认真分析原因,查漏补缺。
4.关注知识拓展:平时多关注化学领域的前沿动态和生活中的化学现象,将质量守恒定
律与实际应用相联系,拓宽知识视野,提高知识迁移能力和解决实际问题的能力。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
10