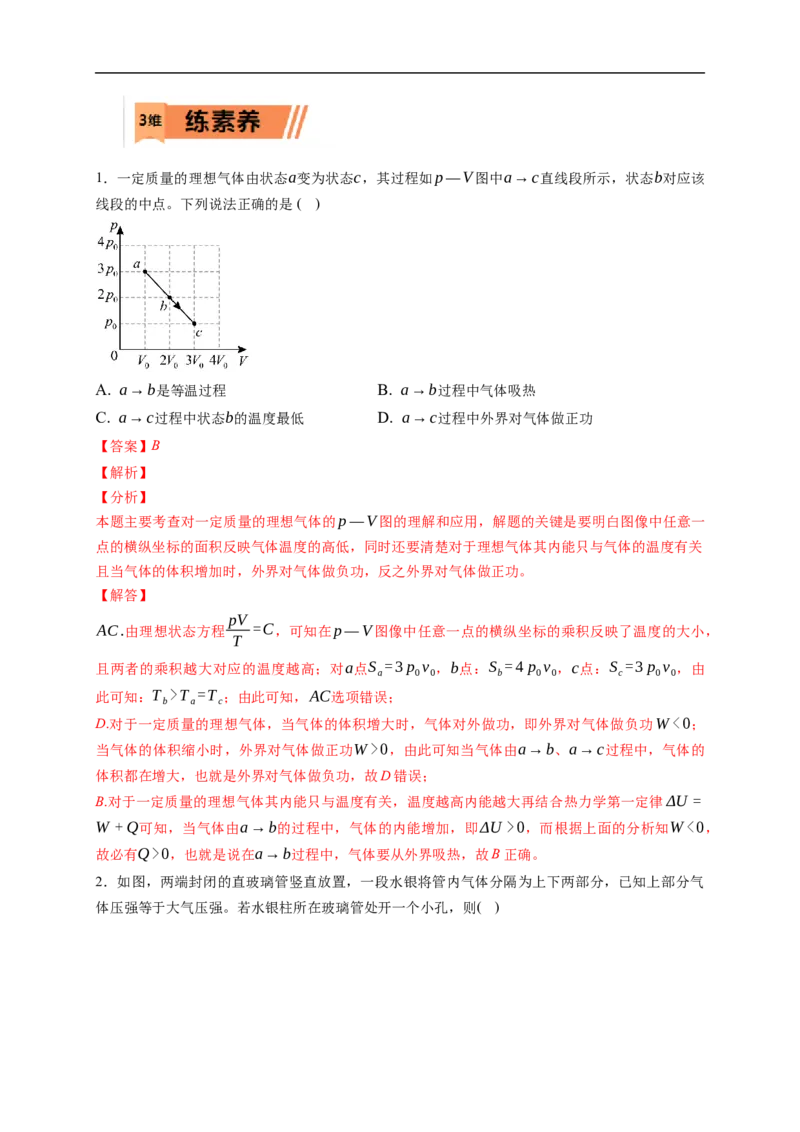
文档内容
T
1 2
C. 图丙说明气体压强的大小既与分子动能有关也与分子的密集程度有关
D. 图丁说明水黾受到了浮力作用
【答案】C
【解析】
【分析】
本题考查晶体与非晶体的性质、气体分子速率的分布、气体压强的决定因数和表面张力等内容,要
求能用相关物理规律解释相关的现象。
【解答】
A.图甲说明薄板具有各向同性,多晶体和非晶体都具有各向同性,说明薄板可能是多晶体,也可能
是非晶体,故A错误;
B.图乙看出温度越高,各速率区间的分子数占总分子数的百分比的最大值向速度大的方向迁移,可
知T >T ,故B错误;
2 1
C.如图丙可以说明,气体压强的大小既与分子动能有关,也与分子的密集程度有关,故C正确;
D.水黾停在水面上的原因是水黾受到了水的表面张力的作用,故D错误。
故选C。
5.水对玻璃是浸润液体,而水银对玻璃是不浸润液体,它们在毛细管中将发生上升或下降的现象,
现把粗细不同的三根毛细管插入水和水银中,液柱如图所示,其中正确的现象应是:
A. B. C. D.
【答案】D
【解析】【分析】
浸润液体在毛细管上升和不浸润液体在毛细管下降的现象称为毛细现象,且在玻璃试管中,如果液
体能够浸润器壁,管的内径越细,液体所能达到的高低越高,且液面呈凹形。
本题考查毛细现象,知道什么是毛细现象,并能从现象区分是浸润和不浸润。
【解答】
AC.水银对玻璃是不浸润液体,细管中液面应下降,且管的内径越细,液面下降应越多,故AC错
误;
BD.水对玻璃是浸润液体,细管中液面应上升,且管的内径越细,液面上升应越多,故B错误,D
正确。
故选D。
6.如图所示,两根粗细相同的玻璃管下端用橡皮管相连,左管内封有一段长30cm的气体,右管开
口,左管水银面比右管内水银面高25cm,大气压强为75cmHg,现移动右侧玻璃管,使两侧管内
水银面相平,此时气体柱的长度为( )
A. 20cm B. 25cm C. 40cm D. 45cm
【答案】A
【解析】解:设玻璃管横截面积为S,初始状态气柱长度为L =30cm=0.3m,密闭气体初始状态:
1
压强p =p -p =(75-25)cmHg=50cmHg,体积V =SL ,移动右侧玻璃管后,压强
1 0 h 1 1
p =p =75cmHg,体积V =SL ,根据玻意耳定律得:
2 0 1 2
p V =p V 代入数据解得:L =0.2m=20cm,
1 1 2 2 2
故A正确,BCD错误。
故选A。
左管内封闭气体温度不变,根据题意求出封闭气体的状态参量,应用玻意耳定律可求出气体末状态
的长度。
本题考查了一定质量理想状态气体方程的应用,根据题意分析清楚气体状态变化过程,求出气体状
态参量,应用玻意耳定律与几何关系即可解题。1.如图所示,内壁光滑的绝热气缸内用绝热活塞封闭一定质量的理想气体,初始时气缸开口向上
放置,活塞处于静止状态,将气缸缓慢转动90❑∘过程中,缸内气体( )
A. 内能增加,外界对气体做正功
B. 内能减小,所有分子热运动速率都减小
C. 温度降低,速率大的分子数占总分子数比例减少
D. 温度升高,速率大的分子数占总分子数比例增加
【答案】C
【解析】
【分析】
根据题意气缸与活塞均为绝热,根据题意分析可知气体体积增大,根据热力学第一定律
△U=Q+W可知气体内能减小,分子平均动能减小,温度降低,速率大的分子数占总分子数的比
例减小。
该题考查一定质量的理想气体在发生相应变化时气体的各状态参数的变化以及热力学第一定律等知
识点,属于常规考点。
【解答】
设大气压强为p ,活塞的质量为m。初始时缸内气体的压强为p ,对活塞受力分析,因为活塞处于
0 1
平衡状态,则有(p -p )s=mg,气缸在缓慢转动的过程中,气缸内外气体对活塞的压力差大于重
1 0
力沿气缸壁的分力,故气缸内气体缓慢的将活塞往外推,最后气缸水平,缸内气压等于大气压。
AB.因为气缸、活塞都是绝热的,故气体与外界没有发生热传递,即Q=0。由于在缓慢转动过程
中,气缸内外气体对活塞的压力差大于重力沿气缸壁的分力,所以活塞向外运动,气体体积增大,
气体对外做功,即W<0,根据热力学第一定律ΔU=Q+W可知:气体内能减小,故缸内理想气体
的温度降低,分子热运动的平均速率减小,但并不是所有分子热运动的速率都减小,AB错误;
CD.因为气体的内能减小,所以缸内气体的温度降低,分子热运动的平均速率减小,即速率大的分
子数占总分子数的比例减小,C正确,D错误。
故选C。
2.一定质量的理想气体从状态a开始,经历ab、bc、ca三个过程回到原状态,其p-T图像如图所
示,下列判断正确的是( )A. 状态a的体积小于状态b的体积 B. 状态b的体积小于状态c的体积
C. 状态a分子的平均动能最大 D. 状态c分子的平均动能最小
【答案】B
【解析】
【分析】
由图示图象判断气体的状态变化过程,应用理想气体的状态方程判断气体体积如何变化;气体分子
平均动能只由温度决定。
本题考查气体的状态方程中对应的图象,要抓住在P-T图象中等容线为过原点的直线,还有要记
住气体分子平均动能只由温度决定。
【解答】
A.由图示可知,ab过程,气体压强与热力学温度成正比,则气体发生等容变化,所以V =V ,故
a b
A错误;
B.由图示图象可知,bc过程气体发生等温变化,气体压强与体积成反比,b的压强大,所以b的体
积小,故B正确;
CD.由图象可知,a、b和c三个状态中,a状态温度最低,分子平均动能最小,则故CD错误。
故选:B。
3.一定质量的理想气体从状态a沿abc过程到状态c,其P-T图象如图,其中ac连线的延长线过原
点O.则在整个过程中气体的内能( )
A. 先增大后不变
B. 先不变后减小
C. 先增大后减小
D. 先减小后增大
【答案】B
【解析】解:由图可知,由a到b为等温变化,温度不变,则内能不变;
由b到c过程中温度降低,内能减小,故B正确,ACD错误。故选:B。
明确图象的性质,根据理想气体状态方程可分析温度的变化,从而确定内能的变化。
本题考查对P-T图象的理解以及对气体内能的理解,要注意明确理想气体分子势能忽略不计,温
度是分子平均动能的标志,根据温度变化即可确定内能的变化。
4.一定质量的理想气体从状态a开始,经a→b、b→c、c→a三个过程后回到初始状态a,其
p-V图像如图所示。已知三个状态的坐标分别为a(V ,2p )、b(2V ,p )、c(3V ,2p )。以下
0 0 0 0 0 0
判断正确的是( )
A. 气体在a→b过程中对外界做的功小于在b→c过程中对外界做的功
B. 气体在a→b过程中从外界吸收的热量大于在b→c过程中从外界吸收的热量
C. 在c→a过程中,外界对气体做的功小于气体向外界放出的热量
D. 气体在c→a过程中内能的减少量大于b→c过程中内能的增加量
【答案】C
【解析】
【分析】本题考查气体的状态方程中对应的图象,分析清楚图示图象、知道理想气体内能由气体的
温度决定即可解题,解题时要抓住p-V图象的面积表示气体做功。
【解答】
A、根据 p-V图象的面积表示气体做功,得气体在 a→b过程中对外界做的功为:
p +2p 3
W = 0 0 ⋅(2V -V )= p V , b→c过 程 中 气 体 对 外 界 做 的 功 为 :
ab 2 0 0 2 0 0
p +2p 3
W = 0 0 ⋅(3V -2V )= p V ,所以气体在a→b过程中对外界做的功等于在b→c过程
bc 2 0 0 2 0 0
中对外界做的功故A错误;
B、气体在a→b过程中,因为a、b两个状态的pV相等,所以T =T ,即△U =0,根据热力学第
a b ab
3
一定律△U=Q+W可知,从外界吸收的热量为Q = p V ;气体在b→c过程中,因为c状态的
ab 2 0 0
pV大于b状态的pV,所以T T =T ;由此可知,AC选项错误;
b a c
D.对于一定质量的理想气体,当气体的体积增大时,气体对外做功,即外界对气体做负功W<0;
当气体的体积缩小时,外界对气体做正功W>0,由此可知当气体由a→b、a→c过程中,气体的
体积都在增大,也就是外界对气体做负功,故D错误;
B.对于一定质量的理想气体其内能只与温度有关,温度越高内能越大再结合热力学第一定律ΔU =
W + Q可知,当气体由a→b的过程中,气体的内能增加,即ΔU >0,而根据上面的分析知W<0,
故必有Q>0,也就是说在a→b过程中,气体要从外界吸热,故B正确。
2.如图,两端封闭的直玻璃管竖直放置,一段水银将管内气体分隔为上下两部分,已知上部分气
体压强等于大气压强。若水银柱所在玻璃管处开一个小孔,则( )A. 上端水银面上升,下端水银面上升
B. 上端水银面上升,下端水银面下降
C. 上端水银面下降,下端水银面上升
D. 上端水银面下降,下端水银面下降
【答案】C
【解析】解:分析题意可知,初态时,上部分气体压强等于大气压强,下部分气体压强等于大气压
强与水银柱产生的压强之和,
当水银柱所在玻璃管处开一个小孔,则此位置的压强等于大气压强,上部分气体会推动水银柱向外
溢出,设上部分气体压强与开口上方水银柱产生的压强之和等于大气压强,则上端水银面下降;
下部分气体也会推动水银柱向外溢出,使大气压强与开口下方水银柱产生的压强之和等于下部分气
体的压强,则下端水银面上升,故C正确,ABD错误。
故选:C。
1
3.如图所示为一定质量气体状态变化时的p- 图象,由图象可知,此气体的温度( )
V
A. 先不变后升高
B. 先不变后降低
C. 先降低后不变
D. 先升高后不变
【答案】D
pV C
【解析】解:根据 =C可得:p= T
T V
则第一阶段为等容变化,体积不变,温度随着压强p增大而升高;
第二阶段等温变化,压强变大,体积减小,
所以气体的温度先升高后不变,故D正确、ABC错误。
故选:D。
逐步分析各状态的状态参量的变化,利用理想状态方程定性分析即可得知气体温度的变化。
该题考查了理想气体状态方程的应用,解答此类问题要注意会对图象的观察和分析,并还能知道p-V、V -T、以及p-T图的特点。会用理想气体状态方程进行定性的分析和定量的计算。
4.一定质量的理想气体从状态a变化到状态b,其体积V和热力学温度T变化图像如图所示,此过
程中该系统( )
A. 对外界做正功 B. 压强保持不变 C. 向外界放热 D. 内能减少
【答案】A
【解析】
【分析】
根据一定质量的理想气体的状态方程pV =CT分析出气体压强的变化,结合热力学第一定律完成分
析。
本题主要考查了一定质量的理想气体的状态方程,结合公式pV =CT以及图像分析出压强的变化,
同时利用热力学第一定律即可完成解答。
【解答】
A.理想气体从状态a变化到状态b,体积增大,理想气体对外界做正功,A正确;
B.由题图可知V =V + kT
0
pV
根据理想气体的状态方程有 =C
T
C
p=
联立有 V
k+ 0
T
可看出T增大,p增大,B错误;
D.理想气体从状态a变化到状态b,温度升高,内能增大,D错误;
C.理想气体从状态a变化到状态b,由选项AD可知,理想气体对外界做正功且内能增大,则根据热
力学第一定律可知气体向外界吸收热量,C错误。
故选A。
5.如图,容积均为V的汽缸A、B下端有细管(容积可忽略)连通,阀门K 位于细管的中部,A、B
2
的顶部各有一阀门K 、K ,B中有一可自由滑动的活塞(质量、体积均可忽略)。初始时,三个阀门
1 3
均打开,活塞在B的底部;关闭K 、K ,通过K 给汽缸充气,使A中气体的压强达到大气压p 的3
2 3 1 0
倍后关闭K 。已知室温为27℃,汽缸导热。
1(1)打开K ,求稳定时活塞上方气体的体积和压强。
2
(2)接着打开K ,求稳定时活塞的位置。
3
(3)再缓慢加热汽缸内气体使其温度升高20℃,求此时活塞下方气体的压强。
【答案】
解:(i)打开K 之前, A缸内气体 p =3p ,B缸内气体 p =p ,体积均为V,温度均为
2 A 0 B 0
T=(273+27)K=300K,打开K 后,B缸内气体(活塞上方)等温压缩,设压缩后体积为V ,A缸
2 1
内气体(活塞下方)等温膨胀,膨胀后体积为2V -V ,活塞上下方压强相等均为p ,
1 1
则:对A缸内(活塞下方)气体:3p V =p (2V -V ),
0 1 1
对B缸内(活塞上方)气体:p V =p V ,
0 1 1
1
联立以上两式得:p =2p ,V = V;
1 0 1 2
1
即稳定时活塞上方体积为 V,压强为2p ;
2 0
(ⅱ)打开K ,活塞上方与大气相连通,压强变为p ,则活塞下方气体等温膨胀,假设活塞下方气体
3 0
压强可降为p ,则降为p 时活塞下方气体体积为V ,则3p V =p V ,
0 0 2 0 0 2
得V =3V >2V,即活塞下方气体压强不会降至p ,此时活塞将处于B气缸顶端,缸内气压为p ,
2 0 2
3
3p V =p ×2V,得p = p ,即稳定时活塞位于气缸最顶端;
0 2 2 2 0
(ⅲ)缓慢加热汽缸内气体使其温度升高,等容升温过程,升温后温度为T =(300+20)K=320K,
3
p p
由 2= 3 得:p =1.6p ,即此时活塞下方压强为1.6p 。
T T 3 0 0
3
1
答:(i)打开K ,稳定时活塞上方气体的体积为 V,压强为2p ;
2 2 0
(ii)打开K ,稳定时位于气缸最顶端;
3
(iii)缓慢加热汽缸内气体使其温度升高20℃,此时活塞下方气体的压强为1.6p 。
0
【解析】(i)分析打开K 之前和打开K 后,A、B缸内气体的压强、体积和温度,根据玻意尔定律
2 2
列方程求解;(ⅱ)打开K ,分析活塞下方气体压强会不会降至p ,确定活塞所处位置;
3 0
p p
(ⅲ)缓慢加热汽缸内气体使其温度升高,等容升温过程,由
2= 3
求解此时活塞下方气体的压强。
T T
3
本题主要是考查了理想气体的状态变化;解答此类问题的方法是:找出不同状态下的三个状态参量,
分析理想气体发生的是何种变化,利用相应的气体实验定律列方程求解;本题要能用静力学观点分
析各处压强的关系,要注意研究过程中哪些量不变,哪些量变化,选择合适的气体实验定律解决问
题。
6.如图,两侧粗细均匀、横截面积相等、高度均为H=18cm的U型管,左管上端封闭,右管上端
开口。右管中有高h =4cm的水银柱,水银柱上表面离管口的距离l=12cm。管底水平段的体积可
0
忽略。环境温度为T =283K,大气压强p =76cmHg。
1 0
(i)现从右侧端口缓慢注入水银(与原水银柱之间无气隙),恰好使水银柱下端到达右管底部。此时水
银柱的高度为多少?
(ii)再将左管中密封气体缓慢加热,使水银柱上表面恰与右管口平齐,此时密封气体的温度为多少?
【答案】
解:(i)设左、右管的截面积为S。
密封气体初始体积为V =(2H-l-h )S=20S,压强为p =76cmHg+4cmHg=80cmHg
1 0 1
经等温压缩过程,密闭气体体积变为V =HS=18S,压强变为p ,
2 2
由玻意耳定律有:p V =p V ,
1 1 2 2
解得:p =88.89cmHg,
2
此时水银柱的高度为:h=88.89cm-76cm=12.89cm;
(ii)密封气体再经等压膨胀过程体积变为V =(2H-h)S,温度变为T ,由盖吕萨克定律有:
3 3
V V
2= 3
,
T T
1 3
代入数据解得:T =363K。
3【解析】(i)求出密封气体初始体积和压强,将密封气体等温压缩,由玻意耳定律列方程求解压强,
再求出此时水银柱的高度h;
(ii)密封气体再经等压膨胀过程体积变为V =(2H-h)S,由盖吕萨克定律求解温度。
3
本题主要是考查了理想气体的状态方程;解答此类问题的方法是:找出不同状态下的三个状态参量,
分析理想气体发生的是何种变化,利用理想气体的状态方程列方程求解。