文档内容
查补易混易错 03 化学用语的判断
化学用语是专门的化学语言,其包含的内容可分为两个大的方面:一是表示化学物质组成、结构的化学用
语,包括元素符号、离子符号、电子式、结构式、结构示意图等;二是表示物质变化的化学用语,如化学
方程式、热化学方程式、离子方程式、电极方程式等。化学用语类试题比较基础,在复习备考中除了需要
注意相关的解题技巧外,还需要对相关知识有比较深入的认识,将知识准确、合理的应用,将相关知识总
结归纳,着重关注易错点,并通过练习加强理解掌握,这样才能通过复习切实提高得分率。
易错01常考化学用语
结构示意图
S2-: Al3+:
电子排布式 S:1s22s22p63s23p4
价电子排布式 S:3s23p4
简化电子排布式 S:[Ne]3s23p4
电子排布图(或轨
道表示式)
S:
电子式 NaO:Na+[OO]2-Na+ HO:HOH
2 2 2
球棍模型
甲烷: 乙烯:
比例模型
甲烷: 乙烯:
结构式 CO:O=C=O HClO:H-O-Cl
2
结构简式 乙烯:CH=CH 乙酸:CHCOOH
2 2 3
分子式 臭氧:O
3
化学式 明矾:KAl(SO )·12H O
4 2 2最简式 烯烃和环烷烃:CH
2
易错02电子式的书写
1.原子的电子式:将原子的所有最外层电子数在元素符号的周围标出,例如:氢原子( )、钠原子( )、
镁原子( )、铝原子( )、碳原子( )、氮原子( )、硫原子( )、氩原子( )。
2.离子的电子式:
(1)阴离子:在书写阴离子的电子式时,须在阴离子符号的周围标出其最外层的 8个电子(H-为2个电子),
外加方括号,再在括号外的右上角注明阴离子所带的电荷数,例如 S2-的电子式为[ ]2- ,OH-的电
子式为 。
(2)阳离子:对于简单阳离子,其电子式即为阳离子符号,如钠离子 Na+、镁离子Mg2+等,对于带正电
荷的原子团,书写方法与阴离子类似,区别在于在方括号右上角标上阳离子所带的正电荷数,如 NH +电
4
子式为 。
3.离子化合物的电子式:离子化合物电子式的书写,是将阴阳离子(阳离子在前,阴离子在后)拼在一起,对
于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写,如CaCl 的电子式应
2
为 。
4.共价型单质分子:必须正确地表示出共用电子对数,并满足每个原子的稳定结构,例如:
。
5.共价化合物:共价化合物电子式的书写,基本与共价型单质分子相同,一般为正价者在前。对于不同价
态的元素的原子,一般将化合价绝对值大的写在中间,绝对值小的写在周边,例如:
。
易错03化学用语常见错误
(1)结构简式需保留官能团,如CH===CH ,不能写成CHCH ,还要注意有机物中原子的连接情况,如
2 2 2 2—NO ,不能写成—ON。
2 2
(2)各“式”切勿张冠李戴:名称还是化学式、分子式还是实验式、结构式还是结构简式、原子还是离
子结构示意图、化学方程式还是离子方程式等。
(3)化学方程式或离子方程式要遵守质量守恒,化学计量数要最简,注明反应条件并注意“↑”“↓”
“”“===”“―→”符号的使用。
(4)化学专用名词书写错误。如“铵盐”写成“氨盐”,“油脂”写成“油酯”,“酯化”写成“脂
化”,“苯”写成“笨”,“硝化”写成“消化”等。
(5)电子式书写错误:书写化合物的电子式时要切实注意明确离子化合物还是共价化合物;切勿漏掉未
成键电子对;理清原子的排列顺序,如HOCl。
(6)混淆物质组成的几种表达方法:任何纯净物均有化学式,只有由分子组成的物质才有分子式,SiO、
2
NaCl属化学式,P、C H 是分子式;球棍模型表示有机分子中各原子之间的键的情况和相对空间位置;比
4 2 4
例模型表示分子中各原子的大小比例和相对位置,两种模型若原子大小比例不同,表示的物质不同,例如
CH 和 CCl 等;结构简式需保留官能团,如CH==CH ,不能写成CHCH ,还要注意有机物中原子的连
4 4 2 2 2 2
接情况,如ON—,不能写成NO —;各“式”切勿张冠李戴,名称还是化学式,分子式还是实验式,结
2 2
构式还是结构简式,原子还是离子结构示意图,化学方程式还是离子方程式等。
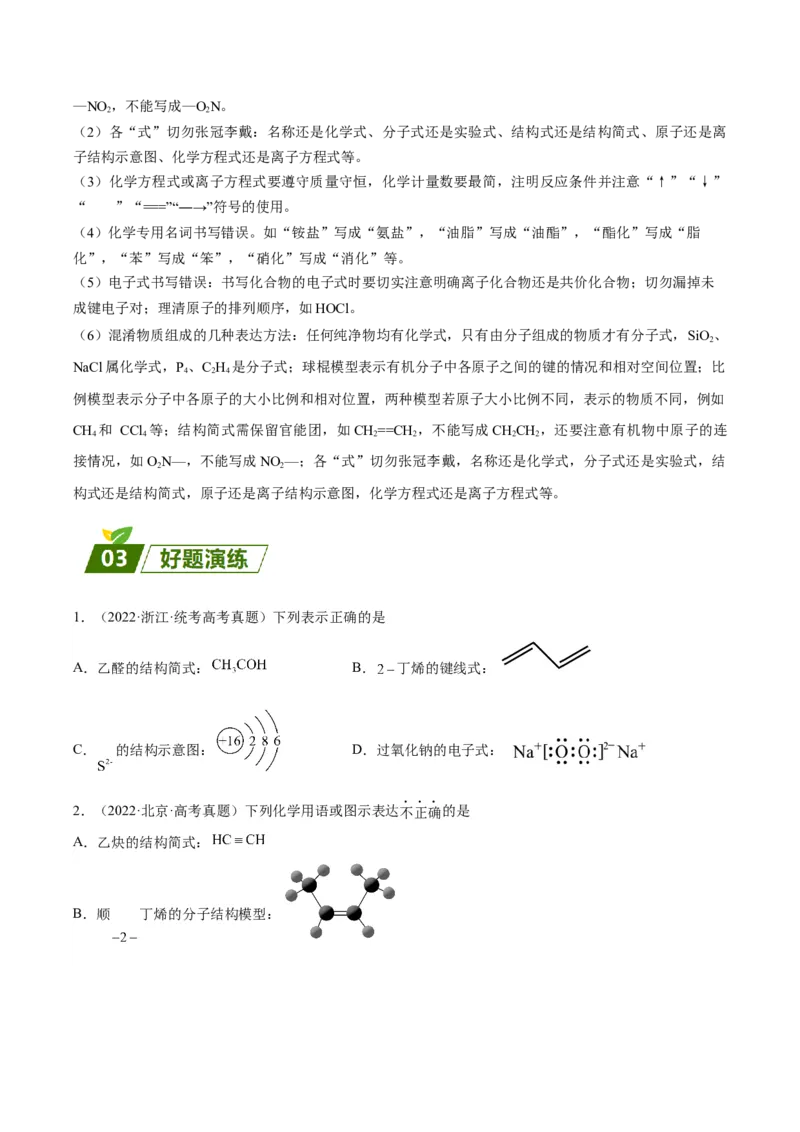
1.(2022·浙江·统考高考真题)下列表示正确的是
A.乙醛的结构简式: B. 丁烯的键线式:
C. 的结构示意图: D.过氧化钠的电子式:
2.(2022·北京·高考真题)下列化学用语或图示表达不正确的是
A.乙炔的结构简式:
B.顺 丁烯的分子结构模型:C.基态 原子的价层电子的轨道表示式:
D. 的电子式:
3.(2022·浙江·统考高考真题)下列表示不正确的是
A.乙炔的结构简式HC≡CH B.KOH的电子式
C.乙烷的球棍模型: D.氯离子的结构示意图:
4.(2022·江苏·高考真题)少量 与 反应生成 和 。下列说法正确的是
A. 的电子式为 B. 的空间构型为直线形
C. 中O元素的化合价为-1 D. 仅含离子键
5.(2022·辽宁·统考高考真题)下列符号表征或说法正确的是
A. 电离: B. 位于元素周期表p区
C. 空间结构:平面三角形 D. 电子式:
6.(2022·重庆·统考高考真题)BCl 水解反应方程式为:BCl +3H O=B(OH) +3HCl,下列说法错误的是
3 3 2 3
A.Cl的原子结构示意图为 B.HO的空间填充模型为
2
C.BCl 的电子式为: D.B(OH) 的结构简式为
3 3
7.(2023·河北·模拟预测)下列化学用语表示正确的是
A.HClO的电子式: B.基态 的价电子轨道表示式:C. 分子的VSEPR模型: D.反-1,4-聚异戊二烯的结构简式:
8.(2023春·重庆沙坪坝·高三重庆一中校考阶段练习)下列有关化学用语的表示错误的是
A.食盐水中存在水合钠离子,其示意图为
B.醛基具有较强的极性,其中碳氧双键中的电荷分布示意图为
C.共价化合物 中所有原子均满足8电子稳定结构,其结构式为
D.硼氢化钠(NaBH )是有机合成中的重要还原剂,其电子式为
4
9.(2023·辽宁沈阳·统考二模)下列化学用语表达中正确的是
A. 用系统命名法命名为:2—甲基丁酸
B.空间填充模型 既可以表示甲烷分子,也可以表示四氯化碳分子
C. 分子中,碳原子与氧原子之间形成的共价键类型为 键
D.基态氧原子核外电子轨道表示式:
10.(2023·上海青浦·统考二模)下列有关化学用语的表述正确的是
A.乙烯的结构简式:CHCH B.乙酸的分子式:CHCOOH
2 2 3
C.铝离子的结构示意图: D.OH—的电子式:11.(2023·浙江嘉兴·统考二模)下列化学用语表示正确的是
A.中子数为16的磷原子:
B.羟基的电子式:
C. 的VSEPR模型: (平面三角形)
D.基态 最高能级的电子云轮廓图:
12.(2023·北京·高三统考专题练习)下列化学用语或图示表达不正确的是
A.氯化钙的电子式:
B.基态C原子的轨道表示式:
C.顺-2-丁烯的分子结构模型:
D.Cl-Cl的p-pσ键电子云图形:
13.(2023·上海金山·统考二模)反应2NH +NaClO=N H+NaCl+HO可用于制备火箭推进剂的燃料
3 2 4 2
NH。下列有关说法正确的是
2 4
A.NH 的结构式: B.中子数为8的氮原子:15N
2 4
C.O原子的最外层电子排布式:2s22p6 D.NaClO的电子式:
14.(2023·浙江·二模)下列化学用语正确的是
A.镁原子最外层电子云轮廓图:B.乙醛空间填充模型:
C.反式聚异戊二烯结构简式:
D.基态铬原子的价层电子排布式:
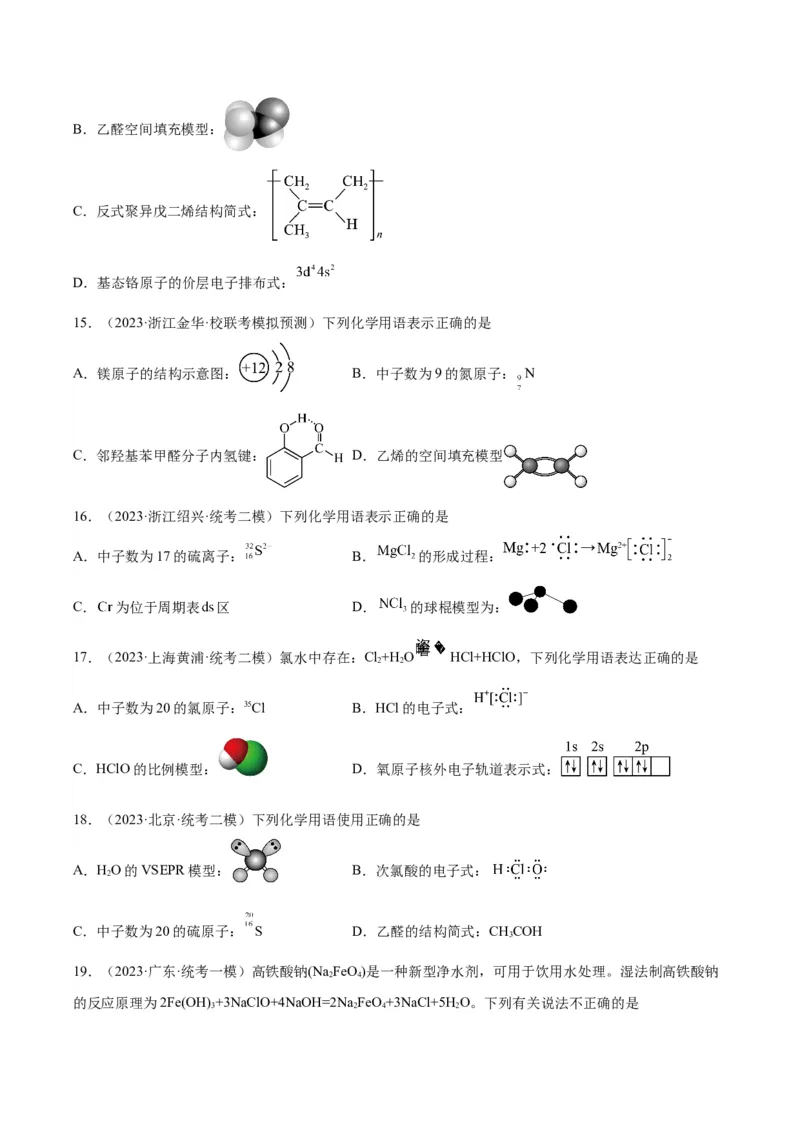
15.(2023·浙江金华·校联考模拟预测)下列化学用语表示正确的是
A.镁原子的结构示意图: B.中子数为9的氮原子: N
C.邻羟基苯甲醛分子内氢键: D.乙烯的空间填充模型
16.(2023·浙江绍兴·统考二模)下列化学用语表示正确的是
A.中子数为17的硫离子: B. 的形成过程:
C. 为位于周期表 区 D. 的球棍模型为:
17.(2023·上海黄浦·统考二模)氯水中存在:Cl+H O HCl+HClO,下列化学用语表达正确的是
2 2
A.中子数为20的氯原子:35Cl B.HCl的电子式:
C.HClO的比例模型: D.氧原子核外电子轨道表示式:
18.(2023·北京·统考二模)下列化学用语使用正确的是
A.HO的VSEPR模型: B.次氯酸的电子式:
2
C.中子数为20的硫原子: S D.乙醛的结构简式:CHCOH
3
19.(2023·广东·统考一模)高铁酸钠(Na FeO)是一种新型净水剂,可用于饮用水处理。湿法制高铁酸钠
2 4
的反应原理为2Fe(OH) +3NaClO+4NaOH=2Na FeO+3NaCl+5HO。下列有关说法不正确的是
3 2 4 2A.HO的球棍模型为 B.基态Fe3+的简化电子排布式为[Ar]3d34s2
2
C.NaClO的电子式为 D.37Cl原子结构示意图为
20.(2023春·重庆沙坪坝·高三重庆南开中学校考阶段练习)下列表示正确的是
A.乙烯的电子式:
B. 的空间充填模型:
C.果糖的结构简式:
D. 的价电子排布式:
21.(2023·重庆渝中·高三重庆巴蜀中学校考阶段练习)已知 。下
列化学用语错误的是
A.基态硫原子的价层电子排布图:
B. 的结构式:
C. 的电子式:
D. 的比例模型:
22.(2023春·辽宁·高三校联考阶段练习)下列有关化学用语表达正确的是
A. 和 的结构示意图均可以表示为B.基态Cu原子的价电子排布式为
C.2,2-二甲基庚烷的键线式为
D. 的空间结构为三角锥形
23.(2023·重庆·重庆八中校联考模拟预测)下列化学用语表示正确的是
A.三氯化氮的电子式: B.镁原子最外层电子的电子云图:
C.溴乙烷的空间填充模型: D.乙酸甲酯的结构简式:
24.(2023·天津南开·统考一模)下列有关化学用语表示正确的是
A.乙醚的结构简式:
B.HClO的电子式:
C.质子数为17、中子数为20的氯原子:
D. 的空间结构:V形
25.(2023·上海宝山·统考一模)科学素养包括规范使用化学用语。下列化学用语表达正确的是
A.氟化氢的电子式: B.甲烷分子的球棍模型:
C.硫离子的最外层电子排布式: D.丙烯的结构简式:
参考答案
1.D【详解】A.乙醛含醛基,其结构简式为:CHCHO,A错误;
3
B.2-丁烯的结构简式为CHCH=CHCH ,键线式为: ,B错误;
3 3
C.硫的原子序数为16,硫原子最外层有6个电子,得2个电子形成硫离子,硫离子的结构示意图为:,C错误;
D.过氧化钠为离子化合物,含离子键和氧氧非极性共价键,其电子式为: ,D正
确;
答案选D。
2.C【详解】A.乙炔中含有碳碳三键,其结构简式为 ,A项正确;
B.顺 丁烯中两个甲基位于双键同侧,其结构模型为 ,B项正确;
C.基态 原子的价层电子排布式为3s23p2,其轨道表示式为 ,C项错误;
D. 是离子化合物,其电子式为 ,D项正确;
答案选C。
3.C【详解】A.乙炔中碳碳之间为三键,故结构简式HC≡CH,选项A正确;
B.KOH为离子化合物,故电子式为 ,选项B正确;
C. 为乙烷的比例模型,不是球棍模型,选项C错误;
D.氯离子的核电荷数是17,电子数为18,氯离子的结构示意图为 ,选项D正确;
故答案是C。
4.C【详解】A.过氧化钠是离子化合物,电子式是 ,A错误;
B. 中氧原子的成键电子对是2,孤电子对是2,根据价层电子对为4,根据价层电子对互斥理论,其
空间构型为V形,B错误;C. 中H显+1价,根据正负化合价为0,可计算出O的化合价为-1,C正确;
D. 中O和H之间是共价键,D错误;
故选C。
5.C【详解】A. 是二元弱酸,电离分步进行,其一级电离方程式为 ,A错误;
B.基态 原子的价电子排布式是 ,最后一个电子填充在s能级,位于元素周期表s区,B错误;
C. 中心碳原子的价层电子对数为 ,故其空间结构为平面三角形,C正确;
D. 是离子化合物,电子式为 ,D错误;
故答案选C。
6.C【详解】A.Cl为荷电核数为17,原子结构示意图为 ,A项正确;
B. 分子为V形结构,且O原子的半径比H原子的半径大,B项正确;
C. 是缺电子化合物,B提供3个电子,与3个Cl分别共用1对电子,电子式应为 ,C项
错误;
D. 的结构简式为 ,D项正确;
答案选C。
7.B【详解】A.HClO的电子式为 ,选项A错误;
B.基态 的价电子数为10,价电子轨道表示式为 ,选项B正确;
C. 分子的中心O原子上孤电子对数为2,选项C错误;D.反-1,4-聚异戊二烯的结构简式为 [点拨:相同的原子或原子团位于双键两
侧的为反式结构],选项D错误;
答案选B。
8.A【详解】A.氧元素的电负性大于氢元素,水分子中共用电子对偏向氧原子一方,氧原子带负电荷、
氢原子带正电荷,则水合钠离子中钠离子带正电,应与氧原子一侧结合,故A错误;
B.氧元素的电负性大于碳元素,醛基中碳氧双键中共用电子对偏向氧原子一方,氧原子带负电荷、碳原
子带正电荷,故B正确;
C.由双聚氯化铝分子中所有原子均满足8电子稳定结构可知,分子中具有空轨道的铝离子与具有孤对电
子的氯离子形成配位键,结构式为 ,故C正确;
D.硼氢化钠是含有离子键和共价键的离子化合物,电子式为 ,故D正确;
故选A。
9.D【详解】A.由结构简式可知,该有机物属于羧酸,含有羧基的最长碳链的碳原子个数为4、侧链为
甲基,名称为3—甲基丁酸,故A错误;
B.碳原子的原子半径大于氢原子,而小于氯原子,所以空间填充模型 不能表示四氯化碳分子,
故B错误;
C.甲醇分子中碳原子和氧原子的杂化方式都为sp3杂化,则碳原子与氧原子之间形成的共价键类型为sp3
—sp3σ键,故C错误;
D.氧元素的原子序数为8,电子排布式为1s22s22p4,电子轨道表示式为 ,
故D正确;
故选D。
10.D【详解】A.乙烯的分子式为C H,结构简式为CH=CH ,故A错误;
2 4 2 2B.乙酸的结构简式为CHCOOH,分子式为C HO,故B错误;
3 2 4 2
C.铝离子的核电荷数为13,核外2个电子层,最外层电子数为8,离子的结构示意图 ,故C
错误;
D.氢氧根离子是带1个单位负电荷的阴离子,电子式为 ,故D正确;
故选D。
11.C【详解】A.中子数为16的磷原子的质量数为15+16=31,核素符号为子 ,故A错误;
B.羟基的电子式为 ,故B错误;
C. 中心原子价层电子对数为2+ =3,VSEPR模型为平面三角形,故C正确;
D.基态 的价层电子排布式为3d6,最高能级为3d,电子云轮廓图是花瓣形,故D错误;
故选C。
12.B【详解】A.氯化钙的电子式为 ,A正确;
B.基态C原子的轨道表示式为 ,B错误;
C.顺-2-丁烯的分子结构模型为 ,C正确;
D.p-pσ键的原子轨道头碰头方式重叠,则Cl-Cl的p-pσ键电子云图形为 ,D正确;
故选B。
13.B【详解】A.NH 中每个氮和氢形成单键,氮氮之间为单键,其结构式: ,故A
2 4
错误;
B.中子数为8的氮原子,其质量数为15,其原子符号为:15N,故B正确;
C.O原子的最外层电子排布式:2s22p4,故C错误;D.NaClO是离子化合物,其电子式: ,故D错误。
综上所述,答案为B。
14.B【详解】A.镁原子价电子排布为3s2,最外层电子云轮廓图为球形,A错误;
B.乙醛结构简式为CHCHO,空间填充模型: ,B正确;
3
C.反式聚异戊二烯结构简式: ,C错误;
D.基态铬原子的价层电子排布式: ,D错误;
故选B。
15.C【详解】A.镁是12号元素,其结构示意图为 ,A错误;
B.中子数为9的氮原子可表示为: N,B错误;
C. 邻羟基苯甲醛分子内氢键可表示为: ,C正确;
D.乙烯的空间填充模型为 ,D错误;
故选C。
16.D【详解】A.中子数为17的硫离子: ,A错误;
B. 的形成过程: ,B错误;
C. 是24号元素,位于周期表 区,C错误;
D.Cl原子半径大于N原子,则 的球棍模型为: ,D正确;
故选D。
17.C【详解】A.中子数为20的氯原子为37Cl,A错误;B.HCl为共价化合物,电子式为 ,B错误;
C.HClO中O原子在中间,氢原子半径最小,O原子次之,氯原子半径最大,HClO的空间构型为V形,
C正确;
D.氧原子核外电子轨道表示式为 ,D错误;
故答案选C。
18.A【详解】A.水分子中氧原子以sp3杂化,故其VSEPR模型为四面体形 ,A正确;
B.次氯酸分子中氧原子分别和氢原子氯原子形成共价键,故电子式为 ,B错误;
C.中子数为20的硫原子: ,C错误;
D.乙醛的结构简式:CHCHO,D错误;
3
故选A。
19.B【详解】A.HO是角形分子,球棍模型为 ,A正确;
2
B.铁原子失去3个电子形成铁离子,基态Fe3+的简化电子排布式为[Ar]3d5,B错误;
C.NaClO是由次氯酸根离子和钠离子构成的离子化合物,电子式为 ,C正确;
D.氯为17号元素,原子结构示意图为 ,D正确;
故选B。
20.A【详解】A.乙烯分子中含有碳碳双键,电子式为 ,故A正确;
B.氯原子半径大于C原子, 不能表示 的空间充填模型,故B错误;
C.果糖的结构简式为CHOH(CHOH) COCH OH, 是葡萄糖的结构简式,故C错误;
2 3 2
D. 的电子排布式为 ,价电子排布式为3d6,故D错误;选A。
21.D【详解】A.基态硫原子的价层电子排布式为3s23p4,则价层电子排布图: ,故A
正确;
B. 有两个非羟基氧,两个羟基,其结构式: ,故B正确;
C. 是每个氧与碳形成两对共用电子对,其电子式: ,故C正确;
D. 中氧原子半径小于硫原子半径,因此 不是 的比例模型,故D错误。
综上所述,答案为D。
22.D【详解】A.题中给出的是氯离子结构示意图,A项错误;
B.基态Cu原子的价电子排布式是 ,B项错误;
C.题中所给键线式的名称应该是2,2—二甲基戊烷,C项错误。
D.NH 中含有4对加层电子,1对孤电子,故其为三角锥形,D项正确;
3
故选D。
23.C【详解】A.NCl 中氮原子最外层有5个电子,和三个氯原子共用三对电子后,还有一孤电子对,故
3
A错误;
B.镁原子最外层电子是3s电子,s电子云图是球形,故B错误;
C.溴乙烷的结构简式为CHCHBr,空间填充模型为 ,故C正确;
3 2
D.乙酸甲酯的结构简式为CHCOOCH ,故D错误;
3 3
故选C。
24.D【详解】A.乙醚的结构简式: ,故A错误;
B.HClO的电子式: ,故B错误;C.质子数为17、中子数为20的氯原子质量数为37,表示为 ,故C错误;
D. 的价电子对数 ,有一对孤对电子,空间构型为V形,故D正确;
故选:D。
25.C【详解】A.氟化氢为共价化合物,电子式为 ,故A错误;
B.甲烷分子的空间构型为正四面体形,球棍模型为 ,故B错误;
C.硫元素的原子序数为16,基态硫离子的最外层电子排布式为3s23p6,故C正确;
D.丙烯的分子式为C H,结构简式为CHCH=CH,故D错误;
3 6 3 2
故选C。