文档内容
姓名: 班级: 成绩:
基础过关检测(50分)
(每小题10分,共50分)
1.【2015年山东省东营市】 在实验室中,化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH) 粉末状试剂。
2
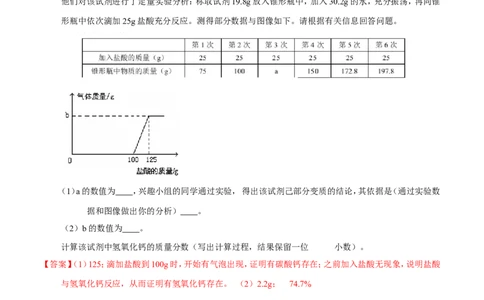
他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥
形瓶中依次滴加25g盐酸充分反应。测得部分数据与图像如下。请根据有关信息回答问题。
(1)a的数值为 ,兴趣小组的同学通过实验, 得出该试剂己部分变质的结论,其依据是(通过实验数
据和图像做出你的分析) 。
(2)b的数值为 。
计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位 小数)。
【答案】(1)125;滴加盐酸到100g时,开始有气泡出现,证明有碳酸钙存在;之前加入盐酸无现象,说明盐酸
与氢氧化钙反应,从而证明有氢氧化钙存在。 (2)2.2g; 74.7%
1故试剂中氢氧化钙的质量为:19.8g-5g=14.8g
氢氧化钙的质量分数为:14.8g/19.8g×100%=74.7%
答:试剂中氢氧化钙的质量分数为74.7% 学科&网
2.【2015年内蒙古自治区赤峰市】某校兴趣小组在实验室做制取氧气的实验,他们取氯酸钾和二氧化锰的混
合物6.0g放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量如下表
反应时间/min 1.0 1.5 2.0 2.5 3.0 3.5
剩余固体质量/g 5.1 4.5 4.2 4.08 4.08 4.08
分析表中数据,完成下列问题(: 1)氯酸钾中钾、氯、氧三种元素的质量比为 (最简整数比)
(2)生成氧气的质量为 g。(3)原混合物中二氧化锰的质量分数是多少?(写出计算过程,计算结果
精确到0.1%)
【答案】(1) 78:71:96;(2)1.92;(3)1.1%
23.【2015年江苏省盐城市】实验室中有一瓶长期使用的氢氧化钠固体样品,某兴趣小组的同学对该样品的成
分及含量进行探究.
【发现问题】该样品中含有哪些物质?
【查阅资料】①NaOH在空气中不会转化成NaHCO .
3
②BaCl 溶液呈中性,Ba(OH) 是可溶性碱
2 2
③CO 在饱和的NaHCO 溶液中几乎不溶解
2 3
【提出猜想】猜想Ⅰ:NaOH 猜想Ⅱ:Na CO 猜想Ⅲ:NaOH和Na CO
2 3 2 3
【设计实验】
实验操作 实验现象
步骤①:样品全部溶解
步骤②:观察到现象A
【收集证据】(1)若现象A是有气泡产生,则X溶液为 ,则 (填“猜想Ⅰ”、“猜想
Ⅱ”或“猜想Ⅲ”)不成立.
3(2)若X溶液为BaCl 溶液,现象A是有白色沉淀生成,则产生沉淀的化学方程式是 ,取反
2
应后的上层清液,测定其PH,当PH 7(填“>”、“<”或“=”),则证明猜想Ⅲ成立.
【定量分析】确定部分变质样品中Na CO 的质量分数.
2 3
兴趣小组的同学用如图所示装置进行实验.
步骤如下:①按图连接好装置,并检查气密性;②准确称取该样品1.0g,放入烧瓶内;③打开活塞,滴加30.0%
的稀硫酸至过量,关闭活塞;④反应结束后,量筒内液体的读数为55.0mL.(已知:室温条件下,CO 的密度为
2
1.6g•L﹣1)
(1)B装置集气瓶内原有的空气对实验结果 (填“有”或“没有”)影响.饱和NaHCO 溶
3
液如果用水代替,则所测CO 体积 (填“偏大”、“偏小”或“不变”).
2
(2)计算该样品中Na CO 的质量分数(写出计算过程,计算结果保留一位小数)
2 3
【实验反思】有同学指出,上述三种猜想并不全面,请再提出一种猜想 .
【答案】【收集证据】(1)稀盐酸或稀硫酸 猜想1 (2)NaCO+BaCl ==BaCO↓+2NaCl 大于
2 3 2 3
【定量分析】(1)没有 偏小 (2)21.2% 学科*网
【实验反思】碳酸钠、氢氧化钠、水 或 氢氧化钠、水 或碳酸钠、水
44.【2015年江苏省泰州市】镁是一种活泼性较强的金属,在空气中易发生缓慢氧化,表面呈灰黑色。
(1)镁与氧气的反应属于 (填基本反应类型)。要观察金属镁的颜色,需将镁条如何处理
。
(2)若30g镁条存放一段时间后,质量变为了34g,则参加反应的氧气为 g(假设镁只与氧气反应)。
若将上述氧化前和氧化后的镁条分别与足量稀硫酸反应,生成硫酸镁的质量关系是前者 后
者(填“>”、“=”或“<”)。
(3)将2.4g未氧化的镁加入到97.8g的稀硫酸中,恰好完全反应。求反应后所得溶液的溶质质量分数
(假设反应过程中水分未损失)。
【答案】(1)化合反应,用砂纸打磨的光亮 (2) 4克;= (3) 12%
55.【2015年江苏省连云港市】(14分)连云港碱厂年产纯碱120万吨,是我国三大纯碱生产企业之一。它的产
品除了纯碱外,还有氯化钙和碳酸氢钠。该厂生产纯碱的工艺流程可简单表示如下:
NH CO
3 2
精制
食盐水 氨化 碳化 过滤 煅烧 纯碱
NH 4 Cl CO 2 和H 2 O
其生产过程中涉及的主要化学反应有:
①NaCl + NH + CO + H O = NH Cl + NaHCO ↓
3 2 2 4 3
②2NaHCO = Na CO+ CO↑+ H O
3 2 3 2 2
请回答:
(1)①“碳化”过程中需要的CO,可由石灰石高温煅烧得到,该反应的化学方程式为 ▲ 。
2
②实验室中,通常用稀盐酸与石灰石反应制取CO 气体,不选用浓盐酸的理由是 ▲ ;干燥CO 气
2 2
体,可用的干燥剂是 ▲ (填字母)。
A.浓硫酸 B.固体氢氧化钠 C.生石灰
(2)①该厂“过滤”所得的NH Cl可作化肥中的 ▲ 肥,它也可与Ca(OH) 在加热时发生反应生成产品
4 2
CaCl ,同时还有NH 和HO生成,写出该反应的化学方程式: ▲ 。学科&网
2 3 2
该厂的另一种产品碳酸氢钠俗称 ▲ ,它的重要用途有 ▲ (只写一种)。
②实验室进行“过滤”操作时,下列说法正确的有 ▲ (填字母)
A.使用的漏斗叫长颈漏斗 B.液面应低于滤纸边缘
C.玻璃棒应不停搅拌 D.漏斗下端的管口要紧靠烧杯内壁
(3)某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量
6分数不低于99.2%),设计了如下两种实验方案:
方案一:称取样品10.65g,加水完全溶解,向其中加入足量的氯化钡溶液,充分反应后,过滤、洗涤,干燥
得固体19.70g。通过计算(写出计算过程)判断该厂的产品是否属于优等品 ▲ 。(杂质可溶
于水且不与氯化钡反应)
方案二:用右图所示的装置,通过准确测量排出水的体积,也可计算样品的纯度。该装置中仪器A的名
称是 ▲ ,但实验后同学们发现所测的碳酸钠的纯度偏低,造成此结果的原因可能是 ▲ 。
(装置的气密性良好)
【答案】(1)①CaCO = CaO + CO ↑;②浓盐酸具有挥发性,使制得的气体不纯,A;(2)①氮 ,2NH Cl
3 2 4
+ Ca(OH) = CaCl + 2NH ↑+ 2H O 小苏打 治疗胃酸过多或制发酵粉等 ②B、D ( 3) 属于
2 2 3 2
;方案二: 锥形瓶 二氧化碳溶于水或与水反应、导管中有水
(3)利用化学方程式,根据反应的质量笔记可计算出碳酸钠的质量;
方案一:解:设碳酸钠的质量为x
Na CO + BaCl = BaCO ↓+ 2NaCl
2 3 2 3
106 197
x 19.70g
解得x=10.60g
7该厂产品中碳酸钠的质量分数为
99.5%>99.2% 属于优等品。
答:略。
方案二:稀硫酸与碳酸钠反应生成二氧化碳,由于二氧化碳易溶于水,故会导致测定的二氧化碳的体积偏
小,即碳酸钠的质量偏小。学科*网
中考面对面
(每小题10分,共50分)
1.【2016年山东省临沂市】(8分)某同学在实验室发现一瓶标签残缺的硫酸铜溶液。为了测定此溶液的溶质
质量分数,他取出50g该溶液,向其中逐滴加入溶质质量分数,他取出50g该溶液,向其中逐滴加入溶质
质量分数为20%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所
示:
请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液 g时,硫酸铜与氢氧化钠恰好完全反应,此时溶液中的溶质为 (填化
学式)。
(2)计算此硫酸铜溶液中溶质的质量分数(写出解题过程)。
【答案】(1)20 Na SO (2)16%
2 4
80 160
20g×20% x
x=8g
硫酸铜溶液的溶质的质量分数为: 100%=16%。 学&科*网
2、【2016年山东省威海市】 实验室有一瓶久置的氢氧化钠固体,某同学想了解其变质情况,称取5g样品于烧
杯中,加入30g水使之完全溶解,再向烧杯中缓缓加入过量的氢氧化钡溶液,完全反应后,生成沉淀
81.97g。
求:(1)样品中碳酸钠的质量分数。 (2)反应后所得溶液中氢氧化钠的质量。
【答案】(1)21.2% (2)4.74g
[来源:学科网]
3、【2016年山东省烟台市】 某化学小组为了探究一瓶久置在空气中的氢氧化钠样品(不含有水分)的变质程
度,进行了如下实验:取该氢氧化钠样品13.3g于烧杯中,加水完全溶解,然后向烧杯中逐渐加入一定溶
质质量分数的氯化钡溶液,反应过程中对加入氯化钡溶液的质量与烧杯中产生沉淀的质量进行了记录,
部分数据见表:
加入氯化钡溶液的质量/g 20 40 80
生成沉淀的质量/g 1.97 3.94 5.91
试分析计算:
(1)13.3g氢氧化钠样品中碳酸钠的质量。
(2)13.3g氢氧化钠样品变质前的质量。(已知:Ba的相对原子质量为137)
【答案】(1)3.18g (2)12.52g
94、【2016年山东省淄博市】 合金的种类很多,用途非常广泛,黄铜是铜和锌的合金,它可以用来制造机器和
电器的零件等,化学兴趣小组的同学欲测定实验室中某铜样品中铜的质量分数(不考虑黄铜中的其他杂
质),请你参与他们的探究过程。
称量10g粉末状黄铜样品放入烧杯中,量取45mL稀盐酸分三次加到其中,每次充分反应后,测定生成氢
气的质量,实验数据如表:
第一次 第二次 第三次
加入稀盐酸的体积(ml) 15 15 15
生成氢气的质量(g) 0.04 m 0.02
试求:
(1)m的数值 。
(2)此黄铜样品中铜的质量分数是多少?(写出计算过程)
【答案】(1)0.04(2)67.5%
【解析】(1)根据表格可以发现,第一次加入15mL盐酸生成0.04g氢气,第三次加入15mL盐酸还能生成并且
只生成0.02g氢气,说明直到第三次反应才结束,并且盐酸有剩余;同时说明第二次加入15mL盐酸时完全反
应,生成氢气的质量可按照第一次的数量关系(15ml对应0.04g)类推,而得出m为0.04g;
105、【2016年四川省巴中市】 巴中某超市卖的纯碱(NaCO)产品往往含有少量的氯化钠(NaCl),化学兴趣小
2 3
组的同学通过实验来测定该纯碱样品中纯碱的质量分数,他们取12g纯碱样品放入烧杯中,逐滴加入稀
盐酸至不再产生气泡为止,共消耗盐酸 100g,烧杯中没有残留不溶物,称得反应后溶液的质量为
107.6g。计算:
(1)生成二氧化碳 g。
(2)样品中纯碱的质量分数是多少?(要求写出计算过程,结果精确到0.1%)
【答案】(1)4.4 (2)88.3%
【解析】(1)生成二氧化碳的质量为:100g+12g﹣107.6g=4.4g;
(2)设参加反应的碳酸钠的质量为x
2HCl+Na CO =2NaCl+H O+CO ↑
2 3 2 2
106 44
x 4.4g
=
高△△温
x=10.6g
所以样品中纯碱的质量分数是 ×100%=88.3%
11