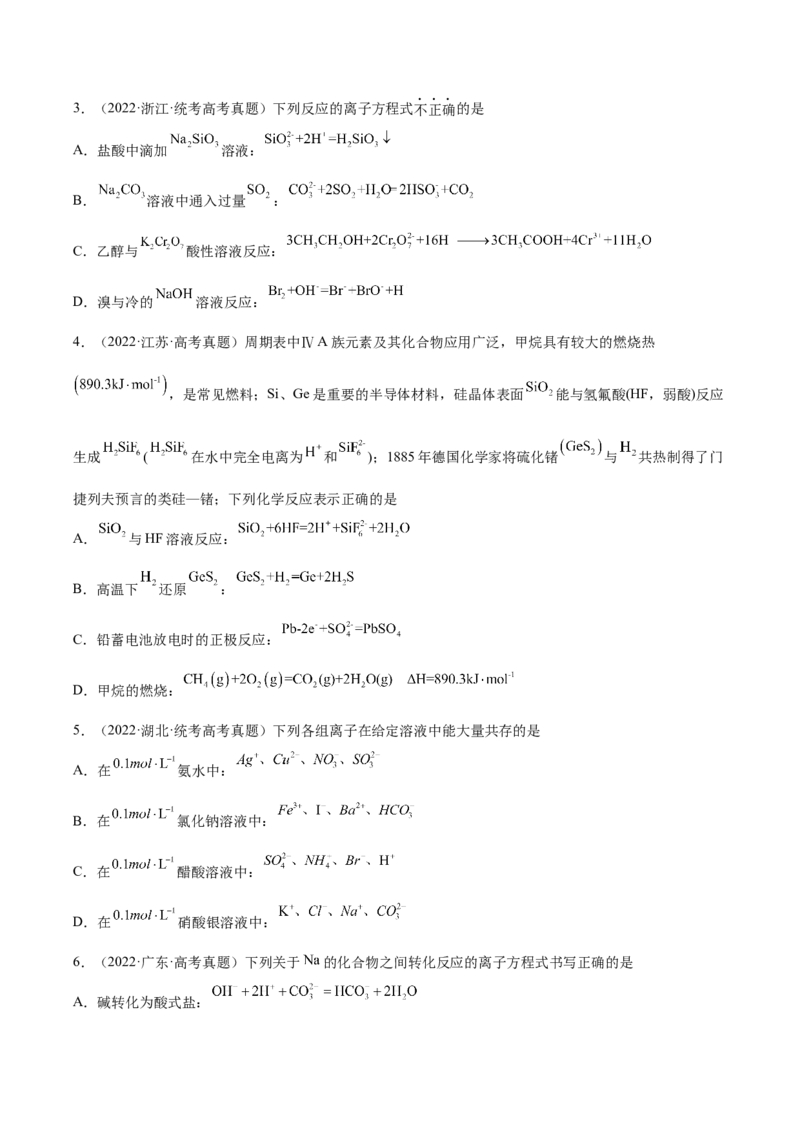文档内容
查补易混易错 04 离子反应
离子反应从微观上建立了认识化学反应的新视角,是电离模型的重要应用,为化学的微观研究奠定了重要
的基础。《课程标准》)要求学生通过实验事实认识离子反应及其发生的条件,能用离子方程式正确表示典
型物质的主要化学性质,该部分知识要求学生能对反应进行"宏观—微观—符号"三重表征分析微观实质,
并能用离子方程式进行符号表征,培养"宏观辨识与微观探析"的核心素养。离子反应贯穿在整个高中化学
教学之中,是每年高考命题中必然要涉及的知识点之一,主要包括离子方程式的书写(或正误判断)、离
子共存及离子的推导(可能出现在非选择题,对离子是否存在要知其然还要知其所以然),在非选择题中
也经常考离子方程式的书写,已知部分反应物和生成物,特别要注意的就是溶液的酸碱环境。
易错01离子方程式正误判断
(1)离子方程式正误判断时,要看是否符合客观事实,如铁与稀盐酸反应:3Fe+6H+=2Fe3++3H↑,书
2
写错误的原因是铁与稀盐酸反应生成Fe2+。
(2)要看拆分是否正确,如石灰石与稀盐酸反应:CO2- +2H+ = CO ↑+ H O,书写错误的原因是难溶的
3 2 2
CaCO 不能拆写;向NaHCO 溶液中滴加盐酸:CO2—+2H+===H O+CO↑,书写错误的原因是弱酸酸式
3 3 3 2 2
根离子HCO —不能拆写;NaO固体与水反应:O2—+HO===2OH-,书写错误的原因是氧化物NaO不能
3 2 2 2
拆写;醋酸溶液与水垢中的CaCO 反应:CaCO +2H+===Ca2++HO+CO↑,书写错误的原因是弱酸醋酸
3 3 2 2
(CHCOOH)不能拆写;Mg(OH) 和稀盐酸的反应:OH-+H+===H O,书写错误的原因是难溶的
3 2 2
Mg(OH) 不能拆写。
2
(3)要看是否符合原子守恒和电荷守恒,如氯化铁溶液与铜反应:Fe3++Cu== Fe2++Cu2+,书写错误的原因
是左右两边电荷不守恒;如金属钠与水反应:Na+HO== Na++OH– +H ↑,书写错误的原因是反应前后H原
2 2
子的数目不等。
(4)要看是否漏写离子反应,如Ba(OH) 溶液与硫酸铜溶液反应:Ba2++SO2-=BaSO ↓,书写错误的原
2 4 4
因是漏掉Cu2+与OH-生成Cu(OH) 沉淀。要看是否符合题设条件,如过量的NaHCO 溶液与Ca(OH) 溶液混
2 3 2
合:HCO - +Ca2+ +OH- = CaCO ↓+ H O,书写错误的原因是该离子方程式表示的是NaHCO 溶液与过量的
3 3 2 3
Ca(OH) 溶液混合。(5)要看是否符合组成,如稀硫酸与 Ba(OH) 溶液反应:H++SO2–+Ba2++OH–==
2 2 4
BaSO↓+H O,书写错误的原因是离子的个数比应与化学式中的组成不一致。
4 2
(6)要看离子方程式的条件注明是否正确,如制取氢氧化铁胶体:Fe3++3HO =Fe(OH) ↓+3H+,书写错
2 3误的原因是未标注加热符号。
易错02离子共存
(1)因生成弱电解质而不能大量共存的离子组:H+与CO、HCO、SO、HSO、S2-、HS-等易挥发的弱酸
的酸根不能共存;OH-与H+、NH、HCO、HSO、HS-、HPO、HPO等不能大量共存。
2
(2)因生成沉淀而不能大量共存的离子组:H+与SiO、AlO等不能大量共存;SO与Ba2+、Ca2+、Ag+等
不能大量共存;CO与Ba2+、Ca2+、Mg2+、Ag+、Cu2+、Zn2+等不能大量共存;S2-与Cu2+、Pb2+、Fe2+、
Hg2+、Ag+等不能大量共存;OH-与Mg2+、Al3+、Fe2+、Fe3+、Cu2+、Ag+、Zn2+等不能大量共存。
(3)因发生氧化还原反应而不能大量共存的离子组:在酸性条件下,NO与I-、Br-、Fe2+、S2-、HS-、
SO、HSO等不能共存,MnO与I-、Br-、Cl-、S2-、HS-、SO、HSO、Fe2+等不能大量共存,ClO-与Fe2
+、I-、S2-、HS-、SO、HSO等不能大量共存,S2-与SO等不能大量共存(碱性条件下可以共存);在碱性
条件下,ClO-与I-、Br-、Cl-、S2-等还原性比较强的离子不能大量共存,MnO与I-、Br-、Cl-、S2-等
还原性比较强的离子不能大量共存;
Fe3+与S2-、HS-、SO、HSO、I-等还原性比较强的离子不能大量共存,MnO与乙醇、苯酚、乙醛等还原
性比较强的分子不能大量共存。
(4)因水解相互促进而不能大量共存的离子组:Al3+与AlO、HCO、CO、HS-、S2-、SO、HSO、SiO、
ClO-、C HO-等不能大量共存;Fe3+与AlO、HCO、CO、SiO、ClO-等不能共存。
6 5
(5)因发生络合反应而不能大量共存的离子组:Fe3+和SCN-、C HO-不能大量共存;Ag+与NH在碱性
6 5
条件下不能大量共存。(1)一色——溶液颜色:
离子 Cu2+ Fe3+ Fe2+ MnO
溶液颜色 蓝色 黄色 浅绿色 紫红色
(2)二性——溶液的酸碱性
①在强酸性溶液中,OH-及弱酸根阴离子(如CO、ClO-、SO、S2-、CHCOO-等)不能大量存在。
3
②在强碱性溶液中,H+及弱碱阳离子(如NH、Al3+、Cu2+、Mg2+、Zn2+、Fe3+等)不能大量存在。
③如HCO、HS-、HSO、HPO、HPO等,在强酸性或强碱性溶液中均不能大量存在。
2
(3)三特殊——三种特殊情况
①AlO与HCO不能大量共存:AlO+HCO+HO===Al(OH) ↓+CO。
2 3
②“NO+H+”组合具有强氧化性,能与S2-、Fe2+、I-、SO等还原性的离子发生氧化还原反应而不能大
量共存。
③NH与CHCOO-、CO,Mg2+与HCO等组合中,虽然两种离子都能水解且水解相互促进,但总的水解
3
程度仍很小,它们在溶液中仍能大量共存。
(4)四反应——四种反应类型反应类型 不能大量共存的离子
如Ca2+ 、Ba2+与CO 、SO、SO;SiO与H+;Ag+与Cl-等不
生成沉淀
能大量共存
复分解 生成气体及易
H+与CO 、HCO、S2-、SO;NH和OH-等不能大量共存
反应 挥发性物质
生成弱
H+与OH-、ClO-、F-、CHCOO-等不能大量共存
3
电解质
Fe3+与S2-、I-等;MnO、ClO-在酸性、碱性、中性条件下与I
氧化还原反应
-、Fe2+、SO不能大量共存
相互促进的水解反应 Al3+、Fe3+与AlO、HCO、CO 等相互促进水解,不能大量共存
络合反应 Fe3+与SCN-;Ag+与NH ·H O不能大量共存
3 2
1.(2022·北京·高考真题)下列方程式与所给事实不相符的是
A.加热 固体,产生无色气体:
B.过量铁粉与稀硝酸反应,产生无色气体:
C.苯酚钠溶液中通入 ,出现白色浑浊:
D.乙醇、乙酸和浓硫酸混合加热,产生有香味的油状液体:
2.(2022·浙江·统考高考真题)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 23.(2022·浙江·统考高考真题)下列反应的离子方程式不正确的是
A.盐酸中滴加 溶液:
B. 溶液中通入过量 :
C.乙醇与 酸性溶液反应:
D.溴与冷的 溶液反应:
4.(2022·江苏·高考真题)周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热
,是常见燃料;Si、Ge是重要的半导体材料,硅晶体表面 能与氢氟酸(HF,弱酸)反应
生成 ( 在水中完全电离为 和 );1885年德国化学家将硫化锗 与 共热制得了门
捷列夫预言的类硅—锗;下列化学反应表示正确的是
A. 与HF溶液反应:
B.高温下 还原 :
C.铅蓄电池放电时的正极反应:
D.甲烷的燃烧:
5.(2022·湖北·统考高考真题)下列各组离子在给定溶液中能大量共存的是
A.在 氨水中:
B.在 氯化钠溶液中:
C.在 醋酸溶液中:
D.在 硝酸银溶液中:
6.(2022·广东·高考真题)下列关于 的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:B.碱转化为两种盐:
C.过氧化物转化为碱:
D.盐转化为另一种盐:
7.(2022·福建·统考高考真题)实验室需对少量污染物进行处理。以下处理方法和对应的反应方程式均错
误的是
A.用硫磺处理洒落在地上的水银:
B.用盐酸处理银镜反应后试管内壁的金属银:
C.用烧碱溶液吸收蔗糖与浓硫酸反应产生的刺激性气体:
D.用烧碱溶液吸收电解饱和食盐水时阳极产生的气体:
8.(2023·辽宁大连·统考一模)下列离子方程式书写正确的是
A.向 溶液中加入稀硫酸:
B.用亚硫酸钠溶液吸收少量氯气:
C.Fe与稀硝酸反应,当 时:
D.用过量苯酚溶液与碳酸钠溶液反应:2 + 2 +H O+CO
2 2
9.(2023·广东惠州·统考一模)下列有关铁及其化合物转化过程中的离子方程式书写正确的是
A.氧化亚铁溶于稀硝酸:
B.铁溶于盐酸:
C.醋酸除铁锈:
D.三氯化铁腐蚀铜板:
10.(2023·吉林长春·统考三模)能正确表示下列反应的离子方程式是A. 溶液中滴入 溶液:
B. 溶液中通入 ,溶液变为黄绿色:
C. 溶液中加入少量盐酸:
D.泡沫灭火器的反应原理:
11.(2023春·重庆沙坪坝·高三重庆一中校考阶段练习)经过指定操作后,下列各组溶液中离子还能大量
共存的是
A.加入 : 、 、Na+、
B.加入FeCl : 、 、 、
3
C.加入AgCl: 、F-、Na+、
D.通入SO :ClO-、Cl-、 、K+
2
12.(2023·广东佛山·统考二模)氯元素的单质及化合物之间可互相转化。下列反应的离子方程式书写错
误的是
A.单质转化为两种盐:
B.盐转化为酸:
C.酸转化为单质和盐:
D.两种盐转化为单质:
13.(2023·广东梅州·统考二模)下列解释事实的离子方程式书写正确的是
A.用含铝粉和氢氧化钠的疏通剂疏通管道:
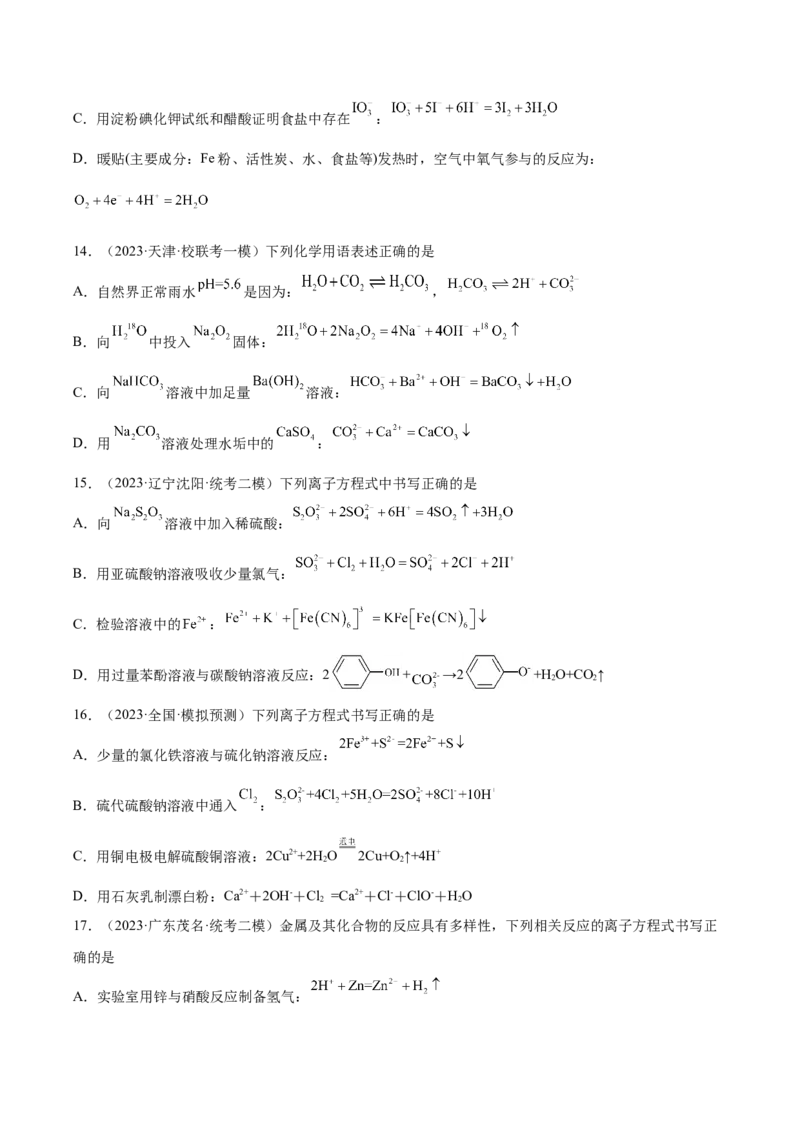
B.用氯化铁溶液蚀刻覆铜板:C.用淀粉碘化钾试纸和醋酸证明食盐中存在 :
D.暖贴(主要成分:Fe粉、活性炭、水、食盐等)发热时,空气中氧气参与的反应为:
14.(2023·天津·校联考一模)下列化学用语表述正确的是
A.自然界正常雨水 是因为: ,
B.向 中投入 固体:
C.向 溶液中加足量 溶液:
D.用 溶液处理水垢中的 :
15.(2023·辽宁沈阳·统考二模)下列离子方程式中书写正确的是
A.向 溶液中加入稀硫酸:
B.用亚硫酸钠溶液吸收少量氯气:
C.检验溶液中的 :
D.用过量苯酚溶液与碳酸钠溶液反应:2 + →2 +H O+CO↑
2 2
16.(2023·全国·模拟预测)下列离子方程式书写正确的是
A.少量的氯化铁溶液与硫化钠溶液反应:
B.硫代硫酸钠溶液中通入 :
C.用铜电极电解硫酸铜溶液:2Cu2++2H O 2Cu+O ↑+4H+
2 2
D.用石灰乳制漂白粉:Ca2++2OH-+Cl =Ca2++Cl-+ClO-+HO
2 2
17.(2023·广东茂名·统考二模)金属及其化合物的反应具有多样性,下列相关反应的离子方程式书写正
确的是
A.实验室用锌与硝酸反应制备氢气:B.腐蚀电路板的刻蚀液再生:
C.用含有 和铝粉的管道疏通剂疏通管道;
D.用 、 和 制备小苏打:
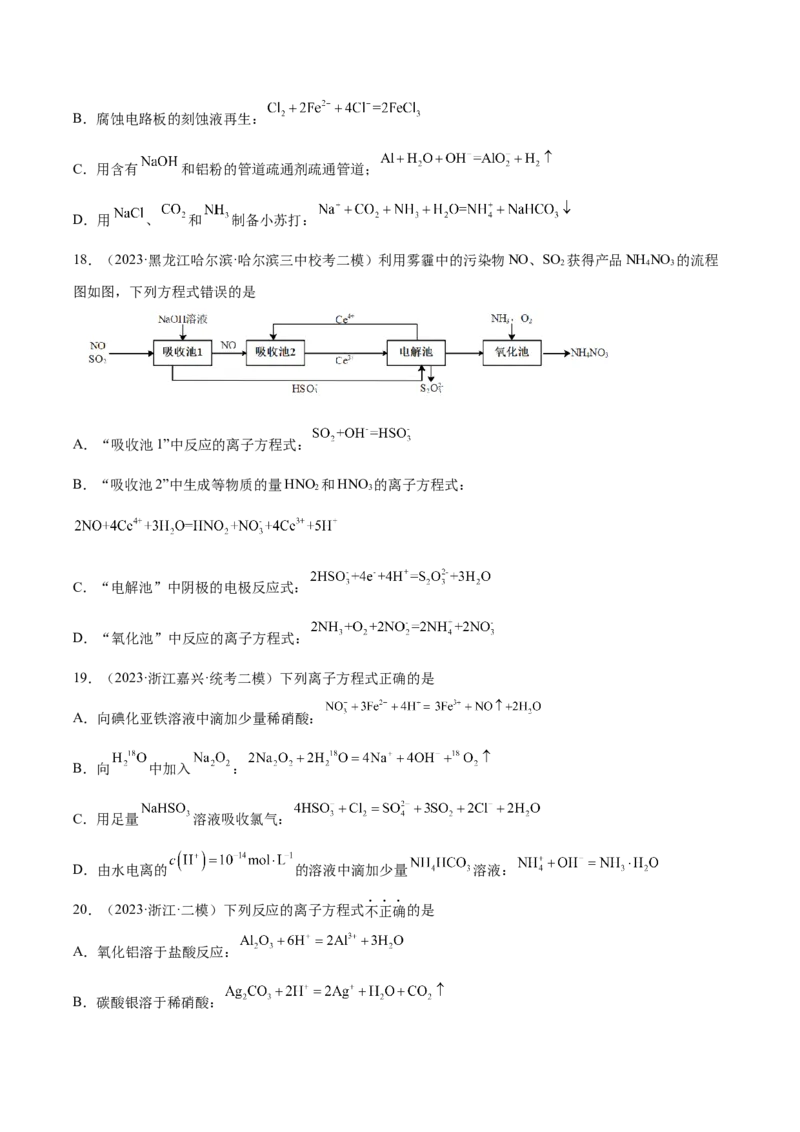
18.(2023·黑龙江哈尔滨·哈尔滨三中校考二模)利用雾霾中的污染物NO、SO 获得产品NH NO 的流程
2 4 3
图如图,下列方程式错误的是
A.“吸收池1”中反应的离子方程式:
B.“吸收池2”中生成等物质的量HNO 和HNO 的离子方程式:
2 3
C.“电解池”中阴极的电极反应式:
D.“氧化池”中反应的离子方程式:
19.(2023·浙江嘉兴·统考二模)下列离子方程式正确的是
A.向碘化亚铁溶液中滴加少量稀硝酸:
B.向 中加入 :
C.用足量 溶液吸收氯气:
D.由水电离的 的溶液中滴加少量 溶液:
20.(2023·浙江·二模)下列反应的离子方程式不正确的是
A.氧化铝溶于盐酸反应:
B.碳酸银溶于稀硝酸:C.次氯酸溶液见光分解:
D. 溶液中通入少量氯气:
21.(2023·湖南·校联考二模)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一
种制备方法如图所示。下列说法错误的是
A.“富集”是为了提高 的浓度
B.“转化”产生的沉淀是Ag
C.“氧化”通入氯气越多越好
D.“氧化”主要发生的离子反应为
22.(2023·辽宁·校联考二模)下列离子方程式书写正确的是
A.Fe与稀硝酸反应,当n(Fe):n(HNO)=1:1时,3Fe+2NO +8H+=3Fe2++2NO↑+4HO
3 2
B.NaSO 溶液与稀HSO 反应的离子方程式:SO +2SO +6H+=4SO↑+3H O
2 2 3 2 4 2 2 2
C.向饱和NaCO 溶液中通入过量CO:CO +CO +H O=2HCO
2 3 2 2 2
D.CuSO 与过量浓氨水反应的离子方程式:Cu2++2NH•H O=Cu(OH) ↓+2NH
4 3 2 2
23.(2023春·湖南长沙·高三雅礼中学校考阶段练习)有一澄清透明的溶液,只可能含有大量的Fe3+、
Fe2+、H+、Al3+、AlO 、CO 、NO 七种离子中的几种,向该溶液中逐滴滴入1mol•L-1NaOH溶液一定体
积后才产生沉淀。则下列判断正确的是
A.溶液中可能含有AlO B.溶液中可能含有Fe2+
C.溶液中一定不含Al3+ D.溶液中一定含有NO
24.(2023·河南郑州·统考二模)化学创造美好生活。下列劳动项目所涉及反应的离子方程式错误的是A.工程师用FeS除去废水中的Hg2+ :FeS(s) + Hg2+ (aq) = HgS(s) + Fe2+ (aq)
B.消防员使用泡沫灭火器灭火:A13+ +3 = Al(OH) ↓+3CO ↑
3 2
C.环保人员用漂白粉溶液脱除废气中的SO :Ca2++2ClO- +SO+H O=CaSO↓+2HClO
2 2 2 3
D.工人用醋酸处理水垢中的氢氧化镁:Mg(OH) + 2CHCOOH= 2CH COO-+Mg2+ +2H O
2 3 3 2
25.(2022·湖南·高考真题)下列离子方程式正确的是
A. 通入冷的 溶液:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
参考答案
1.B【详解】A.碳酸氢钠受热之后分解生成碳酸钠、水和二氧化碳,A正确;
B.过量的铁粉与稀硝酸反应,应该生成Fe2+,B错误;
C.苯酚钠溶液中通入二氧化碳利用强酸制取弱酸生成苯酚和碳酸氢钠,C正确;
D.乙醇和乙酸在浓硫酸混合加热的条件下发生酯化反应产生有香味的油状液体乙酸乙酯和水,D正确;
故选B。
2.C【详解】A. 将碳酸氢钙溶液与过量的澄清石灰水混合,反应生成碳酸钙和水,反应的离子方程式为:
+Ca2++OH-=CaCO ↓+H O,选项A正确;
3 2
B. 将少量NO 通入NaOH溶液,反应生成硝酸钠、亚硝酸钠和水,反应的离子方程式为:2NO +2OH-=
2 2
+ +H O,选项B正确;
2
C. 将少量SO 通入NaClO溶液,反应生成硫酸钠和盐酸,反应的离子方程式为:SO +H O+3ClO-=
2 2 2
+2HClO+Cl-,选项C不正确;
D. 向氨水中滴入少量硝酸银溶液,反应生成氢氧化二氨合银,反应的离子方程式为:Ag++2NH·H O=
3 2
+2H O,选项D正确;
2
答案选C。3.D【详解】A.盐酸中滴加 溶液,发生离子反应生成硅酸沉淀,该反应的离子方程式为
,A正确;
B.亚硫酸的酸性强于碳酸,因此, 溶液中通入过量 发生离子反应生成亚硫酸氢钠和二氧化碳,
该反应的离子方程式为 ,B正确;
C.乙醇与 酸性溶液反应发生反应,乙醇被氧化为乙酸, 被还原为 ,该反应的离子方程
式为 ,C正确;
D.类比氯气与碱反应可知,溴与冷的 溶液反应生成溴化钠、次溴酸钠和水,该反应的离子方程式
为 ,D不正确。
综上所述,本题选D。
4.A【详解】A.由题意可知,二氧化硅与氢氟酸溶液反应生成强酸 和水,反应的离子方程式为
,故A正确;
B.硫化锗与氢气共热反应时,氢气与硫化锗反应生成锗和硫化氢,硫化氢高温下分解生成硫和氢气,则
反应的总方程式为 ,故B错误;
C.铅蓄电池放电时,二氧化铅为正极,酸性条件下在硫酸根离子作用下二氧化铅得到电子发生还原反应
生成硫酸铅和水,电极反应式为正极反应 ,故C错误;
D.由题意可知,1mol甲烷完全燃烧生成二氧化碳和液态水放出热量为890.3kJ,反应的热化学方程式为
,故D错误;
故选A。5.C【详解】A.氨水显碱性,会与 反应,不能大量共存,A项错误;
B. 会发生氧化还原反应,不能大量共存,B项错误;
C.醋酸显酸性,在醋酸溶液中 均不会发生反应,能大量共存,C项正确;
D.硝酸银中的银离子会与氯离子反应生成沉淀,不能大量共存,D项错误;
答案选C。
6.B【详解】A.向氢氧化钠溶液中通入足量的二氧化碳,碱可以转化成酸式盐,离子方程式为:
CO+OH-= ,故A错误;
2
B.氯气通入NaOH溶液中可以生成氯化钠和次氯酸钠两种盐,其离子方程式为:Cl+2OH-=Cl-+ClO-
2
+H O,故B正确;
2
C.钠的过氧化物为NaO,可以和水反应生成氢氧化钠,但在离子方程式里NaO 不能拆成离子,故C错
2 2 2 2
误;
D.硅酸钠溶于水,在离子方程式里要写成离子,故D错误;
故选B。
7.B【详解】A.S和Hg发生化合反应生成HgS,可以用硫磺处理洒落在地上的水银,方程式为:
,处理方法和对应的反应方程式正确,不合题意;
B.Ag不活泼,不能和盐酸反应生成氢气,处理方法和对应的反应方程式均错误,符合题意;
C.蔗糖与浓硫酸反应产生的刺激性气体为SO ,可以用NaOH溶液吸收SO ,离子方程式为:
2 2
,处理方法正确,对应的反应方程式错误,不符合题意;
D.电解饱和食盐水时阳极产生的气体为Cl,可以用NaOH溶液吸收Cl,离子方程式为:
2 2
,处理方法和对应的反应方程式均正确,不符合题意;
故选B。
8.C【详解】A.NaSO 溶液中加入稀硫酸,离子方程式必须满足电荷守恒,正确的离子方程式为:3SO
2 2 3 2
+2H+═2SO +4S↓+H O,故A错误;
2B. 溶液吸收少量氯气,首先两者发生氧化还原反应生成HCl和NaSO ,而生成的少量HCl能和
2 4
过量的 反应生成NaHSO,故离子方程式为: ,故B错误;
3
C.Fe与稀硝酸反应,当 时生成NO和Fe2+,离子方程式为:
,故C正确;
D.用过量苯酚溶液与碳酸钠溶液生成苯酚钠和碳酸氢钠,离子方程式为: +CO
+HCO ,故D错误;
故选C。
9.D【详解】A.氧化亚铁溶于稀硝酸,稀硝酸氧化亚铁离子,会有一氧化氮生成,反应的离子方程式为
3FeO+10H++ =3Fe3++NO↑+5HO,A错误;
2
B.铁溶于盐酸生成二价亚铁, ,B错误;
C.醋酸是弱酸,离子方程式中不能拆开, ,C错误;
D.三价铁离子具有氧化性,会把铜氧化为铜离子, ,D正确;
故选D。
10.B【详解】A. 与 , 在酸性条件下的氧化性比 强,所以反应为:
,A错误;
B. 溶液中通入 ,生成黄绿色的 离子,反应的离子方程式为:
,B正确;C. 溶液中加入少量盐酸,应先反应生成酚羟基,C错误;
D.泡沫灭火器的反应原理: ,D错误;
故选B。
11.A【详解】A.向含有 、 、Na+、 的溶液中加入 ,没有气体、沉淀生成,且
离子间不发生化学反应,能大量共存,故A选;
B.向该溶液中加入氯化铁, 和 发生反应生成血红色硫氰化铁而不能共存,故B不选;
C.向含有 、F-、Na+、 的溶液中加入氯化银,生成硫化银黑色沉淀而不能大量共存,故C不选;
D. 具有强氧化性,向该溶液中通入二氧化硫发生氧化还原反应,不能大量共存,故D不选;
故选A。
12.B【详解】A.氯气与碱反应生成两种盐,离子方程式正确,A正确;
B.次氯酸根与二氧化硫会发生氧化还原反应,离子方程式为 ,B错误;
C.二氧化锰与浓盐酸在加热条件下反应生成氯气和氯化锰,离子方程式正确,C正确;
D.氯酸根和氯离子发生氧化还原反应生成氯气,离子方程式正确,D正确;
故选B。
13.A【详解】A.铝和氢氧化钠反应生成偏铝酸钠和氢气,
,故A正确;
B.铁离子和铜生成亚铁离子和铜离子, ,故B错误 ;
C.碘酸根离子和碘离子在酸性条件下生成碘单质和水,醋酸为弱酸不能拆,
,故C错误;
D.铁和氧气、氯化钠、水发生吸氧腐蚀,O+4e-+2H O=4OH-,而放出热量,故D错误;
2 2
故选A。14.C【详解】A.碳酸是弱酸,分步电离,碳酸的电离方程式为 ,故A错误;
B. 和 固体先发生复分解反应生成氢氧化钠和双氧水,双氧水再分解为水和氧气,氢氧化钠中
的样原子来自水分子,氧气中的氧原子来自过氧化钠,反应的离子方程式为
,故B错误;
C.向 溶液中加足量 溶液生成碳酸钡沉淀和氢氧化钠,反应的离子方程式是
,故C正确;
D.用 溶液处理水垢中的 生成碳酸钙沉淀和硫酸钠,反应的离子方程式是
,故 D错误;
选C。
15.C【详解】A. 在酸性条件下发生歧化反应生成 和S,反应离子方程式为:
,故A错误;
B.亚硫酸钠溶液吸收少量氯气,氯气与亚硫酸根反应生成氯离子和硫酸根,溶液呈碱性,因此生成的氢
离子与亚硫酸根离子结合为亚硫酸氢根,离子方程式为: ,故B错误;
C.亚铁离子与铁氰化钾反应生成蓝色沉淀,反应离子方程式正确,故C正确;
D.苯酚酸性弱于碳酸,但强于碳酸氢根,苯酚于碳酸钠反应生成苯酚钠和碳酸氢钠,离子方程式为:
+ → + ,故D错误;
故选:C。
16.B【详解】A.Fe3+具有氧化性,S2-具有还原性,两者发生氧化还原反应生成Fe2+和S,由于S2-过量,
Fe2+与S2-生成FeS,离子方程式为 ,故A错误;
B.硫代硫酸钠溶液与氯气反应生成硫酸钠、硫酸和盐酸,反应的离子方程式为,故B正确;
C.用铜电极电解硫酸铜溶液,由于Cu是活性电极,在阳极上是Cu电极本身失去电子变为Cu2+进入溶液,
而不是水电离产生的OH-失去电子产生O,故C错误;
2
D.石灰乳在离子方程式书写时不能拆,故用石灰乳制漂白粉的离子方程式为:Ca(OH) +Cl =Ca2++Cl-+
2 2
ClO-+HO,故D错误;
2
答案为B。
17.D【详解】A.硝酸具有强氧化性,锌与硝酸反应生成 气体,不能用于制备氢气,A错误;
B.腐蚀电路板的刻蚀液主要成分为 ,可以通过反应 再生,B错误;
C. 和铝粉反应的离子方程式为: ,C错误;
D.饱和食盐水中通入 和 可以制备小苏打,反应的离子方程式为:
,D正确;
故选D。
18.D【详解】A.根据题目信息,吸收池1中, 溶液和 反应生成 ,反应的离子方程式
为: ,A正确;
B.吸收池2中, 与 反应生成等物质的量 和 ,离子方程式为:
,B正确;
C.电解池中,阴极上 ,电极反应式为: ,C正确;
D.“氧化池”中反应的离子方程式: ,D错误;
故选D。
19.C【详解】A.离子的还原性:I->Fe2+,所以向碘化亚铁溶液中滴加少量稀硝酸时,应该是I-先失去电
子,发生氧化反应,离子方程式应该为: ,故A错误;B.向 中加入 固体, 既做氧化剂又做还原剂, 中的18O全部在NaOH中,因此氧
气的化学式为O,故B错误;
2
C.氯气和足量 溶液反应生成硫酸钠、氯化钠和二氧化硫,离子方程式为:
,故C正确;
D.由水电离的 的溶液中水的电离被抑制,该溶液可能是酸性也可能是碱性,若溶液
为酸性,滴加少量 溶液: ,若溶液为碱性,滴加少量 溶液:
,故D错误;
故选C。
20.D【详解】A.氧化铝与盐酸反应生成氯化铝和水,反应的离子方程式为 ,
故A正确;
B.碳酸银与稀硝酸反应生成硝酸银、二氧化碳和水,反应的离子方程式为
,故B正确;
C.次氯酸遇光分解生成盐酸和氧气,反应的离子方程式为 ,故C正确;
D.亚硫酸钠与少量氯气反应生成硫酸钠、氯化钠和亚硫酸氢钠,反应的离子方程式为
,故D错误;
故选D。
21.C【详解】净化除氯后含I-海水中加入AgNO 生成AgI悬浊液,该过程可以提高 的浓度,再加入Fe
3
粉发生反应Fe+2Ag+=2Ag+Fe2+,过滤掉析出的Ag,向FeI 中加入Cl,生成I,以此解答。
2 2 2
A.由分析可知,“富集”是为了提高 的浓度,故A正确;
B.由分析可知,“转化”过程中发生反应Fe+2Ag+=2Ag+Fe2+,产生的沉淀是Ag,故B正确;C.“氧化”通入氯气过多容易发生副反应,氯气进一步将碘单质氧化为 ,故C错误;
D.“氧化”过程中向FeI 中加入Cl,使碘离子转化生成I,主要发生的离子反应为 ,
2 2 2
故D正确;
故选C。
22.A【详解】A.当 时,Fe过量应生成 ,A选项正确;
B. 溶液与稀 反应的离子方程式: ,B选项错误;
C.向饱和 溶液中通入过量 ,离子方程式为: ,C选项
错误;
D. 与过量浓氨水反应形成配合物,离子方程式: ,D选
项错误;
故选A。
23.D【详解】澄清透明的溶液,只可能含有大量的 、 、 、 、 、 、 七种离
子中的几种,向该溶液中逐滴滴入1 NaOH溶液一定体积后才产生沉淀,说明溶液中一定含有 ,
和 、 不能大量共存,则一定没有 、 ,溶液中必有阴离子,则一定有 ,酸性条
件下, 具有强氧化性,和 能发生氧化还原反应,则一定不存在 ,加入NaOH一定体积后才有
沉淀生成,则 、 至少含一种,所以溶液中一定含有 、 ,一定不含有 、 、 ,
而 、 至少含一种,以此解答。
A.由分析可知,溶液中一定不含有 ,故A错误;
B.由分析可知,溶液中一定不含有 ,故B错误;C.由分析可知,溶液中含有 、 至少一种,故C错误;
D.由分析可知,溶液中含有 、 ,故D正确;
故选D。
24.C【详解】A.硫化汞溶度积小于硫化亚铁,硫化亚铁与汞离子反应生成硫化汞和亚铁离子,实现沉淀
的转化,A正确;
B.灭火器中铝离子与碳酸氢根发生双水解产生二氧化碳,B正确;
C.次氯酸根具有氧化性,二氧化硫具有还原性,发生氧化还原反应:
,C错误;
D.醋酸及氢氧化镁均为弱电解质,不能拆,D正确;
故答案为:C。
25.AC【详解】A.Cl 通入冷的 NaOH溶液中发生反应生成氯化钠和次氯酸钠,该反应的离子方程式为
2
Cl+2OH-=Cl-+ClO-+H O,A正确;
2 2
B.用醋酸和淀粉-KI溶液检验加碘盐中的 的原理是 在酸性条件下与I-发生归中反应生成I 而遇淀
2
粉变蓝,由于醋酸是弱酸,在离子方程式中不能用H+表示,因此B不正确;
C.+2价的铁被双氧水氧化为+3价,反应的离子方程式为2Fe2++H O+4H O=2Fe(OH) ↓+4H+,C正确;
2 2 2 3
D.NaHCO 溶液与少量的Ba(OH) 溶液混合后发生反应生成碳酸钡沉淀、碳酸钠和水,NaHCO 过量,
3 2 3
Ba(OH) 全部参加反应,因此该反应的离子方程式为2 +Ba2++2OH-=BaCO ↓+ +2H O,D不正确;
2 3 2
综上所述,本题选AC。