文档内容
查补易混易错 09 电化学基础
电化学基础是高考每年必考内容,主要题型是选择题,有时也会在非选择题中出现,命制的角度有电极反
应式的正误判断与书写,电池反应式的书写,正负极的判断,电池充、放电时离子移动方向的判断,电极
附近离子浓度的变化,电解的应用与计算,金属的腐蚀与防护等。同时通过陌生化学电源的装置图,考查
学生接受、吸收、整合化学信息的能力,也体现了对“宏观辨识与微观探析”的学科核心素养考查。
易错01 常见考点归纳
负极:元素化合价升高或发生氧化反应的物质
电极判断 正极:元素化合价降低或发生还原反应的物质
阴极:“放电”时的负极在“充电”时为阴极
阳极:“放电”时的正极在“充电”时为阳极
电子流向 原电池:负极→正极
电解池:电源负极→阴极,阳极→电源正极
离子流向 原电池:阳离子移向正极,阴离子移向负极
电解池:阳离子移向阴极,阴离子移向阳极
“放电”时依据条件,指出参与负极和正极反应的物质,根据化合价的
变化,判断转移电子的数目;根据守恒书写负极(或正极)反应式,特别应
电极反应式
注意电极产物是否与电解质溶液共存
充电时的电极反应与放电时的电极反应过程相反,充电的阳极反应为放
电时正极反应的逆过程,充电的阴极反应为放电时负极反应的逆过程
易错02 电极判断
1.原电池中正负极的判断
依据 正负极判断
依据构成原电池两极的电极材料判断 一般是较活泼的金属为负极,活泼性较弱的
金属或能导电的非金属为正极
依据原电池两极发生的变化判断 原电池的负极发生氧化反应;正极发生还原
反应
依据电子流动方向或电流方向判断 电子由负极流向正极;电流由正极流向负极
依据原电池电解质溶液中离子的移动方向判断 阳离子向正极移动,阴离子向负极移动
依据原电池盐桥中离子的移动方向判断 阳离子向正极移动,阴离子向负极移动2.电解池中阴阳极的判断
依据 阴阳极判断
根据所连接的外加电源判断 与直流电源正极相连的为阳极,与直流电源
负极相连的为阴极
根据电子流动方向判断 电子从电源负极流向阴极,从阳极流向电源
正极
根据电解池电解质溶液中离子的移动方向判断 阳离子向阴极移动,阴离子向阳极移动
根据电解池两极产物判断 一般情况下:阴极上的现象是析出金属(质量
增加)或有无色气体(H )放出;阳极上的现象
2
是有非金属单质生成,呈气态的有Cl 、O
2 2
或电极质量减小(活性电极作阳极)
易错03 化学电源
1.新型电池的电极反应式
总反应:Ag O+Zn+HO 2Ag+Zn(OH)
2 2 2
锌银电池 正极:Ag O+HO+2e-===2Ag+2OH-
2 2
负极:Zn+2OH--2e-===Zn(OH)
2
总反应:NiO+Fe+2HO Fe(OH) +Ni(OH)
2 2 2 2
镍铁电池
正极:NiO+2e-+2HO===Ni(OH) +2OH-
2 2 2
负极:Fe-2e-+2OH-===Fe(OH)
2
总反应:3Zn+2KFeO+8HO 3Zn(OH) +2Fe(OH) +4KOH
2 4 2 2 3
高铁电池
正极:FeO+3e-+4HO===Fe(OH) +5OH-
2 3
负极:Zn-2e-+2OH-===Zn(OH)
2
总反应:Cd+2NiOOH+2HO Cd(OH) +2Ni(OH)
2 2 2
镍镉电池
正极:NiOOH+HO+e-===Ni(OH) +OH-
2 2
负极:Cd-2e-+2OH-===Cd(OH)
2
总反应:HO+2H++Mg===Mg2++2HO
2 2 2
MgHO 电池 正极:HO+2H++2e-===2H O
2 2 2 2 2
负极:Mg-2e-===Mg2+
MgAgCl电池 总反应:Mg+2AgCl===2Ag+MgCl
2正极:2AgCl+2e-===2Ag+2Cl-
负极:Mg-2e-===Mg2+
总反应:2Na+xS===Na S
2 x
钠硫电池 正极:xS+2e-===S
负极:2Na-2e-===2Na+
总反应:VO+2H++V2+ V3++VO2++HO
2
全钒液流电池
正极:VO+2H++e-===VO2++HO
2
负极:V2+-e-===V3+
总反应:2Li+Cu O+HO===2Cu+2Li++2OH-
2 2
锂铜电池 正极:Cu O+HO+2e-===2Cu+2OH-
2 2
负极:Li-e-===Li+
总反应:Li CoO+LiC LiCoO +C (x<1)
1-x 2 x 6 2 6
锂离子电池
正极:Li CoO+xe-+xLi+===LiCoO
1-x 2 2
负极:LiC -xe-===xLi++C
x 6 6
2.燃料电池的电极反应式(以CH OH为例)
3
电池类型 导电介质 反应式
总反应:2CHOH+3O===2CO ↑+4HO
3 2 2 2
酸性燃料电池 H+ 正极:O+4e-+4H+===2H O
2 2
负极:CHOH-6e-+HO=== CO↑+6H+
3 2 2
总反应:2CHOH+3O+4OH-===2CO+6HO
3 2 2
碱性燃料电池 OH- 正极:O+4e-+2HO===4OH-
2 2
负极:CHOH-6e-+8OH-=== CO+6HO
3 2
总反应:2CHOH+3O===2CO ↑+4HO
3 2 2 2
熔融碳酸盐燃料电池 CO 正极:O+4e-+2CO===2CO
2 2
负极:CHOH-6e-+3CO===4CO ↑+2HO
3 2 2
总反应:2CHOH+3O===2CO ↑+4HO
3 2 2 2
固态氧化物燃料电池 O2- 正极:O+4e-===2O2-
2
负极:CHOH-6e-+3O2-===CO ↑+2HO
3 2 2
总反应:2CHOH+3O===2CO ↑+4HO
3 2 2 2
质子交换膜燃料电池 H+ 正极:O+4e-+4H+===2H O
2 2
负极:CHOH-6e-+HO=== CO↑+6H+
3 2 2
易错04 金属腐蚀与保护
1.析氢腐蚀和吸氧腐蚀类型 析氢腐蚀 吸氧腐蚀
条件 水膜呈酸性 水膜呈弱酸性或中性
正极反应 2H++2e-===H ↑ O+2HO+4e-===4OH-
2 2 2
负极反应 Fe-2e-===Fe2+
Fe2++2OH-===Fe(OH) ↓
2
其他反应 4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
Fe(OH) 失去部分水转化为铁锈
3
2.金属腐蚀的防护方法
(1)加防护层:如在金属表面加上油漆、搪瓷、沥青、塑料、橡胶等耐腐蚀的非金属材料;采用电镀或
表面钝化等方法在金属表面镀上一层不易被腐蚀的金属或生成一层致密的薄膜。
(2)电化学防护法:牺牲阳极的阴极保护法——原电池原理:正极为被保护的金属,负极为比被保护的
金属活泼的金属;外加电流的阴极保护法——电解原理:阴极为被保护的金属,阳极为惰性电极。
1.(2022·天津·统考高考真题)实验装置如图所示。接通电源后,用碳棒( 、 )作笔,在浸有饱和NaCl
溶液和石蕊溶液的湿润试纸上同时写字, 端的字迹呈白色。下列结论正确的是
A.a为负极
B. 端的字迹呈蓝色
C.电子流向为:
D.如果将 、 换成铜棒,与碳棒作电极时的现象相同
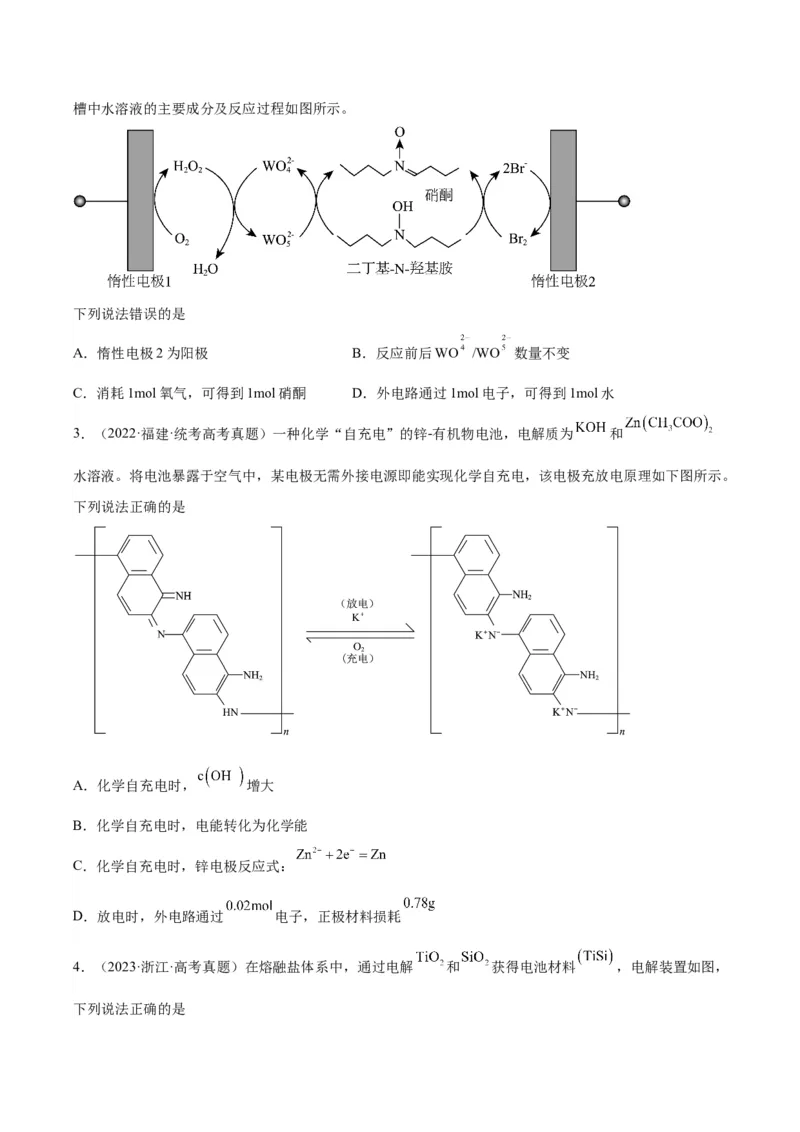
2.(2022·重庆·统考高考真题)硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解槽中水溶液的主要成分及反应过程如图所示。
下列说法错误的是
A.惰性电极2为阳极 B.反应前后WO /WO 数量不变
C.消耗1mol氧气,可得到1mol硝酮 D.外电路通过1mol电子,可得到1mol水
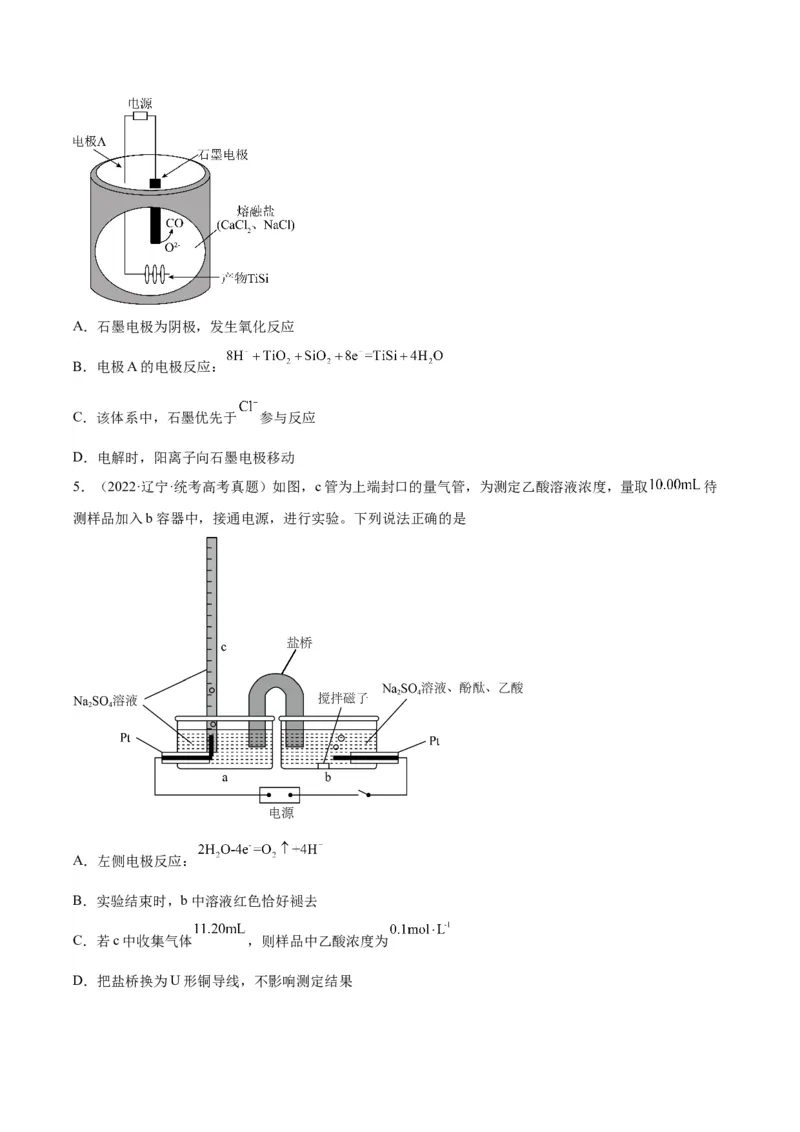
3.(2022·福建·统考高考真题)一种化学“自充电”的锌-有机物电池,电解质为 和
水溶液。将电池暴露于空气中,某电极无需外接电源即能实现化学自充电,该电极充放电原理如下图所示。
下列说法正确的是
A.化学自充电时, 增大
B.化学自充电时,电能转化为化学能
C.化学自充电时,锌电极反应式:
D.放电时,外电路通过 电子,正极材料损耗
4.(2023·浙江·高考真题)在熔融盐体系中,通过电解 和 获得电池材料 ,电解装置如图,
下列说法正确的是A.石墨电极为阴极,发生氧化反应
B.电极A的电极反应:
C.该体系中,石墨优先于 参与反应
D.电解时,阳离子向石墨电极移动
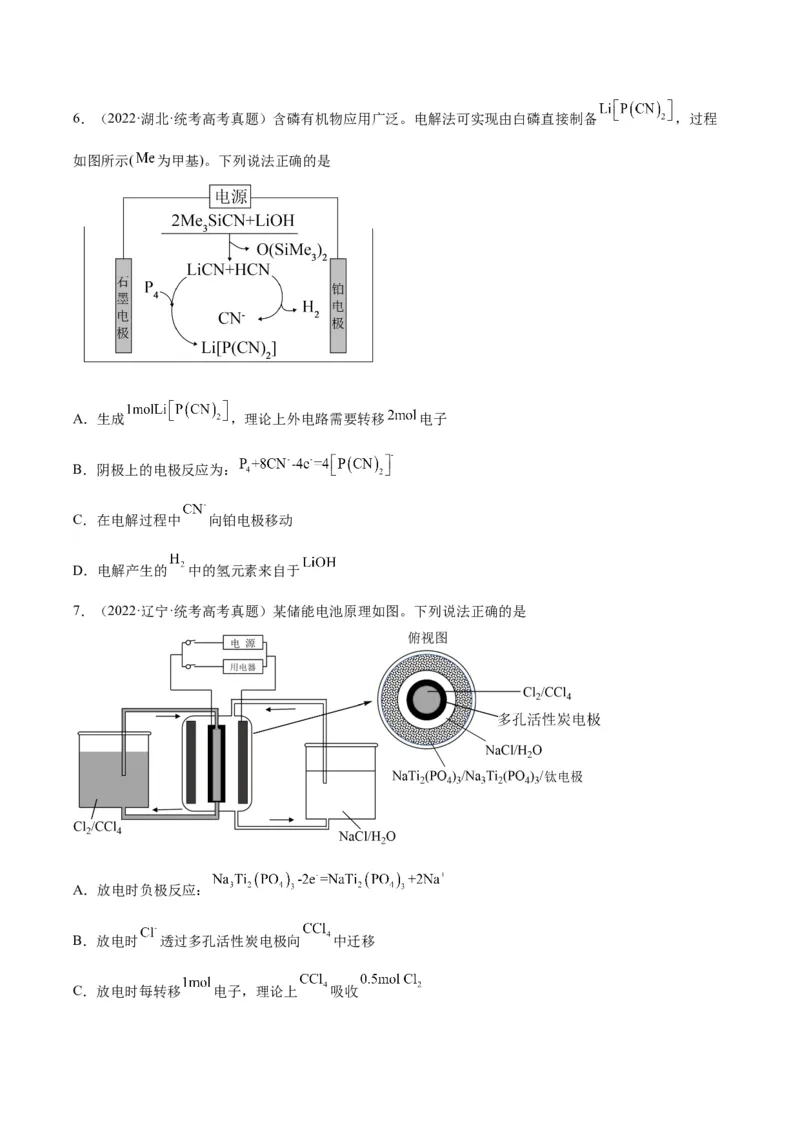
5.(2022·辽宁·统考高考真题)如图,c管为上端封口的量气管,为测定乙酸溶液浓度,量取 待
测样品加入b容器中,接通电源,进行实验。下列说法正确的是
A.左侧电极反应:
B.实验结束时,b中溶液红色恰好褪去
C.若c中收集气体 ,则样品中乙酸浓度为
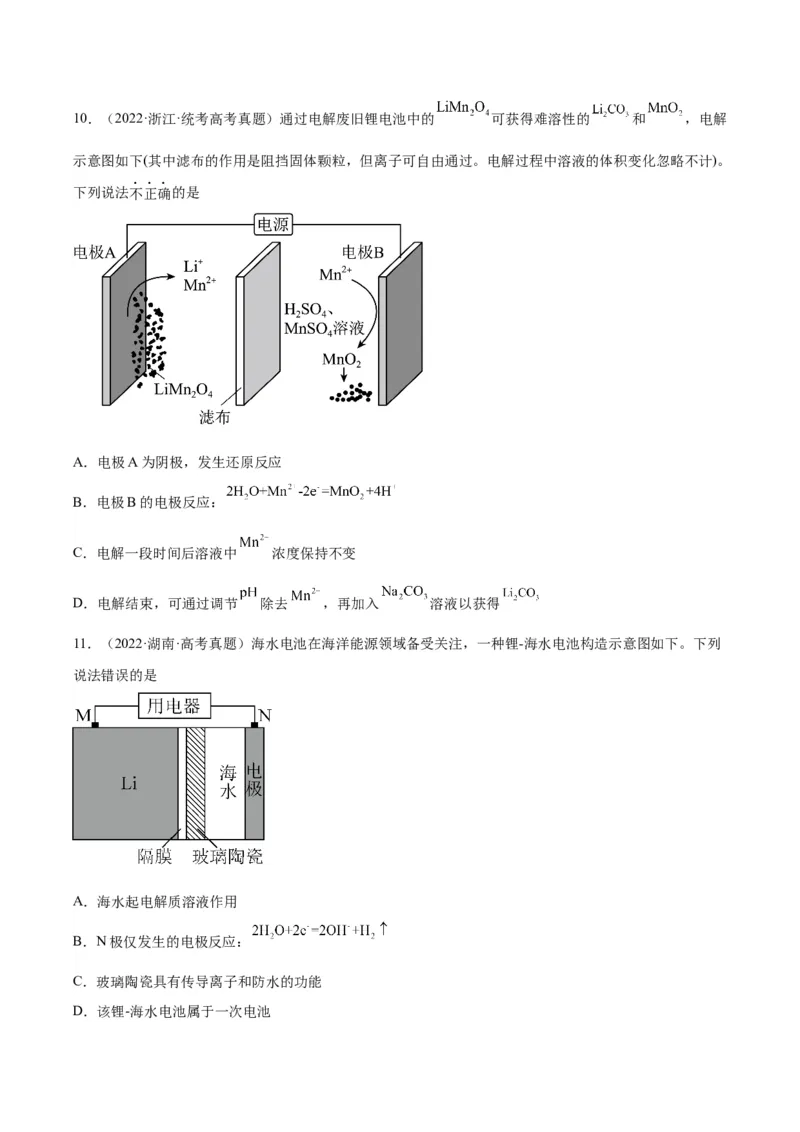
D.把盐桥换为U形铜导线,不影响测定结果6.(2022·湖北·统考高考真题)含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程
如图所示( 为甲基)。下列说法正确的是
A.生成 ,理论上外电路需要转移 电子
B.阴极上的电极反应为:
C.在电解过程中 向铂电极移动
D.电解产生的 中的氢元素来自于
7.(2022·辽宁·统考高考真题)某储能电池原理如图。下列说法正确的是
A.放电时负极反应:
B.放电时 透过多孔活性炭电极向 中迁移
C.放电时每转移 电子,理论上 吸收D.充电过程中, 溶液浓度增大
8.(2022·海南·统考高考真题)一种采用 和 为原料制备 的装置示意图如下。
下列有关说法正确的是
A.在b电极上, 被还原
B.金属Ag可作为a电极的材料
C.改变工作电源电压,反应速率不变
D.电解过程中,固体氧化物电解质中 不断减少
9.(2022·北京·高考真题)利用下图装置进行铁上电镀铜的实验探究。
序
装置示意图 电解质溶液 实验现象
号
0.1mol/LCuSO +少量 阴极表面有无色气体,一段时间后阴极表面有红色固
① 4
HSO 体,气体减少。经检验电解液中有
2 4
0.1mol/LCuSO +过量 阴极表面未观察到气体,一段时间后阴极表面有致密红
② 4
氨水 色固体。经检验电解液中无 元素
下列说法不正确的是
A.①中气体减少,推测是由于溶液中 减少,且 覆盖铁电极,阻碍 与铁接触
B.①中检测到 ,推测可能发生反应:
C.随阴极析出 ,推测②中溶液 减少, 平衡逆移
D.②中 生成 ,使得 比①中溶液的小, 缓慢析出,镀层更致密10.(2022·浙江·统考高考真题)通过电解废旧锂电池中的 可获得难溶性的 和 ,电解
示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。
下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极反应:
C.电解一段时间后溶液中 浓度保持不变
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
11.(2022·湖南·高考真题)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列
说法错误的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池12.(2022·广东·高考真题)科学家基于 易溶于 的性质,发展了一种无需离子交换膜的新型氯流
电池,可作储能设备(如图)。充电时电极a的反应为: 。下列说
法正确的是
A.充电时电极b是阴极
B.放电时 溶液的 减小
C.放电时 溶液的浓度增大
D.每生成 ,电极a质量理论上增加
13.(2022·全国·统考高考真题) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来
科学家研究了一种光照充电 电池(如图所示)。光照时,光催化电极产生电子 和空穴 ,驱动阴
极反应 和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是
2 2 2
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
14.(2022·全国·高考真题)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以
2
Zn(OH) 存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O
2 2
15.(2022·浙江·统考高考真题)pH计是一种采用原电池原理测量溶液pH的仪器。如图所示,以玻璃电
极(在特制玻璃薄膜球内放置已知浓度的HCl溶液,并插入Ag—AgCl电极)和另一Ag—AgCl电极插入待测
溶液中组成电池,pH与电池的电动势E存在关系:pH=(E-常数)/0.059。下列说法正确的是
A.如果玻璃薄膜球内电极的电势低,则该电极反应式为:AgCl(s)+e-=Ag(s)+Cl-(0.1mol·L-1)
B.玻璃膜内外氢离子浓度的差异不会引起电动势的变化
C.分别测定含已知pH的标准溶液和未知溶液的电池的电动势,可得出未知溶液的pHD.pH计工作时,电能转化为化学能
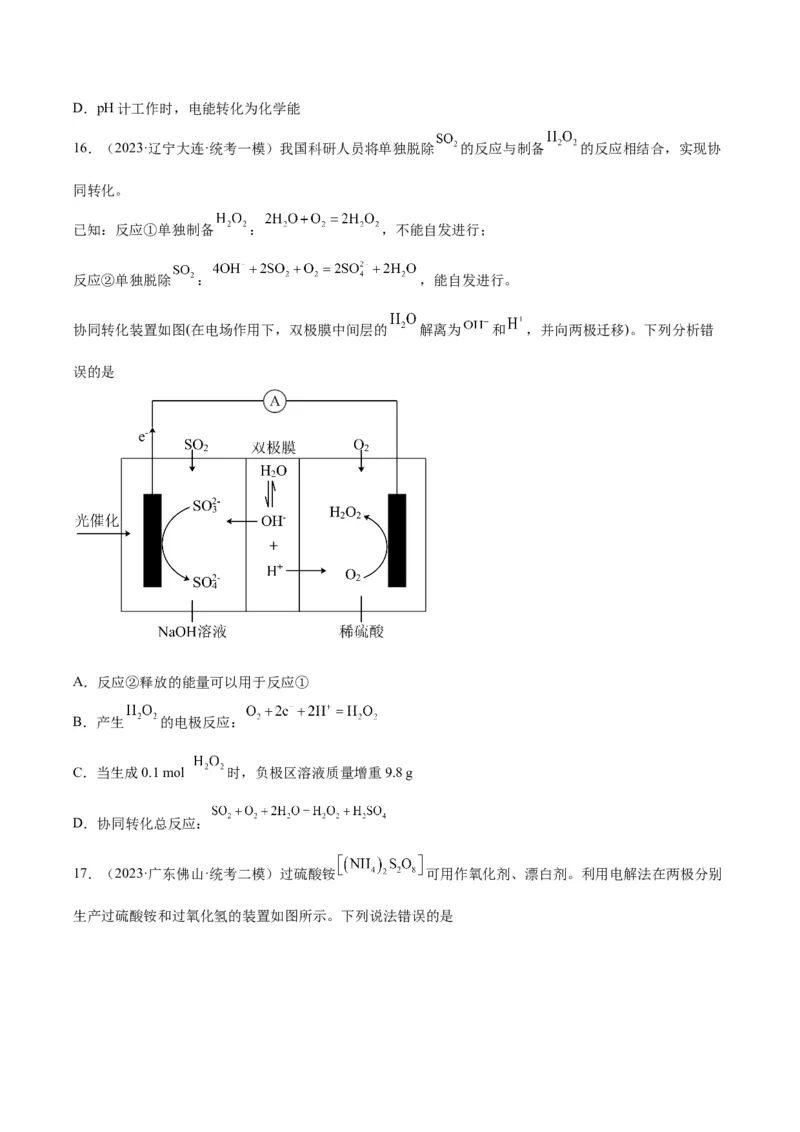
16.(2023·辽宁大连·统考一模)我国科研人员将单独脱除 的反应与制备 的反应相结合,实现协
同转化。
已知:反应①单独制备 : ,不能自发进行;
反应②单独脱除 : ,能自发进行。
协同转化装置如图(在电场作用下,双极膜中间层的 解离为 和 ,并向两极迁移)。下列分析错
误的是
A.反应②释放的能量可以用于反应①
B.产生 的电极反应:
C.当生成0.1 mol 时,负极区溶液质量增重9.8 g
D.协同转化总反应:
17.(2023·广东佛山·统考二模)过硫酸铵 可用作氧化剂、漂白剂。利用电解法在两极分别
生产过硫酸铵和过氧化氢的装置如图所示。下列说法错误的是A.a为外接电源的负极
B.电解总反应:
C.阴离子交换膜可用阳离子交换膜替代
D.电解池工作时,I室溶液质量理论上逐渐减小
18.(2023·北京门头沟·统考一模)二氧化氯(ClO ,黄绿色易溶于水的气体)是一种安全稳定、高效低毒的
2
消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备ClO 的原理如下图。
2
下列说法正确的是
A.a极与电源的负极连接
B.X溶液显碱性,在b极区流出的Y溶液是浓盐酸
C.电解池a极上发生的电极反应为 NH -6e- + 3C1- + 4OH- =NCl + 4H O
3 2
D.ClO 发生器内发生的氧化还原反应中,生成的ClO 与NH 的物质的量之比为6:1
2 2 3
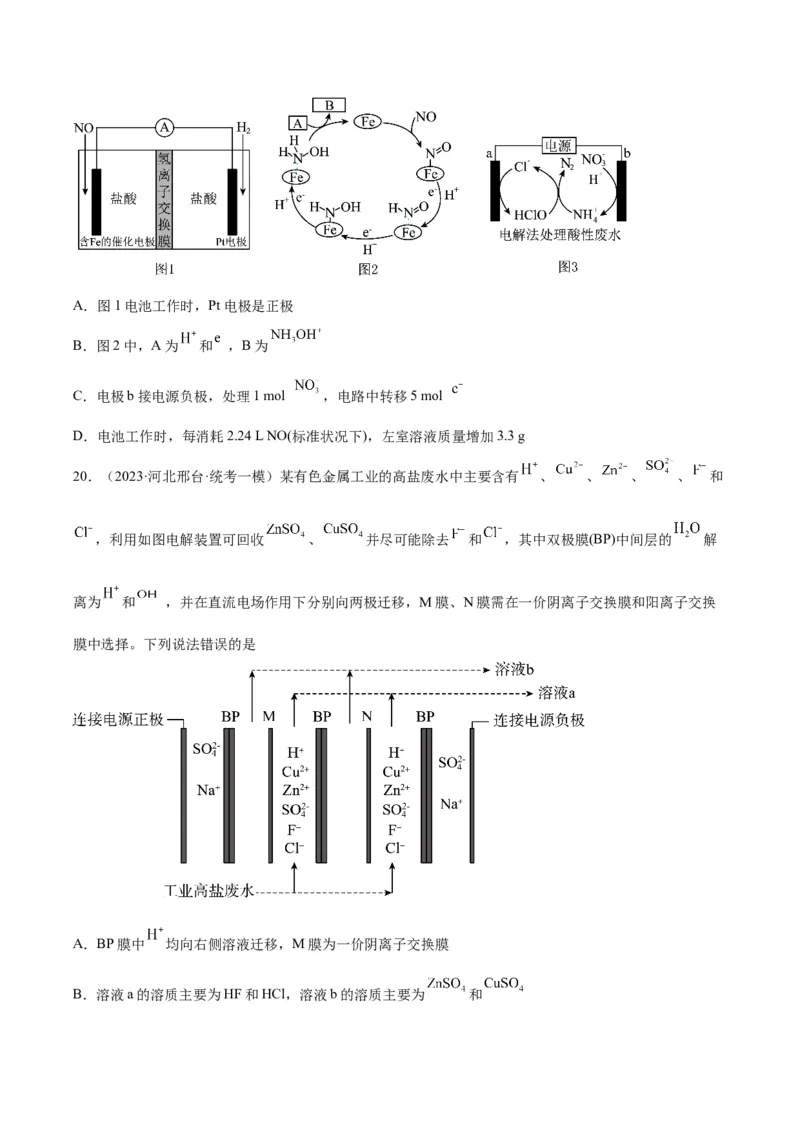
19.(2023·河北保定·统考一模)化学性质类似 的盐酸羟胺( )是一种常见的还原剂和显像
剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用
图1的电池电解处理含有( 、 的酸性废水的装置。下列说法正确的是A.图1电池工作时,Pt电极是正极
B.图2中,A为 和 ,B为
C.电极b接电源负极,处理1 mol ,电路中转移5 mol
D.电池工作时,每消耗2.24 L NO(标准状况下),左室溶液质量增加3.3 g
20.(2023·河北邢台·统考一模)某有色金属工业的高盐废水中主要含有 、 、 、 、 和
,利用如图电解装置可回收 、 并尽可能除去 和 ,其中双极膜(BP)中间层的 解
离为 和 ,并在直流电场作用下分别向两极迁移,M膜、N膜需在一价阴离子交换膜和阳离子交换
膜中选择。下列说法错误的是
A.BP膜中 均向右侧溶液迁移,M膜为一价阴离子交换膜
B.溶液a的溶质主要为HF和HCl,溶液b的溶质主要为 和C.当阳极产生22.4L气体(标准状况)时,有4mol离子通过N膜
D.电解过程中,应控制高盐废水的pH不能过高
21.(2023·辽宁·模拟预测)某团队基于光激发碳纤维上的聚[1,4-二(2-噻吩基)]苯(PDTB)和二氧化钛(
)半导体构建了一种夹心三明治结构的高性能锌-空气电池,该装置利用充放电过程中 与 的相
互转化,能够提升电池的放电电压,降低电池的充电电压,其工作原理如图所示。下列有关说法错误的是
A.该装置可实现光能向电能和化学能的转化
B.电极电势:
C.开关K置于M处时,电子由 极通过导线流向PDTB极
D.开关K置于N处时, 极的电极反应式为
22.(2023·上海闵行·统考二模)国产航母山东舰采用模块制造,然后焊接组装而成。实验室模拟海水和
淡水对焊接金属材料的影响,结果如图所示。下列分析正确的是
A.舰艇被腐蚀是因为形成了电解池
B.甲是海水环境下的腐蚀情况
C.被腐蚀时正极反应式为:Fe-2e→Fe2+
D.焊点附近用锌块打“补丁”延缓腐蚀
23.(2022·河北·高考真题)科学家研制了一种能在较低电压下获得氧气和氢气的电化学装置,工作原理
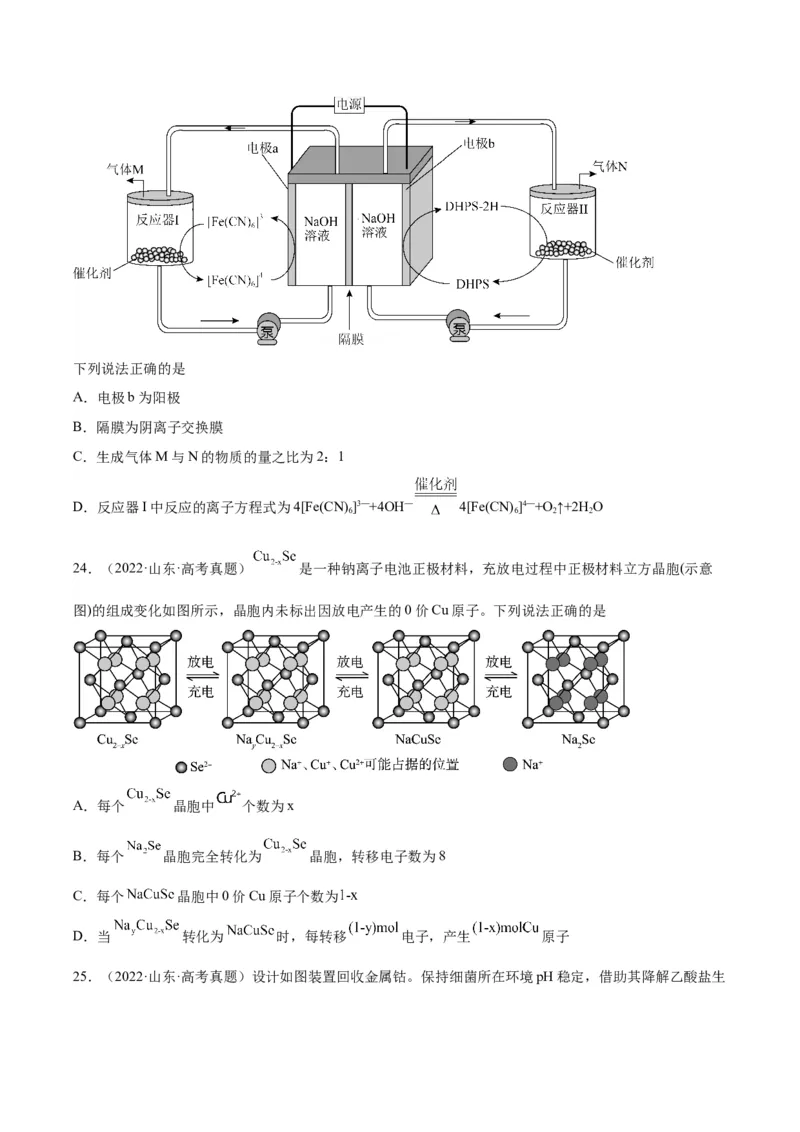
示意图如图。下列说法正确的是
A.电极b为阳极
B.隔膜为阴离子交换膜
C.生成气体M与N的物质的量之比为2:1
D.反应器I中反应的离子方程式为4[Fe(CN) ]3—+4OH— 4[Fe(CN) ]4—+O ↑+2H O
6 6 2 2
24.(2022·山东·高考真题) 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意
图)的组成变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是
A.每个 晶胞中 个数为x
B.每个 晶胞完全转化为 晶胞,转移电子数为8
C.每个 晶胞中0价Cu原子个数为
D.当 转化为 时,每转移 电子,产生 原子
25.(2022·山东·高考真题)设计如图装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成 ,将废旧锂离子电池的正极材料 转化为 ,工作时保持厌氧环境,并定时将乙室溶液
转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法正确的是
A.装置工作时,甲室溶液pH逐渐增大
B.装置工作一段时间后,乙室应补充盐酸
C.乙室电极反应式为
D.若甲室 减少 ,乙室 增加 ,则此时已进行过溶液转移
参考答案
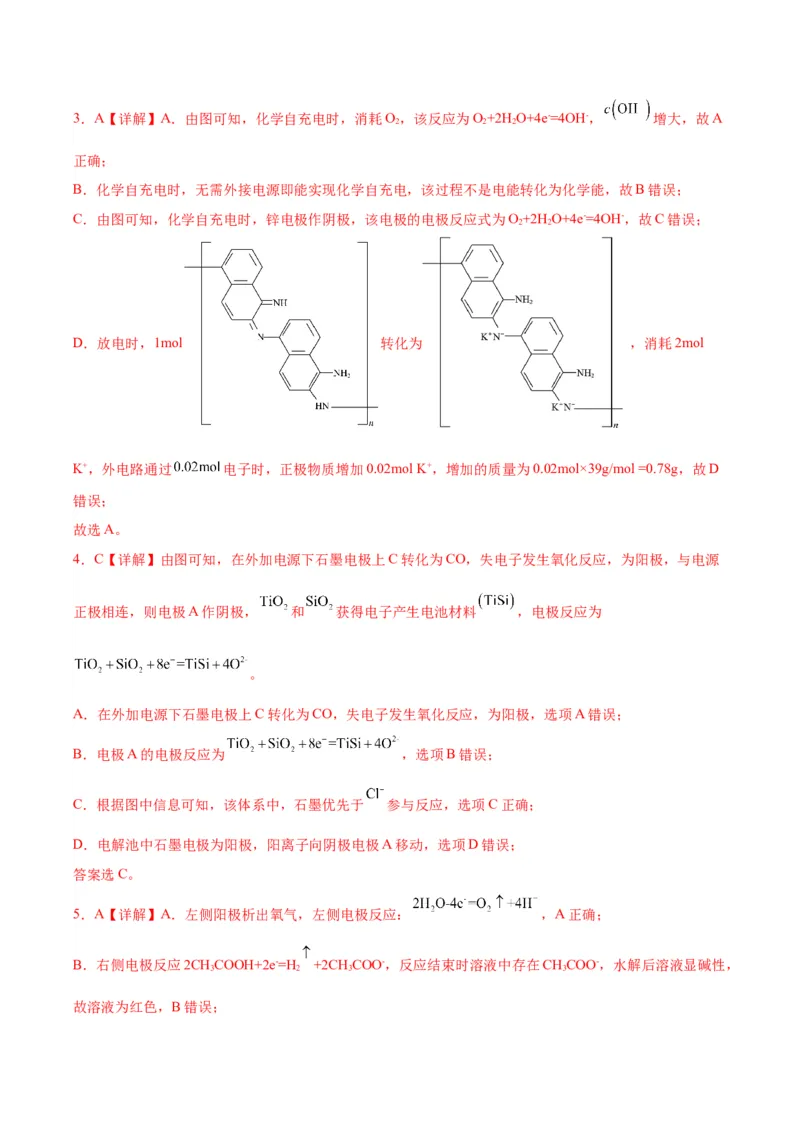
1.B【详解】A.根据实验现象,a'端呈白色,即生成了氯气,即氯离子失去电子,为阳极,即a为正极,
A错误;
B.b'端为阴极,水得到电子放电的同时,生成氢氧根离子,遇石蕊变蓝,B正确;
C.电子从电源的负极出来,即从a极出来,而不是b极,C错误;
D. 如果换成铜棒,铜做阳极放电,现象与碳作电极时不相同,D错误;
故选B。
2.C【详解】A.惰性电极2,Br-被氧化为Br ,惰性电极2为阳极,故A正确;
2
B.WO /WO 循环反应,反应前后WO /WO 数量不变,故B正确;
C.总反应为氧气把二丁基-N-羟基胺氧化为硝酮,1mol二丁基-N-羟基胺失去2molH原子生成1mol硝酮,
氧气最终生成水,根据氧原子守恒,消耗1mol氧气,可得到2mol硝酮,故C错误;
D.外电路通过1mol电子,生成0.5molHO,HO 最终生成水,根据氧原子守恒,可得到1mol水,故D
2 2 2 2
正确;
选C。3.A【详解】A.由图可知,化学自充电时,消耗O,该反应为O+2H O+4e-=4OH-, 增大,故A
2 2 2
正确;
B.化学自充电时,无需外接电源即能实现化学自充电,该过程不是电能转化为化学能,故B错误;
C.由图可知,化学自充电时,锌电极作阴极,该电极的电极反应式为O+2H O+4e-=4OH-,故C错误;
2 2
D.放电时,1mol 转化为 ,消耗2mol
K+,外电路通过 电子时,正极物质增加0.02mol K+,增加的质量为0.02mol×39g/mol =0.78g,故D
错误;
故选A。
4.C【详解】由图可知,在外加电源下石墨电极上C转化为CO,失电子发生氧化反应,为阳极,与电源
正极相连,则电极A作阴极, 和 获得电子产生电池材料 ,电极反应为
。
A.在外加电源下石墨电极上C转化为CO,失电子发生氧化反应,为阳极,选项A错误;
B.电极A的电极反应为 ,选项B错误;
C.根据图中信息可知,该体系中,石墨优先于 参与反应,选项C正确;
D.电解池中石墨电极为阳极,阳离子向阴极电极A移动,选项D错误;
答案选C。
5.A【详解】A.左侧阳极析出氧气,左侧电极反应: ,A正确;
B.右侧电极反应2CHCOOH+2e-=H +2CH COO-,反应结束时溶液中存在CHCOO-,水解后溶液显碱性,
3 2 3 3
故溶液为红色,B错误;C.若c中收集气体 ,若在标况下,c中收集气体的物质的量为0.5×10-3mol,转移电子量为0.5×10-
3mol×4=2×10-3mol,故产生氢气:1×10-3mol,则样品中乙酸浓度为:2×10-3mol ÷10÷10-3= ,并且
题中未给定气体状态不能准确计算,C错误;
D.盐桥换为U形铜导线则不能起到传递离子使溶液呈电中性的效果,影响反应进行,D错误;
答案选A。
6.D【详解】A.石墨电极发生反应的物质:P→ 化合价升高发生氧化反应,所以石墨电极为
4
阳极,对应的电极反应式为: ,则生成 ,理论上外电路需要转
移 电子,A错误;
B.阴极上发生还原反应,应该得电子, 为阳极发生的反应, B错误;
C.石墨电极:P→ 发生氧化反应,为阳极,铂电极为阴极, 应该向阳极移动,即移向石
4
墨电极,C错误;
D.由所给图示可知HCN在阴极放电,产生 和 ,而HCN中的H来自 ,则电解产生的 中的
氢元素来自于 ,D正确;
故选D。
7.A【详解】放电时负极反应: ,正极反应:Cl+2e-=2Cl-,消耗氯
2
气,放电时,阴离子移向负极,充电时阳极:2Cl--2e-=Cl,由此解析。
2
A. 放电时负极失电子,发生氧化反应,电极反应: ,故A正确;
B. 放电时,阴离子移向负极,放电时 透过多孔活性炭电极向NaCl中迁移,故B错误;
C. 放电时每转移 电子,正极:Cl+2e-=2Cl-,理论上 释放 ,故C错误;
2
D. 充电过程中,阳极:2Cl--2e-=Cl,消耗氯离子, 溶液浓度减小,故D错误;
2
故选A。
8.A【详解】由装置可知,b电极的N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,因此
2 3
b为阴极,电极反应式为N+3H O+6e-=2NH+3O2-,a为阳极,电极反应式为2O2--4e-=O ,据此分析解答;
2 2 3 2A.由分析可得,b电极上N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,即N 被还原,
2 3 2
A正确;
B.a为阳极,若金属Ag作a的电极材料,则金属Ag优先失去电子,B错误;
C.改变工作电源的电压,电流强度发生改变,反应速率也会改变,C错误;
D.电解过程中,阴极电极反应式为N+3H O+6e-=2NH+3O2-,阳极电极反应式为2O2-+4e-=O ,因此固体
2 2 3 2
氧化物电解质中O2-不会改变,D错误;
答案选A。
9.C【详解】由实验现象可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生
成亚铁离子、氢气和铜,一段时间后,铜离子在阴极得到电子发生还原反应生成铜;实验②中铜离子与过
量氨水反应生成四氨合铜离子,使得溶液中铜离子浓度比①中要小,电解速率减慢,铜离子在阴极得到电
子缓慢发生还原反应生成铜,在铁表面得到比实验①更致密的镀层。
A.由分析可知,实验①时,铁会先与溶液中的氢离子、铜离子反应,当溶液中氢离子浓度减小,反应和
放电生成的铜覆盖铁电极,阻碍氢离子与铁接触,导致产生的气体减少,故A正确;
B.由分析可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生成亚铁离子、
氢气和铜,可能发生的反应为 ,故B正确;
C.由分析可知,铜离子在阴极得到电子发生还原反应,在阴极析出铜,但阳极发生Cu-2e-=Cu2+的反应,
铜离子浓度不变, 平衡不移动,故C错误;
D.由分析可知,实验②中铜离子与过量氨水反应生成四氨合铜离子,使得溶液中铜离子浓度比①中要小,
电解速率减慢,铜离子在阴极得到电子缓慢发生还原反应生成铜,在铁表面得到比实验①更致密的镀层,
故D正确;
故选C。
10.C【详解】A.由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则电
2
极B为阳极,电极A为阴极,得电子,发生还原反应,A正确;
B.由电解示意图可知,电极B上Mn2+失电子转化为了MnO ,电极反应式为:2HO+Mn2+-2e-
2 2
=MnO+4H+,B正确;
2
C.电极A为阴极, LiMn O 得电子,电极反应式为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失
2 4 2 4 2
电子守恒,电解池总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,
2 4 2 2
C错误;
D.电解池总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,电解结束后,可通过调节溶液pH将锰离
2 4 2 2子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;
答案选C。
11.B【详解】锂海水电池的总反应为2Li+2HO═2LiOH+H ↑, M极上Li失去电子发生氧化反应,则M
2 2
电极为负极,电极反应为Li-e-=Li+,N极为正极,电极反应为2HO+2e-=2OH-+H ↑,同时氧气也可以在N
2 2
极得电子,电极反应为O+4e-+2H O=4OH-。
2 2
A.海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶液,故A正确;
B.由上述分析可知,N为正极,电极反应为2HO+2e-=2OH-+H ↑,和反应O+4e-+2H O=4OH-,故B错误;
2 2 2 2
C.Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传导离子,故C正确;
D.该电池不可充电,属于一次电池,故D正确;
答案选B。
12.C【详解】A.由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电极
b是阳极,故A错误;
B.放电时电极反应和充电时相反,则由放电时电极a的反应为 可
知,NaCl溶液的pH不变,故B错误;
C.放电时负极反应为 ,正极反应为 ,反应后
Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,故C正确;
D.充电时阳极反应为 ,阴极反应为 ,由得失电
子守恒可知,每生成1molCl ,电极a质量理论上增加23g/mol 2mol=46g,故D错误;
2
答案选C。
13.C【详解】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(LiO+2h+=2Li++O ),则充电时总反应为LiO=2Li+O ,结合图示,充电时金属Li电极为阴极,光催化
2 2 2 2 2 2
电极为阳极;则放电时金属Li电极为负极,光催化电极为正极;据此作答。
A.光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳
极反应,充电时电池的总反应为LiO=2Li+O ,A正确;
2 2 2
B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率
与光照产生的电子和空穴量有关,B正确;
C.放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
D.放电时总反应为2Li+O=Li O,正极反应为O+2Li++2e-=Li O,D正确;
2 2 2 2 2 2
答案选C。14.A【详解】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-
+4OH-=Zn(OH) ,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,
2 2 2
由于两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,
因此可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 向Ⅱ区移动,Ⅲ区消耗OH-,
生成Zn(OH) ,Ⅱ区的SO 向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
B.根据分析,Ⅰ区的SO 向Ⅱ区移动,B正确;
C.MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
D.电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O,D正确;
2 2
故答案选A。
15.C【详解】A. 如果玻璃薄膜球内电极的电势低,则该电极为负极、负极发生氧化反应而不是还原反
应,A错误;
B.已知:pH与电池的电动势E存在关系:pH=(E-常数)/0.059,则玻璃膜内外氢离子浓度的差异会引起电
动势的变化,B错误;
C.pH与电池的电动势E存在关系:pH=(E-常数)/0.059,则分别测定含已知pH的标准溶液和未知溶液的
电池的电动势,可得出未知溶液的pH,C正确;
D. pH计工作时,利用原电池原理,则化学能转化为电能,D错误;
答案选C。
16.D【详解】根据电子流向可知,左边电极为负极,电极反应式为SO +4OH--2e-=SO +2H O,右边电极
2 2
为正极,电极反应式为O+2H++2e-=H O。
2 2 2
A.反应②能自发进行,反应放出能量,反应①不能自发进行,需要吸收能量,反应②释放的能量可以用
于反应①,故A正确;
B.由分析可知,O 在右侧电极得到电子生成HO,电极方程式为: ,故B正确;
2 2 2
C.当正极生成0.1 mol 时,得到0.2mol电子,左边电极为负极,电极反应式为SO +4OH--2e-=SO
2+2H O,当得到0.2mol电子时,吸收0.1mol SO ,同时双极膜电离出0.2molOH-进入负极,负极区溶液质
2 2
量增重0.1mol 64g/mol+0.2mol 17g/mol=9.8 g,故C正确;
D.负极电极反应式为SO +4OH--2e-=SO +2H O,正极电极反应为O+2H++2e-=H O,协同转化总反应为:
2 2 2 2 2
,故D错误;
故选D。
17.C【详解】S元素化合价由+6价升高为+7价,化合价升高被氧化,故右侧Pt电极为阳极,b为外接
电源正极,a为外接电源负极,左侧Pt电极为阴极。
A.根据分析,a为外接电源的负极,A正确;
B.根据分析,阴极氧气被还原,阳极硫酸根被氧化,电解总反应正确,B正确;
C.根据阳极产物可知,反应需要消耗硫酸根,阴离子交换膜不可用阳离子交换膜替代,C错误;
D.电解池工作时,I室溶液中氢离子移向阴极,硫酸根移向阳极,消耗硫酸,I室溶液质量理论上逐渐减
小,D正确;
故选C。
18.D【详解】该装置为电解池,a极铵根离子失去电子生成NCl ,则a为阳极,b为阴极,阴极区氢离子
3
得到电子生成氢气,氯离子从右侧经过阴离子交换膜到左侧,在ClO 发生器中NCl 和NaClO 反应生成
2 3 2
NH 和ClO 。
3 2
A.据分析可知,a极为阳极,与电源的正极连接,A错误;
B.在ClO 发生器中,发生反应 ,则X溶液显碱性,b
2
为阴极,阴极区氢离子得到电子生成氢气,氯离子从右侧经过阴离子交换膜到左侧,则在b极区流出的Y
溶液是稀盐酸,B错误;
C.a极铵根离子失去电子生成NCl ,电极反应为 NH -6e- + 3C1-=NCl + 4H+,C错误;
3 3
D.在ClO 发生器中,发生反应 ,生成的ClO 与NH
2 2 3
的物质的量之比为6:1,D正确;
故选D。
19.D【详解】A.铁电极上, ,N元素的化合价降低,为正极,Pt电极上, ,
元素化合价升高,发生氧化反应,为负极,A错误;B.根据题意可知, 与 的性质相似,能与盐酸反应生成 ,所以缺少反应:
,所以图2中,a为 ,B为 ,B错误;
C.电解时,b电极发生: ,发生还原反应,为阴极,接电源的负极,处理1
mol ,电路中转移8mol ,C错误;
D.含铁的催化电极为正极,发生反应: ,4个氢离子中有1个是左侧溶
液中盐酸提供的,3个是右侧迁移的,标况下消耗的 ,左室增加的质量为0.1molNO和
0.3mol氢离子,质量为: ,D正确;
故选D。
20.B【详解】由图可知,最左侧为阳极室,水放电生成氧气和氢离子;最右侧为阴极室,水放电生成氢
气和氢氧根离子;
A.电解池中阳离子向阴极移动,BP膜中 均向右侧溶液迁移;氟离子、氯离子通过M膜向左侧迁移,
故M膜为一价阴离子交换膜,A正确;
B.溶液a中氟离子、氯离子通过M膜向左侧迁移,氢离子与右侧双极膜迁移出来的OH-中和,故反应后
溶液a的溶质主要为 和 ;溶液b的溶质主要为右侧迁移过来的氟离子、氯离子与左侧前过来
的氢离子生成的为HF和HCl,B错误;
C.阳极反应为 ,当阳极产生22.4L气体(标准状况下为1mol)时,根据电子守恒可知,
有4mol离子通过N膜,C正确;
D.电解过程中,若pH过高则会导致锌离子、铜离子转化为沉淀,故应控制高盐废水的pH不能过高,D
正确;
故选B。
21.B【详解】A.由图可知,开关K置于M处时,该装置为原电池,需要利用光能,开关K置于N处时,
该装置为电解池,也需要光能,则该装置可实现光能向电能和化学能的转化,选项A正确;B.原电池中正极的电势大于负极,则电极电势: ,电解池中阳极的电势大于阴极,则电
极电势: ,选项B错误;
C.原电池工作时,电子由负极通过导线流向正极,则开关K置于M处时,电子由 极通过导线流
向 极,选项C正确;
D.开关K置于N处时,该装置为电解池, 极为阴极,其电极反应式为 ,
选项D正确;
答案选B。
22.D【详解】A.由图可知,舰艇腐蚀是形成原电池,加快反应速率,A错误;
B.海水环境下电解质浓度较大,腐蚀更严重,乙是在海水环境下的腐蚀情况,B错误;
C.两种环境下,正极反应式为 ,C错误;
D.锌可以和铁形成原电池,但是此时锌为负极,保护了舰体不被腐蚀,D正确;
故选D。
23.BD【详解】由图可知,a电极为阳极,碱性条件下[Fe(CN) ]4—离子在阳极失去电子发生氧化反应生成
6
[Fe(CN) ]3—离子,催化剂作用下,[Fe(CN) ]3—离子与氢氧根离子反应生成[Fe(CN) ]4—离子、氧气和水,b电
6 6 6
极为阴极,水分子作用下DHPS在阴极得到电子发生还原反应生成DHPS—2H和氢氧根离子,催化剂作用
下,DHPS—2H与水反应生成DHPS和氢气,氢氧根离子通过阴离子交换膜由阴极室向阳极室移动,则M
为氧气、N为氢气。
A.由分析可知,b电极为电解池的阴极,故A错误;
B.由分析可知,氢氧根离子通过阴离子交换膜由阴极室向阳极室移动,则隔膜为阴离子交换膜,故B正
确;
C.由分析可知,M为氧气、N为氢气,由得失电子数目守恒可知,氧气和氢气的的物质的量之比为1:
2,故C错误;
D.由分析可知,反应器I中发生的反应为催化剂作用下,[Fe(CN) ]3—离子与氢氧根离子反应生成
6
[Fe(CN) ]4—离子、氧气和水,反应的离子方程式为4[Fe(CN) ]3—+4OH— 4[Fe(CN) ]4—
6 6 6
+O ↑+2H O,故D正确;
2 2
故选BD。24.BD【详解】A.由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,位于体内的铜离子
和亚铜离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化合价代
数和为0可得2a+b=4×2,解得a=4x,故A错误;
B.由题意可知,NaSe转化为Cu Se的电极反应式为NaSe-2e-+(2-x)Cu=Cu Se+2Na+,由晶胞结构可知,
2 2-x 2 2-x
位于顶点和面心的硒离子个数为8× +6× =4,则每个晶胞中含有4个NaSe,转移电子数为8,故B正确;
2
C.由题意可知,Cu Se转化为NaCuSe的电极反应式为Cu Se+ e-+Na+=NaCuSe+(1-x)Cu,由晶胞结构可
2-x 2-x
知,位于顶点和面心的硒离子个数为8× +6× =4,则每个晶胞中含有4个NaCuSe,晶胞中0价铜而个数
为(4-4x),故C错误;
D.由题意可知,NaCu Se转化为NaCuSe的电极反应式为NaCu Se+(1-y) e-+(1-y) Na+=NaCuSe+(1-
y 2-x y 2-x
x)Cu,所以每转移(1-y)电子,产生(1-x)mol铜,故D正确;
故选BD。
25.BD【详解】A.电池工作时,甲室中细菌上乙酸盐的阴离子失去电子被氧化为CO 气体,同时生成
2
H+,电极反应式为CHCOO--8 e-+2 H O =2CO ↑+7 H+,H+通过阳膜进入阴极室,甲室的电极反应式为Co2+
3 2 2
+2e-=Co,因此,甲室溶液pH逐渐减小,A错误;
B.对于乙室,正极上LiCoO 得到电子,被还原为C o2+,同时得到Li+,其中的O2-与溶液中的H+结合
2
HO,电极反应式为2LiCoO +2e-+8H+=2Li++2Co2++4H O,负极发生的反应为CHCOO--8 e-+2 H O
2 2 2 3 2
=2CO ↑+7 H+,负极产生的H+通过阳膜进入正极室,但是乙室的H+浓度仍然是减小的,因此电池工作一段
2
时间后应该补充盐酸,B正确;
C.电解质溶液为酸性,不可能大量存在OH-,乙室电极反应式为:LiCoO +e-+4H+=Li++Co2++2H O,C错
2 2
误;
D.若甲室Co2+减少200 mg,则电子转移物质的量为n(e-)= ;若乙室Co2+增加300
mg,则转移电子的物质的量为n(e-)= ,由于电子转移的物质的量不等,说明此时已
进行过溶液转移,即将乙室部分溶液转移至甲室,D正确;
故合理选项是BD。