文档内容
(2)反应热的计算—高一化学人教版暑假作业本
1.盖斯定律:不管化学反应是一步完成还是分几步完成,其反应热是相同的。即反应热只有
反应的始态与终态有关,而与反应途径无关。
2.催化剂不会改变反应吸热或放热多少,只是降低了反应的活化能,使反应更容易进行。
3.反应热计算的常见方法:
①应用盖斯定律——“三调一加”
一调:根据目标的热化学方程式,调整已知热化学方程式中的反应物或生成物的位置,改写
已知的热化学方程式。
二调:根据改写的热化学方程式调整相应>∆H符号。
三调:调整中间物质的化学计量系数。
一加:将调整好的热化学方程式及其∆H进行加合。
②根据反应物和生成物的能量计算
1′∆H=E −E
生成物的总能量 反应物的总能量
2′根据燃烧热Q =n ×∆H
放 (可燃物)
③根据反应物和生成物的键能:∆H=E −E
反应物的键能之和 生成物的键能之和
13.配位化合物的形成条件 ①配体有孤电子对 ②中心离子有空轨道
14.在配合物中,中心离子与配体的配位原子间以配位键相结合,配合物的内界与外界之间
以离子键相结合。
15.在水溶液中,配合物易电离出外界离子,而配离子难电离;配合物中配位键越强,配合
物越稳定。
1.已知:下列关于上述反应焓变的判断正确的是( )
A. B.
C. D.
2.在298K、100kPa时,已知:
则 与 和 间的关系正确的是( )
A. = +2 B. = +
C. = -2 D. = -
3.二氧化碳加氢制甲醇的总反应可表示为: ,该反
应一般认为通过如下步骤来实现:
①
②
若反应①为慢反应,下图中能体现上述反应能量变化的是( )
A. B.C. D.
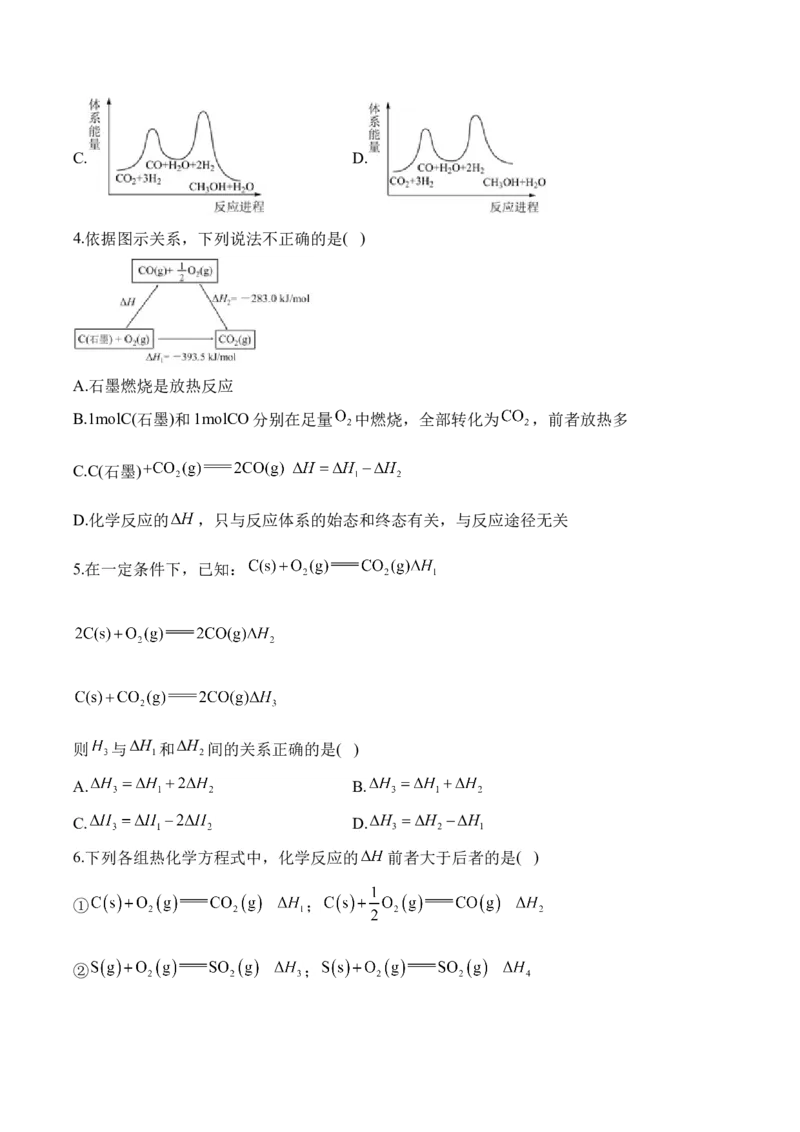
4.依据图示关系,下列说法不正确的是( )
A.石墨燃烧是放热反应
B.1molC(石墨)和1molCO分别在足量 中燃烧,全部转化为 ,前者放热多
C.C(石墨)
D.化学反应的 ,只与反应体系的始态和终态有关,与反应途径无关
5.在一定条件下,已知:
则 与H 和H 间的关系正确的是( )
1 2
A. B.
C. D.H H H
3 2 1
6.下列各组热化学方程式中,化学反应的 前者大于后者的是( )
① ;
② ;③ ;
④ ;
A.①② B.②④ C.③④ D.①③
7.下列说法正确的是( )
A.已知C(石墨,s) C(金刚石,s)H 1.9kJmol1,则金刚石比石墨稳定
B.已知2C(s)2O (g) 2CO (g)H ,2C(s)O (g) 2CO(g)H ,则
2 2 1 2 2
H H
1 2
C.氢气的燃烧热为285.8kJmol1,则表示氢气燃烧热的热化学方程式为
1
H (g) O (g) H O(g)H 285.8kJmol1
2 2 2 2
D.在一定条件下,将1molSO (g)和0.5molO (g)置于密闭容器中充分反应,放出热量79.2 kJ,
2 2
则该反应的热化学方程式为2SO (g)O (g)2SO (g)H 158.4kJmol1
2 2 3
8.下列各组热化学方程式中,化学反应的H 前者小于后者的是( )
①S(g)O (g) SO (g);S(s)O (g) SO (g)
2 2 2 2
1
②C(s) O (g) CO(g);C(s)O (g) CO (g)
2 2 2 2
③2KOH(aq)H SO 浓 K SO (aq)2H O1
2 4 2 4 2
2KOH(aq)H SO (aq) K SO (aq)2H O1
2 4 2 4 2
1
④2H (g)O (g) 2H O1;H (g) O (g) H O1
2 2 2 2 2 2 2
A.①③④ B.②③④ C.①②③ D.①②③④
9.已知断开1molH-H键吸收的能量为436kJ,形成1molH-N键放出的能量为391kJ,根据化学
高温、高压
方程式:N 3H 2NH ,反应完1molN 该反应放出的能量为92.4kJ,则断开
2 2催化剂 3 21molN N键需吸收的能量是( )
A.431kJ B.945.6kJ C.649kJ D.869kJ
10.已知:1mol 与0.5mol 完全燃烧生成1mol (g)时放出241.8kJ热量,有关键能数
据如下:
化学键 H—O O=O
键能/( ) 463.4 498
则H—H键键能为( )
A.436 B.557 C.221.6kJmol1 D.413kJmol1
11.已知: 。若断裂1molN≡N、1molN-H需要
吸收的能量分别为945.6kJ、391kJ,则断裂1molH-H需要吸收的能量是( )
A.618.4kJ B.436kJ C.256kJ D.1308kJ
12.单质硫在蒸气状态时,含有 、 、 及 等多种同素异形体,其中 的结构如图所
示,已知断开 键需要的能量为 ,断开 键需要的能量为 ,根据以
上信息和数据,判断下列热化学方程式正确的是( )
A.4S S ΔH (4a8b)kJmol1
2 8
1
B.S (g) S (g) ΔH (a2b)kJ
2 4 8
1
C.S (g) S (g) ΔH (2ba)kJmol1
2 4 8
D.4S (g) S (g) ΔH (4a8b)kJmol1
2 8
13.根据如下能量关系示意图,下列说法正确的是( )A. 与 的能量之和为393.5kJ
B.反应 中,生成物的总能量大于反应物的总能量
C.由 的热化学方程式为:
D.热值指一定条件下1g物质完全燃烧所放出的热量,则 热值
14.100 0.200 溶液与1.95g锌粉在量热计中充分反应。测得反应前温度为
20.1℃,反应后最高温度为30.1℃。
已知:反应前后,溶液的比热容均近似为4.18 、溶液的密度均近似为1.00 ,
忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量 _____________J。
(2)反应 的 _____________
15.随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问
题,如何降低大气中 的含量及有效地开发利用 引起了全世界的普遍重视。
(1)把煤作为燃料可通过下列两种途径:
途径Ⅰ: ①
途径Ⅱ:先制成水煤气: ②
再燃烧水煤气: ③
④则途径Ⅰ放出的热量___________(填“大于”“等于”或“小于”)途径Ⅱ放出的热量;
的数学关系式是___________。
(2)在25℃、101kPa下,1克甲醇完全燃料放热22.68kJ,写出甲醇燃烧热的热化学方程式
___________。
(3)已知①
②
③
试计算④ 的ΔH=___________。
(4)臭氧可用于净化空气、饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、
金、铱、氟以外 所有单质反应。如:
的
已 知 : ; 则 转 化 为 的 热 化 学 方 程 式 为
___________。
答案以及解析
1.答案:D
2.答案:A
解析:①
②
③则由盖斯定律可知,反应③=①+2×②, = +2 ,故选A。
3.答案:A
解析:由盖斯定律可知,反应①十反应②得总反应方程式,则总反应的
,则该总反应是放热反应,生成物的总能量比反应物的总能量
低,B、D错误;反应①为慢反应,是总反应的决速步骤,则反应①的活化能比反应②的大,
A正确,C错误;答案选A。
4.答案:C
解析:A.所有的燃烧都是放热反应,根据图示,
C(石墨)O (g) CO (g)H 393.5kJ/mol, ,则石墨燃烧是放热反应,故A正
2 2 1
确;
B.根据图示,C(石墨) O (g) CO (g)H 393.5kJ/mol,
2 2 1
,根据反应可知都是放热反应,1mol
C(石墨)和1molCO分别在足量 中燃烧,全部转化为CO ,1mol 放热多,故B正
2
确;
C.根据B项分析,① ,②
,根据盖斯定律①-②×2可得:
,故C错误;
D.根据盖斯定律可知,化学反应的焓变只与反应体系的始态和终态有关,与反应途径无关,
故D正确;
故选C。
5.答案:D
解析:根据盖斯定律,反应③可由反应②—反应①得到,所以 = - ,故本题正确答
案 为D。6.答案:C
解析:碳完全燃烧放出的热量多,但放热越多, 越小,所以①中 前者小于后者;②中
都是中和热, 相等;消耗的氢气越多,放出的热量越多,同样放热越多, 越小,所以
③中 前者大于后者;④中前者是吸热反应,后者是放热反应, 前者大于后者,答案选
C。
7.答案:B
解析:B.已知 前者完全反应,放
出的热量多,焓变反而小,则 ,故B正确;
答案为B。
8.答案:A
解析:放热反应中 <0,放出热量越多, 越小。①由于S(g)→S(s)放热,则前者
放出的热量多,H H ,正确;②后者完全反应,放出的热量多,H H ,
前者 后者 前者 后者
错误;③浓硫酸稀释放热,H H ,正确;④消耗的氢气越多,放出的热量越多,
前者 后者
H H
,正确。故选A。
前者 后者
9.答案:B
10.答案:A
解析:已知:1mol 与0.5mol 完全燃烧生成1mol (g)时放出241.8kJ热量,则2mol
与1mol 完全燃烧生成2mol (g)时放出483.6kJ热量,
,设H—H键键能为a,反应焓变等于反应物的
键能和减去生成物的键能和,则 ,
;
故选A。
11.答案:B
解析:化学反应的过程就是原子重新组合的过程,在这个过程中要断裂反应物化学键,同时
形成生成物的化学键。反应热等于断裂反应物化学键吸收的总能量与形成生成物化学键释放
的总能量的差,则[945.6kJ+3×E(H-H)]-6×391kJ=-92.4kJ,解得E(H-H)=436kJ,故合理选项是
B。
12.答案:D解析:由 的结构知, 分子中含有8 mol S—S键。反应 的 反应
物的键能总和一生成物的键能总和 ,D项正确。
13.答案:D
14.答案:(1)
(2)−209
解析:(1)由于反应前后溶液的密度均近似为 ,忽略溶液体积和质量的变化,故
溶液反应前后的质量 。又知溶液比热容近似为 ,
所以该反应放出的热量
。
(2)Zn和 的物质的量分别为
,根据关系式
可知,Zn过量, 完全反应,即 与Zn完全反应放出
的热量,得
。
15.(1)答案: 等于;
(2)答案:
(3)答案: -339.2kJ/mol
(4)答案: