文档内容
第 1 讲 物质的分类
Part 1 物质分类的方法
知识精讲
( )
例1:(2020•合肥市期中)下列物质属于纯净物的是
A.空气 B.盐酸 C.粗盐 D.冰水混合物
【考点】物质的分类
【答案】D
【解析】A.空气中含有氧气、氮气、二氧化碳、稀有气体等物质,属于混合物,
故A错误;
B.盐酸是氯化氢的水溶液,属于混合物,故B错误;
C.粗盐主要成分是氯化钠,还含沙子,钙离子,镁离子等物质,故C错误;
D.冰水混合物是由水这一种物质组成,属于纯净物,故D正确。故选:D
例2:(2020•金水区期中)一瓶气体经过检验只含有一种元素,则该气体( )
A.只能是一种单质
B.不可能是混合物
C.可能含有化合物
D.可能是一种单质,也可能是几种单质组成的混合物
【考点】物质的分类
【答案】D
【解析】氧气中只有氧元素一种元素,则氧气属于单质,属于纯净物的范畴,而
氧气和臭氧的混合物中,也是只有一种氧元素,所以仅含一种元素的物质可能是
一种单质或纯净物,也可能是混合物。故选:D。
例3:天然气的主要成分是甲烷,还含有硫化氢、氰化氢等气体。你认为天然气
第1页(共14页)( )
是
A.一种纯净物
B.全部由无机化合物组成的混合物
C.全部由有机化合物组成的混合物
D.由无机化合物和有机化合物组成的混合物
【考点】物质的分类
【答案】D
【解析】A.天然气是一种多组分的混合气体,主要成分是甲烷,故 A项错误;
B.天然气的主要成分甲烷为有机物,故 B项错误;
C.H S、HCN为无机物,故 C 项错误;
2
D.天然气是由无机化合物和有机化合物组成的一种多组分的混合气体,故 D项
正确。
故选:D
例4:下列关于物质分类的叙述不正确的是( )
A.HNO 属于酸
3
B.Mg(OH) 属于碱
2
C.SO 属于氧化物
2
D.液氯属于混合物
【考点】物质的分类
【答案】D
【解析】选项A:HNO 在水溶液中电离生成氢离子和硝酸根离子,属于酸,故
3
A项正确;
选项B:Mg(OH) 由镁离子和氢氧根离子构成,属于碱,故 B项正确;
2
选项C:SO 由S、O元素组成,属于氧化物,故 C 项正确;
2
选项D:液氯是液态氯气,由一种物质组成,属于单质,是纯净物,故 D项错
误;
第2页(共14页)故选:D。
典型例题
【例 01】★☆☆☆☆
Na CO Na SO K CO K SO
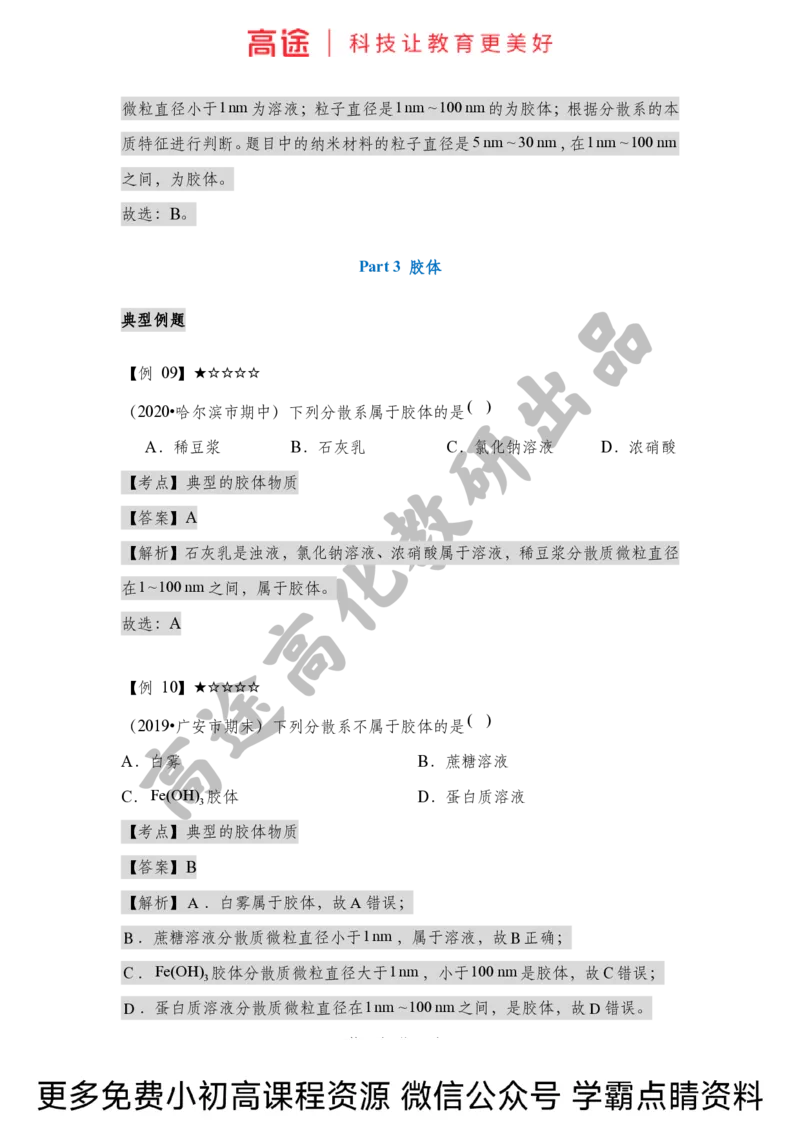
(2020•哈尔滨市期末)如图所示是对 2 3、 2 4、 2 3、 2 4四种物
质进行的分类,这种分类方法的名称是( )
A.交叉分类法 B.树状分类法 C.圈图法 D.链状箭头法
【考点】物质的分类方法
【答案】A
【解析】交叉分类法是对同一化学物质或化学反应采用不同的“标准”进行分类,
Na CO
这种分类方法有利于我们获得更多的信息。例如,对于 2 3,从组成的阳离
子来看,其属于钠盐,而从组成的阴离子来看,其又属于碳酸盐。可以看到,从
Na CO
不同的角度分类, 2 3属于不同的类别,出现了交叉现象,其他三种物质亦
然。因此题述分类方法属于交叉分类法。
故选:A
【例 02】★☆☆☆☆
( )
(2016•浙江卷)下列属于酸的是
A.H SO B.CO C.NaCl D.NaOH
2 4 2
【考点】物质的分类
【答案】A
【解析】酸是指电离时产生的阳离子全部是氢离子的化合物,则选项 A正确。
第3页(共14页)故选:A
【例 03】★★☆☆☆
物质的分类是化学研究的重要方法之一,化学工作者经常根据物质的组成对物质
C O
进行分类研究。近年来发现,在金星的大气层中存在三氧化二碳( 2 3 )。下
列物质与它属于同类的是( )
A.石墨、氧气
B.H O、N O
2 2 4
C.H SO 、HClO
2 4
D.NaCl、Na CO
2 3
【考点】物质的分类
【答案】B
【解析】选项A:石墨、氧气是由同种元素组成的纯净物属于单质,故选项 A
错误;
选项B:H O、N O 是两种元素组成,其中一种是氧元素的化合物,属于氧化
2 2 4
物,与三氧化二碳属于同类物质,故选项 B正确;
选项C:H SO 、HClO 是电离时生成的阳离子全部是氢离子的化合物,属于酸,
2 4
故选项C 错误;
选项D:NaCl、Na CO 是由金属离子和酸根离子组成的化合物,属于盐,故选
2 3
项D错误。
故选:B
【例 04】★★☆☆☆
(2019•哈尔滨市期末)如将物质按照单质、氧化物、酸、碱、盐分类,下列各
( )
组物质中,类别相同的是
A.氧气、氧化镁、四氯化碳、水
B.硫酸铜、氯化钠、碳酸钙、硫化钾
第4页(共14页)C.硫酸、碳酸钠、氯化镁、氧化钠
D.硝酸银、氢氧化钠、醋酸钠、氯化钾
【考点】物质的分类
【答案】B
【解析】选项A:氧气是单质;氧化镁和水是氧化物;四氯化碳是氯化物,它们
的分类不同,故A 项错误;
选项B:硫酸铜、氯化钠、碳酸钙、硫化钾都是盐,种类相同,故 B 项正确;
选项C:硫酸是酸;碳酸钠、氯化镁是盐;氧化钠是氧化物,物质的分类不同,
故C 项错误;
选项D:硝酸银、醋酸钠、氯化钾是盐,氢氧化钠是碱,物质的分类不同,故 D
项错误;
故选:B
【例 05】★★☆☆☆
下列有关物质分类标准和分类均正确的是( )
A B C D
CaO、MgO、 H 、Cl 、 O 、Fe 、 HCl 、H O 、
2 2 2 2
物质
CO 、CuO N 、Cu Cu 、Zn H SO 、HNO
2 2 2 4 3
分类标准 金属氧化物 金属单质 金属单质 含氧酸
不属于该类别
CuO Cu O HCl
2
的物质
【考点】物质的分类
【答案】C
【解析】选项A:金属氧化物有两种元素,一种是金属元素,一种是氧元素,非
金属氧化物也有两种元素,一种是非金属元素,一种是氧元素,所以CaO、MgO、
CuO是金属氧化物,CO 是非金属氧化物,故 A错误;
2
第5页(共14页)选项B:非金属单质是由非金属元素组成的,一般的单质带金字旁的是金属,带
气字头的是气态单质,带石字旁、三点水旁的是固态或液态非金属,所以H 、Cl 、
2 2
N 是非金属单质,Cu 是金属单质,故B错误;
2
选项C:O 是非金属单质, Fe 、Cu 、Zn 属于金属单质,故 C 正确;
2
选项D:酸是指电离时产生的阳离子全部是氢离子的化合物,含有氧元素的酸是
含氧酸, H SO 、HNO 为含氧酸,HCl为无氧酸,H O属于氧化物。故 D项
2 4 3 2
错误。
故选:C。
Part 2混合物的分类——分散系
典型例题
【例 06】★☆☆☆☆
( )
(2019•开平市期末)下列有关说法正确的是
A.氯化钠溶液均一、稳定、透明,不是分散系
B.冰水混合物是一种分散系
C.分散系有的是纯净物有的是混合物
D.分散系都是混合物,按分散质和分散剂所处的状态,分散系的组合有 9种方
式
【考点】分散系的种类和特点
【答案】D
【解析】A.氯化钠溶液均一、稳定、透明,是氯化钠和水形成的分散系,故 A
错误;
B.冰水是纯净物,不是分散系,故 B错误;
C.分散系都是混合物,故 C 错误;
D.分散质为固体、液体、气体,分散剂为固体、液体、气体,组合分析,分散
系的组合有9种方式,故 D正确。故选:D
第6页(共14页)【例 07】★☆☆☆☆
( )
(2020•贵定期末)下列关于分散系的说法不正确的是
A.分散系的稳定性:溶液 胶体 浊液
B.分散质粒子的大小:溶液 胶体 浊液
C.分散质粒子的直径为几纳米或几十纳米的分散系是胶体
D.可以用过滤的方法将悬浊液中的分散质从分散剂中分离出来
【考点】分散系的种类和特点
【答案】B
【解析】A.溶液均一稳定,胶体具有介稳性,浊液不能稳定存在,所以分散系
的稳定性:溶液 胶体 浊液,故A项正确;
B.浊液分散质粒子直径 100nm,胶体分散质粒子直径1nm~100nm,溶液分
散质粒子直径 1nm,分散质粒子的大小: 浊液 胶体 溶液,故B项错误;
C.胶体分散质粒子直径在1nm~100nm,分散质粒子的直径为几纳米或几十纳
米的分散系是胶体,故 C 项正确;
D.悬浊液中有不能溶解的固体颗粒,可以用过滤的方法将悬浊液中的分散质从
分散剂中分离出来,故 D项正确。故选:B
【例 08】★☆☆☆☆
(2019•旅顺口区期末) 2008年北京“奥运标准线”中重要组成部分﹣﹣运通104
路是北京首条“无菌”公交路线。公交车上采用了一种纳米材料清洁技术,这种纳
5nm~30nm
米材料的粒子直径是 ,若将这种纳米材料分散到液体分散剂中,下
( )
列各组混合物和该分散系具有相同数量级的是
A.溶液 B.胶体 C.悬浊液 D.乳浊液
【考点】分散系的种类和特点
【答案】B
【解析】分散系的区别是分散质的微粒直径大小,微粒直径大于100nm是浊液;
第7页(共14页)微粒直径小于1nm为溶液;粒子直径是1nm~100nm的为胶体;根据分散系的本
质特征进行判断。题目中的纳米材料的粒子直径是5nm~30nm,在1nm~100nm
之间,为胶体。
故选:B。
Part 3 胶体
典型例题
【例 09】★☆☆☆☆
( )
(2020•哈尔滨市期中)下列分散系属于胶体的是
A.稀豆浆 B.石灰乳 C.氯化钠溶液 D.浓硝酸
【考点】典型的胶体物质
【答案】A
【解析】石灰乳是浊液,氯化钠溶液、浓硝酸属于溶液,稀豆浆分散质微粒直径
在1~100nm之间,属于胶体。
故选:A
【例 10】★☆☆☆☆
( )
(2019•广安市期末)下列分散系不属于胶体的是
A.白雾 B.蔗糖溶液
C.Fe(OH) 胶体 D.蛋白质溶液
3
【考点】典型的胶体物质
【答案】B
【解析】A.白雾属于胶体,故A错误;
B.蔗糖溶液分散质微粒直径小于1nm,属于溶液,故B正确;
C.Fe(OH) 胶体分散质微粒直径大于1nm,小于100nm是胶体,故C错误;
3
D.蛋白质溶液分散质微粒直径在1nm~100nm之间,是胶体,故D错误。
第8页(共14页)故选:B
【例 11】★★☆☆☆
下列关于胶体的叙述中,不正确的是( )
...
A.用半透膜除去淀粉胶体中的NaCl
B.胶体中分散质粒子的直径小于1nm
C.丁达尔效应可以区分溶液和胶体
D.胶体粒子可以透过滤纸
【考点】胶体的性质
【答案】B
【解析】选项A:胶体中分散质粒子不能透过半透膜,小分子、离子能透过半透
膜,用半透膜除去淀粉胶体中的NaCl,方法为渗析法;故 A项正确;
选项B:胶体中分散质粒子的直径介于1-100nm之间,故B项错误;
选项C:丁达尔效应是胶体特有的性质,可用来区分胶体和溶液,故 C 项正确。
选项D:胶体中分散质粒子和溶液中溶质粒子都能透过滤纸,不能用滤纸分离,
故D项正确。
故选:B
【例 12】★★☆☆☆
(2020•洛阳市期中)下列关于胶体的叙述中,不正确的是( )
A.向胶体中加入蔗糖溶液,产生聚沉现象
B.可见光透过胶体时,发生丁达尔现象
C.用渗析的方法“净化”胶体时,使用的半透膜只能让分子、离子通过
D.胶体能吸附阳离子或阴离子,故在电场作用下会产生电泳现象
【考点】胶体的性质
【答案】A
【解析】选项A:向胶体加入电解质溶液会产生聚沉现象,蔗糖溶液不是电解质
第9页(共14页)溶液,故A错误;
选项B:胶体具有丁达尔效应,即可见光透过胶体时,出现一条光亮的通路,故
B正确;
选项C:半透膜只允许小分子、离子通过,大分子通不过,通常用渗析的方法分
离和提纯胶体,故 C 正确;
选项D:大多数胶体中的胶粒可以吸附电荷,在外加电场的作用下发生定向运动,
故D正确;故选:A
【例 13】★★☆☆☆
( )
(2020•黄山市期末)下列有关胶体的说法不正确的是
...
A.Fe(OH) 胶体制好后可以用渗析的方法进一步净化
3
B.电泳现象可以证明胶体都带电
C.利用丁达尔效应可以区分溶液和胶体
D.由于胶粒之间有排斥作用,胶粒不易聚集成大的颗粒,这是胶体具有介稳性
的主要原因
【考点】胶体的性质
【答案】B
【解析】A.制备出的氢氧化铁胶体中混有氢离子和氯离子,而胶粒不能透过半
透膜,离子可以透过半透膜,故可以用渗析的方法来提纯制得的氢氧化铁胶体,
故A正确;
B.胶体不带电,胶粒吸附带电粒子带电,故 B错误;
C.丁达尔效应是胶体所特有的性质,溶液没有,故可以用丁达尔效应来区分溶
液和胶体,故C 正确;
D.由于同种电荷的静电排斥作用,胶体相对比较稳定,故 D正确。故选:B
【例 14】★☆☆☆☆
( )
(2019•咸阳市期中)下列关于溶液和胶体的叙述,正确的是
第10页(共14页)A.溶液是电中性的,胶体是带电的
B.一束光线分别通过溶液和胶体时,后者会出现明显光带,前者则没有
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运
动
D.通电时,溶液中的溶质粒子不会向两极移动,胶体的分散质粒子向某一极移
动
【考点】胶体的性质
【答案】B
【解析】A.胶体微粒吸附带电离子,胶体分散系是电中性的,故 A错误;
B.丁达尔效应是胶体特有性质,故 B正确;
C.溶液中溶质微粒不断无规律的运动,故 C 错误;
D.通电时,溶液中阳离子移向阴极,阴离子移向阳极。胶体微粒移向某一电极
发生电泳现象。故 D错误。
故选:B
知识精讲
( )
例:(2020•江门市期中)胶体与溶液的本质区别是
A.能否产生丁达尔效应
B.能否稳定存在
C.分散质粒子直径大小不同
D.分散剂不同
【考点】胶体的性质
【答案】C
【解析】胶体和溶液的本质区别是分散质粒子直径的大小不同,故选:C。
第11页(共14页)典型例题
【例 15】★★☆☆☆
( )
(2020•昌吉市期中)有关胶体的认识不正确的是
A.FeCl 饱和溶液滴入沸水可制得胶体
3
B.胶体粒子直径在1~100 nm之间
C.胶体粒子可以透过滤纸
D.是否有丁达尔现象是胶体和溶液的本质区别
【考点】胶体的性质及制备
【答案】D
【解析】A.向沸水中滴饱和氯化铁溶液制备胶体,故 A项正确;
B.溶液分散质微粒直径小于1nm,胶体分散质微粒直径介于1~100nm之间,浊
液分散质微粒直径大于100nm,故B项正确;
C.胶体粒子直径在1~100nm之间,胶体粒子直径较大,可通过滤纸,故 C 项
正确;
D.当光束通过胶体时,可看到一条光亮的“通路”,这种现象称为丁达尔效应,
溶液没有,可鉴别胶体和溶液,但胶体和溶液的本质区别是分散质微粒直径大小,
故D项错误。故选:D
【例16】★★☆☆☆
FeCl Na SiO
(2020•南岗区期末)已知有三种溶液: 3的浓溶液、 2 3溶液、稀盐酸,
现有下列说法:
① 将FeCl 溶液滴入冷水中,边滴边振荡,便可制得Fe(OH) 胶体;
3 3
② 已知向稀盐酸中滴加硅酸钠溶液可制得硅酸胶体,那么此分散系中的分散质
微粒直径大小在1~100 nm之间;
③ 用光照射硅酸胶体时,胶体微粒会使光发生散射;
④ FeCl 溶液和Fe(OH) 胶体都能透过滤纸;
3 3
第12页(共14页)⑤ 胶体、溶液和浊液属于不同的分散系,其中胶体最稳定;
⑥ 往Fe(OH) 胶体中加入盐酸,先沉淀后消失。
3
其中正确的是( )
A.① ④ ⑥
B.② ③ ⑤
C.② ③ ④ ⑥
D.① ② ③ ④ ⑤ ⑥
【考点】胶体的性质及制备
【答案】C
【解析】① 将FeCl 溶液滴入沸水中,并继续煮沸至生成红褐色液体,故① 错
3
误;
② 向稀盐酸中滴加硅酸钠溶液可制得硅酸胶体,胶体粒子的直径大小在
1~100 nm之间,故② 正确;
③ 胶体的丁达尔现象是由于光发生散射形成的,故③ 正确;
④ FeCl 溶液和Fe(OH) 胶体粒子都能透过滤纸,故④ 正确;
3 3
⑤ 胶体、溶液和浊液属于不同的分散系,其中溶液最稳定,故⑤ 错误;
⑥ 电解质溶液能使胶体产生聚沉,故往Fe(OH) 胶体中逐滴加入稀盐酸溶液时,
3
开始时会出现氢氧化铁沉淀,当继续滴加时,氢氧化铁沉淀会溶于过量的盐酸,
即沉淀消失,故⑥ 正确,故C 正确。
故选:C
【例17】★★☆☆☆
Fe(OH)
(2020•海口市期中)实验室制取 3胶体的实验操作
是 ,可以利用 (方
Fe(OH) Fe(OH)
法)检验 3胶体已生成。利用 (方法)提纯 3胶体,
证明
Fe(OH) 3胶体与Cl-
已分离完全的实验方法是 。
第13页(共14页)【考点】胶体的性质及制备
【答案】向沸水中逐滴加入几滴饱和FeCl 饱和溶液,煮沸至液体呈红褐色即可;
3
丁达尔现象;渗析;向半透膜中加入硝酸银溶液,无白色沉淀产生,证明已完全
分离。
【解析】实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,向
沸水中逐滴加入5-6滴FeCl 饱和溶液,继续煮沸至溶液呈红褐色,停止加热,即
3
制得Fe(OH) 胶体
3
证明Fe(OH) 胶体已制成的方法为丁达尔效应,溶液能透过半透膜,胶粒不能透
3
过半透膜,利用渗析能提纯胶体,证明Fe(OH) 胶体与Cl-已分离完全的实验方法
3
是:向半透膜中加入硝酸银溶液,无白色沉淀产生,证明已完全分离。
第14页(共14页)