文档内容
(12)化学反应与电能—高二化学人教版暑假作业本
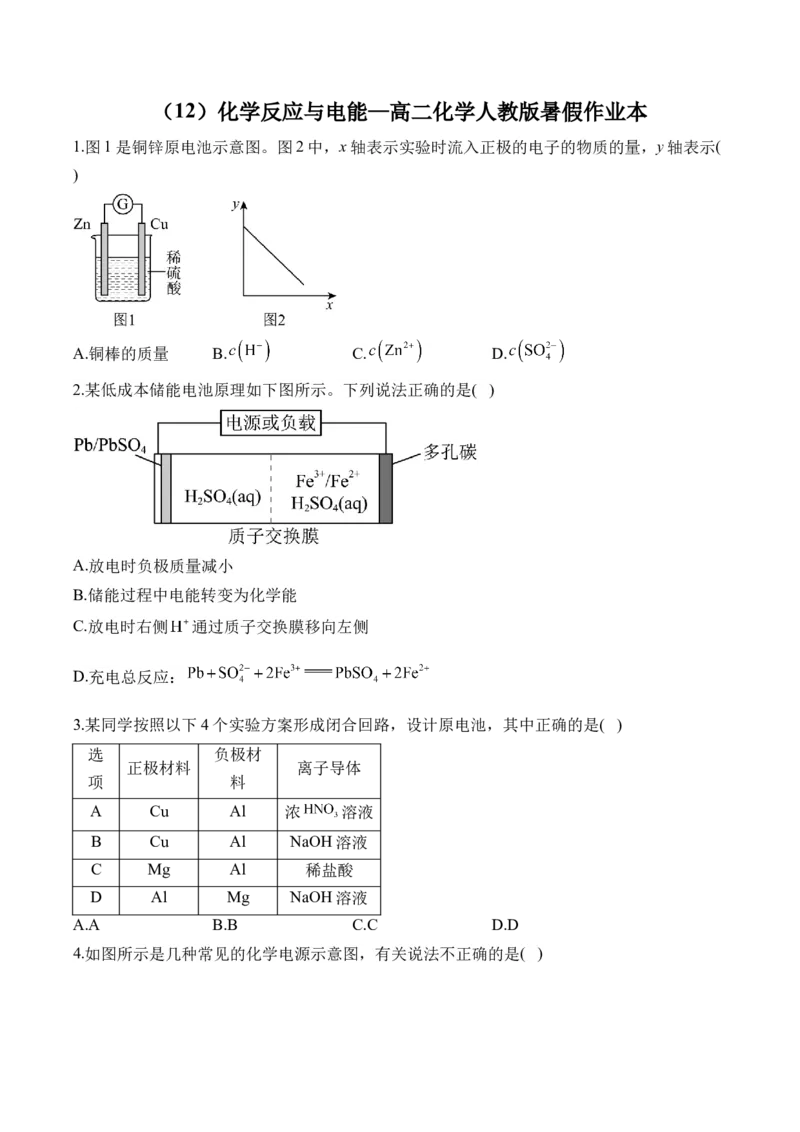
1.图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示(
)
A.铜棒的质量 B. C. D.
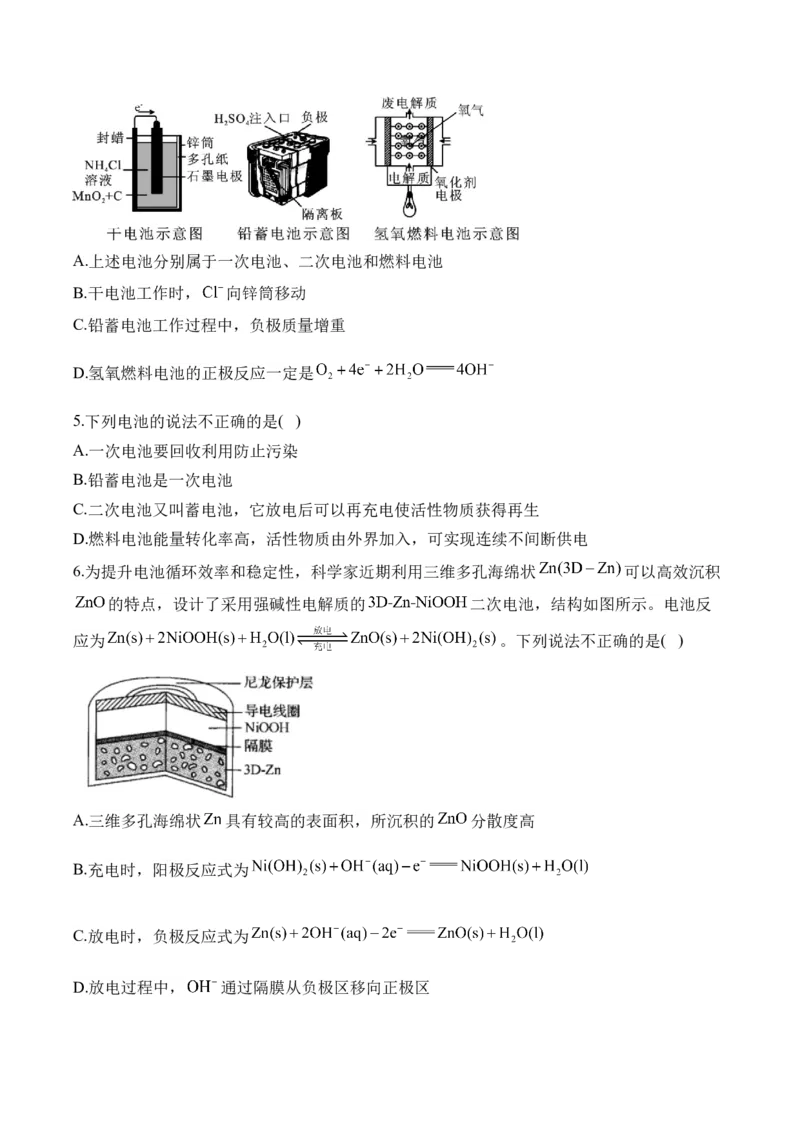
2.某低成本储能电池原理如下图所示。下列说法正确的是( )
A.放电时负极质量减小
B.储能过程中电能转变为化学能
C.放电时右侧 通过质子交换膜移向左侧
D.充电总反应:
3.某同学按照以下4个实验方案形成闭合回路,设计原电池,其中正确的是( )
选 负极材
正极材料 离子导体
项 料
A Cu Al 浓 溶液
B Cu Al NaOH溶液
C Mg Al 稀盐酸
D Al Mg NaOH溶液
A.A B.B C.C D.D
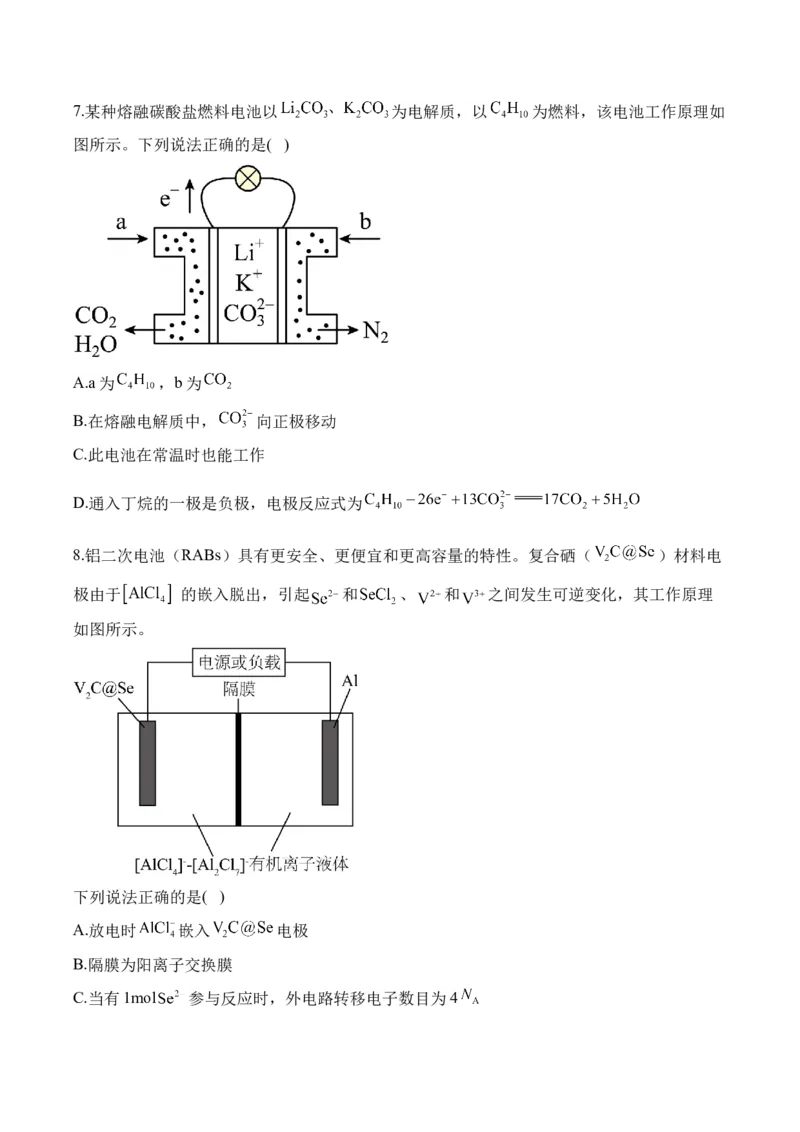
4.如图所示是几种常见的化学电源示意图,有关说法不正确的是( )A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池工作时, 向锌筒移动
C.铅蓄电池工作过程中,负极质量增重
D.氢氧燃料电池的正极反应一定是
5.下列电池的说法不正确的是( )
A.一次电池要回收利用防止污染
B.铅蓄电池是一次电池
C.二次电池又叫蓄电池,它放电后可以再充电使活性物质获得再生
D.燃料电池能量转化率高,活性物质由外界加入,可实现连续不间断供电
6.为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状 可以高效沉积
的特点,设计了采用强碱性电解质的 二次电池,结构如图所示。电池反
应为 。下列说法不正确的是( )
A.三维多孔海绵状 具有较高的表面积,所沉积的 分散度高
B.充电时,阳极反应式为
C.放电时,负极反应式为
D.放电过程中, 通过隔膜从负极区移向正极区7.某种熔融碳酸盐燃料电池以 为电解质,以 为燃料,该电池工作原理如
图所示。下列说法正确的是( )
A.a为 ,b为
B.在熔融电解质中, 向正极移动
C.此电池在常温时也能工作
D.通入丁烷的一极是负极,电极反应式为
8.铝二次电池(RABs)具有更安全、更便宜和更高容量的特性。复合硒( )材料电
极由于 的嵌入脱出,引起 和 、 和 之间发生可逆变化,其工作原理
如图所示。
下列说法正确的是( )
A.放电时 嵌入 电极
B.隔膜为阳离子交换膜
C.当有1mol 参与反应时,外电路转移电子数目为4D.充电时 发生的反应为
9. 常用作强还原剂、供氢剂和真空管除气剂,遇水蒸气剧烈反应。某小组利用如图装置
(部分夹持装置未画出)制备 和 。下列叙述正确的是( )
A.装置Ⅱ中的试剂为NaOH溶液,作用是吸收气体中的
B.可以较长时间观察到装置Ⅰ中产生白色沉淀
C.装置Ⅳ的作用是干燥并吸收尾气
D.用水可以检验装置Ⅲ中钡是否过量
10.将铁粉和活性炭的混合物用 溶液湿润后,置于如图所示装置中,进行铁的电化学腐
蚀实验。下列有关该实验的说法正确的是( )
A.铁被氧化的电极反应式为
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替 溶液,铁不能发生吸氧腐蚀
11.人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发
展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_____。
A. 与 反应 B. 与 燃烧反应
C.灼热的炭与 反应 D.氢氧化钠与稀盐酸反应(2)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下
列问题:
①下列说法正确的是_____。
A.甲中铜片质量减少、乙中铁片质量减少
B.甲、乙均为化学能转变为电能的装置
C.乙中铜片上没有明显变化
D.甲、乙两烧杯中 均减小
②在相同时间内,两烧杯中产生气泡的速度:甲_____乙(填“>”、“<”或“=”)。
③请写出甲、乙中构成原电池的正极电极反应式:_____。电池工作时,溶液中 向_____
极(填“正”或“负”)移动。当甲中溶液质量增重27g时,电极上转移电子数目为_____。
④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为_____。
(3)图丙为甲烷氧气燃料电池的构造示意图,电解质溶液的溶质是KOH.通甲烷一极是电
池的____极,电极反应为______。
答案以及解析
1.答案:B解析:A.Cu作正极,氢离子得电子生成氢气,铜棒质量不变,故A错误;
B.Cu作正极,氢离子得电子生成氢气,随反应进行,氢离子浓度减小,故B正确;
C.锌作负极失电子生成锌离子,溶液中锌离子浓度增大,故C错误;
D.硫酸根离子不参与电池反应,故硫酸根离子浓度不变,故D错误;
故选:B。
2.答案:B
解析:该储能电池放电时,Pb为负极,失电子结合硫酸根离子生成PbSO ,则多孔碳电极为
4
正极,正极上 得电子转化为 ,充电时,多孔碳电极为阳极, 失电子生成 ,
电极为阴极, 得电子生成Pb和硫酸。
A.放电时负极上Pb失电子结合硫酸根离子生成 附着在负极上,负极质量增大,A错
误;
B.储能过程中,该装置为电解池,将电能转化为化学能,B正确;
C.放电时,右侧为正极,电解质溶液中的阳离子向正极移动,左侧的 通过质子交换膜移向
右侧,C错误;
D.充电时,总反应为 ,D错误;
故答案选B。
3.答案:B
解析:A.常温下,浓硝酸使铝钝化,铜与浓硝酸反应,因此金属铜为负极,铝为正极,故A
错误;B.铝与氢氧化钠溶液反应而铜不反应,所以铝做负极,铜做正极,故B正确;C.镁的
活泼性大于铝,镁与盐酸反应,因此金属镁为原电池的负极材料,金属铝为正极材料,故C
错误;D.金属铝与氢氧化钠溶液反应而镁与氢氧化钠溶液不反应,所以铝失电子、作负极,
镁作正极,故D错误;故选B。
4.答案:D
5.答案:B
解析:一次电池中主要含Fe、Zn、Mn等,此外还含有微量的Hg,Hg是有毒的金属,电池
要回收利用防止污染,A正确;铅蓄电池为可充电电池,是二次电池,B错误;二次电池又
称为可充电电池或蓄电池,是指在电池放电后,通过充电的方式使活性物质激活而继续使用
的电池,C正确;燃料电池是一种把燃料所具有的化学能直接转化成电能的化学装置,能量
转化率高,活性物质由外界加入,可实现连续不间断供电,D正确。
6.答案:D
解析:原电池放电过程中,阳离子通过隔膜从负极区移向正极区,阴离子 通过隔膜从正极区移向负极区,D错误。
7.答案:D
解析:A.燃料电池中通入燃料的电极是负极、通入氧化剂的电极是正极,根据电子流向知,
左边电极是负极、右边电极是正极,所以a为 ,b为 ,故A错误;B.原电池放电时,
阴离子移向负极,故 向负极移动,故B错误;C.电解质为熔融碳酸盐,需要高温条件,
常温下不能工作,故C错误;D.通入丁烷的一极是负极,发生失电子的氧化反应,电极反应
式为 ,故D正确。故选D。
8.答案:D
解析:A.电池放电时, 为正极, 发生的反应式为
, 嵌出 电极,A错误;
B. 、 通过离子交换膜嵌入和嵌出,隔膜为阴离子交换膜,B错误;
C.当有1mol 参与反应时, 也在同时发生的反应,外电路转移电子数目不止4 ,C
错误;
D.根据分析,充电时 发生的反应为 ,D正
确;
故选D。
9.答案:B
解析:A.由分析可知,装置Ⅱ中的试剂为浓硫酸,用于干燥 ,故A错误;
B.Ⅰ为电解饱和食盐水的装置,Fe为阳极,电极方程式为: ,阴极产生
,该装置中阳极用苯隔绝空气,可以较长时间观察到 白色沉淀,故B正确;
C.由分析可知,装置Ⅳ的作用是防止空气中的水蒸气进入装置Ⅲ, 不能用碱石灰除去,故
C错误;
D.Ba和 都可以和水反应,不能用水可以检验装置Ⅲ中钡是否过量,故D错误;
故选B。10.答案:
解析:在铁的电化学腐蚀中, 失去电子转化为 ,即负极反应式为 ,A
错误;铁的腐蚀过程中化学能除了转化为电能,还有一部分转化为热能,B错误;活性炭与
铁混合,在 溶液中构成了无数微小的原电池,加速了铁的腐蚀,C正确;以水代替
溶液,水也呈中性,铁在中性或碱性条件下易发生吸氧腐蚀,D错误。
11.答案:(1)B
(2)CD;>; ;负; ;
(3)负;
解析:(1)A. 与 反应为非氧化还原反应,不能设计成原电池,故A错
误;B. 与 燃烧反应为能自发进行的氧化还原反应,且是放热反应,能设计成原电池,
故B正确;C.灼热的炭与 反应为吸热反应,一般不能设计成原电池,故C错误;D.氢氧
化钠与稀盐酸反应为非氧化还原反应,不能设计成原电池,故D错误;故答案为:B;
(2)①A、甲、乙中铁片质量都减少,铜的质量不变,故A错误;B.甲装置是原电池,将化学
能转变为电能,乙不能形成原电池,故B错误;C.乙装置中铜片不反应,也没构成原电池的
正极,所以铜片上没有明显变化,故C正确;D.两个烧杯中都产生氢气, 都降低,故D
正确;故答案为:CD;②甲装置是原电池,乙不能形成原电池,原电池反应能加快反应速
率,则两烧杯中产生气泡的速度:甲>乙,故答案为:>;②甲装置是原电池,乙不能形成原电
池,原电池反应能加快反应速率,则两烧杯中产生气泡的速度甲>乙,故答案为:>;③甲形成
原电池,乙不能形成原电池,甲中Fe作负极,Cu作正极,正极上 得电子生成氢气 ,正
极反应为 ,负极反应式为 ,电池工作时,溶液中 向
负极移动,总反应为 ,1molFe参与反应时溶液增重
,所以当甲中溶液质量增重27g时,有0.5molFe参加反应,转移电子 ,数目为,故答案为: ;负; ;
④若将甲中的稀硫酸换为浓硝酸,常温下Fe发生钝化,Cu能与浓硝酸反应生成硝酸铜、二
氧化氮,电池总反应的离子方程式为 ,故答案为:
;
(3)碱性甲烷燃料电池中,甲烷发生失电子的氧化反应生成 ,则通甲烷Pt电极为负
极,通入氧气的Pt极为正极,负极反应式为 ,故答案为:
负; 。