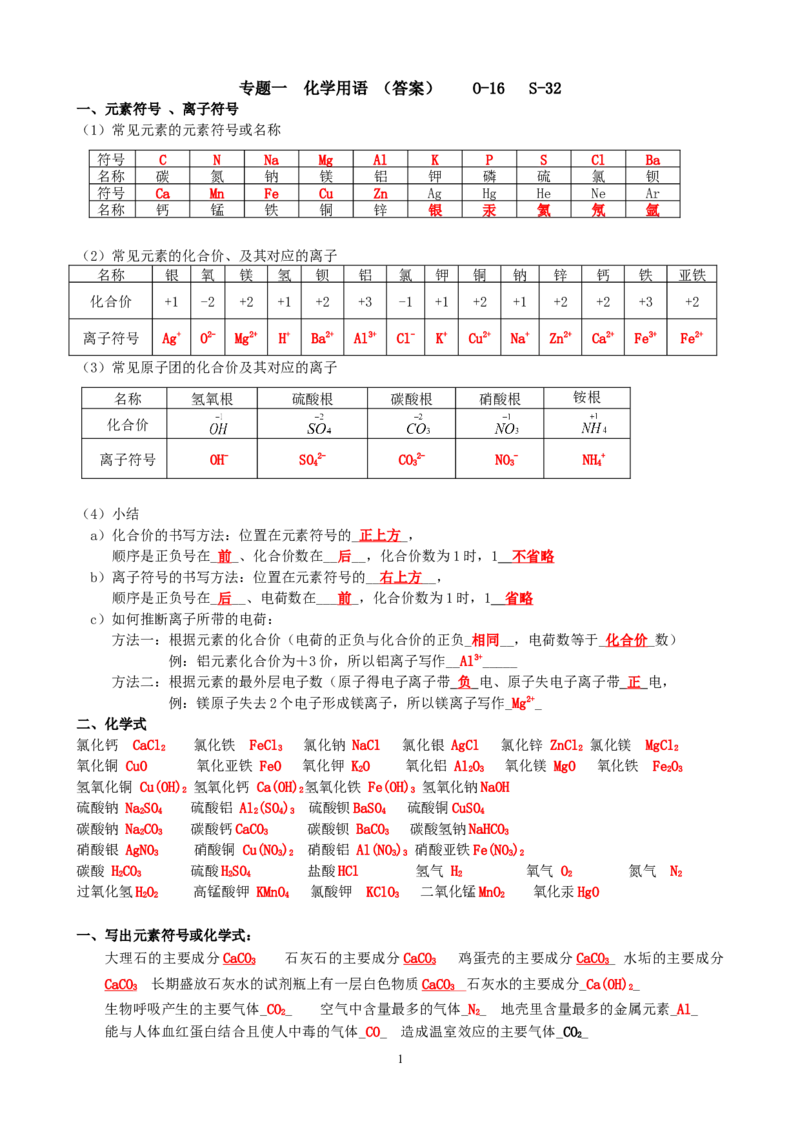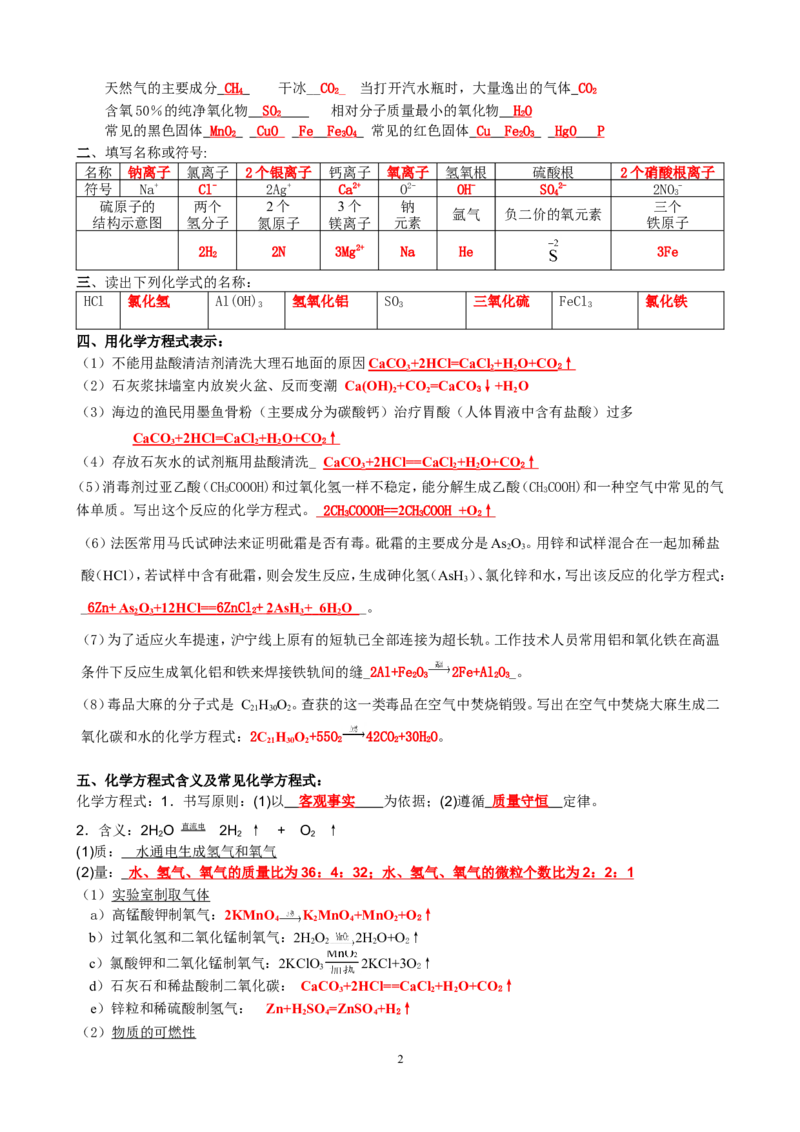文档内容
专题一 化学用语 (答案) O-16 S-32
一、元素符号 、离子符号
(1)常见元素的元素符号或名称
符号 C N Na Mg Al K P S Cl Ba
名称 碳 氮 钠 镁 铝 钾 磷 硫 氯 钡
符号 Ca Mn Fe Cu Zn Ag Hg He Ne Ar
名称 钙 锰 铁 铜 锌 银 汞 氦 氖 氩
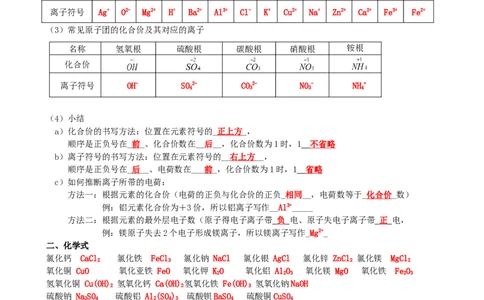
(2)常见元素的化合价、及其对应的离子
名称 银 氧 镁 氢 钡 铝 氯 钾 铜 钠 锌 钙 铁 亚铁
化合价 +1 -2 +2 +1 +2 +3 -1 +1 +2 +1 +2 +2 +3 +2
离子符号 Ag+ O2- Mg2+ H+ Ba2+ Al3+ Cl- K+ Cu2+ Na+ Zn2+ Ca2+ Fe3+ Fe2+
(3)常见原子团的化合价及其对应的离子
名称 氢氧根 硫酸根 碳酸根 硝酸根 铵根
化合价
离子符号 OH- SO2- CO2- NO- NH+
4 3 3 4
(4)小结
a)化合价的书写方法:位置在元素符号的_正上方_,
顺序是正负号在_前_、化合价数在__后__,化合价数为1时,1 不省略
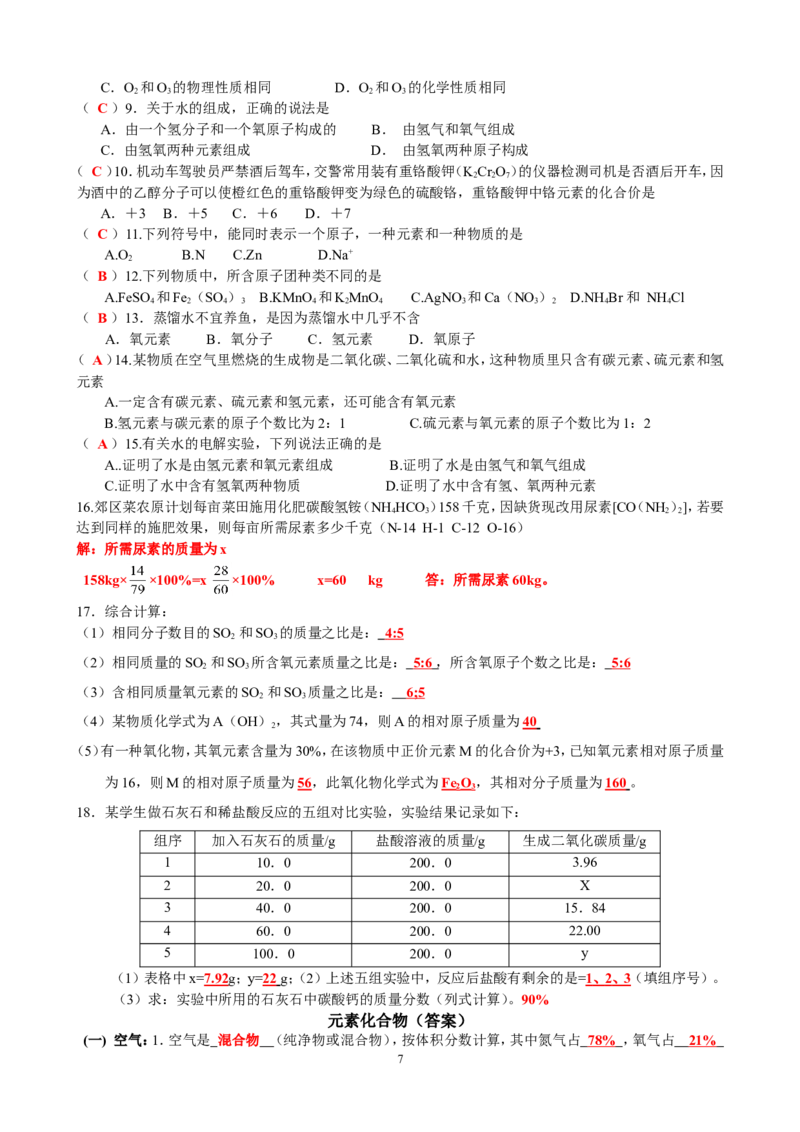
b)离子符号的书写方法:位置在元素符号的__右上方__,
顺序是正负号在_后__、电荷数在___前_,化合价数为1时,1 省略
c)如何推断离子所带的电荷:
方法一:根据元素的化合价(电荷的正负与化合价的正负_相同__,电荷数等于_化合价_数)
例:铝元素化合价为+3价,所以铝离子写作__Al3+_____
方法二:根据元素的最外层电子数(原子得电子离子带 负 电、原子失电子离子带 正 电,
例:镁原子失去2个电子形成镁离子,所以镁离子写作_Mg2+_
二、化学式
氯化钙 CaCl 氯化铁 FeCl 氯化钠 NaCl 氯化银 AgCl 氯化锌 ZnCl 氯化镁 MgCl
2 3 2 2
氧化铜 CuO 氧化亚铁 FeO 氧化钾 KO 氧化铝 AlO 氧化镁 MgO 氧化铁 FeO
2 2 3 2 3
氢氧化铜 Cu(OH) 氢氧化钙 Ca(OH) 氢氧化铁 Fe(OH) 氢氧化钠NaOH
2 2 3
硫酸钠 NaSO 硫酸铝 Al(SO) 硫酸钡BaSO 硫酸铜CuSO
2 4 2 4 3 4 4
碳酸钠 NaCO 碳酸钙CaCO 碳酸钡 BaCO 碳酸氢钠NaHCO
2 3 3 3 3
硝酸银 AgNO 硝酸铜 Cu(NO) 硝酸铝 Al(NO) 硝酸亚铁Fe(NO)
3 3 2 3 3 3 2
碳酸 HCO 硫酸HSO 盐酸HCl 氢气 H 氧气 O 氮气 N
2 3 2 4 2 2 2
过氧化氢HO 高锰酸钾 KMnO 氯酸钾 KClO 二氧化锰MnO 氧化汞HgO
2 2 4 3 2
一、写出元素符号或化学式:
大理石的主要成分CaCO 石灰石的主要成分CaCO 鸡蛋壳的主要成分CaCO_ 水垢的主要成分
3 3 3
CaCO 长期盛放石灰水的试剂瓶上有一层白色物质CaCO 石灰水的主要成分_Ca(OH)_
3 3 2
生物呼吸产生的主要气体_CO_ 空气中含量最多的气体_N_ 地壳里含量最多的金属元素_Al_
2 2
能与人体血红蛋白结合且使人中毒的气体_CO_ 造成温室效应的主要气体_CO_
2
1天然气的主要成分 C H 干冰__CO_ 当打开汽水瓶时,大量逸出的气体 CO
4 2 2
含氧50%的纯净氧化物 S O 相对分子质量最小的氧化物 HO
2 2
常见的黑色固体 Mn O Cu O F e F eO 常见的红色固体 C u F eO Hg O P
2 3 4 2 3
二、填写名称或符号:
名称 钠离子 氯离子 2个银离子 钙离子 氧离子 氢氧根 硫酸根 2个硝酸根离子
符号 Na+ Cl- 2Ag+ Ca2+ O2- OH- SO2- 2NO-
4 3
硫原子的 两个 2个 3个 钠 三个
氩气 负二价的氧元素
结构示意图 氢分子 氮原子 镁离子 元素 铁原子
2H 2N 3Mg2+ Na He 3Fe
2
三、读出下列化学式的名称:
HCl 氯化氢 Al(OH) 氢氧化铝 SO 三氧化硫 FeCl 氯化铁
3 3 3
四、用化学方程式表示:
(1)不能用盐酸清洁剂清洗大理石地面的原因CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
(2)石灰浆抹墙室内放炭火盆、反而变潮 Ca(OH) +CO=CaCO ↓+H O
2 2 3 2
(3)海边的渔民用墨鱼骨粉(主要成分为碳酸钙)治疗胃酸(人体胃液中含有盐酸) 过多
CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
(4)存放石灰水的试剂瓶用盐酸清洗_ CaCO +2HCl==CaCl +H O+CO ↑
3 2 2 2
(5)消毒剂过亚乙酸(CHCOOOH)和过氧化氢一样不稳定,能分解生成乙酸(CHCOOH)和一种空气中常见的气
3 3
体单质。写出这个反应的化学方程式。 2 C H COOOH= = 2 C H COO H +O ↑
3 3 2
(6)法医常用马氏试砷法来证明砒霜是否有毒。砒霜的主要成分是As O。用锌和试样混合在一起加稀盐
2 3
酸(HCl),若试样中含有砒霜,则会发生反应,生成砷化氢(AsH )、氯化锌和水,写出该反应的化学方程式:
3
_ 6Zn + A s O +12HCl== 6ZnCl + 2 AsH + 6H O _。
2 3 2 3 2
(7)为了适应火车提速,沪宁线上原有的短轨已全部连接为超长轨。工作技术人员常用铝和氧化铁在高温
条件下反应生成氧化铝和铁来焊接铁轨间的缝_2Al+FeO 2Fe+AlO_。
2 3 2 3
(8)毒品大麻的分子式是 C H O。查获的这一类毒品在空气中焚烧销毁。写出在空气中焚烧大麻生成二
21 30 2
氧化碳和水的化学方程式:2C H O+55O 42CO+30HO。
21 30 2 2 2 2
五、化学方程式含义及常见化学方程式:
化学方程式:1.书写原则:(1)以 客观事实 为依据;(2)遵循 质量守恒 定律。
2.含义:2H O 直流电 2H ↑ + O ↑
2 2 2
(1)质: 水通电生成氢气和氧气
(2)量: 水、氢气、氧气的质量比为 36 : 4 : 32 ;水、氢气、氧气的微粒个数比为 2 : 2 : 1
(1)实验室制取气体
a)高锰酸钾制氧气:2KMnO KMnO +MnO +O ↑
4 2 4 2 2
b)过氧化氢和二氧化锰制氧气:2HO 2HO+O↑
2 2 2 2
c)氯酸钾和二氧化锰制氧气:2KClO 2KCl+3O ↑
3 2
d)石灰石和稀盐酸制二氧化碳: CaCO +2HCl==CaCl +H O+CO ↑
3 2 2 2
e)锌粒和稀硫酸制氢气: Zn+H SO =ZnSO +H ↑
2 4 4 2
(2)物质的可燃性
2a)铁丝燃烧: 3Fe+2O FeO
2 3 4
b)硫燃烧:S+O SO
2 2
c)红磷燃烧:4P+5O 2PO
2 2 5
d)白磷自燃:4P+5O ==2P O
2 2 5
e)镁条燃烧:2Mg+O 2MgO
2
f)木炭的充分燃烧:C+O CO
2 2
g)木炭的不充分燃烧:2C+O 2CO
2
h)氢气燃烧: 2H+O 2HO
2 2 2
i)一氧化碳燃烧:2CO+O 2CO
2 2
j)甲烷(CH)燃烧: CH +2O CO +2H O
4 4 2 2 2
k)酒精(C HOH)燃烧:CHOH+3O 2CO +3H O
2 5 2 5 2 2 2
(3)物质的还原性
a)氢气还原氧化铜:H +CuO Cu+H O
2 2
b)碳粉还原氧化铜: C+2CuO 2Cu+CO ↑
2
c)碳粉还原氧化铁: 3C+2Fe O 4Fe+3CO ↑
2 3 2
d)一氧化碳还原氧化铜: CO+CuO Cu+CO
2
e)一氧化碳还原氧化铁:3CO+Fe O 2Fe+3CO
2 3 2
(4)其它
a)二氧化碳与水:CO +H O= HCO
2 2 2 3
b)二氧化碳与澄清石灰水:CO + Ca(OH) = CaCO ↓+H O
2 2 3 2
c)二氧化碳与碳: CO +C 2CO
2
d)电解水: 2HO 2H↑+O ↑
2 2 2
e)铁与硫酸铜溶液:Fe+CuSO =Cu+FeSO
4 4
f)氢氧化钠溶液和硫酸铜溶液:2NaOH+CuSO =Cu(OH) ↓+Na SO
4 2 2 4
g)碳酸不稳定分解: HCO = HO+CO ↑
2 3 2 2
i)碳酸钠和稀盐酸:NaCO +2HCl==2NaCl+H O+CO ↑
2 3 2 2
j)镁带和稀盐酸:Mg+2HCl==MgCl +H ↑
2 2
六、选择题
( A )1、下列物质中,不含原子团的是
A. NaCl B. HSO C. Fe(NO) D. Ca(OH)
2 4 3 3 2
( B )2、下列物质的化学式,书写错误的是
A.硫酸HSO B.氯化铁FeCl C.氧化镁MgO D.氢氧化钙Ca(OH)
2 4 2
( D )3、下列含氮物质中,氮元素的化合价由高到低顺序排列的一组是
A. NO、N、HNO B. HNO、N、NO C.N、HNO、NO D. HNO、NO、N
2 3 3 2 2 3 3 2
( C )4、下列说法正确的是
A. 水中氧元素的化合价是+2 价 B. 铁单质中铁元素的化合价是+3价
C.氧气中氧元素的化合价是0价 D. 水中氢气的化合价是0价
( C )5、某元素X的原子最外层有2个电子,而Y原子的最外层有7个电子。则这两种元素组成的化合物
的化学式可能为
A. XY B. XY C. XY D. XY
2 7 7 2 2 2
( C )6、下列物质中,由地壳中含量最多的金属元素、非金属元素和空气中含量最多的元素组成的物质
的化学式是
A. CaCO B. Al(SO) C. Al(NO) D. Fe(OH)
3 2 4 3 3 3 3
3( B ) 7、某元素R的相对原子质量为56,在它的某种氧化物中显+3价,则该元素在这种氧化物中的质
量分数为
A. 30% B. 70% C. 50% D. 60%
( B )8、下列同组物质中,同种元素具有不同化合价的是
A. HO,CO B. KMnO , KMnO C. ZnSO ,CuSO D. HSO , SO
2 2 4 2 4 4 4 2 4 3
( B )9、有五种含氮元素的物质:NH 、( )、NO、NO 、KNO,按它们的排列规律,( )中应填的物质
3 2 3 2 3
是
A. NO B. NO C. NaNO D. Cu(NO )
2 5 2 3 2
( B )10、溴元素具有多种化合价,下列单质或化合物中,溴元素化合价最低的是
A. KBrO B. MgBr C. Br D. HBrO
3 2 2 4
( C )11、X、Y、Z三种元素的化合价分别是+1、+5、-2,这三种元素组成的化合物的化学式为
A. XYZ B. XYZ C. XYZ D. XYZ
3 2 2 3 3 4 4 3
( A )12、某三价金属元素A,它的氧化物中含A元素的质量分数是70%,则A的相对原子质量是
A.56 B.27 C.32 D.16
七、推断题
A元素原子核外有三个电子层,最外层和第一层电子数相同,B元素是地壳中含量最多的元素,C元素形成
的单质是最轻的气体,请回答:
(1)写出B单质的化学式__O__ (2)写出C单质的化学式____H___
2 2
(3)A元素和B元素组成的化合物的化学式___MgO____
(4)B元素和C元素组成的化合物的化学式__HO___、_HO__
2 2 2
基本概念和原理(答案)
一、物质的变化
1、物理变化和化学变化的本质区别是有无新物质生成 ,下列变化属于化学变化的是 D 、 F 、 J 、 I 。
A 气球爆炸、B 氯化钠溶于水C酒精挥发、D“瓦斯”爆炸、E 蜡烛融化 F 煤分解成煤气、煤焦油、焦炭、G石
油蒸馏、H干冰升华、J 炭粉还原氧化铜、I电解水。
2. 基本反应类型:
类型 (模式)特点 例(化学方程式)
1)化合反应 A + B = AB多变 一 HO+CO =H CO
2 2 2 3
2)分解反应 AB = A + B一变 多 HCO =H O+CO ↑
2 3 2 2
3.氧化反应和还原反应─碳还原氧化铜:C +2 CuO — 2Cu+CO ↑
2
C: 得到 氧 、具有 还原 性、是 还原 剂
CuO: 失去 氧 、具有 氧化性 性、是 氧化 剂
4.质量守恒定律:(1)内容: 参加反应的各物质的质量总和等于生成物中各物质的质量总和 。
(2)微观解释:在任何化学反应前后原子的 种类、个数、质量均不变
(3)应用: ①A+B=2C, 10克A跟4克B恰好完全反应生成 14 克C。
②A+B=C+2D,10克A跟6克B恰好完全反应生成8克C和 8 克D。
二、物质的性质
物质常见的化学性质有 可燃性、氧化性、还原性、酸碱性、稳定性 , 常见的物理性质有 颜色、气味、溶解
性、密度、硬度、导电性 ,下列性质属于物理性质的有 E 、 F 。
4A氢气能在空气中燃烧、B铁在潮湿的空气中易生锈、C碳酸不稳定、D古字画不易退色、E二氧化碳能溶于
水、F活性炭具有较强的吸附性、G碳在氧气中燃烧、H CO有毒、J双氧水易分解生成氧气
〖练习〗
( B )1.下列变化中,属于物理变化的是
A.白磷自然 B.分离液态空气制氧气 C.钢铁生锈 D.火药爆炸
( C )2.在化学反应中一定没有发生变化的是
A. 物质的种类 B. 分子的种类 C. 原子的种类 D. 分子个数
( B )3.在化学反应A+B=C+D中,5克A和B充分反应生成3克C和8克D,则参加反应的B是
A. 5克 B. 6克 C. 7克 D. 8克
( A )4.根据质量守恒定律,在2X +Y =2Z中,Z的化学式可表示为
2 2
A. X Y B. XY C. XY D. XY
2 3 2 4
( B )5.根据质量守恒定律,镁带在空气中完全燃烧后,生成物的质量 应
A.小于镁带的质量 B.大于镁带的质量 C.等于镁带的质量 D.无法比较
( D )6.下列说法和质量守恒定律相矛盾的是
A.反应物与生成物的总质量不变 B.蜡烛燃烧后,生成物的总质量比蜡烛重
C.16克硫与16克氧气反应,生成32克二氧化硫 D.8克氢气与8克氧气反应,生成16克水
7.判断下列反应的基本反应类型:
A. 2HO 直流电 2H↑+ O ↑ ( 分解反应 )
2 2 2
B. 3Fe + 2O 点燃 Fe O ( 化合反应)
2 3 4
三、物质的构成
1.构成物质的基本粒子有原子、分子、离子;水由水分子构成,铁由铁原子构成,氯化钠由 Na + 、 Cl -构成。
2.分子和原子对比表:
基本微粒 定义 联系 区别
分子 保持物质 ( 化学性质 ) 的 ( 最小 ) 粒子 分子由原子 化学变化中分子可破裂成原子,
原子 ( 化学 ) 变化中的 ( 最小粒子 ) 粒子 构成 而原子可以重新组合成分子
3.原子的构成:原子是由居于 原子中心 的原子核和核外带 负电的电子 构成。
原子核 质子:每个质子带 1 个 单位 正 电荷.
(1) 原子 中子:不带电
电子: 分层排布,每个电子带 1 个 单位 负 电荷.
(2)为什么原子成电中性? 原子核所带的正电荷和核外电子所带负电荷,电量相等、电性相反 。
核电荷数= 核 外电子数 = 质子数 = 原子序数
4.相对原子质量: (1) 定义公式:A的相对原子质量=
(2)近似公式:相对原子质量≈ 质子数 + 中子数
5. 结构示意图:
特点 原因(判断依据) 例(填序号)
原子结构示意图 不带电 核电荷数 = 电子总数 ACDF
离子结构 阳 带 正 电 核电荷数 ﹥ 电子总数 BE
示意图 阴 带 负 电 核电荷数 ﹤ 电子总数 GH
( C )1. 1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量的
新值。铟元素的核电荷数为49,相对原子质量为115,铟原子的中子数为
5A.115 B.49 C.66 D.164
( D )2.下列物质中,含有氧分子的
A.CO B.H O C.Ca(OH) D.液态氧(O)
2 2 2 2 2
( C )3.在SO 、CO、NO 各一个分子中
2 2 2
A.均含有一个氧分子 B.氧元素的质量分数相等 C.含氧原子的个数相等 D.都含有两个氧元素
( C )4.元素X和Y的原子核外都有三个电子层,X原子的最外层有1个电子,Y原子的最外层有6个电子,
当这两种元素的原子相互化合后,生成物的化学式可能是
A.XY B.XY C.X Y D.XY
6 2 2
四、物质的分类和组成
1.元素是具有相同的核电荷数数 ( 即 质子数 )的同一类 原子 的总称。
2. 元素的种类由 质子数 决定;元素的性质特别是化学性质由 最外层电子数 决定。
3.地壳中含量最多的元素: O ,含量最高的金属元素 A l ,前五位是 O Si Al F e 。
4. 将下列物质的序号标在上面表格的相应位置处:
A铁粉 B冰水混合物 C石灰石 D干冰 E五氧化二磷 F氢气 G空气 H食盐水
I石油 J煤 K天然气 L 酒精 M液氧 N不锈钢 O稀有气体
_混合物__:如 C 、 G 、 H 、 I 、 J 、 K 、 N 、 O 等
金属 单质:如 A FeCuHg 等
单质 非金属 单质:如 FM CSPH ON 等
2 2 2
物质 稀有气体 单质:如 He 等
无机物 氧化物:如 BDE H OCO MgO 等
2 2
_纯净物_ 化合物 其他:如 KClO 等
3
有机物:如 L CH 等
4
(C )1.元素的化学性质主要决定于原子的
A.核外电子数 B. 核内质子数 C. 最外层电子数 D. 核内中子数
(B)2.元素的种类主要决定于原子的
A.核外电子数 B. 核内质子数 C. 最外层电子数 D. 核内中子数
( B )3.按物质的分类方法,前者包含后者的是
A.纯净物、混合物 B.纯净物、化合物 C.化合物、单质 D.金属、单质
( D )4.列物质的性质中,属于物理性质的是
A.硫酸有酸性 B.氢气有还原性 C.一氧化碳有可燃性 D.浓氨水有挥发性
( A )5.燃烧、缓慢氧化、自燃的相同点是
A.都是氧化反应 B.都是化合反应 C.反应都很剧烈 D.反应都需要点燃
( C )6.列说法中,正确的是
A.用过氧化氢制氧气时,加入二氧化锰可使生成的氧气质量增加
B.没有二氧化锰,过氧化氢不会产生氧气
C.加入二氧化锰可使过氧化氢迅速放出氧气 D.二氧化锰在任何反应里都可作为催化剂
( C )7.能量守恒定律是自然界的基本定律之一,下列能量转化过程中,化学能转化成电能的是
A.使用太阳能热水器 B.用电灯照明
C.用干电池作电源 D.用电动机带动水泵将水抽到高处
( B )8. 打雷放电时,空气中极少量氧气会转化成臭氧(3O→2O),下列有关说法中正确的是
2 3
A.O 和O 是同一种物质 B.O 和O 都是单质
2 3 2 3
6C.O 和O 的物理性质相同 D.O 和O 的化学性质相同
2 3 2 3
( C )9.关于水的组成,正确的说法是
A.由一个氢分子和一个氧原子构成的 B. 由氢气和氧气组成
C.由氢氧两种元素组成 D. 由氢氧两种原子构成
( C )10.机动车驾驶员严禁酒后驾车,交警常用装有重铬酸钾(KCr O)的仪器检测司机是否酒后开车,因
2 2 7
为酒中的乙醇分子可以使橙红色的重铬酸钾变为绿色的硫酸铬,重铬酸钾中铬元素的化合价是
A.+3 B.+5 C.+6 D.+7
( C )11.下列符号中,能同时表示一个原子,一种元素和一种物质的是
A.O B.N C.Zn D.Na+
2
( B )12.下列物质中,所含原子团种类不同的是
A.FeSO 和Fe (SO ) B.KMnO 和KMnO C.AgNO 和Ca(NO ) D.NH Br和 NH Cl
4 2 4 3 4 2 4 3 3 2 4 4
( B )13.蒸馏水不宜养鱼,是因为蒸馏水中几乎不含
A.氧元素 B.氧分子 C.氢元素 D.氧原子
( A )14.某物质在空气里燃烧的生成物是二氧化碳、二氧化硫和水,这种物质里只含有碳元素、硫元素和氢
元素
A.一定含有碳元素、硫元素和氢元素,还可能含有氧元素
B.氢元素与碳元素的原子个数比为2:1 C.硫元素与氧元素的原子个数比为1:2
( A )15.有关水的电解实验,下列说法正确的是
A..证明了水是由氢元素和氧元素组成 B.证明了水是由氢气和氧气组成
C.证明了水中含有氢氧两种物质 D.证明了水中含有氢、氧两种元素
16.郊区菜农原计划每亩菜田施用化肥碳酸氢铵(NH HCO )158千克,因缺货现改用尿素[CO(NH )],若要
4 3 2 2
达到同样的施肥效果,则每亩所需尿素多少千克(N-14 H-1 C-12 O-16)
解:所需尿素的质量为x
158kg× ×100%=x ×100% x=60 kg 答:所需尿素60kg。
17.综合计算:
(1)相同分子数目的SO 和SO 的质量之比是: 4: 5
2 3
(2)相同质量的SO 和SO 所含氧元素质量之比是: 5: 6 ,所含氧原子个数之比是: 5: 6
2 3
(3)含相同质量氧元素的SO 和SO 质量之比是: 6; 5
2 3
(4)某物质化学式为A(OH),其式量为74,则A的相对原子质量为 4 0
2
(5)有一种氧化物,其氧元素含量为30%,在该物质中正价元素M的化合价为+3,已知氧元素相对原子质量
为16,则M的相对原子质量为56,此氧化物化学式为FeO,其相对分子质量为 160 。
2 3
18.某学生做石灰石和稀盐酸反应的五组对比实验,实验结果记录如下:
组序 加入石灰石的质量/g 盐酸溶液的质量/g 生成二氧化碳质量/g
1 10.0 200.0 3.96
2 20.0 200.0 X
3 40.0 200.0 15.84
4 60.0 200.0 22.00
5 100.0 200.0 y
(1)表格中x=7.92g;y= 22 g;(2)上述五组实验中,反应后盐酸有剩余的是= 1 、 2 、 3 (填组序号)。
(3)求:实验中所用的石灰石中碳酸钙的质量分数(列式计算)。90%
元素化合物(答案)
(一) 空气:1.空气是 混合物 (纯净物或混合物),按体积分数计算,其中氮气占 78% ,氧气占 21%
7,空气中含量最多的元素是 N 元素。
2.空气是一种宝贵的自然资源,空气中的主要污染性气体包括 CO 、 H S 、 SO 、 SO 、 NO 、 NO 等。
2 2 3 2
(二)水:1.电解水实验:
现象:和电源正极相连的一端产生 O ,和电源负极相连的一端产生 H ,VH:VO = 2: 1 ,反应的化学方
2 2 2 2
程式为2H O 2H ↑ +O ↑ 。
2 2 2
2.水的组成和构成:(1)水是由 氢、氧两种元素 组成的;
(2)每个水分子由 2 个氢原子 和 1 个氧原子 构成。
(3)天然水是 混合物 (纯净物或混合物)。水是人及一切生物生存所必需的,为了人类和社会经济的
可持续发展,我们必须爱护水资源,一方面要节约用水,另一方面要防止水体污染。水体污染的来源主要有
工业污染 、 农业污染 和 生活污染 。
(4)天然水有硬水和软水之分。含有 较多可溶性钙镁离子的化合物 的水叫做硬水,软水是
的水。检验硬水和软水的试剂是: 肥皂水 。降低水的硬度的方法是 煮沸或蒸馏 。
[ 练习 ]
( B )1.下列关于空气的叙述,错误的是
A.空气中最多的气体是氮气 B.空气中二氧化碳的含量是始终不变的
C.空气是一种重要的化工原料 D.空气是由多种单质和多种化合物组成的混合物
( A )2.下列气体中,均属于大气污染的一组是
A.CO SO NO B.N O CO C.H N SO D.CO CO SO
2 2 2 2 2 2 2 2 2 2
(D )3.地球上可以直接利用的淡水不足总水量的1%,节约用水、保护水资源是每个公民应尽的义务。下
列做法中,不正确的是
A.北京市政府给每户居民发放节水龙头 B.用喷灌、滴灌的方法浇灌园林或农田
C.将工业废水处理达标后排放 D.将生活污水任意排放
(A )4.下列说法中错误的是
A.电解水时生成氢气和氧气,说明水是由氢气和氧气组成的
B.氢气和氧气反应时只生成水,说明水是由氢、氧两种元素组成的
C.海水、湖水是混合物,氢气燃烧生成的水是纯净物
D.氢气燃烧生成水是化合反应,水电解生成氢气和氧气是分解反应
( B )5.为除去密闭容器中空气里的氧气,以测定空气中氧气的含量,可燃物最好选用
A.碳 B.磷 C.铁 D.石蜡
(A ) 6.北京是极度缺水的城市之一,所以我们在生产、生活中不仅要节约用水,也要防止水被污染。下
列做法正确的是
A.使用节水型洗衣机 B.使用含磷洗衣粉C.任意施用农药、化肥D.使用工业废水喷灌草地
(三)氧气:1.氧气的组成和构成:a)氧气由 氧元素 组成;b)每个氧分子是由 2 个氧原子 构成的。
2.氧气的物理性质:常温下,氧气为 无 色、 无 味的气体;加压降温后能转变成 淡蓝 色的液氧或固
态氧;氧气的密度比空气 大 ;氧气 不易 溶于水。
3.氧气的化学性质:
化学反应 现象 化学反应方程式、基本反应类型
碳在氧气 发出 白光 ,放出 大量热 , 生成使澄清石 C+O CO 化合反应
2 2
中燃烧 灰水变 浑浊 的气体。
硫在氧气 在空气中发出 淡蓝 色 火焰,在氧气中发 S+O SO 化合反应
2 2
中燃烧 出 蓝紫 色 火焰,放出 热 ,生成
_ 无色有刺激性气味 _ 的气体。
磷在氧气 火焰呈 黄 色燃烧产生大量的 白烟 ,同时 4P+5O 2PO 化合反应
2 2 5
中燃烧 放热。
镁在氧气 燃烧发出耀眼的 白光 ,生成 白色 固 2Mg+O 2MgO 化合反应
2
中燃烧 体,同时放热。
铁在氧气 剧烈燃烧, 火星四射 ,生成 黑 色固体,同 3Fe+2O FeO 化合反应
2 3 4
中燃烧 时放出热量。
8氢气在空 安静燃烧,发出 淡蓝 色的火焰,同时放 2H+O 2HO化合反应
2 2 2
气中燃烧 热,罩一个干冷烧杯,烧杯内壁出现 无色液
滴
CO 在空 燃烧发出 蓝 色火焰,放热,生成使澄清石 2CO+O 2CO 化合反应
2 2
气中燃烧 灰水变 浑浊 的气体。
甲烷在空 发出 蓝色 色火焰,罩一个干冷烧杯,烧杯内 CH +2O CO +2H O
4 2 2 2
气中燃烧 壁出现 无色液滴 ,加入澄清石灰水变 浑
浊 . 。
4.氧气的工业制法:分离液态空气——这是一个 物理 变化。
5. 氧气的用途:炼钢、 气焊、宇航飞行 、潜水 等。
[ 练习 ]
( B )1.中考体育测试中,运动场上发令枪打响时,产生白烟主要是
A.SO B.PO C.HO(气) D.CO
2 2 5 2 2
( C )2.下列实验现象叙述错误的是
A.硫在氧气中燃烧发出蓝紫色火焰 B.铁在氧气中燃烧时火星四射
C.木炭在氧气中燃烧发出淡蓝色火焰 D.一氧化碳在空气中燃烧发出蓝色火焰
(A)3.做铁丝在氧气里燃烧的实验时,预先在集气瓶里装少量水或细沙所起的主要作用是
A.防止瓶底炸裂 B.降低瓶内温度 C.增加氧气含量 D.吸收生成的物质
( D )4.做硫在氧气里燃烧的实验时,预先在集气瓶里装少量水或氢氧化钠溶液所起的主要作用是
A.防止瓶底炸裂 B.降低瓶内温度 C.增加氧气含量 D.吸收生成的物质
5.某气体为氢气、一氧化碳、甲烷中的一种,点燃该气体后,在火焰上方罩一个干燥而冷的烧杯,烧杯内壁
出现无色液滴,再向烧杯中注入少量澄清石灰水,振荡后澄清石灰水变浑浊,该气体的化学式为 C H 。
4
(四)二氧化碳:1.二氧化碳的组成和构成:
a)二氧化碳是由 C 、 O 两种 组成的;b)一个二氧化碳分子由 1 个碳原子 和 2 个氧原子 构成。
2.二氧化碳的物理性质:常温常压下为无色气体,密度比空气 大 , 能 溶于水。加压、降温,二氧化碳可
转化为固态;固态的二氧化碳叫做 干冰 。
3.二氧化碳的化学性质:
(1)一般情况下,既不燃烧也不支持燃烧:如下图所示,点燃两支短蜡烛,然后沿烧杯内壁倾倒二氧化碳。根
据实验回答:观察两支蜡烛的变化,写出实验现象。
现象: 蜡烛 从下往上依次 熄灭。
结论:这个实验说明了什么? (1)一般情况下,二氧化碳 , 本身不燃烧,不支持燃烧
(2)二氧化碳的密度 密度比空气大
(2)与水反应;现象:能使紫色石蕊试液变 红色 ,化学方程式:CO +H O= H CO;加热后又变为 紫色
2 2 2 3
色,化学方程式:HCO= H O+CO ↑ 。
2 3 2 2
(3)与澄清石灰水反应; 现象: 澄清石灰水变浑浊 。
化学方程式:CO + Ca(OH) = CaCO ↓ +H O
2 2 3 2
4.二氧化碳的用途:灭火剂、化工原料、 气体肥料、干冰作制冷剂、人工降雨 等。
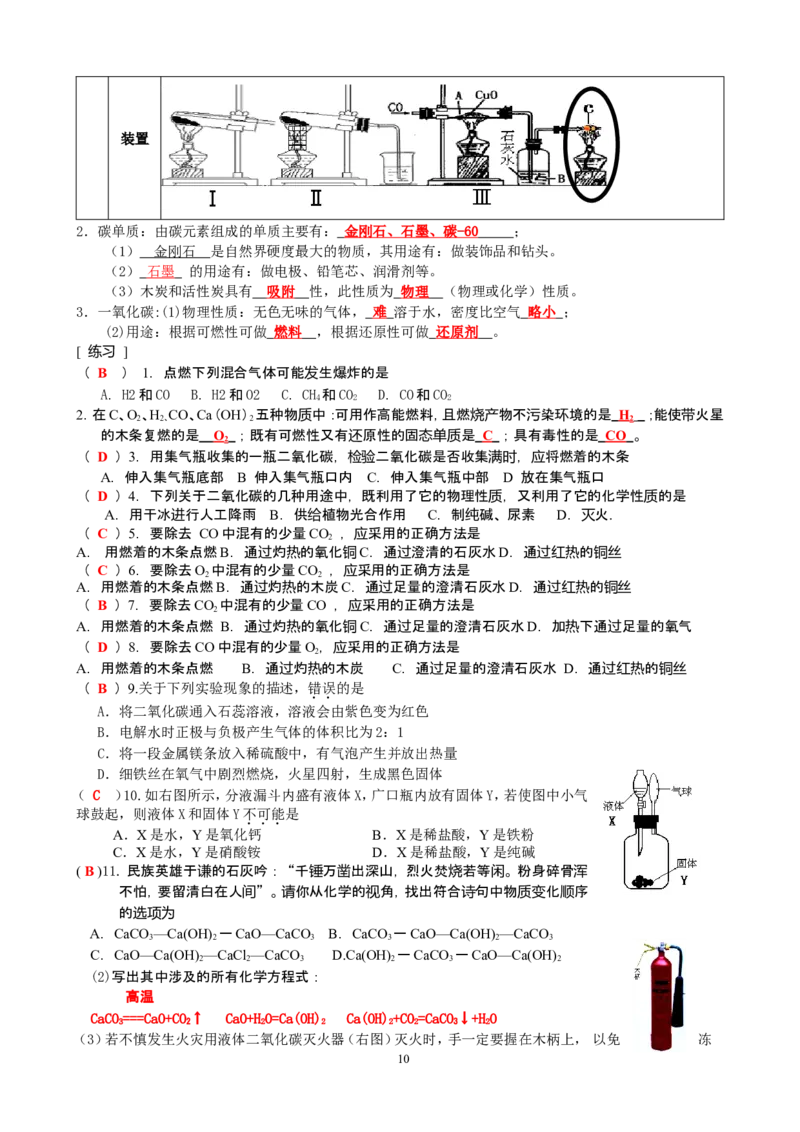
(五)碳、一氧化碳和氢气: 1.碳、一氧化碳和氢气性质对比表
物质 H C CO
2
性质
方程 2H+O 2HO C+O CO 2CO+O 2CO
2 2 2 2 2 2 2
可 式
燃 现象 安静燃烧,发出 淡蓝 发出 白 色光,生成气体通 发出 蓝 色火焰,生成气体通
性 色火焰,火焰上罩一干冷的 入石灰水,澄清石灰水变 入石灰水,澄清石灰水变浑浊
烧杯,内壁出现 无色液滴 。 浑浊 。 。
方程 △ 高温 △
还 式 H 2 +CuO==Cu+H 2 O C+2CuO==2Cu+CO 2 ↑ CO+CuO==Cu+CO 2
原 现象 黑色粉末逐渐变红色,试管 黑色粉末逐渐变 红色 ,生 黑色粉末逐渐变 红色 ,生成
性 口处有 无色液滴 出现。 成气体通入石灰水,澄清石 气体通入石灰水,澄清石灰水
灰水变浑浊 。 变 浑浊 。
9装置
2.碳单质:由碳元素组成的单质主要有: 金刚石、石墨、碳 -6 0 ;
(1) 金刚石 是自然界硬度最大的物质,其用途有:做装饰品和钻头。
(2) 石墨 的用途有:做电极、铅笔芯、润滑剂等。
(3)木炭和活性炭具有 吸附 性,此性质为 物理 (物理或化学)性质。
3.一氧化碳:(1)物理性质:无色无味的气体, 难 溶于水,密度比空气 略小 ;
(2)用途:根据可燃性可做 燃料 ,根据还原性可做 还原剂 。
[ 练习 ]
( B ) 1.点燃下列混合气体可能发生爆炸的是
A.H2和CO B.H2和O2 C.CH 和CO D.CO和CO
4 2 2
2.在C、O、H CO、Ca(OH)五种物质中:可用作高能燃料,且燃烧产物不污染环境的是 H ;能使带火星
2 2、 2 2
的木条复燃的是 O ;既有可燃性又有还原性的固态单质是 C ;具有毒性的是 CO 。
2
( D )3.用集气瓶收集的一瓶二氧化碳,检验二氧化碳是否收集满时,应将燃着的木条
A.伸入集气瓶底部 B 伸入集气瓶口内 C.伸入集气瓶中部 D 放在集气瓶口
( D )4.下列关于二氧化碳的几种用途中,既利用了它的物理性质,又利用了它的化学性质的是
A.用干冰进行人工降雨 B.供给植物光合作用 C.制纯碱、尿素 D.灭火.
( C )5.要除去 CO中混有的少量CO ,应采用的正确方法是
2
A.用燃着的木条点燃B.通过灼热的氧化铜C.通过澄清的石灰水D.通过红热的铜丝
( C )6.要除去O 中混有的少量CO ,应采用的正确方法是
2 2
A.用燃着的木条点燃B.通过灼热的木炭C.通过足量的澄清石灰水D.通过红热的铜丝
( B )7.要除去CO 中混有的少量CO ,应采用的正确方法是
2
A.用燃着的木条点燃 B.通过灼热的氧化铜C.通过足量的澄清石灰水D.加热下通过足量的氧气
( D )8.要除去CO中混有的少量O,应采用的正确方法是
2
A.用燃着的木条点燃 B.通过灼热的木炭 C.通过足量的澄清石灰水 D.通过红热的铜丝
( B )9.关于下列实验现象的描述,错误的是
A.将二氧化碳通入石蕊溶液,溶液会由紫色变为红色
B.电解水时正极与负极产生气体的体积比为2:1
C.将一段金属镁条放入稀硫酸中,有气泡产生并放出热量
D.细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
( C )10.如右图所示,分液漏斗内盛有液体X,广口瓶内放有固体Y,若使图中小气
球鼓起,则液体X和固体Y不可能是
A.X是水,Y是氧化钙 B.X是稀盐酸,Y是铁粉
C.X是水,Y是硝酸铵 D.X是稀盐酸,Y是纯碱
( B )11. 民族英雄于谦的石灰吟:“千锤万凿出深山,烈火焚烧若等闲。粉身碎骨浑
不怕,要留清白在人间”。请你从化学的视角,找出符合诗句中物质变化顺序
的选项为
A.CaCO —Ca(OH) 一CaO—CaCO B.CaCO 一CaO—Ca(OH) —CaCO
3 2 3 3 2 3
C.CaO—Ca(OH) —CaCl —CaCO D.Ca(OH) 一CaCO 一CaO—Ca(OH)
2 2 3 2 3 2
(2)写出其中涉及的所有化学方程式:
高温
CaCO===CaO+CO↑ CaO+HO=Ca(OH) Ca(OH)+CO=CaCO↓+HO
3 2 2 2 2 2 3 2
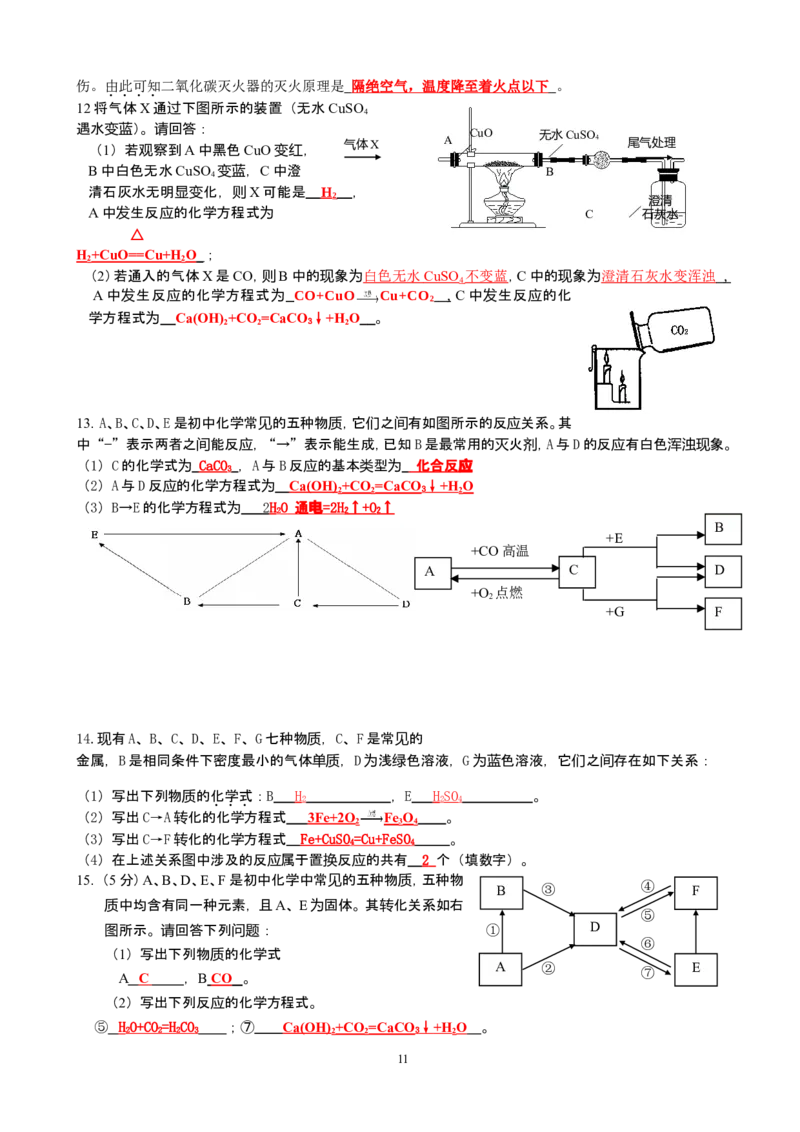
(3)若不慎发生火灾用液体二氧化碳灭火器(右图)灭火时,手一定要握在木柄上, 以免 冻
10伤。由此可知二氧化碳灭火器的灭火原理是 隔绝空气,温度降至着火点以下 。
12将气体X通过下图所示的装置(无水CuSO
4
遇水变蓝)。请回答:
CuO 无水CuSO
(1)若观察到A中黑色CuO变红, 气体X A 4 尾气处理
B中白色无水CuSO 变蓝,C中澄 B
4
清石灰水无明显变化,则X可能是 H ,
2
澄清
A中发生反应的化学方程式为 C 石灰水
△
H+CuO==Cu+H O ;
2 2
(2)若通入的气体X是CO,则B中的现象为 白色无水 CuSO 不 变蓝 ,C中的现象为 澄清石灰水 变浑浊 ,
4
A中发生反应的化学方程式为 CO+CuO Cu+CO , C中发生反应的化
2
学方程式为 Ca(OH) +CO=CaCO ↓+H O 。
2 2 3 2
13.A、B、C、D、E是初中化学常见的五种物质,它们之间有如图所示的反应关系。其
中“—”表示两者之间能反应,“→”表示能生成,已知B是最常用的灭火剂,A与D的反应有白色浑浊现象。
(1)C的化学式为 CaC O ,A与B反应的基本类型为 化合反应
3
(2)A与D反应的化学方程式为 Ca(OH ) +CO=CaCO ↓ +H O
2 2 3 2
(3)B→E的化学方程式为 2 H O 通电 =2 H ↑ + O↑
2 2 2
B
+E
+CO高温
A C D
+O 点燃
2
+G F
14.现有A、B、C、D、E、F、G七种物质,C、F是常见的
金属,B是相同条件下密度最小的气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如下关系:
(1)写出下列物质的化学式:B H ,E HSO 。
2 2 4
(2)写出C→A转化的化学方程式 3Fe+2O FeO 。
2 3 4
(3)写出C→F转化的化学方程式 Fe+CuS O=Cu+FeSO 。
4 4
(4)在上述关系图中涉及的反应属于置换反应的共有 2 个(填数字)。
15.(5分)A、B、D、E、F是初中化学中常见的五种物质,五种物
B ③ ④ F
质中均含有同一种元素,且A、E为固体。其转化关系如右
⑤
图所示。请回答下列问题: ① D
⑥
(1)写出下列物质的化学式
A ② E
⑦
A C ,B CO 。
(2)写出下列反应的化学方程式。
⑤ H O+CO=HCO ;⑦ Ca(OH ) +CO=CaCO ↓ +H O 。
2 2 2 3 2 2 3 2
11(3)已知A和D在高温条件下发生反应生成B,写出该反应的化学方程式
高温
C+CO ==2CO___________
2
16. A、B、C、D、X为初中常见的物质,其转化关系如
右图所示:
(1)若A、D为单质,其余均为化合物,则反应②的基本反应类型为_置换 反应,
反应的化学方程式为_ Zn+FeSO ==Fe+ZnSO 。
4 4
(2)若A、B、C均为氧化物,则气体X为_O_,反应②的化学方程式为_
2
CO+CuO Cu+CO _。
2
化学实验(答案)
一、基本操作
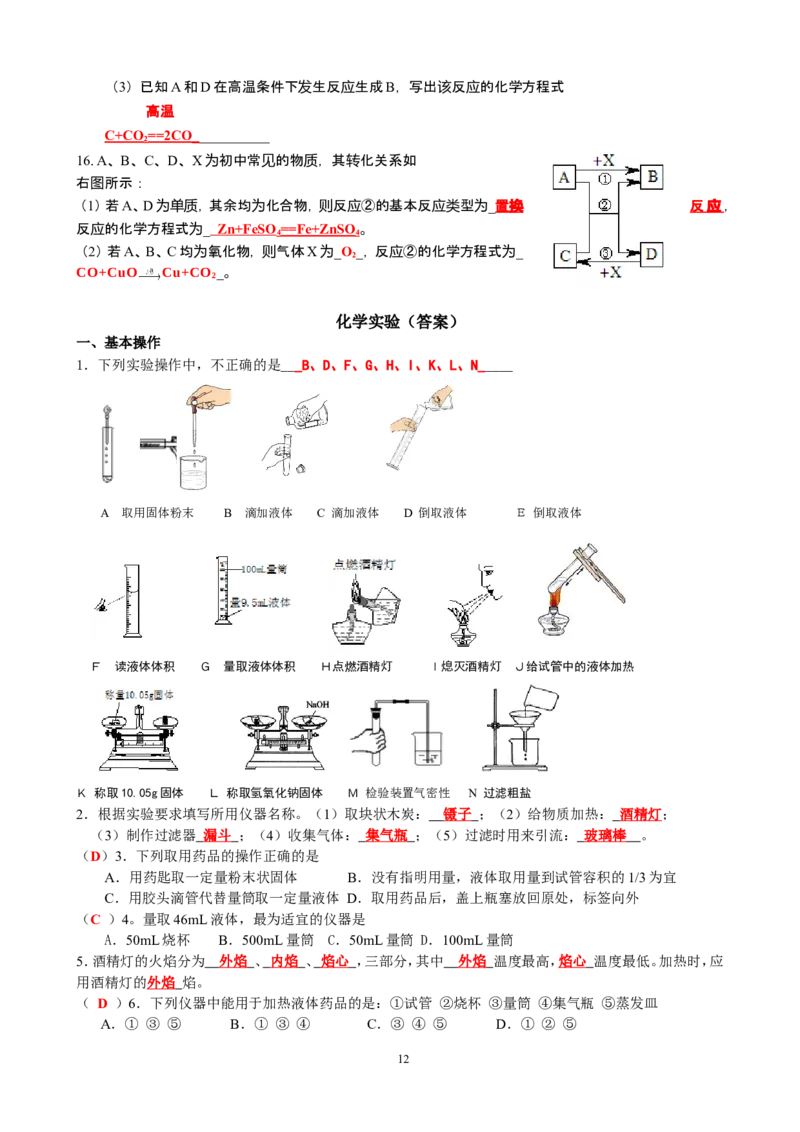
1.下列实验操作中,不正确的是___B、D、F、G、H、I、K、L、N_____
A 取用固体粉末 B 滴加液体 C 滴加液体 D 倒取液体 E 倒取液体
点燃
F 读液体体积 G 量取液体体积 H点燃酒精灯 I熄灭酒精灯 J给试管中的液体加热
K 称取10.05g固体 L 称取氢氧化钠固体 M 检验装置气密性 N 过滤粗盐
2.根据实验要求填写所用仪器名称。(1)取块状木炭: 镊子 ;(2)给物质加热: 酒精灯 ;
(3)制作过滤器 漏斗 ;(4)收集气体: 集气瓶 ;(5)过滤时用来引流: 玻璃棒 。
(D)3.下列取用药品的操作正确的是
A.用药匙取一定量粉末状固体 B.没有指明用量,液体取用量到试管容积的1/3为宜
C.用胶头滴管代替量筒取一定量液体 D.取用药品后,盖上瓶塞放回原处,标签向外
(C )4。量取46mL液体,最为适宜的仪器是
A.50mL烧杯 B.500mL量筒 C.50mL量筒 D.100mL量筒
5.酒精灯的火焰分为 外焰 、 内焰 、 焰心 ,三部分,其中 外焰 温度最高, 焰心 温度最低。加热时,应
用酒精灯的 外焰 焰。
( D )6.下列仪器中能用于加热液体药品的是:①试管 ②烧杯 ③量筒 ④集气瓶 ⑤蒸发皿
A.① ③ ⑤ B.① ③ ④ C.③ ④ ⑤ D.① ② ⑤
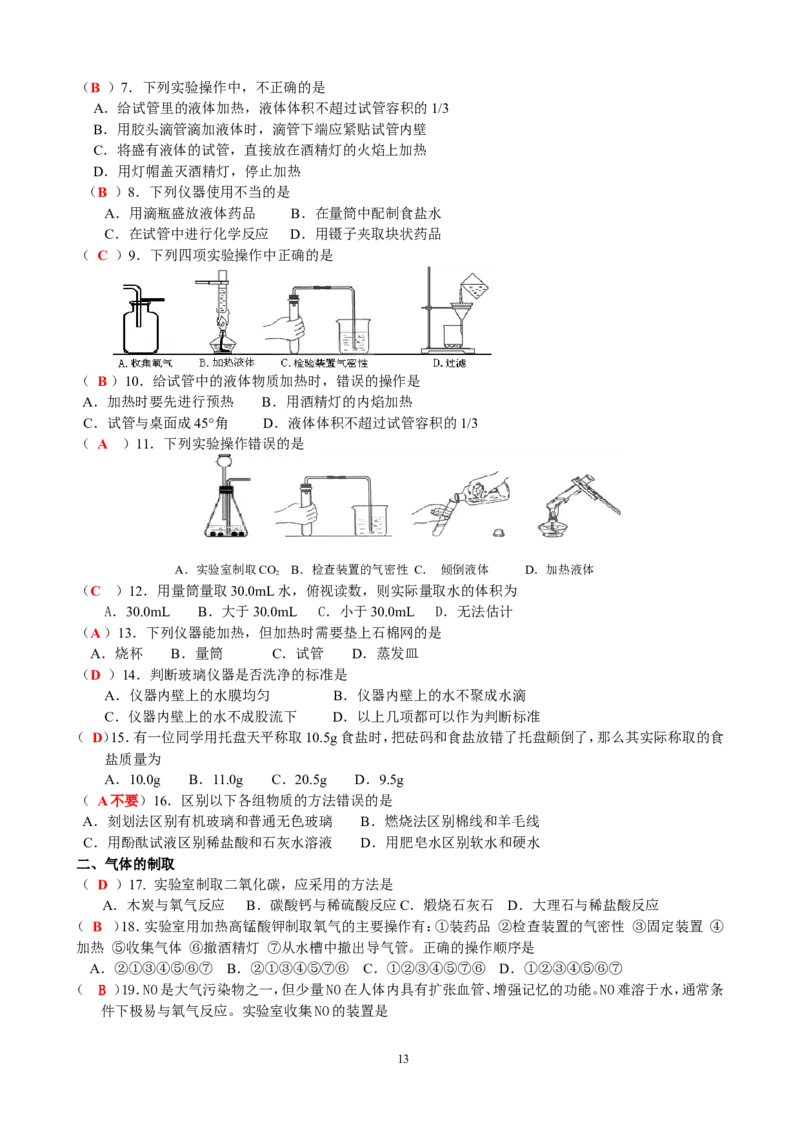
12(B )7.下列实验操作中,不正确的是
A.给试管里的液体加热,液体体积不超过试管容积的1/3
B.用胶头滴管滴加液体时,滴管下端应紧贴试管内壁
C.将盛有液体的试管,直接放在酒精灯的火焰上加热
D.用灯帽盖灭酒精灯,停止加热
(B )8.下列仪器使用不当的是
A.用滴瓶盛放液体药品 B.在量筒中配制食盐水
C.在试管中进行化学反应 D.用镊子夹取块状药品
( C )9.下列四项实验操作中正确的是
( B )10.给试管中的液体物质加热时,错误的操作是
A.加热时要先进行预热 B.用酒精灯的内焰加热
C.试管与桌面成45°角 D.液体体积不超过试管容积的1/3
( A )11.下列实验操作错误的是
A.实验室制取CO B.检查装置的气密性 C. 倾倒液体 D.加热液体
2
(C )12.用量筒量取30.0mL水,俯视读数,则实际量取水的体积为
A.30.0mL B.大于30.0mL C.小于30.0mL D.无法估计
(A )13.下列仪器能加热,但加热时需要垫上石棉网的是
A.烧杯 B.量筒 C.试管 D.蒸发皿
(D )14.判断玻璃仪器是否洗净的标准是
A.仪器内壁上的水膜均匀 B.仪器内壁上的水不聚成水滴
C.仪器内壁上的水不成股流下 D.以上几项都可以作为判断标准
( D)15.有一位同学用托盘天平称取10.5g食盐时,把砝码和食盐放错了托盘颠倒了,那么其实际称取的食
盐质量为
A.10.0g B.11.0g C.20.5g D.9.5g
( A 不要)16.区别以下各组物质的方法错误的是
A.刻划法区别有机玻璃和普通无色玻璃 B.燃烧法区别棉线和羊毛线
C.用酚酞试液区别稀盐酸和石灰水溶液 D.用肥皂水区别软水和硬水
二、气体的制取
( D )17. 实验室制取二氧化碳,应采用的方法是
A.木炭与氧气反应 B.碳酸钙与稀硫酸反应C.煅烧石灰石 D.大理石与稀盐酸反应
( B )18.实验室用加热高锰酸钾制取氧气的主要操作有:①装药品 ②检查装置的气密性 ③固定装置 ④
加热 ⑤收集气体 ⑥撤酒精灯 ⑦从水槽中撤出导气管。正确的操作顺序是
A.②①③④⑤⑥⑦ B.②①③④⑤⑦⑥ C.①②③④⑤⑦⑥ D.①②③④⑤⑥⑦
( B )19.NO是大气污染物之一,但少量NO在人体内具有扩张血管、增强记忆的功能。NO难溶于水,通常条
件下极易与氧气反应。实验室收集NO的装置是
13A. B. C. D.
(D )20.用集气瓶收集的一瓶二氧化碳,检验二氧化碳是否收集满时,应将燃着的木条
A.伸入集气瓶底部 B 伸入集气瓶口内 C.伸入集气瓶中部 D 放在集气瓶口
21.下面是实验室制取气体的装置图,回答下列问题:
(1)写出装置中有标号的仪器名称:① 试管 ② 集气瓶 ③ 酒精灯
(2)按要求填写装置代号
制取气体 发生装置 收集装置 制取气体反应的化学方程式
H CE 2KMnO KMnO+MnO+O↑
4 2 4 2 2
氧气
B CE 2HO 2HO+O↑
2 2 2 2
H CE
2KClO 2KCl+3O↑
3 2
二氧化碳 B C CaCO+2HCl=CaCl+HO+CO↑
3 2 2 2
22.根据题目要求回答下列问题:
A B C D E
(1)若用碳还原氧化铜,应选择的装置为 _ D ,如图实验可观察到的现象是 黑色粉末变红色,澄清石灰水
变浑浊 ,写出碳与氧化铜反应的化学方程式为C+2CuO 2Cu+CO ↑ ;
2
(2)如果实验室又为你提供如下仪器(见下图),请你组装两套制取和收集二氧化碳的装置(用序号填空)。
方案一:__ahbk 或 aibk_ _;方案二:_ghbk或 gibk __。
a b c d e f g h i z k
23.实验室中常用氯酸钾受热分解制取氧气。
(1)写出该反应的化学方程式___2KClO 2KCl+3O↑_____
3 2
(2)为组装制氧发生装置,请你从下图a-i中选择所需的仪器(填序号,下同)__adhg___ ______。
装药品前应首先进行 ___检查装置的气密性____。
14(3)实验室里还可采用右上图装置,通过分解过氧化氢(H0)的方法制取氧气。此装置中锥形瓶可用
2 2
上图中的哪些仪器替代 f_,收集氧气的方法还可以用__ 向上排气法 _。上右图发生装
置还可用于制取的气体有__ H_______。
2
三、实验探究
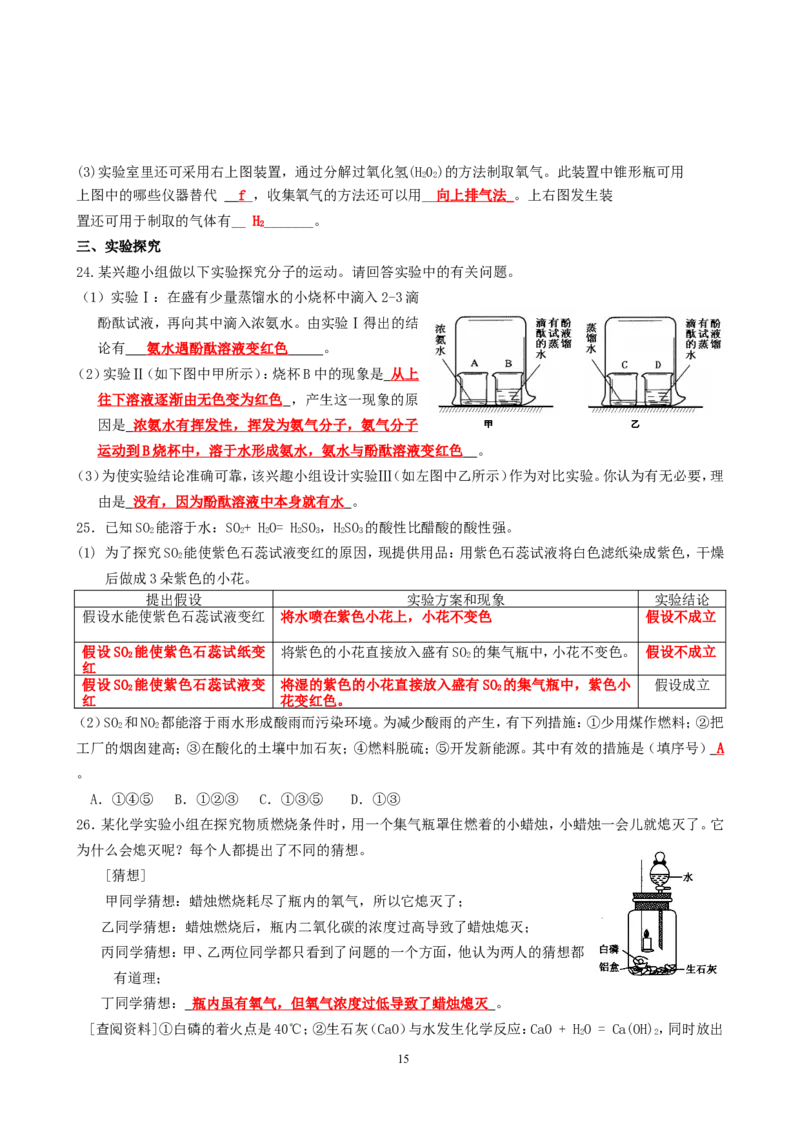
24.某兴趣小组做以下实验探究分子的运动。请回答实验中的有关问题。
(1)实验Ⅰ:在盛有少量蒸馏水的小烧杯中滴入2-3滴
酚酞试液,再向其中滴入浓氨水。由实验Ⅰ得出的结
论有 氨水遇酚酞溶液变红色 。
(2)实验Ⅱ(如下图中甲所示):烧杯B中的现象是 从上
往下溶液逐渐由无色变为红色 ,产生这一现象的原
因是 浓氨水有挥发性,挥发为氨气分子,氨气分子
运动到 B 烧杯中,溶于水形成氨水,氨水与酚酞溶液变红色 。
(3)为使实验结论准确可靠,该兴趣小组设计实验Ⅲ(如左图中乙所示)作为对比实验。你认为有无必要,理
由是 没有,因为酚酞溶液中本身就有水 。
25.已知SO 能溶于水:SO+ HO= HSO,HSO 的酸性比醋酸的酸性强。
2 2 2 2 3 2 3
(1) 为了探究SO 能使紫色石蕊试液变红的原因,现提供用品:用紫色石蕊试液将白色滤纸染成紫色,干燥
2
后做成3朵紫色的小花。
提出假设 实验方案和现象 实验结论
假设水能使紫色石蕊试液变红 将水喷在紫色小花上,小花不变色 假设不成立
假设SO 能使紫色石蕊试纸变 将紫色的小花直接放入盛有SO 的集气瓶中,小花不变色。 假设不成立
2 2
红
假设SO 能使紫色石蕊试液变 将湿的紫色的小花直接放入盛有SO 的集气瓶中,紫色小 假设成立
2 2
红 花变红色。
(2)SO 和NO 都能溶于雨水形成酸雨而污染环境。为减少酸雨的产生,有下列措施:①少用煤作燃料;②把
2 2
工厂的烟囱建高;③在酸化的土壤中加石灰;④燃料脱硫;⑤开发新能源。其中有效的措施是(填序号) A
。
A.①④⑤ B.①②③ C.①③⑤ D.①③
26.某化学实验小组在探究物质燃烧条件时,用一个集气瓶罩住燃着的小蜡烛,小蜡烛一会儿就熄灭了。它
为什么会熄灭呢?每个人都提出了不同的猜想。
[猜想]
甲同学猜想:蜡烛燃烧耗尽了瓶内的氧气,所以它熄灭了;
乙同学猜想:蜡烛燃烧后,瓶内二氧化碳的浓度过高导致了蜡烛熄灭;
丙同学猜想:甲、乙两位同学都只看到了问题的一个方面,他认为两人的猜想都
有道理;
丁同学猜想: 瓶内虽有氧气,但氧气浓度过低导致了蜡烛熄灭 。
[查阅资料]①白磷的着火点是40℃;②生石灰(CaO)与水发生化学反应:CaO + HO = Ca(OH),同时放出
2 2
15大量的热。
[实验设计]大家激烈地讨论,很难达成一致。于是丁同学设计了如右图所示的装置来验证自己的猜想。
实验步骤 实验现象 实验分析 实验结论
1. 取一小块白磷放在一铝箔制的
蜡烛燃烧需满足的条件:
小盒中,然后放入装有生石灰的集 燃烧的蜡烛一会儿就
①温度达到着火点;
气瓶内。点燃蜡烛,塞紧胶塞,观察 熄灭了。
② 与氧气接触 。 丁同学的
现象。
猜想是正
2. 待冷却后,打开分液漏斗活塞, 白磷燃烧需满足的条件与
铝盒中的白磷燃烧, 确的。
向集气瓶中注入少量水,立即关闭 蜡烛燃烧的条件相同,白
放出热量的同时产生
活塞,观察现象。 磷燃烧的化学方程式:
了 白烟 。
4P + 5O ==㎏2PO
2 2 5
[实验反思]①在该实验中,生石灰的主要作用是与水反应放热使瓶内温度达到白磷的着火点 。
②实验结束后,集气瓶底部的固体中可能含有哪些成分?(写出三种即可) CaO 、 Ca(OH) 、 CaCO 、 (P O)
2 3 2 5
。
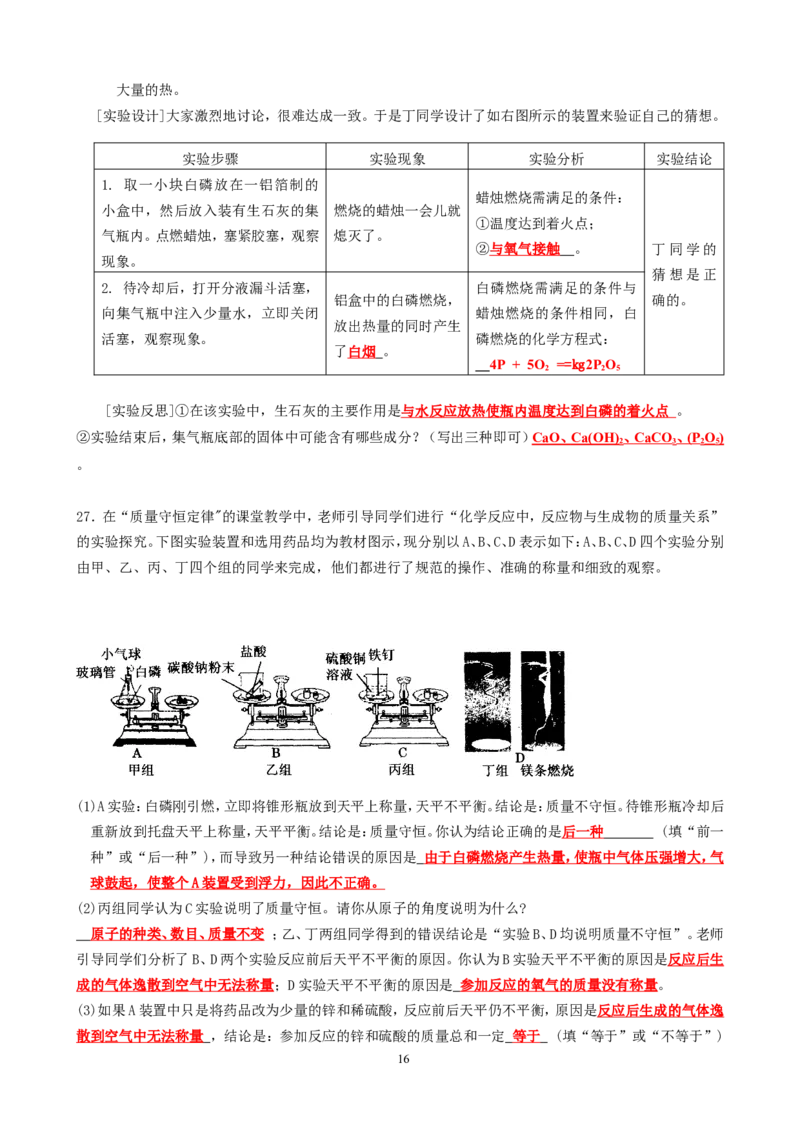
27.在“质量守恒定律"的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”
的实验探究。下图实验装置和选用药品均为教材图示,现分别以A、B、C、D表示如下:A、B、C、D四个实验分别
由甲、乙、丙、丁四个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察。
(1)A实验:白磷刚引燃,立即将锥形瓶放到天平上称量,天平不平衡。结论是:质量不守恒。待锥形瓶冷却后
重新放到托盘天平上称量,天平平衡。结论是:质量守恒。你认为结论正确的是 后一种 (填“前一
种”或“后一种”),而导致另一种结论错误的原因是 由于白磷燃烧产生热量,使瓶中气体压强增大,气
球鼓起,使整个 A 装置受到浮力,因此不正确。
(2)丙组同学认为C实验说明了质量守恒。请你从原子的角度说明为什么?
原子的种类、数目、质量不变 ;乙、丁两组同学得到的错误结论是“实验B、D均说明质量不守恒”。老师
引导同学们分析了B、D两个实验反应前后天平不平衡的原因。你认为B实验天平不平衡的原因是反应后生
成的气体逸散到空气中无法称量;D实验天平不平衡的原因是 参加反应的氧气的质量没有称量 。
(3)如果A装置中只是将药品改为少量的锌和稀硫酸,反应前后天平仍不平衡,原因是反应后生成的气体逸
散到空气中无法称量 ,结论是:参加反应的锌和硫酸的质量总和一定 等于 (填“等于”或“不等于”)
16生成的硫酸锌和氢气的质量总和。
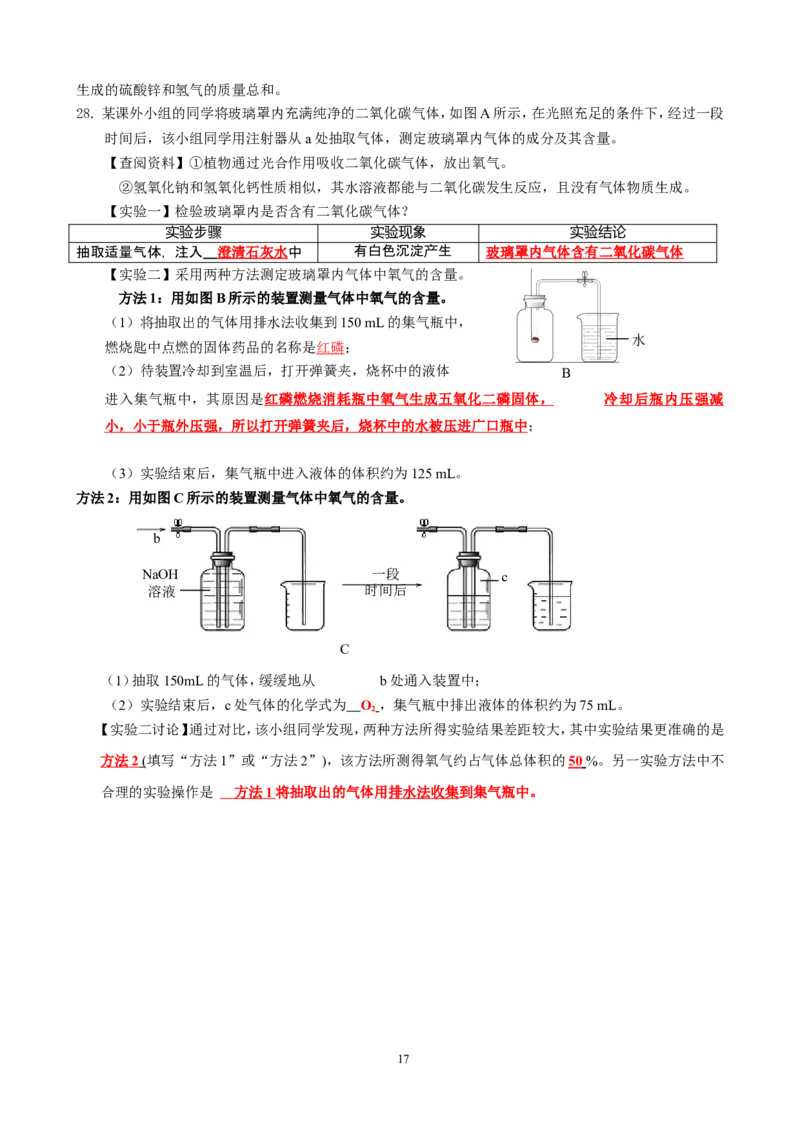
28. 某课外小组的同学将玻璃罩内充满纯净的二氧化碳气体,如图A所示,在光照充足的条件下,经过一段
时间后,该小组同学用注射器从a处抽取气体,测定玻璃罩内气体的成分及其含量。
【查阅资料】①植物通过光合作用吸收二氧化碳气体,放出氧气。
②氢氧化钠和氢氧化钙性质相似,其水溶液都能与二氧化碳发生反应,且没有气体物质生成。
【实验一】检验玻璃罩内是否含有二氧化碳气体?
实验步骤 实验现象 实验结论
抽取适量气体,注入 澄清石灰水 中 有白色沉淀产生 玻璃罩内气体含有二氧化碳气体
【实验二】采用两种方法测定玻璃罩内气体中氧气的含量。
方法1:用如图B所示的装置测量气体中氧气的含量。
(1)将抽取出的气体用排水法收集到150 mL的集气瓶中,
水
燃烧匙中点燃的固体药品的名称是红磷;
(2)待装置冷却到室温后,打开弹簧夹,烧杯中的液体 B
进入集气瓶中,其原因是 红磷燃烧消耗瓶中氧气生成五氧化二磷固体 , 冷却后瓶内压强减
小,小于瓶外压强 , 所以打开弹簧夹 后 ,烧杯中的水被压进广口瓶中 ;
(3)实验结束后,集气瓶中进入液体的体积约为125 mL。
方法2:用如图C所示的装置测量气体中氧气的含量。
b
NaOH 一段 c
溶液 时间后
C
(1)抽取150mL的气体,缓缓地从 b处通入装置中;
(2)实验结束后,c处气体的化学式为 O ,集气瓶中排出液体的体积约为75 mL。
2
【实验二讨论】通过对比,该小组同学发现,两种方法所得实验结果差距较大,其中实验结果更准确的是
方法 2 (填写“方法1”或“方法2”),该方法所测得氧气约占气体总体积的 50 %。另一实验方法中不
合理的实验操作是 方法 1 将抽取出的气体用排水法收集到集气瓶中。
17