文档内容
zxxk.com
身边的化学物质--酸、碱、盐、化肥
题一: 下列四种物质久置空气中,质量增加且没有新物质生成的是( )
A.浓氨水 B.烧碱 C.浓硫酸 D.浓盐酸
题二: 两只完全相同的烧杯,分别装有质量相等的浓盐酸和浓硫酸,将它们放置在空气中一段时间,
在这过程中( )
A.浓盐酸会吸收空气中的水
B.浓盐酸中溶质的质量分数逐渐增大
C.浓硫酸会吸收空气中的水
D.浓硫酸中溶质的质量分数逐渐增大
题三: 甲、乙、丙、丁四种溶液中,分别含有Ba2+、Mg2+、Na+、H+、Cl、OH、CO 、SO 中的一种阳
离子和一种阴离子。为确定四种溶液中分别含有哪种阳离子或阴离子,进行了下面实验:
①将甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成;
②将乙、丁溶液混合,有气泡产生;
③向丙溶液中滴入AgNO 溶液,可明显观察到白色沉淀,加稀硝酸后,沉淀不消失。
3
分析实验得到的以下结论,不正确的是( )
A.甲溶液中一定含有Ba2+ B.乙溶液中可能含有SO
[来源:学科网ZXXK]
C.丙溶液中一定含有Cl D.丁溶液中一定含有Na+
题四: 下图中的六个圆A、B、C、D、E、F分别表示六种物质,蓝色溶液A与C反应能生成两种沉淀,
B为氧化物,C、D、E、F分别是碳酸钠溶液、稀硫酸、氢氧化钡溶液和氢氧化钠溶液中的一种,E中溶质
可用于生产洗涤剂。用“→”表示一种物质能转化为另一种物质,用两圆相切或“——”表示两种物
质可以发生化学反应,六种物质之间的部分反应及转化关系如图所示。请利用初中化学知识回答下列
问题:
(1)在图中标出六种物质(或溶质)的化学式。
(2)C与F反应的化学方程式为________________。
(3)E与F反应的实验现象为__________________。
题五: 向甲物质中逐渐加入乙物质至过量。若x轴表示加入乙物质的质量,则下列选项与下图不相
符合的是 ( )
选项 甲物质 乙物质 y轴表示的含义
A 二氧化锰 过氧化氢溶液 二氧化锰的质量
B t℃的水 硝酸钾 t℃时硝酸钾的溶解度
C 氯化银 稀硝酸 氯化银的质量
D 饱和石灰水 生石灰 溶液的质量
0zxxk.com
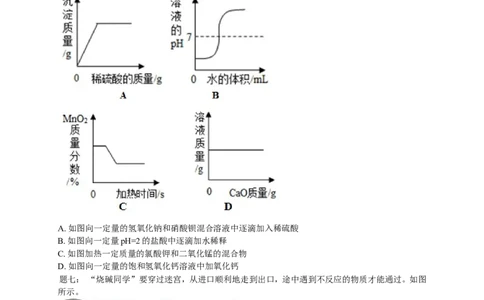
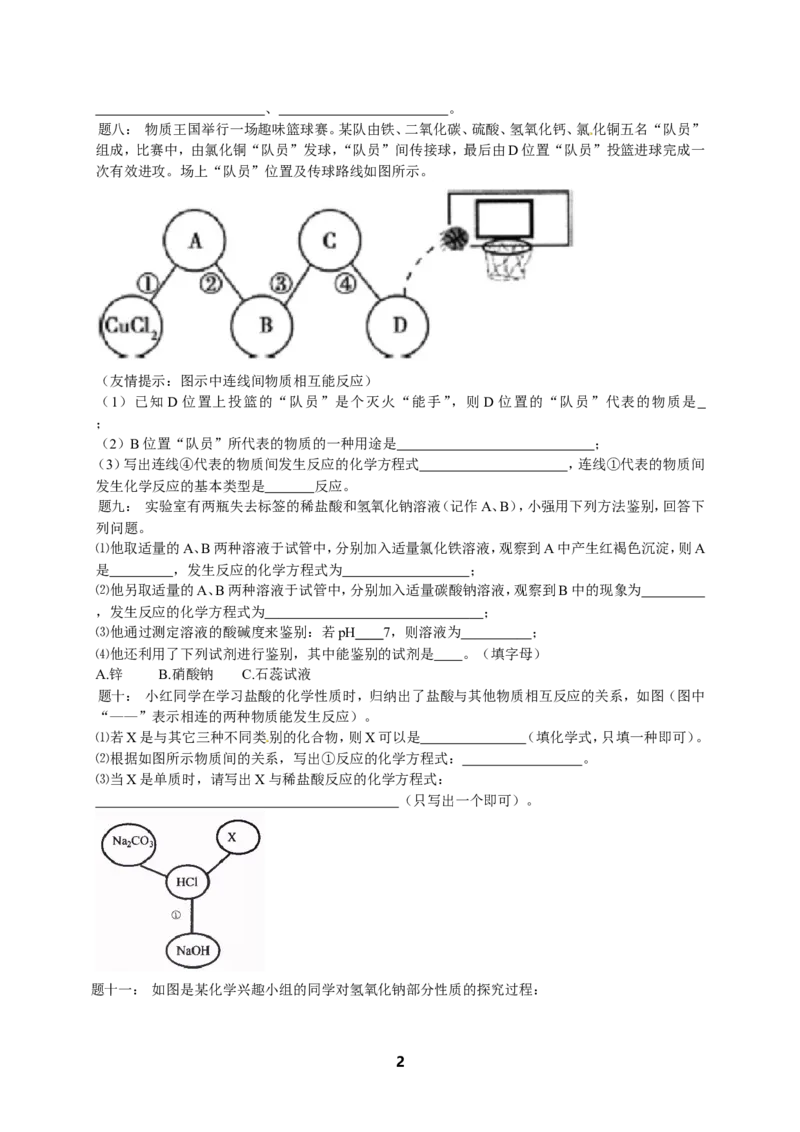
题六: 下列图象与对应的叙述相符合的是( )
A. 如图向一定量的氢氧化钠和硝酸钡混合溶液中逐滴加入稀硫酸
B. 如图向一定量pH=2的盐酸中逐滴加水稀释
C. 如图加热一定质量的氯酸钾和二氧化锰的混合物
D. 如图向一定量的饱和氢氧化钙溶液中加氧化钙
[来源:学科网]
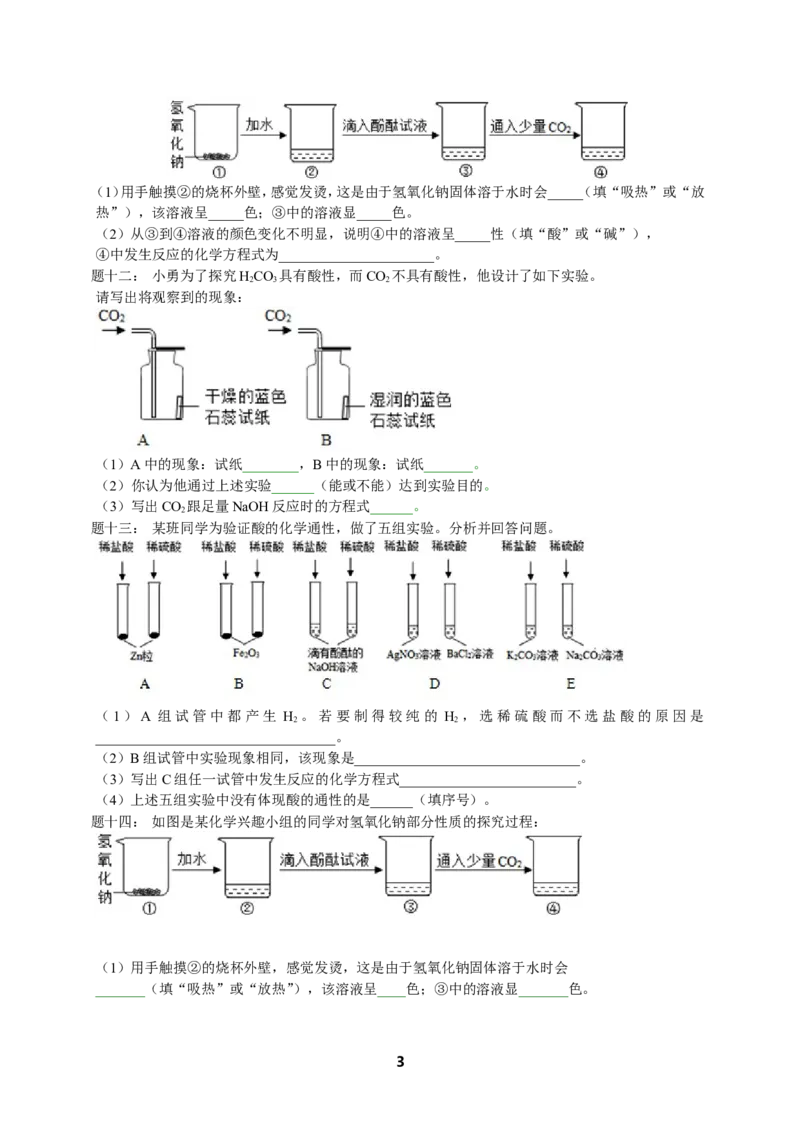
题七: “烧碱同学”要穿过迷宫,从进口顺利地走到出口,途中遇到不反应的物质才能通过。如图
所示。
⑴请你在答题卡中用“连续线”画出烧碱应行走的路线。
⑵烧碱在刚进迷宫时,碰到了两种阻止他前进的物质,请写出化学反应的方程式:
1zxxk.com
、 。
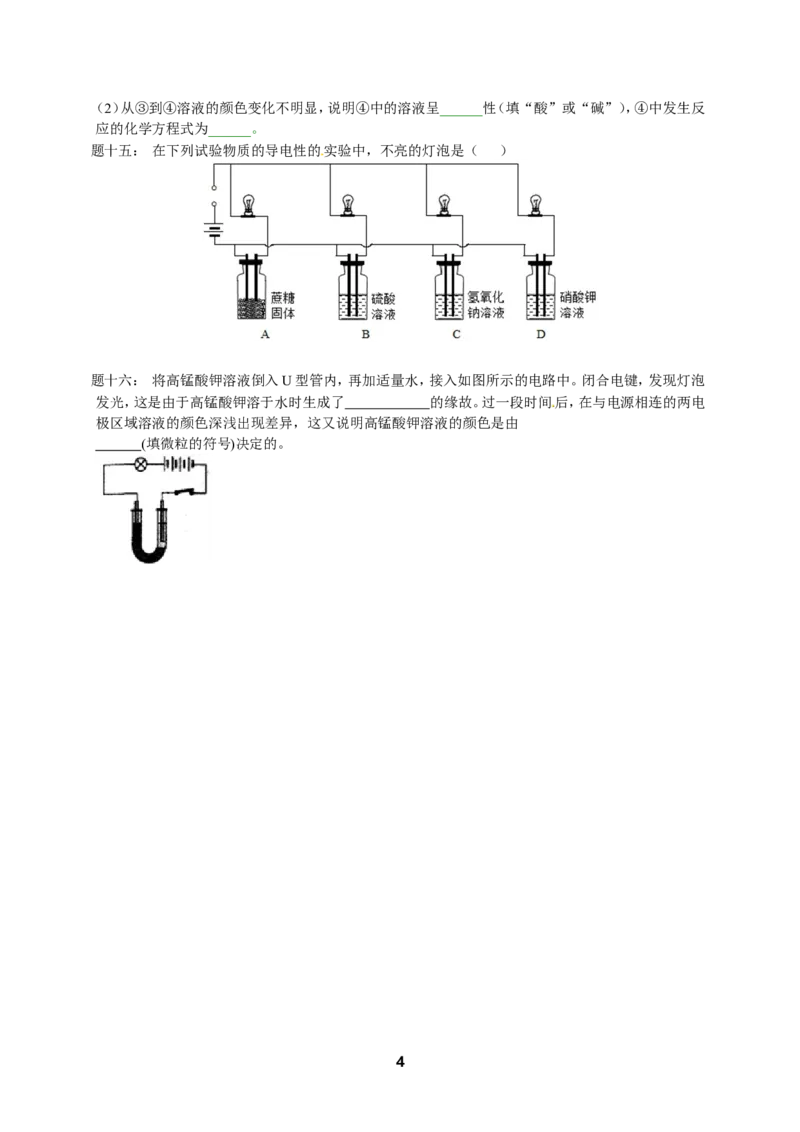
题八: 物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、硫酸、氢氧化钙、氯化铜五名“队员”
组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成一
次有效进攻。场上“队员”位置及传球路线如图所示。
(友情提示:图示中连线间物质相互能反应)
(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置的“队员”代表的物质是
;
(2)B位置“队员”所代表的物质的一种用途是 ;
(3)写出连线④代表的物质间发生反应的化学方程式 ,连线①代表的物质间
发生化学反应的基本类型是 反应。
题九: 实验室有两瓶失去标签的稀盐酸和氢氧化钠溶液(记作A、B),小强用下列方法鉴别,回答下
列问题。
⑴他取适量的A、B两种溶液于试管中,分别加入适量氯化铁溶液,观察到A中产生红褐色沉淀,则A
是 ,发生反应的化学方程式为 ;
⑵他另取适量的A、B两种溶液于试管中,分别加入适量碳酸钠溶液,观察到B中的现象为
,发生反应的化学方程式为 ;
⑶他通过测定溶液的酸碱度来鉴别:若pH 7,则溶液为 ;
⑷他还利用了下列试剂进行鉴别,其中能鉴别的试剂是 。(填字母)
A.锌 B.硝酸钠 C.石蕊试液
题十: 小红同学在学习盐酸的化学性质时,归纳出了盐酸与其他物质相互反应的关系,如图(图中
“——”表示相连的两种物质能发生反应)。
⑴若X是与其它三种不同类别的化合物,则X可以是 (填化学式,只填一种即可)。
⑵根据如图所示物质间的关系,写出①反应的化学方程式: 。
⑶当X是单质时,请写出X与稀盐酸反应的化学方程式:
(只写出一个即可)。
题十一: 如图是某化学兴趣小组的同学对氢氧化钠部分性质的探究过程:
2zxxk.com
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会_____(填“吸热”或“放
热”),该溶液呈_____色;③中的溶液显_____色。
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈_____性(填“酸”或“碱”),
④中发生反应的化学方程式为______________________。
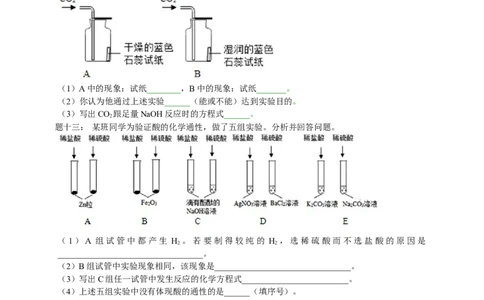
题十二: 小勇为了探究HCO 具有酸性,而CO 不具有酸性,他设计了如下实验。
2 3 2
请写出将观察到的现象:
(1)A中的现象:试纸________,B中的现象:试纸_______。
(2)你认为他通过上述实验______(能或不能)达到实验目的。
(3)写出CO 跟足量NaOH反应时的方程式______。
2
题十三: 某班同学为验证酸的化学通性,做了五组实验。分析并回答问题。
(1)A 组试管中都产生 H 。若要制得较纯的 H ,选稀硫酸而不选盐酸的原因是
2 2
__________________________________。
(2)B组试管中实验现象相同,该现象是________________________________。
(3)写出C组任一试管中发生反应的化学方程式_________________________。
(4)上述五组实验中没有体现酸的通性的是______(填序号)。
题十四: 如图是某化学兴趣小组的同学对氢氧化钠部分性质的探究过程:
(1)用手触摸②的烧杯外壁,感觉发烫,这是由于氢氧化钠固体溶于水时会
_______(填“吸热”或“放热”),该溶液呈____色;③中的溶液显_______色。
3zxxk.com
(2)从③到④溶液的颜色变化不明显,说明④中的溶液呈______性(填“酸”或“碱”),④中发生反
应的化学方程式为______。
题十五: 在下列试验物质的导电性的实验中,不亮的灯泡是( )
题十六: 将高锰酸钾溶液倒入U型管内,再加适量水,接入如图所示的电路中。闭合电键,发现灯泡
发光,这是由于高锰酸钾溶于水时生成了 的缘故。过一段时间后,在与电源相连的两电
极区域溶液的颜色深浅出现差异,这又说明高锰酸钾溶液的颜色是由
[来源:Z&xx&k.Com]
(填微粒的符号)决定的。
4zxxk.com
身边的化学物质--酸、碱、盐、化肥课后练习参考答案
题一: C
详解:浓氨水、浓盐酸都具有挥发性,都会因挥发出溶质而使溶液质量减小;烧碱固体在空气中易潮
解并能与二氧化碳发生化学反应而变质(生成碳酸钠),从而使固体质量增加;浓硫酸具有吸水性,露
置会因吸收空气中的水蒸气而使质量增加,由于不发生化学变化,因而没有新物质生成。本题应选
C。
题二: C
详解:浓盐酸具有挥发性,会使溶液中的溶质质量减少(溶剂质量不变),则浓盐酸中溶质的质量分数
逐渐减小,A、B项均错误;浓硫酸具有吸水性,会吸收空气中的水蒸气,溶质质量不变,溶剂质量增加,
浓硫酸中溶质的质量分数会逐渐减小,C项正确、D项错误。
题三: D
详解:由“将乙、丁溶液混合,有气泡产生”可推断出乙、丁两溶液中一定含有H+和CO 两种离子,
由于BaCO 难溶于水、MgCO 微溶于水,可确定乙、丁中含CO 的溶液一定是NaCO,则乙、丁中
3 3 2 3
的另一种物质是HCl或HSO ;由“甲溶液分别与其他三种溶液混合,都观察到白色沉淀生成”可推
2 4
断出甲溶液中一定含有 Ba2+,由于OH与Mg2+ 和H+ 都不能共存于同一溶液中,则可确定甲是
Ba(OH) ,可进一步确定乙、丁中的另一种物质是HSO [HCl与Ba(OH) 反应的产物中没有沉淀],则
2 2 4 2
余下的Mg2+ 和Cl便存在于丙溶液中(即丙是MgCl ,实验③也印证了该推断是正确的),由于只能
2
确定乙、丁为HSO 和NaCO 中的一种,因此无法确定丁溶液中是否一定含有Na+。D项结论不正确。
2 4 2 3
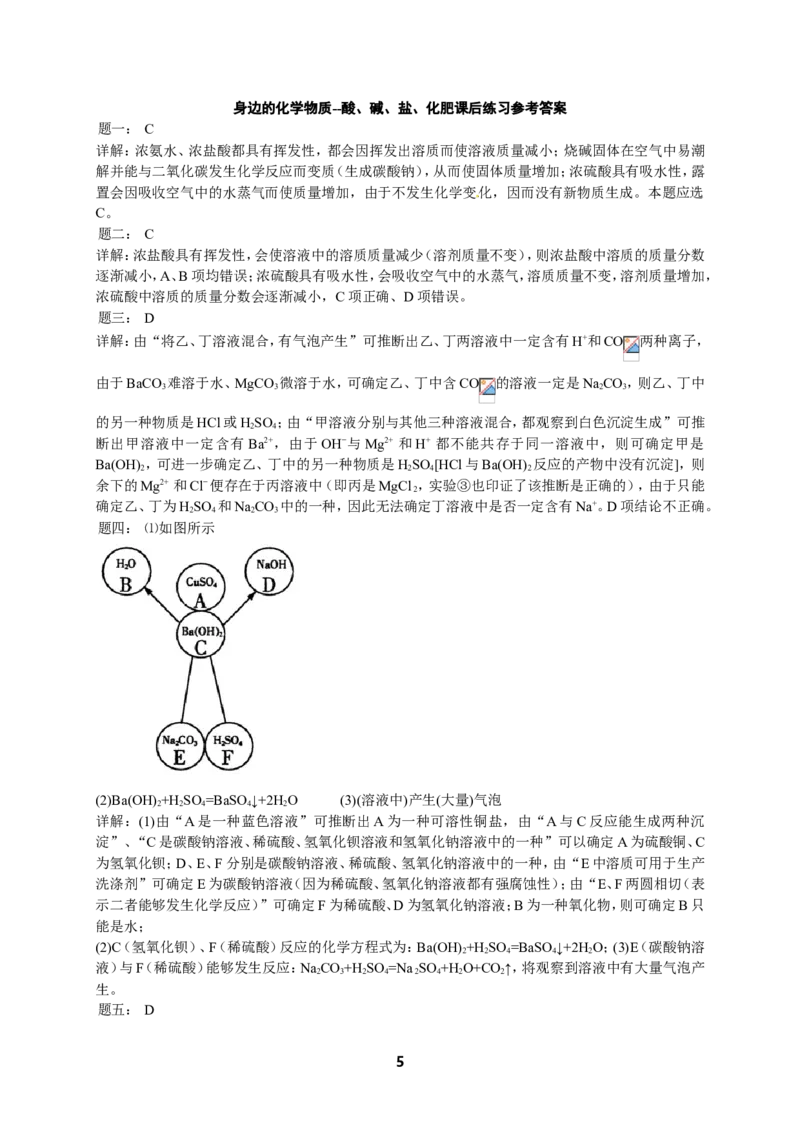
题四: ⑴如图所示
(2)Ba(OH) +H SO =BaSO ↓+2H O (3)(溶液中)产生(大量)气泡
2 2 4 4 2
详解:(1)由“A是一种蓝色溶液”可推断出A为一种可溶性铜盐,由“A与C反应能生成两种沉
淀”、“C是碳酸钠溶液、稀硫酸、氢氧化钡溶液和氢氧化钠溶液中的一种”可以确定A为硫酸铜、C
为氢氧化钡;D、E、F分别是碳酸钠溶液、稀硫酸、氢氧化钠溶液中的一种,由“E中溶质可用于生产
洗涤剂”可确定E为碳酸钠溶液(因为稀硫酸、氢氧化钠溶液都有强腐蚀性);由“E、F两圆相切(表
示二者能够发生化学反应)”可确定F为稀硫酸、D为氢氧化钠溶液;B为一种氧化物,则可确定B只
能是水;
(2)C(氢氧化钡)、F(稀硫酸)反应的化学方程式为:Ba(OH) +H SO =BaSO ↓+2H O;(3)E(碳酸钠溶
2 2 4 4 2
液)与F(稀硫酸)能够发生反应:NaCO+H SO =Na SO +H O+CO↑,将观察到溶液中有大量气泡产
2 3 2 4 2 4 2 2
生。
题五: D
5zxxk.com
详解:在用二氧化锰催化分解过氧化氢制取氧气的反应中,二氧化锰做该反应的催化剂,其质量在反
应前后不变,A项正确;固体物质的溶解度与温度有关,若温度不变,则硝酸钾的溶解度不变,B项正
确;氯化银沉淀不能溶于稀硝酸,C项正确;向饱和石灰水中加入生石灰,生石灰能与水反应生成氢
氧化钙,会使溶液中溶剂的质量减少而导致一部分氢氧化钙从溶液中析出,氢氧化钙的溶解度随温度
升高而减小,由于生石灰和水反应放出的大量热量使溶液的温度升高,又会导致一部分氢氧化钙从溶
液中析出,使反应后所得溶液的质量会减小,D项错误。
题六: A
详解:向一定量的氢氧化钠和硝酸钡混合溶液中逐滴加入稀硫酸时,稀硫酸能同时和氢氧化钠及硝
酸钡反应,生成不溶于稀硝酸的硫酸钡沉淀,当硝酸钡完全反应后,沉淀质量不再增大,A项图象与
对应的叙述相符合;稀释盐酸时,酸性减弱,pH升高,但所得溶液的pH始终小于7,不会等于或大于
7,B项图象与对应的叙述不符合;加热一定质量的氯酸钾和二氧化锰的混合物时,由于二氧化锰做该
反应的催化剂,其质量在反应前后不变,随着产生氧气质量的增多,试管中固体质量不断变小,二氧
化锰的质量分数不断增大,当氯酸钾完全分解后质量不变,则二氧化锰的质量分数在反应过程中不断
增大,至反应完全时不变,C项图象与对应的叙述不符合;向一定量的饱和氢氧化钙溶液中加氧化钙
时,氧化钙能够与溶液中的水发生反应,使氢氧化钙溶液中的溶剂减少,导致溶质析出,使氢氧化钙
溶液的质量减少(另外,该反应会放出大量热量,也会使溶液温度升高,氢氧化钙的溶解度随温度的
升高而减小,溶液中也会析出溶质,导致溶液质量减少),D项图象与对应的叙述不符合。
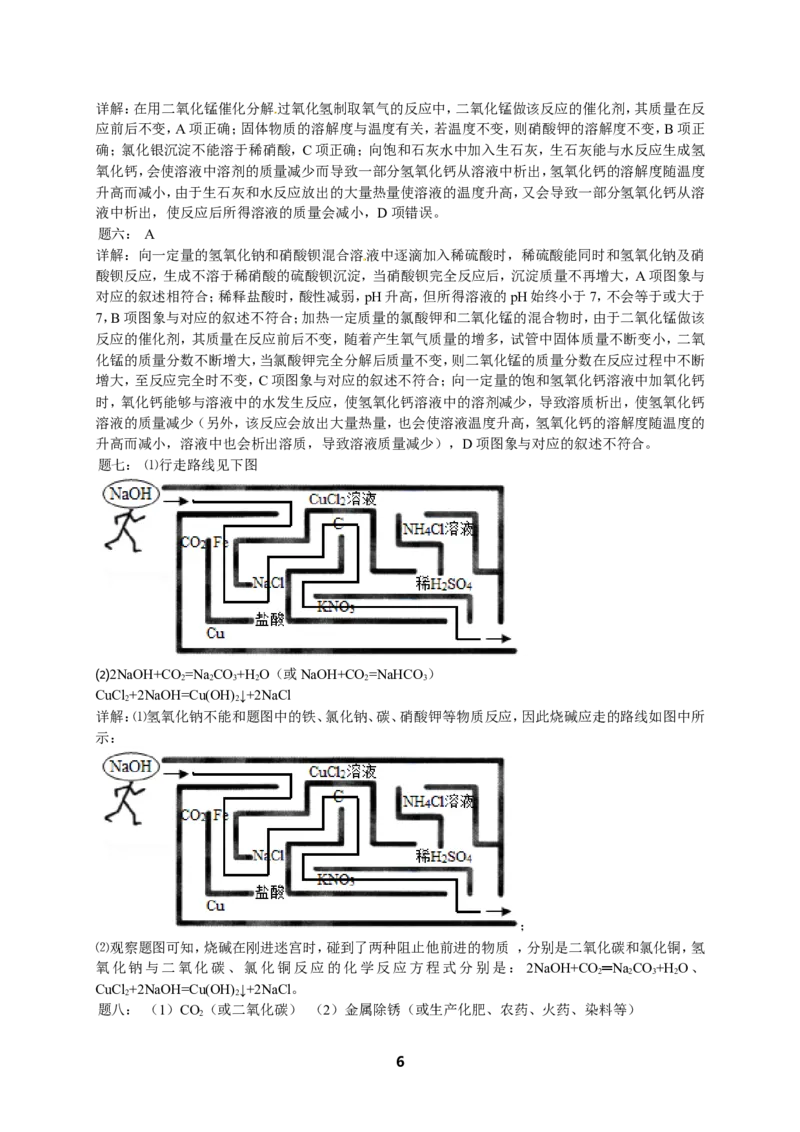
题七: ⑴行走路线见下图
[来源:学科网]
⑵2NaOH+CO =Na CO+H O(或NaOH+CO =NaHCO)
2 2 3 2 2 3
CuCl +2NaOH=Cu(OH) ↓+2NaCl
2 2
详解:⑴氢氧化钠不能和题图中的铁、氯化钠、碳、硝酸钾等物质反应,因此烧碱应走的路线如图中所
示:
;
⑵观察题图可知,烧碱在刚进迷宫时,碰到了两种阻止他前进的物质 ,分别是二氧化碳和氯化铜,氢
氧化钠与二氧化碳、氯化铜反应的化学反应方程式分别是: 2NaOH+CO ═Na CO+H O、
2 2 3 2
CuCl +2NaOH=Cu(OH) ↓+2NaCl。
2 2
题八: (1)CO(或二氧化碳) (2)金属除锈(或生产化肥、农药、火药、染料等)
2
6zxxk.com
(3)CO+Ca(OH) =CaCO ↓+H O;置换
2 2 3 2
详解:(1)根据D是个灭火“能手”可知,D为二氧化碳;
(2)二氧化碳只能和题目所给物质中的氢氧化钙发生化学反应,可推断出C是氢氧化钙;除氯化铜、
二氧化碳外,氢氧化钙只能和硫酸发生中和反应,可确定B是硫酸,则A是铁(铁既能与硫酸反应又
能与氯化铜反应);硫酸可用于金属除锈,也是一种重要的化工原料;
(3)反应④是二氧化碳与氢氧化钙的反应,方程式为CO+Ca(OH) =CaCO ↓+H O;反应①是氯化铜与
2 2 3 2
铁的反应,该反应符合“一种单质和一种化合物起反应,生成另一种单质和另一种化合物”的反应特
点,属于置换反应。
题九: ⑴NaOH 3NaOH+FeCl ═Fe(OH)↓+3NaCl
3 3
⑵有气泡产生 2HCl+Na CO═2NaCl+H O+CO↑
2 3 2 2
⑶> 氢氧化钠(或 < 盐酸) ⑷AC
详解:⑴稀盐酸与氯化铁溶液不反应,而氢氧化钠溶液能与氯化铁溶液反应生成氢氧化铁红褐色沉淀
和氯化钠;⑵稀盐酸能与碳酸钠溶液反应生成氯化钠、水和二氧化碳气体,而氢氧化钠与碳酸钠不反
应;⑶稀盐酸是一种酸,pH<7;氢氧化钠是一种碱,pH>7;⑷锌能与盐酸反应生成氢气,而锌与氢氧
化钠溶液不反应,A可鉴别;稀盐酸和氢氧化钠溶液均不能与硝酸钠溶液反应,B不能鉴别;稀盐酸
能使石蕊试液变红色,氢氧化钠溶液能使石蕊试液变蓝色,C可鉴别。
题十: ⑴Fe O(NaO或CuO或CaO等)
2 3 2 [来源:学科网]
⑵NaOH+HCl=NaCl+H O ⑶Fe+2HCl=FeCl +H ↑
2 2 2
详解:⑴依据对酸的化学性质的理解可知,酸除能与指示剂、碱和盐发生化学反应外,还能够与活泼
的金属单质和金属氧化物发生化学反应,则X可能是Fe O、NaO、CuO、CaO、MgO等金属氧化物;
2 3 2
⑵反应①是盐酸和氢氧化钠发生的中和反应:NaOH+HCl=NaCl+H O;
2
⑶ X是单质时,则X可以是Mg、Al、Fe等活泼的金属单质,则X与稀盐酸反应的化学方程式可以是:
Mg+2HCl=MgCl +H ↑、Fe+2HCl=FeCl +H ↑、2Al+6HCl=2AlCl +3H ↑等。
2 2 2 2 3 2
题十一: (1)放热;无;红;(2)碱;CO+2NaOH═Na CO+H O
2 2 3 2
详解:(1)氢氧化钠固体溶解于水放热、溶液呈无色、氢氧化钠的溶液呈碱性,能使酚酞溶液变红;
(2)溶液颜色仍显红色,说明二氧化碳和氢氧化钠反应后的溶液仍然显碱性;二氧化碳与氢氧化钠溶
液反应生成碳酸钠和水,化学方程式为:CO+2NaOH═Na CO+H O。
2 2 3 2
题十二: (1)不变色;变红色 (2)能 (3)CO+2NaOH=NaCO+HO
2 2 3 2
解析:(1)二氧化碳不能使石蕊试纸变色,二氧化碳和水反应生成碳酸使石蕊试纸变红,所以他将观
察到的现象是:A集气瓶中试纸不变色,B集气瓶中试纸变红色;
(2)通过两个对比实验可以证明HCO 具有酸性,而CO 不具有酸性,能够达到实验目的;
2 3 2
(3)CO 跟足量NaOH反应的方程式:CO+2NaOH=NaCO+HO。
2 2 2 3 2
题十三:(1)盐酸有挥发性或盐酸会挥发出氯化氢气体(或制得的氢气中混有氯化氢气体) (2)红色
(或红棕色)固体逐渐减少,溶液变成黄色
(3)NaOH+HCl=NaCl+H O(或2NaOH+H SO =Na SO +2H O) (4)D
2 2 4 2 4 2
详解:(1)实验室制氢气选稀硫酸而不选盐酸的原因是因为盐酸具有挥发性,挥发出的氯化氢气体混
入氢气中会使制得的氢气不纯;
(2)稀盐酸和稀硫酸都能用于除铁锈,这是因为二者都能够与铁锈的主要成分Fe O 发生反应,使红
2 3
棕色的固体溶解,生成黄色的铁盐溶液:Fe O+6HCl=2FeCl +3H O、Fe O+3H SO =Fe (SO )+3H O;
2 3 3 2 2 3 2 4 2 4 3 2
(3)盐酸和硫酸都能与氢氧化钠发生中和反应,化学方程式:NaOH+HCl=NaCl+H O(或
2
2NaOH+H SO =Na SO +2H O);
2 4 2 4 2
(4)D项中的两只试管中都产生白色沉淀[HCl+AgNO =AgCl↓+HNO 、HSO +BaCl =BaSO ↓+2HCl],
3 3 2 4 2 4
以上两个反应的发生均与H+无关。
题十四: (1)放热;无;红;(2)碱;CO+2NaOH═Na CO+H O
2 2 3 2
7zxxk.com
解析:(1)氢氧化钠固体溶解于水放热、溶液呈无色、氢氧化钠的溶液呈碱性,能使酚酞溶液变红;
(2)溶液颜色仍显红色,说明二氧化碳和氢氧化钠反应后的溶液仍然显碱性;二氧化碳与氢氧化钠反
应生成碳酸钠和水,方程式为:CO+2NaOH═Na CO+H O。
2 2 3 2
题十五: A
详解:固体蔗糖中不存在自由移动的带电的微粒,不能导电;硫酸在溶液中能解离出自由移动的氢离
子和硫酸根离子,氢氧化钠在溶液中能解离出自由移动的钠离子和氢氧根离子,硝酸钾在溶液中能解
离出自由移动的钾离子和硝酸根离子,由于以上物质的溶液中都含有自由移动的带电的微粒,因而都
能导电。本题应选A。
题十六:自由移动的离子;MnO
详解:由离子构成的物质,在溶解于水后,在水分子的作用下,能够解离成自由移动的离子,因而酸、
碱、盐的溶液具有导电性。由于在电极的正负极的作用下,带电离子发生定向运动,导致高锰酸根离
子分布不均,而产生了不同的颜色深度,所以高锰酸钾溶液的颜色由高锰酸根离子来决定。
8