文档内容
东营市广饶县2007年毕业班化学竞赛试题
(时间:60分钟 分值:100分)
可能用到的相对原子质量:H:1 C:12 O:16 S:32 Cu:64
一、选择题(下列各题均只有一个选项符合题意,请将其序号填入题后面的括号内。每小题
2.5分,共50分)
1、下列说法不正确的是
A.铅笔不是铅 B.生铁不含铁 C.水银不是银 D.纯碱不属于碱
2、现榨的苹果汁在空气中会由淡绿色变为棕黄色。你猜测其原因可能是
A.苹果汁中的Fe2+变成Fe3+ B.苹果汁中含有Cu2+
C.苹果汁中含有OH- D.苹果汁中含有Na+
3、不法分子常用金光闪闪的“假金元宝”(铜锌合金)蒙骗人们,下列鉴别方法中错误的是
A.加盐酸 B.测密度 C.用火烧 D.看颜色
4、用pH试纸测定白醋的酸碱度时,如果先将试纸用蒸馏水润湿,再把白醋滴到试纸上,则测
得的结果与白醋的实际的pH比较
A.偏低 B.偏高 C.相等 D.无法比较
5、用密度为1.84g·cm-3的浓硫酸与水配成10mL溶液,吸取上层溶液测得密度为1.08g·cm-3,
如果吸取下层溶液测量密度,则数值为
A.大于1.08g·cm-3 B.小于1.08g·cm-3
C.1.08g·cm-3 D.数据不全,不能确定
6、下列叙述中,正确的是
A.含有氧元素的化合物都是氧化物
B.物质跟氧发生的反应是氧化反应
C.有盐和水生成的反应一定是中和反应
D.由不同种元素组成的物质一定是混合物
7、将一定量铝粉和氧化铜混合加热,反应的化学方程式为3CuO+2Al 高温 3 Cu+Al O。反应
2 3
结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸,充分反
应后,将铁片插入溶液中。下列叙述现象中,能够说明氧化铜没有完全反应的是①加入稀
硫酸后,有气泡生成 ②加入稀硫酸后,没有气泡生成 ③加入稀硫酸后,溶液中有红色
不溶物质 ④插入溶液中的铁片表面有红色物质析出
A.只有① B.②③ C.只有④ D.①③④
8、下列有关溶液的说法中,正确的是
A.不饱和溶液转化为饱和溶液,溶液中溶质的质量分数一定增大
B.将一定质量某物质的饱和溶液降温析出晶体后,所得溶液中溶质的质量一定减小
C.饱和溶液不一定是浓溶液,不饱和溶液一定是稀溶液
D.将5g某物质完全溶解于95g水中,所得溶液中溶质的质量分数一定是5%
9、现有甲、乙、丙、丁四种化合物,甲能跟 BaCl 溶液反应生成两种盐;乙能跟NaOH溶液反
2
应生成盐和水;丙能跟盐酸反应生成盐和水;丁呈中性并能跟CaO反应生成碱。则下列说
法不正确的是
A.甲可能是MgSO B.乙一定是HSO
4 2 4
C.丙可能是NaOH D.丁一定是HO
2
10、不另加任何试剂,就能鉴别的一组溶液是
A.NaSO BaCl KCO KNO B.NaCl AgNO CaCl Na CO
2 4 2 2 3 3 3 2 2 3C.HCl Na CO BaCl HSO D.NaSO BaCl NaOH NaCl
2 3 2 2 4 2 4 2
11、现有6种物质:Fe粉、CO、NaOH溶液、CuSO 溶液、稀HSO 、BaCl 溶液,两两混合后,能发
2 4 2 4 2
生的反应有
A.5个 B.6个 C.7个 D.8个
12、为检验某化合物是否由碳、氢、氧三种元素组成,取一定质量该化合物在氧气中充分燃烧
后,还须进行的实验有:①用带火星木条检验O;②用无水硫酸铜检验HO;③用澄清石
2 2
灰水检验CO;④测定生成物的质量
2
A.①②③④ B.①②③ C.②③④ D.②③
13、下列是四位同学分别设计的实验方案,你认为可行的是
A.某白色固体化合物溶于水,向所得的无色溶液中滴入几滴酚酞试剂,溶液呈红色,证明
该白色固体化合物一定是碱
B.向某无色溶液加入氯化钡溶液,产生白色沉淀,再加稀硝酸,白色沉淀不溶解,证明该
无色溶液中一定含有硫酸根离子
C.不用其他试剂就可鉴别氢氧化钠、氯化镁、硫酸铜和硝酸钾四种溶液
D.把燃着的木条插入某瓶无色气体中,木条火焰熄灭,证明瓶中的气体一定是二氧化碳
14、2004年,美国科学家通过“勇气”号太空探测火星大气中含有一种称为硫化羰(化学式
为COS)的物质,已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧,下列有关
硫化羰(音tang)的说法正确的是
A.硫化羰可用作灭火剂 B.相同条件下硫化羰的密度比空气小
C.硫化羰是酸性氧化物 D.硫化羰在氧气中完全燃烧后生成物是CO 和
2
SO
2
15、下列各组物质能在pH=1的溶液中大量共存,且得到无色透明溶液的是
A.BaCl 、NaNO 、MgCl B.Cu(NO )、NaCl、HSO 、KNO
2 3 2 3 2 2 4 3
C.NaCO、NaCl、KNO、 NH Cl D.ZnSO、Mg(NO)、NaNO 、BaCl
2 3 3 4 4 3 2 3 2
16、Cu O与硫酸反应的化学方程式为Cu O+HSO ==Cu+CuSO +H O。氧化铜与氢气反应后,
2 2 2 4 4 2
得到的Cu中常常单混有少量的Cu O。将以上10gCu和Cu O的混合物放入足量的稀硫
2 2
酸中充分反应,过滤得到9.5g固体,则原混合物中含Cu O的质量分数为
2
溶
A.9.5% B.9% C.5% 解 D.4.5%
度
17 、 甲 、 乙 两 种 固 体 物 质 的 溶 解 度 曲 线 如 图 所 示 。 现 将 两 支 分 别 装 有
乙
甲、乙两种物质饱和溶液(底部均有未溶解的固体)的试管浸入盛有
水 的 烧 杯 里 , 然 后 向 烧 杯 中 加 入 一 定 量 的 浓 硫 酸 , 则 对 相 关 变 化 判 断
甲
正确的是
A.甲溶液中溶质的质量分数增大 B .乙溶液中 未溶解的固体质量减小
温度/℃
C.甲、乙物质的溶解度都增大 D.乙溶液中溶质的质量分数减小
x
18、下列各组物质,不能按照关系图y z(“→”表示反应一步完成)相互转化的是
选项 A B C D
x CaO BaCl Cu(NO ) KSO
2 3 2 2 4
y CaCl Ba(NO ) Cu(OH) KCl
2 3 2 2
Z CaCO BaCO CuSO KNO
3 3 4 3
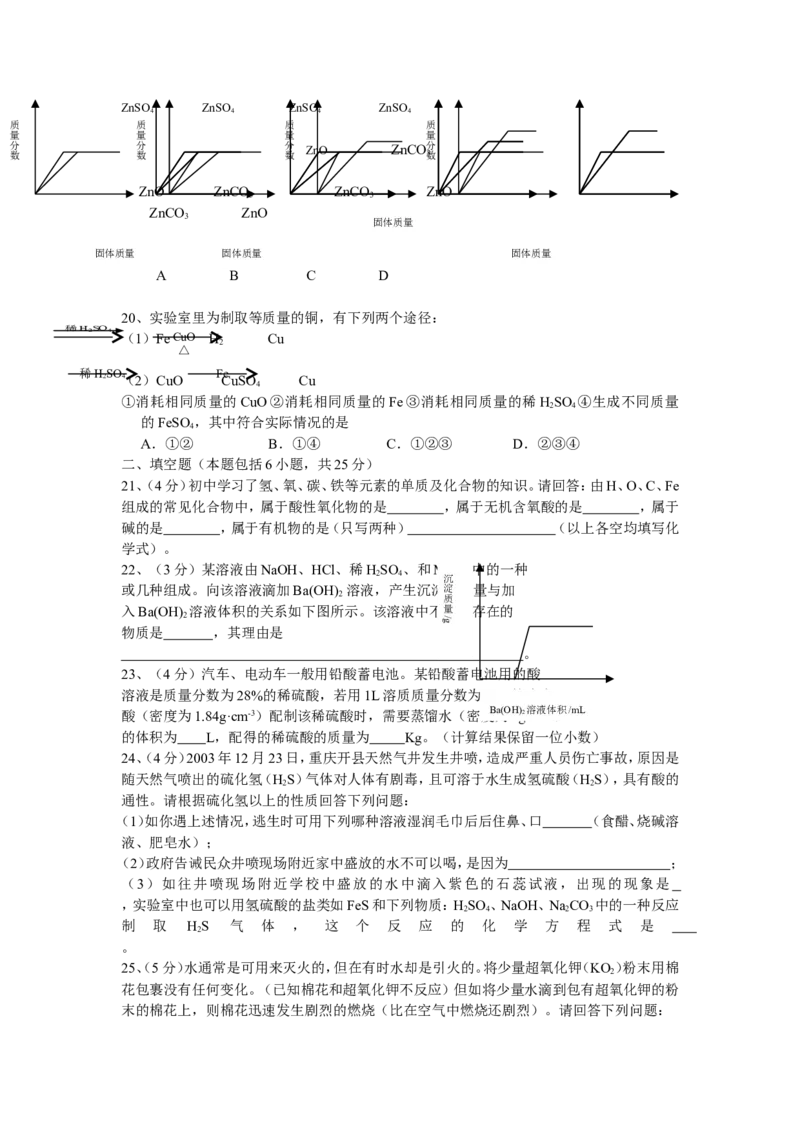
19、将某HSO 溶液分成两等份,分别向其中加入足量的ZnO、ZnCO 固体,充分反应,所得
2 4 3
ZnSO 溶液质量分数与所加质量关系图正确的是
4
/gZnSO ZnSO ZnSO ZnSO
4 4 4 4
质 质 质 质
量 量 量 量
分 分 分
ZnO
ZnCO分
数 数 数 数3
ZnO ZnCO ZnCO ZnO
3 3
ZnCO ZnO
3
固体质量
固体质量 固体质量 固体质量
A B C D
20、实验室里为制取等质量的铜,有下列两个途径:
稀H 2SO4
(1)Fe C u O H
2
Cu
△
稀HSO Fe
2 (4 2)CuO CuSO Cu
4
①消耗相同质量的CuO②消耗相同质量的Fe③消耗相同质量的稀HSO ④生成不同质量
2 4
的FeSO ,其中符合实际情况的是
4
A.①② B.①④ C.①②③ D.②③④
二、填空题(本题包括6小题,共25分)
21、(4分)初中学习了氢、氧、碳、铁等元素的单质及化合物的知识。请回答:由H、O、C、Fe
组成的常见化合物中,属于酸性氧化物的是 ,属于无机含氧酸的是 ,属于
碱的是 ,属于有机物的是(只写两种) (以上各空均填写化
学式)。
22、(3分)某溶液由NaOH、HCl、稀HSO 、和MgCl 中的一种
2 4 沉 2
或几种组成。向该溶液滴加Ba(OH) 溶液,产生沉淀淀的质量与加
2 质
入Ba(OH) 溶液体积的关系如下图所示。该溶液中不可量能存在的
2
物质是 ,其理由是
。
23、(4分)汽车、电动车一般用铅酸蓄电池。某铅酸蓄电池用的酸
溶液是质量分数为28%的稀硫酸,若用1L溶质质量分数为98%的浓硫
酸(密度为1.84g·cm-3)配制该稀硫酸时,需要蒸馏水(密度为1g·cm-3)
的体积为 L,配得的稀硫酸的质量为 Kg。(计算结果保留一位小数)
24、(4分)2003年12月23日,重庆开县天然气井发生井喷,造成严重人员伤亡事故,原因是
随天然气喷出的硫化氢(HS)气体对人体有剧毒,且可溶于水生成氢硫酸(HS),具有酸的
2 2
通性。请根据硫化氢以上的性质回答下列问题:
(1)如你遇上述情况,逃生时可用下列哪种溶液湿润毛巾后后住鼻、口 (食醋、烧碱溶
液、肥皂水);
(2)政府告诫民众井喷现场附近家中盛放的水不可以喝,是因为 ;
(3)如往井喷现场附近学校中盛放的水中滴入紫色的石蕊试液,出现的现象是
,实验室中也可以用氢硫酸的盐类如FeS和下列物质:HSO 、NaOH、NaCO 中的一种反应
2 4 2 3
制 取 HS 气 体 , 这 个 反 应 的 化 学 方 程 式 是
2
。
25、(5分)水通常是可用来灭火的,但在有时水却是引火的。将少量超氧化钾(KO )粉末用棉
2
花包裹没有任何变化。(已知棉花和超氧化钾不反应)但如将少量水滴到包有超氧化钾的粉
末的棉花上,则棉花迅速发生剧烈的燃烧(比在空气中燃烧还剧烈)。请回答下列问题:
/g
Ba(OH) 溶液体积/mL 2(1)超氧化钾是 (选填:氧化物、酸、碱、盐)
(2)从这一实验现象作出的对该反应结果的推理是a ;b ;
(3)某探究小组拟用右图装置进行实验,以证明上述推理。
用以证明推理a的实验方法是:反应发生时, ;
用以证明推理b的实验方法是 。
三、简答题(本题包括1小题,共6分)
27、(6分)(1)以铁为研究对象,依照图中实例在框图处填写物质的化学式(所填写的反应物
不属同一类别的物质,生成物必须填写铁的化合物)
Fe O
3 4
O
2
Fe
(2)实验室中要除去细碎铜屑中的少量铁屑,请用化学方法和物理方法将其除去。(不必叙述
操作步骤,只用简单的原理描述即可)
四、实验题(本题包括2小题,共10分)
29、(3分)氨气(NH )密度比空气小,极易溶于水,它的水溶液叫氨水。氨水呈碱性,是一种
3
速效肥料。实验室是用加热氯化铵晶体和消石灰固体的混合物制取氨气的。试回答:
氨气
(1)实验室收集氨气的方法是 ;
(2)将收集满干燥氨气的试管,倒插入滴有酚酞试液的蒸馏
水中(如右图),可能发生的现象是 。 酚酞+蒸馏水
30、(7分)现有下图所示的实验装置:
(1)现有稀HSO 、CuO、Fe粉3种物质,请设计两种制取铜的实验方案。填写下表。
2 4
实验方案 有关反应的化学方程式
方案一
方案二
(2)用水、生石灰、碳酸钠制取固体NaOH,有关反应的化学方程式为:
五、计算题(本题包括1小题,共9分)
通常状况下,氢气是所有气体中密度最小的。因此氢气以前曾被用于飞艇
和载人气球。
31、(9分)某实验小组同学设计了右图装置模拟氢气探空气球
(装置中气球固定在矿泉水瓶上)。
将气球中的镁条加入到硫酸溶液中,恰好完全反应。 (2B T39图)
(1)计算反应生成氢气的质量;(4分)
(2)计算所用硫酸溶液的质量;(3分)
(3)假设反应后装置内外压强相等,通过估算后回答:
该装置在空气中能否上浮,并说明理由。 (不必写出具体估算过程)(2分)
估算时参考的数据有:①空气的密度可按1.3g·L-1计算;
②氢气的密度可按0.09g·L-1计算;
③矿泉水瓶和气球皮的质量约为20g。
参考答案及评分标准
一、
题号 1 2 3 4 5 6 7 8 9 10
答案 B A D B C B B B C
题号 11 12 13 14 15 16 17 18 19 20
答案 D C C D A B B D A B
(每小题2.5分,共50分)
二、21、CO、HCO、Fe(OH) 或Fe(OH) 、CH、C HOH
2 2 3 2 3 4 2 5
22、NaOH和HSO 。由图可知,反就开始时无沉淀,说明溶液中无HSO ,而一定有HCl,有
2 4 2 4
HCl则没有NaOH,反应一段时间后,产生沉淀说明有MgCl 。
2
23、4.6;6.4
24、(1)烧碱溶液(2)HS可溶于水,且HS有剧毒。
2 2
(3)紫色石蕊试液呈红色;FeS+HSO =FeSO+H S↑
2 4 4 2
25、(1)氧化物(2)a、有O 生成;b、放出大量的热
2
(3)用带火星的木条放在导管P的出口处,观察木条是否复燃;将连接在锥形瓶上的导管Q
插入水中,反应时观察导管口是否有气泡产生。
26、(1)HCl+NaOH=NaCl+H O
2
(2)KOH,NaCO
2 3
(3)HSO +2NaOH=Na SO +2H O
2 4 2 4 2
CuSO +2NaOH=Cu(OH) ↓+Na SO
4 2 2 4
三、27、(1)FeSO 、CuSO ,HCl、FeCl
4 4 2
(2)物理方法:用一块磁铁把铜屑中少量铁屑吸出来;
化学方法:用盐酸或稀硫酸酸洗后过滤。
四、28、(1)向下排空气法;(2)滴有酚酞的蒸馏水变红,且充满试管。
29、(1)方案一、Fe+H SO =FeSO+H ↑ H+CuO △ C u+H O B C
2 4 4 2 2 2
方案二、CuO+HSO =CuSO+H O Fe+CuSO =FeSO+Cu D E
2 4 4 2 4 4
(2)D E F
五、30、(1)设反应生成氢气的质量为x
Mg+HSO =MgSO +H
2 4 4 2
24 2
7.2g x
计算得x=0.6g
(2)设参加反应的硫酸的质量为y
Mg+HSO =MgSO +H
2 4 4 2
74 98
7.2g y
计算得=29.4g
所用硫酸溶液的质量为29.4g/30%=98g
(3)不能。因为该装置所受的重力远远大于装置所受的浮力,所以该装置不能上浮。