文档内容
3.掌握复分解反应的定义。
二、学习重难点
学习重点:粗盐提纯的操作方法
学习难点:碳酸根离子的鉴别方法
三、学习过程
第一课时
【自主导学】
1.日常生活中所说的盐,通常指食盐,主要成分为 ,而化学中的盐是指一
类组成里含有 和 的化合物,如 、
等。
2.氯化钠的用途很多,医疗上 可以做 ,农业上可以做
,工业上可以做 ,日常生活中可以做 。
3.将难溶于液体的固体与液体分离可采用 的操作,该操作中要注意一
,二 ,三 ,粗盐提纯的步骤为 、 、 、
,在这四步操作中都要用到一种玻璃仪器是 ,其作用分别是
、 、 、 。
【探究新知】
1.生活中常见的盐有:食盐(主要成分) 、 、 、 、
。
2.盐:由 和 组成的化合物。
3.工业用盐: (有剧毒)。
4.学生阅读教材P72页,归纳氯化钠的用途:
⑴在生活上:
⑵在农业上:
⑶在工业上:
⑷在医疗上:
5.学生活动与探究(P87页)
⑴如何将粗盐转化为精盐?
⑵过滤器由 和 组成。⑶粗盐提纯的步骤是什么?
⑷操作中应注意什么问题?
课堂小结:
【巩固练习】
1.下列各组物质的名称、俗名、化学式表示同一种物质的是( )
A.氢氧化钠、烧碱、NaCO B.碳酸钠、小苏打、NaCO
2 3 2 3
C.碳酸氢钠、小苏打、NaHCO D.氢氧化钙、生石灰、Ca(OH)
3 2
2.在粗盐提纯的实验中,若过滤后滤液浑浊,一定不是其原因的是( )
A.滤纸破了 B.漏斗下端没有紧靠烧杯内壁
C.液面高于滤纸边缘 D.承接滤液的烧杯没洗干净
3.某市发生了一起亚硝酸钠中毒事件,由于它与食盐外观相似,且有咸味的有毒物质。
亚硝酸钠和食盐的有关资料如下:
项目 亚硝酸钠 氯化钠
水溶性 易溶,S =81.5g 易溶,S =35.8g
15℃ 15℃
熔点 271℃ 801℃
沸点 328℃会分解放出有臭味气体 1413℃
水溶液酸碱性 碱性 中性
与稀盐酸作用 放出红棕色NO 气体 无反应
2
⑴根据表写出亚硝酸钠的两条物理性质:
⑵用三种方法鉴别亚硝酸钠和氯化钠。
【反馈检测】
1.在过滤的操作中用到的玻璃仪器有 ;粗盐提纯的操
作步骤是 ;其中第二步使用玻璃棒的作用是
。
2.NaCl+AgNO3=AgCl↓+Na NO3,人的汗液中含有氯化钠,手摸过物体后,手指指纹上
的汗液就留在了物体上,因此法医做指纹鉴定时,可选用的试剂是A、酸碱指示剂 B、AgNO3溶液 C、酒精 D、碘酒
3.用化学用语表示:
水银不是银,它是 ; 纯碱不是碱,它是 ;
干冰不是冰,它是 ; 食盐的主要成分是 。
第二课时
【自主导学】
1.碳酸钠,俗称 、 ,白色粉末,易溶于水,其水溶液显 性,广泛
用于 、 、 等。
2.碳酸氢钠,俗称 ,白色粉末,可溶于水,其水溶液显弱 性,是
主要成分之一,医疗上可用于 。
3.碳酸钙,是 和 的主要成分,不溶于水,在高温下分解可生成
和二氧化碳。
4.由两种化合物互相 ,生成 的反应叫复分解
反应。复分解反应的发生条件:只有当两种化合物互相交换成分,生成物中有
或有 或有 生成时,复分解反应才可以发生。
【探究新知】
1.学生回顾实验室制CO 的原理(用化学方程式表示)
2
2.演示实验11-1
碳酸钠+盐酸 碳酸氢钠+盐酸
[来源:学.科.网Z.X.X.K]
现象
分析
[来源:学*科*网Z*X*X*K]
3.归纳:组成里含有 或 的盐,都能跟盐酸反应生成二氧化
碳气体,利用此原理可以检验盐的组成里是否含有 或 离子。
[来源:Zxxk.Com]
4.演示实验11-2:碳酸钠与氢氧化钙反应
现象
分析
结论
上述反应可用于工业上制NaOH。
5.由以上反应归纳复分解反应的定义及发生的条件
定义:
条件:
6.活动与探究:根据书后附录Ⅰ,判断下列四种化合物的溶液两两之间是否发生复
分解反应,写出相关的化学方程式。
HSO Ba(NO ) NaOH KCO
2 4 3 2 2 3HSO
2 4
Ba(NO )
3 2
NaOH
KCO
2 3
课堂小结:
【巩固练习】
1.我国化学家侯德榜改进了一种化工产品的生产技术,其产品获得美国费城万国博
览会金奖,这种技术的产品是( )
A.烧碱 B.纯碱 C.精制食盐 D.尿素
2.下列各组物质名称不代表同一物质的一组是( )
A.氯化钠、食盐 B.氧化钙、生石灰
C.碳酸钠、纯碱 D.碳酸氢钠、苏打
3.实验室用石灰石、水、纯碱三种原料来制备烧碱,写出相应的化学方程式:
[来源:Z*xx*k.Com]
(1)高温煅烧石灰石 (2)用生石灰制熟石灰
(3)用纯碱和熟石灰制烧碱 。
4.怎样鉴别纯碱溶液和烧碱溶液?试写出你的实验方案。
【反馈检测】
1. 某市的水质硬度较大,易产生水垢(主要成分是CaCO ),可用厨房中的哪一种物质
3
将水垢除去( )
A.食盐B.蔗糖 C.花生油 D.食醋
2.某同学发现,上个月做实验用的氢氧化钠溶液忘了盖试剂瓶盖。对于该溶液是否变
质同学们提出了如下假设:(1)该溶液没变质;(2)该溶液部分变质;(3)该溶液全部变
质
请设计实验方案,分别验证以上假设。3.小明在厨房取得一种白色粉末A,到化学实验室进行实验,结果如下图,请回答:
⑴若A中含有氢元素,则A的名称是 , B(含钠元素的盐)
A 加入
它与盐酸反应的化学方程式为 白色固体 稀盐酸 C(一种常用溶剂)
D(无色无味气体)
⑵若A中不含氢元素,则A的名称是 ,
加入
它与石灰水反应的化学方程式为 E(白色沉淀) 澄清石灰水
⑶写出D→E的化学方程式 。
第三课时 复分解反应
一、基础知识
1.填表(按要求各写一个相应的化学式)
金属单质 非金属单质 金属氧化物 非金属氧化物 酸 碱 盐
2.完成下列化学方程式:
⑴ NaOH + HCl
⑵ NaCO + HCl
2 3
⑶ NaCO + Ca(OH)
2 3 2
⑷ NaCO + BaCl
2 3 2
叫复分解反应。一般有如下几
类 反 应 ① , ②
, ③ , ④
。
3.复分解反应发生的条件:生成物有 或 或 。
4.判断下列反应能否发生,能反应的写出相应的化学方程式,不能反应的说明理由。
⑴ HSO + Ba(NO )
2 4 3 2
⑵ HSO + NaOH
2 4
⑶ HSO + KCO
2 4 2 3
⑷ NaOH + Ba(NO )
3 2
⑸ KCO + Ba(NO )
2 3 3 2
⑹ NaOH + KCO
2 3⑺ NaCl + AgNO
3
⑻ CuSO + NaOH
4
⑼ FeCl + NaOH
3
⑽ MgSO + NaOH
4
5.我知道AgCl、BaSO 、CaCO 、BaCO 、Mg(OH) 均为 ,其中
4 3 3 2
AgCl、BaSO 溶于稀硝酸,CaCO 、BaCO 、Mg(OH) 均可溶于稀硝酸,其反应的
4 3 3 2
化学方程式为① CaCO + HNO =
3 3
② BaCO + HNO =
3 3
③ Mg(OH) + HNO =
2 3
新制的Cu(OH) 为 色沉淀,Fe(OH) 为 色沉淀,Cu(OH) 、Fe(OH) 沉淀也
2 3 2 3
可溶于酸,其反应的化学方程式为① Cu(OH) + HNO =
2 3
② Fe(OH) + HNO =
3 3 [来源:学科网]
二、能力训练
1.下列各组能反应的写出化学方程式:
⑴ KNO + NaCl
3
⑵ KNO + HSO
3 2 4
⑶ KCO + HCl
2 3
⑷ KCO + BaCl
2 3 2
⑸ KCO + Ca(OH)
2 3 2
⑹ NaSO + BaCl
2 4 2
⑺ AgNO + BaCl
3 2
⑻ Fe (SO ) + NaOH
2 4 3
⑼ CuCl + NaOH
2
⑽ Mg(NO) + NaOH
3 2
⑾ CuSO + Ba(OH)
4 2
⑿ NaCO + Ba(OH)
2 3 2
[来源:Z+xx+k.Com]
课题 2.化学肥料一、学习目标
1.了解化学元素对植物生长的重要性,了解常见化肥的种类并能举例。
2.通过观察和探究常见的化肥,了解化肥对人类生活的影响和对环境的影响。
二、学习重难点
学习重点:常见化肥的种类和简单鉴别
学习难点:培养学生解决实际问题的能力
三、学习过程
【自主导学】
1.农作物的生长需要量较大的元素是 、 、 ,因此主要的化学肥
料是 、 、 。
2.常见的氮肥有 、 和铵盐,如 、
、 等。
3.常见的磷肥有 、 、 。
4.常见的钾肥有 、 。
5.复合肥是指 ,如 、
、 。
[来源:学#科#网Z#X#X#K]
6.氮肥中的 是液态, 有强烈的氨味,磷肥通常呈
色,氮肥和钾肥通常呈 色。铵态的氮肥加熟石灰研磨会产生
,因此不能与 性肥料混合施用。
【探究新知】
1.常见的化学肥料
氮肥
铵盐
磷肥 钾肥
复合肥料: ,如 、
。
2.活动与探究:探究初步区分常用氮肥、磷肥、钾肥的方法
⑴比较
氮肥 磷肥 钾肥
[来源:学科网ZXXK]
碳酸氢铵
[来源: 氯化铵 磷矿粉 过磷酸钙 硫酸钾 氯化钾
学科网ZXXK]
外观气味
溶解性
⑵取下列化肥各少许,分别加入熟石灰粉末,研磨。
氮肥 钾肥
碳酸氢铵 氯化铵 硫酸钾 氯化钾
加熟石灰研磨
⑶归纳区分化肥的步骤和方法:
课堂小结:
【巩固练习】
1.草木灰是农家肥料,它的主要成分是一种含钾的盐,取一些草木灰加到盐酸中,生
成的气体可使澄清的石灰水变浑浊,由此推断草木灰的主要成分是 。
2.硝酸钾、硫酸铵、磷酸铵中属于复合肥料的是 和 ,它
们所含的营养元素分别是 和 、 和 。
[来源:学&科&网Z&X&X&K]
3.碳铵(NH HCO )能使作物枝繁叶茂,果实硕大,碳铵属于( )
4 3
A.钾肥 B.磷肥 C.氮肥 D.复合肥
[来源:Z#xx#k.Com]
4.某不纯的硝酸铵样品,经分析知道其中氮元素的质量分数为20%,且知样品中只
混有下列物质中的一种,则样品中混入的物质是( )
A.(NH )SO B.NH HCO C.CO(NH) D.(NH )CO
4 2 4 4 3 2 2 4 2 3
5.已知硝酸铵的化学式为NH NO 。求:
4 3
⑴硝酸铵中氮、氢、氧三种元素的质量比。
⑵多少克硝酸铵中含氮3.5g?
【反馈检测】
1.农家肥草木灰可以起到化肥的作用,草木灰的主要成分是( )
A.NH Cl B.KCO C.NH HCO D.Ca(HPO )
4 2 3 4 3 2 4 2
2.下列化肥中属于复合肥料的是( )
A.NH HCO B.KSO C.Ca (PO) D.KNO
4 3 2 4 3 4 2 3
3.下列化学肥料的区别方法可行的是( )
A.NH Cl和KCl 观察外观
4
B.NH HCO 和KCl 加水
4 3
C.KSO 和Ca (PO ) 闻气味
2 4 3 4 2
D.(NH )SO 和KSO 加熟石灰研磨后闻气味
4 2 4 2 44.下列化肥中含氮量最高的是( )
A.(NH )SO B.NH NO C.NH HCO D.NH Cl
4 2 4 4 3 4 3 4
5.某硝酸铵样品中NH NO 的质量分数为90%,求该样品中氮元素的质量分数。
4 3
第十一单元小结
一、基本训练
1..写出下列常见的盐的化学式:
⑴碳酸钠 ,碳酸钙 ,碳酸氢钠 ,碳酸钡 ,它
们统称碳酸盐。
⑵硫酸钠 ,氯化钠 ,硝酸钠 ,碳酸钠 ,它们
统称为钠盐。
⑶硫酸铵 ,硝酸铵 ,碳酸氢铵 ,氯化铵 ,
它们统称 盐。
2.盐的组成里含有 和 ,有的盐溶液显中性,如NaCl;有的盐
溶液显碱性,如 ;有的盐溶液显酸性,如 。
3.盐的化学性质
发生的条件 举例 反应类型
与金属反应
与酸反应
与碱反应
与盐反应
4.回忆酸、碱、盐的化学性质,说说有盐生成但反应物的物质类别不同的化学反应有
哪几种?(口答)据此写出用不同方法制备MgSO 的化学方程式。
4
(1)活泼金属+酸 (5)碱+盐(行吗?)(2)金属氧化物+酸 (6)盐+酸
(3)碱+酸 (7)盐+盐
(4)金属+盐溶液
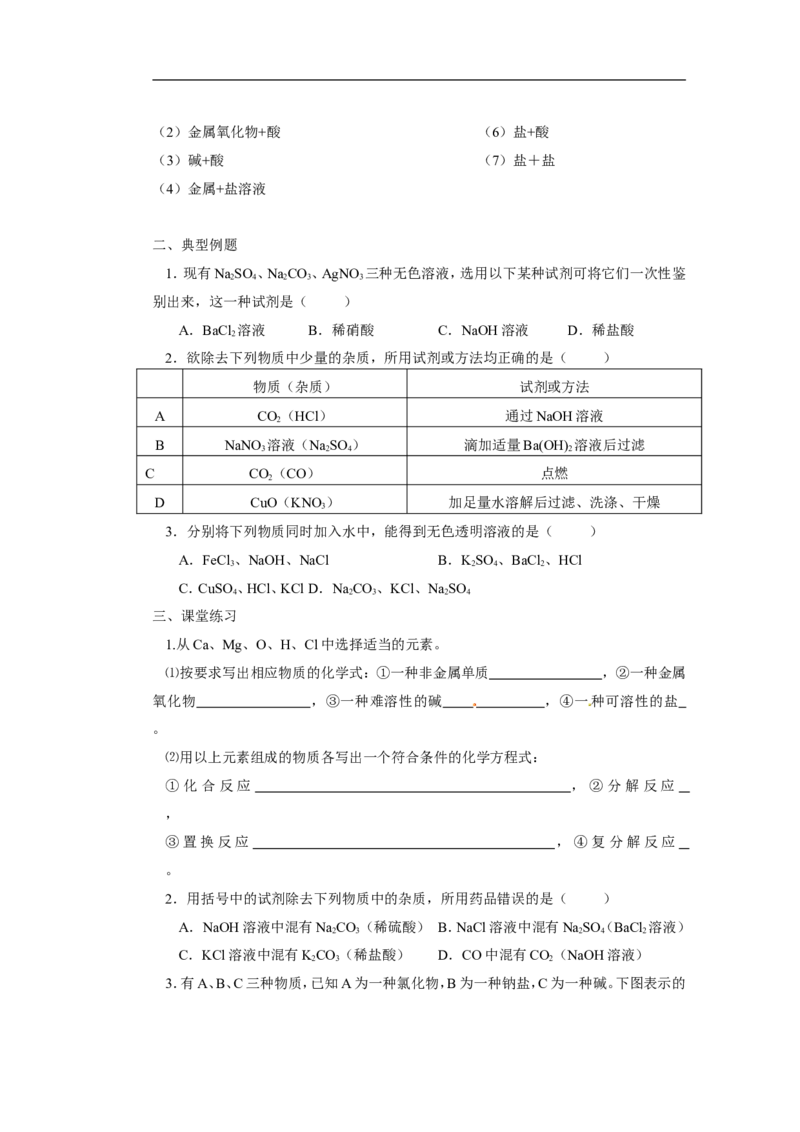
二、典型例题
1.现有NaSO 、NaCO、AgNO 三种无色溶液,选用以下某种试剂可将它们一次性鉴
2 4 2 3 3
别出来,这一种试剂是( )
A.BaCl 溶液 B.稀硝酸 C.NaOH溶液 D.稀盐酸
2
2.欲除去下列物质中少量的杂质,所用试剂或方法均正确的是( )
[来源:学+科+网Z+X+X+K]
物质(杂质) 试剂或方法
A CO(HCl) 通过NaOH溶液
2
B NaNO 溶液(NaSO ) 滴加适量Ba(OH) 溶液后过滤
3 2 4 2
C CO(CO) 点燃
[来源:Zxxk.Com] 2 [来源:Z,xx,k.Com]
D CuO(KNO) 加足量水溶解后过滤、洗涤、干燥
3
3.分别将下列物质同时加入水中,能得到无色透明溶液的是( )
A.FeCl 、NaOH、NaCl B.KSO 、BaCl 、HCl
3 2 4 2
C.CuSO 、HCl、KCl D.NaCO、KCl、NaSO
4 2 3 2 4
三、课堂练习
1.从Ca、Mg、O、H、Cl中选择适当的元素。
⑴按要求写出相应物质的化学式:①一种非金属单质 ,②一种金属
氧化物 ,③一种难溶性的碱 ,④一种可溶性的盐
。
⑵用以上元素组成的物质各写出一个符合条件的化学方程式:
①化合反应 ,②分解反应
,
③置换反应 ,④复分解反应
。
2.用括号中的试剂除去下列物质中的杂质,所用药品错误的是( )
A.NaOH溶液中混有NaCO(稀硫酸) B.NaCl溶液中混有NaSO(BaCl 溶液)
2 3 2 4 2
C.KCl溶液中混有KCO(稀盐酸) D.CO中混有CO(NaOH溶液)
2 3 2
3.有A、B、C三种物质,已知A为一种氯化物,B为一种钠盐,C为一种碱。下图表示的是A、B、C的溶液两两反应的实验现象,试回答:
A
⑴A的化学式
D的化学式 无明显现象 蓝色沉淀
B C
⑵B与C反应的化学方程式:
不溶于稀硝酸
的白色沉淀
⑶A溶液与洁净铁钉反应的化学方程式:
4.能将NaCO、(NH )SO 、NaCl、NH Cl四瓶无色溶液一次性鉴别出来的试剂可以是
2 3 4 2 4 4
(
)
A.盐酸 B.CaCl 溶液 C.Ba(OH) 溶液 D.NaOH溶液
2 2
5.分别将下列各组物质同时加入到水中能大量共存的是( )
A.NaCl、AgNO、NaSO B.HSO 、NaCl、NaCO
3 2 4 2 4 2 3
C.NaSO 、KNO、NaOH D.BaCl 、NaCO、KOH
2 4 3 2 2 3
6.将部分被氧化的镁条样品6.4g加入到100g稀盐酸中,恰好完全反应后得到106.2g
溶液。试求:
⑴生成氢气的质量。
⑵6.4g样品中镁元素的质量。
⑶所得溶液中溶质的质量分数。