文档内容
2013.12
可能用到的相对原子质量:Fe-56 O-16 H-1 Cl-35.5 Na-23 B-11
一、选择题(1-8题每题1分,9-12题每题2分,共16分)
1.沈阳是2008年北京奥运会足球比赛分赛场之一。兴奋剂检测是对足球运动员的一项重要检测。
诺龙是兴奋剂中的一种,化学式是C H O。下列关于诺龙说法正确的是 ( )
18 26 2
A.诺龙中含有氧分子
B.一个诺龙分子中含有46个原子
C.诺龙中碳、氢、氧元素质量比为9:13:1
D.诺龙由18个碳原子、26个氢原子、2个氧原子构成
[来源:学科网ZXXK]
2.下列物质的化学式书写正确的是 ( )
A氧化铝AlO B .氦气He C.氯化亚铁FeCl D.氢氧化钾 KOH
2 3
3.图为元素周期表中氟元素的相关信息,下列说法错误的是 ( )
A氟原子核内质子数为9 B.氟原子为非金属元素
C.氟元素的质量为19.00 D.氟元素符号为F
4. 卟啉铁(C H ClFeNO)对缺铁性贫血有显著疗效。以下说法正确的是 ( )
34 32 4 4
A.卟啉铁中含有5种元素 B.1个卟啉铁分子中含有34个碳原子
C.人体补铁的唯一方法是服用卟啉铁 D.“缺铁性贫血”中的“铁”指单质铁
5.下列符号:2N、N 、HO 、2CO、SO 中,数字“2”的意义能用来表示分子个数的有 ( )
2 2 2
A.2个 B.1个 C. 4个 D. 5个
6.2007年诺贝尔化学奖授予德国化学家Gerhard Ertl,以表彰他在表面化学领域研究所取得的
开拓性成就。下图表示某反应在催化剂Pt/ AlO/Ba表面进行的过程(图中nitrate指硝酸盐)。
2 3
判断下列说法中正确的是 ( )
A.CO、AlO 属于金属氧化物 B.CO、HO属于非金属氧化物
2 2 3 2
C.NO与O 生成NO 的反应属于置换反应 D.硝酸根离子中氮元素的化合价
2 2
8.2008年初,一场大范围历史罕见的低温雨雪冰冻袭击了中国南方部分省区市,此次雪灾给
我国造成了巨大的经济损失。下列说法正确的是 ( )
A.雪是一种单质 B.冰和雪的主要成分都水
C.当雨雪成为冰冻时,分子的运动就停止了 D.冰雪融化的过程是一种化学变化9.物质X可发生下列所示的两个反应,则X是 ( )
①X+酸→盐+水 ②X+水→碱
A.CaO B.FeO C.CO D.NaOH
2 3 2
10.2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest),有一类物质也好似鸟巢,
如化学式是BH 的五硼烷。下列有关五硼烷的说法错误的是 ( )
5 9
A.五硼烷属于化合物
B.五硼烷的相对分子质量是64
C.五硼烷中硼元素和氢元素的质量比为5∶9
D.1个五硼烷分子由5个硼原子和9个氢原子构成
北京奥运会主体育场模 BH 五硼烷
11.右图所示微观变化的化学反应类型,与下列反应 型
5 9
的反应类型一致的是 ( )
12.某物质在空气中完全燃烧生成8.8g二氧化碳和5.4g水,则关于这种物质的组成描述正确的
是 ( )
A.该物质只含有碳元素和氢元素
B.该物质中碳元素与氯元素的质量比为12:1
C.该物质一定含有碳元素和氢元素,可能含有氧元素
D.该物质的分子中碳原子与氢原子的个数比为1:2
二、填空题(共16分,每空1分)
13.现有H、S、O、Na四种元素,请选用其中元素写出符合下列要求的化学式各一个:
⑴相对分子质量最小的氧化物_________;⑵用于金属表面除锈的酸____________;
⑶厨房清洁剂中含有的碱_____________;⑷由三种元素组成的一种盐__________。
14.行态各异的物质可按一定规律分类。现有A.石墨 B.二氧化锰 C.氢氧化钾 D.硝酸钾
E.海水 F.硫酸六种物质,请选用各物质名称前的字母序号填涂在答题卡 相应位置。
(1)属于非金属单质的是 ;(2)属于氧化物的是 ;
(3)属于易溶性盐的是 ;(4)属于易溶性碱的是 ;
(5)属于混合物的是 ;(6)属于不挥发性酸的是 。
15.天然水中含有的部分杂质如下表所示:
溶 解 物 质 悬浮物质
主要气体 主要离子 生物生成物
细菌、藻类及
氧气 钙离子、氯离子、 NH+、NO-、
4 2
原生物、泥
二氧化碳 硫酸根离子 HPO2-、Fe3+、
[来源:学&科&网Z&X&X&K][来源:学 4 沙、黏土等
科网ZXXK]
硫化氢等 镁离子 HPO-等
2 4
[来源:学_科_网]
请根据上表内容回答:
(1)写出“主要气体”中两种气体的化学式__________、__________;
(2)写出“主要离子”中一种阳离子和一种阴离子的符号_________、_________;
(3)写出由“生物生成物”中的离子组成的磷酸二氢铵的化学式______________,磷酸二氢铵中
硫元素的化合价为
三、简答题(共20分,每空1分,17题3分)
16. 下面是五种粒子的结构示意图:(1)图中粒子共能表示 种元素。A所表示的元素位于元素周期表的第 周期。
(2)图中表示的阳离子是 (用离子符号表示),表示的阴离子是 (用离子符号表示),
二者形成的化合物的化学式为 。
17. 氮化硅是一种耐高温陶瓷材料,它的硬度大、熔点高、化学性质稳定。工业制得氮化硅的化学
方程式为:3Si+2N R(R为氮化硅),高温则氮化硅的化学式为_______,你推断的理由是
2
______________________________________________ _ __ _。
18. 在家庭生活中,自来水经过处理后,用途更加广泛。
(1)净水器可以净化自来水,获得更优质的饮用水。①净水器中装有活性炭,其作用是
________________;②净水器接通电源时产生紫外线与自来水生产中加氯气的目的相同,其作用
是________________。
(2)用自来水养金鱼时为除去其中少量的余氯,可放入少许大苏打(NaSO·5HO),大苏打由_
2 2 3 2
____种元素组成,其中Na、S、O、H的原子个数比为___________,式量(分子量)为____________。
19. 苹果醋是一种利用苹果发酵制成的饮料,具有一定的保健功能。苹果酸(化学式为CHO)是
4 6 5
这种饮料的有效成分。计算:
(1)苹果酸的相对分子质量是 ;
(2)苹果酸中碳、氢、氧三种元素的质量比是(化成最简整数比) ;
(3)苹果酸中碳元素的质量分数是(计算结果精确到0.1%) 。
20.元素周期表是化学学习和研究的重要工具。右图
是元素周期表的一部分,根据表中信息回答下列问题。
⑴硫元素的原子序数是 ,相对原子质量是 。
⑵第15号元素的符号是 ;
⑶利用右表中元素,写出一种分子构成与微
粒模型 相似的物质的化学式
四、实验与探究题(共20分,每空2分)
21.现有①四氧化三铁, ②空气, ③铁粉,, ④氯酸钾, ⑤液态氧, ⑥水, ⑦氯化钾,⑧海水⑨
冰水混合物等物质,其中属于化合物的是 ;属于氧化物的是 ,属于纯净物的
是 。
22.人们为揭示原子结构奥秘,经历了漫长探究过程。1897年汤姆生发现电子并提出类似“西
瓜”的原子模型;1911年卢瑟福等人为探索原子内部结构又进行了下面实验:用一束带正电的、
质量比电子大得多的高速运动的a粒子轰击金箔,发现:①大多数a粒子能穿透金箔而不改变原
来运动方向;②一小部分a粒子改变了原来的运动方向;③极少数a粒子被弹了回来。
请你根据对原子结构的认识,分析出现上述现象的原因:
(1)现象①: ;
(2)现象②: ;(3)现象③: 。
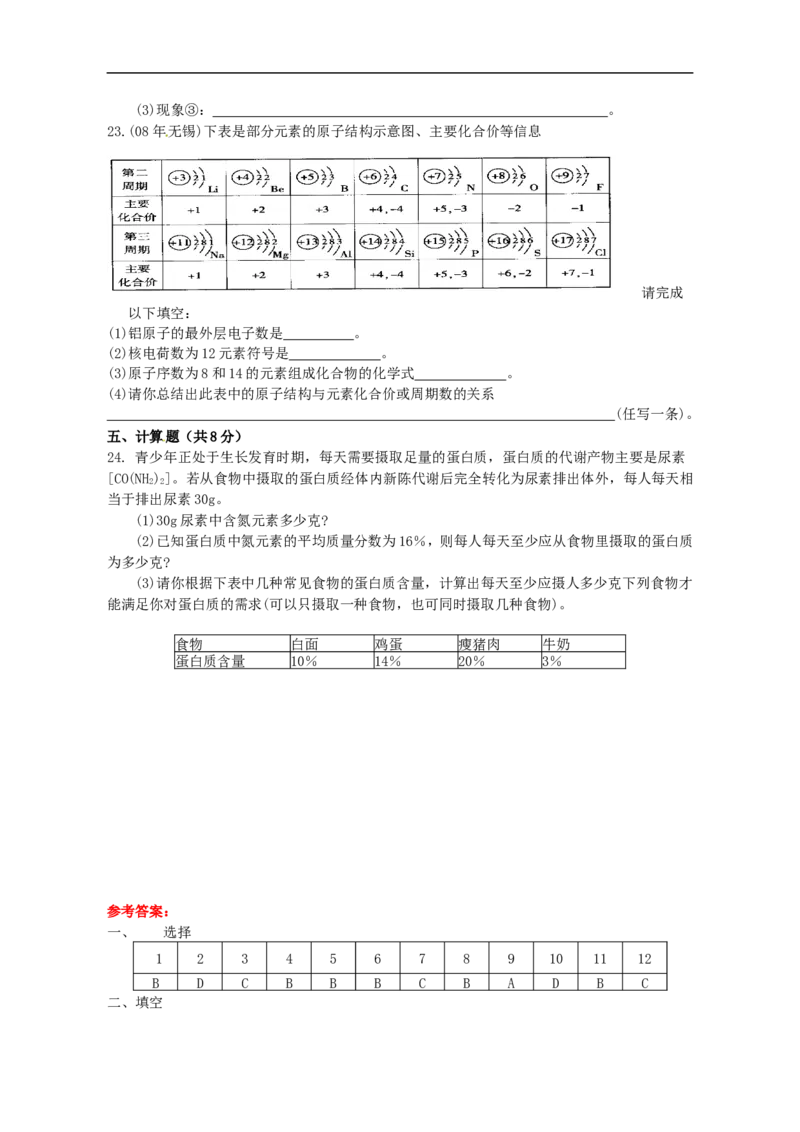
23.(08年无锡)下表是部分元素的原子结构示意图、主要化合价等信息
请完成
以下填空:
(1)铝原子的最外层电子数是 。
(2)核电荷数为12元素符号是 。
(3)原子序数为8和14的元素组成化合物的化学式 。
(4)请你总结出此表中的原子结构与元素化合价或周期数的关系
(任写一条)。
五、计算题(共8分)
24. 青少年正处于生长发育时期,每天需要摄取足量的蛋白质,蛋白质的代谢产物主要是尿素
[CO(NH)]。若从食物中摄取的蛋白质经体内新陈代谢后完全转化为尿素排出体外,每人每天相
2 2
当于排出尿素30g。
(1)30g尿素中含氮元素多少克?
(2)已知蛋白质中氮元素的平均质量分数为16%,则每人每天至少应从食物里摄取的蛋白质
为多少克?
(3)请你根据下表中几种常见食物的蛋白质含量,计算出每天至少应摄人多少克下列食物才
能满足你对蛋白质的需求(可以只摄取一种食物,也可同时摄取几种食物)。
食物 白面 鸡蛋 瘦猪肉 牛奶
蛋白质含量 10% 14% 20% 3%
参考答案:
一、 选择
1 2 3 4 5 6 7 8 9 10 11 12
B D C B B B C B A D B C
二、填空13.⑴HO ⑵HSO ⑶NaOH ⑷NaSO(或NaSO)
2 2 4 2 4 2 3
14.ABDCEF
15.⑴CO、O 或HS ⑵Ca2+或Mg2+、Cl-或SO2- ⑶NHHPO
2 2 2 4 4 2 4
三、简答
16.(1)四 三 (2)Mg2+ Cl— MgCl
2
17.
18. (1)①吸附 ②杀菌消毒 (2)4、1 : 1 : 4 : 5(或2 : 2 : 8 : 10)、248
19.(1)134 (2)24:3:40 (3)35.8%
20.⑴16 32.07 ⑵P ⑶O(或Cl、N、F)
2 2 2 2
四、实验与探究
21.①④⑥⑦ ①⑥
22. (1)原子核很小,原子内部有很大的空间
(2)原子核带正电,α粒子途经金原子核附近时,受到斥力而改变了运动方向
(3)金原子核质量比α粒子大得多,α粒子碰撞到金原子核时被弹了回来
23. (1) 3 (2) Mg (3) SiO (4)周期数=电子层数,或最外层电子数=正价数,或负
2
价数=8-最外层电 子数
五、计算
24.答案:33.
(1)30g尿素中氮元素的质量为:30gX2N/CO(NH)×100% =30g×28/60×100% =14g(2分)
2 2
(2)至少应摄取的蛋白质质量为:14g/16% = 87.5g(1分)
(3)若只摄取白面,摄取量至少为:87.5/10% =875g (其它正确方案亦得分。2分)