文档内容
zxxk.com
身边的化学物质--水与常见的溶液(提高篇)课后练习
题一: 下图是电解水的示意图。关于电解水的下列说法中正确的是( )
A. 理论上得到氧分子和氢分子的个数比为2 : 1
B. 理论上若得到8 mL的氧气,可同时得到1 mL氢气
C. 理论上若得到4 g氢气,可同时得到32 g氧气
D. 该反应说明水是由氢气和氧气组成的
题二: 如图是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子。下列说法不正确
的是( )
A. 图中能表示氢分子的是“ ”
B. 反应前后,原子的种类、数目不变
C. 该反应中共涉及两种单质和三种化合物
D. 该反应中参加反应的两种分子的个数比为1:1
题三: 为了探究“水的净化”过程,某实验小组从东昌湖某区域中取了水样,观察到:
水样呈淡黄色,有异味;水样浑浊,有固体小颗粒。现对水样进行如下处理:
(1)将水样经过沉降、过滤、 、杀菌消毒等步骤,可初步净化为自来水 。
(2)通入氯气杀菌消毒,发生的反应为:Cl + H O = HCl + HClO(次氯酸)。请判断次氯酸(HClO)中氯元
2 2
素的化合价为 。
(3)含有较多的可溶性钙、镁化合物的天然水称为 。
(4)铁制品在空气中锈蚀的实质就是铁与空气中的 (填序号)等发生了化学反应。
A.氧气 B.二氧化碳 C.水 D.氮气
题四: 像科学家一样“观察与思考”——探秘水世界。
如图所示的照片拍摄于我市某处天然温泉,请回答下列问题。
(1)观察:当你用一种或多种感官去搜集有关这个世界的信息时,就是在观察。
这幅实景图片包含了与水有关的信息,请你从化学的视角观察图片,然后列出你观察到的关于水的性
0zxxk.com
质的一条信息。
[来源:学.科.网Z.X.X.K]
。
(2)推理:当你对观察到的现象进行解释时,就是在推理,也叫推论。根据你观察到的结果,请做出一个
推论。
。
(3)理性思维:对比是常用的思维方法,比较是为了找出事物的相同点,对比是为了找出事物的不同点。
比较/对比图中①、②、③三处分子的特征、性质的异同,将结果填在表中。(如果不同,需按从大到小进
行排序,填序号)
比较/对比项目 比较/对比结果
水分子的能量
水分子的运动速率
水分子的质量
水分子之间的相互作用力
水的化学性质
(4)物质的分类与符号表征:
天然温泉是大自然赐给人类的宝物。天然温泉富含人体所需的多种化学元素,但不同地区的温泉其成
分也不完全相同。已知上述温泉富含如下成分:一是钾、钠、钙、镁、铁等阳离子,二是氟、氯、碘、碳酸
根、硫酸根等阴离子,三是硫磺、二氧化碳、二氧化硅、偏硅酸等物质。其中,属于单质的有(用化学符
号表示) ;由硫酸根离子和铁离子构成的盐是(用化学符号表示) 。
(5)用微粒的观点认识水:
在100多年的近代自然科学史上,最有影响力的成果莫过于物质的原子/分子模型及物质构成的理论,
因为该理论不仅可以很好地解释前人百思不得其解的某些自然现象,还可以指导我们更好地认识和
改造物质。
请你从物质的构成、分子的构成和原子的构成等层面,描述水的微观构成(任选其中2个层面即可)
A. 。
B. 。
题五: 2016年我国纪念“世界水日”和“中国水周”活动的主题是“落实五大发展理念,推进最
严格水资源管理”。某校化学兴趣小组进行了一系列探究小实验。
(1)取回大明湖水样,静置后过滤并用液氯消毒。若想测试水样酸碱性的强弱程度,可选用 (填
序号)。
A.石蕊试液 B.酚酞试液 C.pH试纸 D.硝酸银溶液
(2)取上述清液滴在洁净的玻璃片上,慢慢加热至水分消失,该实验操作中若出现
现象时,可证明大明湖水样中含有可溶的矿物质。
(3)现有甲、乙两种固体的溶解度曲线如图所示。
1zxxk.com
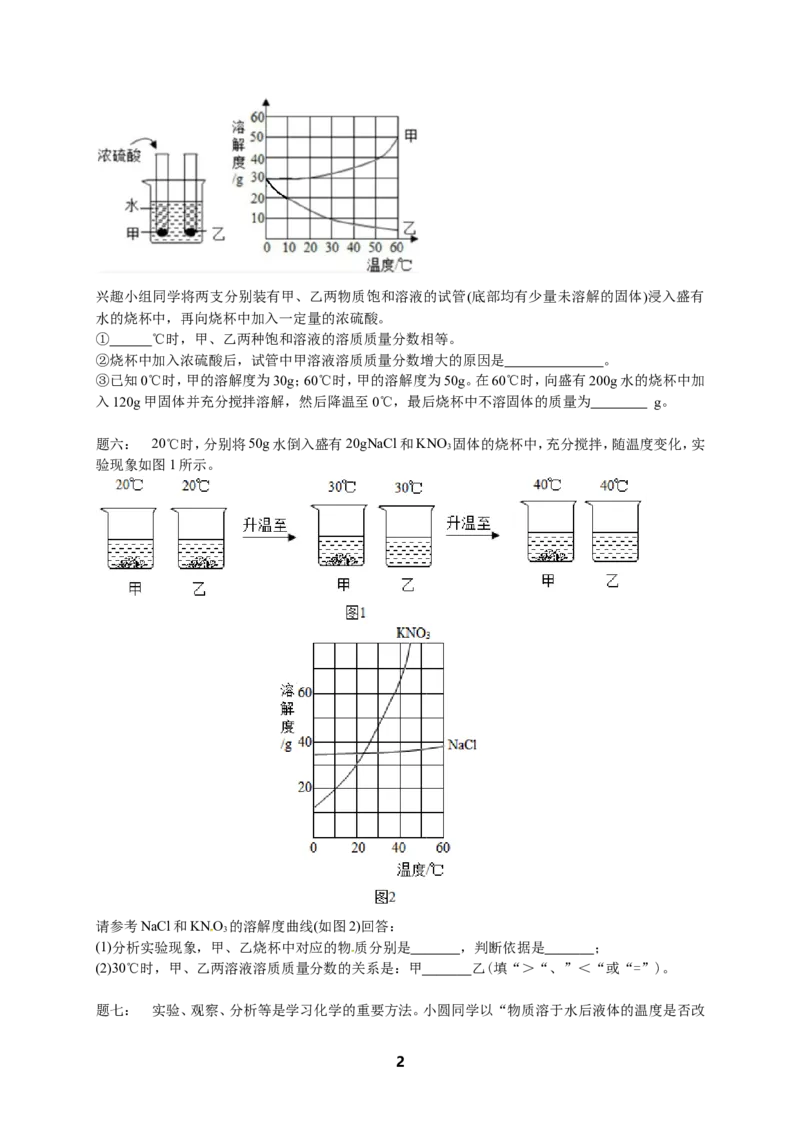
兴趣小组同学将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有
水的烧杯中,再向烧杯中加入一定量的浓硫酸。
① ℃时,甲、乙两种饱和溶液的溶质质量分数相等。
②烧杯中加入浓硫酸后,试管中甲溶液溶质质量分数增大的原因是 。
③已知0℃时,甲的溶解度为30g;60℃时,甲的溶解度为50g。在60℃时,向盛有200g水的烧杯中加
入120g甲固体并充分搅拌溶解,然后降温至0℃,最后烧杯中不溶固体的质量为 g。
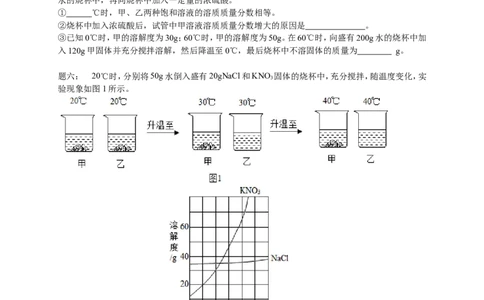
题六: 20℃时,分别将50g水倒入盛有20gNaCl和KNO 固体的烧杯中,充分搅拌,随温度变化,实
3
验现象如图1所示。
请参考NaCl和KNO 的溶解度曲线(如图2)回答:
3
(1)分析实验现象,甲、乙烧杯中对应的物质分别是 ,判断依据是 ;
(2)30℃时,甲、乙两溶液溶质质量分数的关系是:甲 乙(填“>“、”<“或“=”)。
题七: 实验、观察、分析等是学习化学的重要方法。小圆同学以“物质溶于水后液体的温度是否改
2zxxk.com
变?”为课题进行探究。
实验用品:药匙、烧杯、玻璃棒、温度计、水、氢氧化钠、氯化钠、硝酸铵
实验操作:她取三只烧杯,向烧杯中各注入30mL水,测得水的初温为12℃。再向三只烧杯中分别加
入三药匙的氢氧化钠、氯化钠、硝酸铵固体,搅拌,待溶解后用温度计分别测三只烧杯中溶液的温度。
(1)下列数据是实验记录的三种溶液的温度,则氢氧化钠溶液温度是________。(填字母序号)
A.2℃ B.12℃ C.46℃
(2)溶解硝酸铵固体时,小圆发现在烧杯________ (选填“内壁”或“外壁”)有水珠产生,其原因是
________。
由此探究实验可知物质溶于水的过程中通常伴随热量的变化。
题八: 下列数据是硝酸钾和氯化钠在不同温度时的溶解度。
(1)30℃时,向l00g水中加入45.8g硝酸钾,充分溶解后得到________(选填“饱和”或“不饱和”)溶
液;
(2)从NaCl溶液中得到NaCl晶体的方法是 ;
(3)40℃时,氯化钠的溶解度 (填“无法确定”、“大于”、“小于”)硝酸钾的溶解度;
[来源:Zxxk.Com]
(4)如图所示,小烧杯中盛放的是上述(1)中所得的硝酸钾溶液。若将少量的下列物质,分别小心地加入
到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是 (填字母)。
A.冰 B.浓硫酸 C.硝酸铵 D.氢氧化钠
[来源:学+科+网]
[来源:Zxxk.Com]
3zxxk.com
身边的化学物质--水与常见的溶液(提高篇)
课后练习参考答案
题一: C
解析:电解水时,正极产生的是氧气,负极产生的是氢气,氧气与氢气的体积比为1:2,氧气与氢气的
质量比为8:1;故理论上得到氧分子和氢分子的个数比为1:2;理论上若得到8 mL的氧气,可同时得
到16mL氢气;理论上若得到4 g氢气,可同时得到32 g氧气;该反应说明水是由氢元素和氧元素组
成的。故选择C。
题二: C
解析:由题目给出的微观示意图和信息可知:参加反应的是两种化合物,生成物是一种单质和一种化
合物。A. 一个氢分子是由两个氢原子构成的,故图中能表示氢分子的是“ ”A正确;B. 在化学反
应前后,原子的种类和数目没有变化,分子的种类发生变化,B正确;C. 参加反应的是两种化合物,生
成物是一种单质和一种化合物,C错误;D. 参加反应的两种分子的个数比为1 : 1,D正确。故选C。
题三: (1)吸附 (2)+1价 (3)硬水 (4)AC
详解:(1)根据净化水的原理,将水样经过沉降、过滤、吸附、杀菌消毒等步骤,可初步净化为自来水;
(2)氧元素和氢元素在化合物中通常显-2价和+1价,设HClO中氯元素的化合价为x,依据化合物中各
元素正、负化合价的代数和为零的规律可列式得:(+1)+x+(-2)=0,解得:x=+1;(3)含有较多的可溶性钙、
镁矿物质的天然水称为硬水;(4)铁制品在空气中锈蚀的实质就是铁与空气中的氧气和水等发生了复
杂的化学反应。
题四: (1)看到了水、雪和水雾(或:水雾和雪是白色的;或:温泉区的水同时存在三种状态)(2)推论:
天气寒冷,气温低于0℃以下,依据:因为只有温度在0℃以下,水才能以雪的这种固态的形式存在
(或:③处池中水温度较高。因为温度高水蒸发得快,而水蒸气在气温低时又凝结为水的小液滴,从而
形成水雾;或:②处池中的水温低。因为当水温低时,水蒸发的少,形不成水雾;或:时间为冬天,气温
低于0℃以下,之前下过一场雪。)
(3)
比较/对比项目 比较/对比结果
水分子的能量 ③②①
水分子的运动速率 ③②①
水分子的质量 相同
水分子之间的相互作用力 ①②③
水的化学性质 相同
[来源:Zxxk.Com]
(4)S Fe (SO )
2 4 3
(5)A.水是由水分子构成的
B.水分子是由氢原子和氧原子构成的(或:每个水分子是由两个氢原子和一个氧原子构成的;或:氢原
子是由氢原子核和核外电子构成的,其中原子核内有1个质子,原子核外有1个电子;氧原子是由氧
原子核和核外电子构成的,其中原子核内有8个质子,原子核外有8个电子,最外层有6个电子)
详解:(1)从化学的视觉可以观察到温泉区的水同时存在三种状态,可以看到水、雪和水雾;(2)根据水
能以雪这种固体状态的形式存在,可知天气寒冷,气温应低于0℃,同时也可推知温池中的水温度高,
因为温度高所以水蒸发得快,而水蒸气在低温时又凝结为小液滴,从而形成水雾;(3)三种状态的水分
子中,气体分子的能量最大,运动速率最快;三种分子的质量相同,固体分子之间的相互作用力最大,
气体分子之间的相互作用力最小;三种状态的水分子化学性质相同;(4)单质是由同种元素组成的纯
4zxxk.com
净物,所以硫磺属于单质,硫酸根离子和铁离子构成的盐是硫酸铁,其化学式为Fe (SO );(5)从物质
2 4 3
构成的角度,水是由水分子构成的;从分子的构成角度,水分子是由氢原子和氧原子构成的;每个水
分子是由2个氢原子和1个氧原子构成的;从原子的构成角度,氢原子是由氢原子核和核外电子构成,
其中原子核内有1个质子,原子核外有1个电子,氧原子是由氧原子核和核外电子构成,其中原子核
内有8个质子,原子核外有8个电子,最外层有6个电子。
题五: (1)C (2)玻璃片上有固体残留 (3)①0 ②浓硫酸溶于水放热,温度升高,使甲的溶解度增大,
剩余固体继续溶解 ③60
详解:本题考查pH和溶解度曲线的应用等知识。(1)石蕊、酚酞只能鉴别物质的酸碱性,鉴别酸碱度需
用pH试纸,本题应选C;(2)取上述清液滴在洁净的玻璃片上,慢慢加热至水分消失,该加热过程中若
玻璃片上出现固体残留现象时,可证明大明湖水样中含有可溶的矿物质;(3)①观察题中溶解度曲线
可知,0℃时,甲、乙两物质的溶解度相同,则0℃时,甲、乙两物质的饱和溶液的溶质质量分数相等;
②向烧杯中加入浓硫酸后,浓硫酸溶于水放出大量热量而使溶液温度升高,由于甲物质的溶解度随温
度的升高而增大,所以试管中的甲物质会继续溶解而使甲溶液的溶质质量分数增大;③已知0℃时甲
的溶解度为30g、60℃时甲的溶解度为50g,在60℃时,向盛有200g水的烧杯中加入120g甲固体搅
拌至充分溶解,然后降温至0℃,由于0℃时200g水中最多溶解60g甲固体,因此最后烧杯中剩余不
溶固体的质量为60g。
题六: (1)氯化钠、硝酸钾 甲物质的溶解度受温度变化影响较小(或乙物质的溶解度受温度变化影
响较大) (2)<
详解:(1)20℃时,分别将50 g水倒入盛有20 g NaCl和KNO 固体的烧杯中,充分搅拌,随温度升高,
3
乙烧杯中的固体明显减少,甲烧杯中的固体变化不明显,可推断出甲、乙烧杯中对应的物质分别是氯
化钠、硝酸钾;(2)由图1可知,当温度升高到30℃,乙烧杯中的固体完全溶解,说明在等量的溶剂中,
乙溶液含溶质更多,乙溶液的溶质质量分数更大。
题七: (1)C;(2)外壁;硝酸铵溶于水吸热,使烧杯温度降低,水蒸气冷凝成小水滴
解析:(1)水的初温为12℃,由于氢氧化钠溶于水时放出大量的热量,故三只烧杯中溶液的温度高于
12℃的是氢氧化钠;(2)溶解硝酸铵固体的烧杯外壁有水珠产生,是因为硝酸铵溶于水吸热,使烧杯温
度降低,水蒸气冷凝成小水滴;故答案为:(1)C;(2)外壁;硝酸铵溶于水吸热,使烧杯温度降低,水蒸气
冷凝成小水滴。
题八: (1)饱和 (2)蒸发结晶 (3)小于 (4)AC
详解:(1)30℃时,硝酸钾的溶解度是45.8g,在该温度下向l00g水中加入45.8g硝酸钾至充分溶解后,
恰好形成饱和溶液;(2)分析表中数据可知,NaCl的溶解度受温度影响变化较小,因此从NaCl溶液中
得到NaCl晶体应采用蒸发溶剂结晶的方法;(3)氯化钠和硝酸钾的溶解度都随温度的升高而增大,则
40℃时,氯化钠的溶解度在36.3~37.0之间、硝酸钾的溶解度在45.8~85.5g之间,可判断出40℃时,
氯化钠的溶解度小于硝酸钾的溶解度;(4)若要使小烧杯中的硝酸钾饱和溶液析出晶体,则需使大烧
杯中水的温度降低,冰会与水之间发生热传递而使水温降低,硝酸铵溶于水因吸收热量也会使大烧杯
中的水温降低(浓硫酸、氢氧化钠溶于水时都会因放出热量而使溶液温度升高),本题应选AC。
5