文档内容
(9)化学反应的热效应—高二化学人教版暑假作业本
1. 代表阿伏加德罗常数的值。下列说法正确的是( )
A.在氢氧燃料电池中,负极有11.2L(标准状况)气体参与反应时,转移的电子数为2
B.在氯碱工业中,制备80g烧碱时,阴极生成气体的分子数为
C.在钢铁吸氧腐蚀中,若有1molFe被腐蚀,被还原的 分子数最多为0.5
D.甲烷燃烧热 ,当0.5mol甲烷完全燃烧放出445kJ热量时,生成
(g)为
2.下列变化属于吸热反应的是:①液态水汽化;② 晶体与 晶体
混合搅拌有氨气放出;③浓硫酸稀释;④石灰石高温分解;⑤生石灰跟水反应( )
A.② B.①②④ C.②④ D.①④⑤
3.对于化学反应中的能量变化,表述正确的是( )
A.需要加热的化学反应都是吸热反应
B.中和反应都是放热反应
C.浓硫酸溶于水为放热反应
D.反应中旧键断裂放出的能量大于新键形成吸收的能量时,反应为放热反应
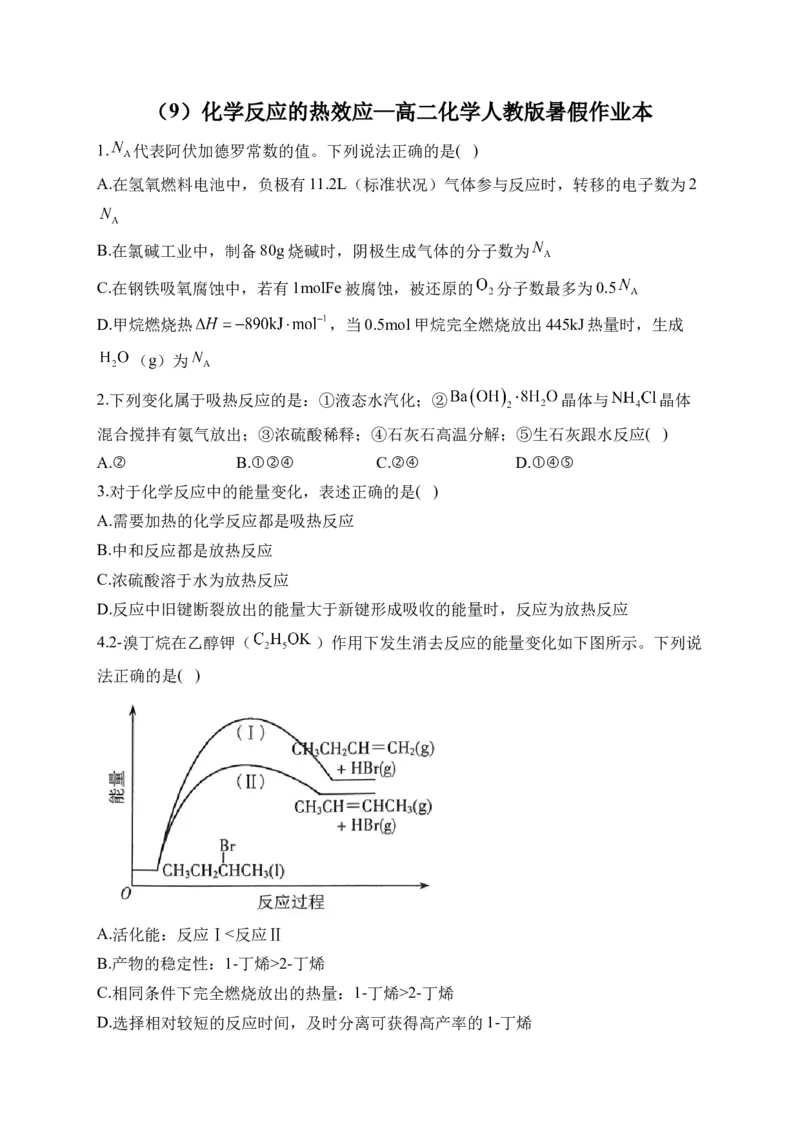
4.2-溴丁烷在乙醇钾( )作用下发生消去反应的能量变化如下图所示。下列说
法正确的是( )
A.活化能:反应Ⅰ<反应Ⅱ
B.产物的稳定性:1-丁烯>2-丁烯
C.相同条件下完全燃烧放出的热量:1-丁烯>2-丁烯
D.选择相对较短的反应时间,及时分离可获得高产率的1-丁烯5.“即食即热型快餐”适合外出旅行时使用,其内层是用铝箔包裹的并加工好的真空包装
食品,包层则是分别包装的两包化学物质, 使用时拉动预留在外的拉线使这两种化学物
质反应,放出的热量便可对食物进行加热,这两包化学物质最适合的选择是( )
A. 浓硫酸和水 B. 生石灰和水 C. 熟石灰和水 D. 氯化钠和水
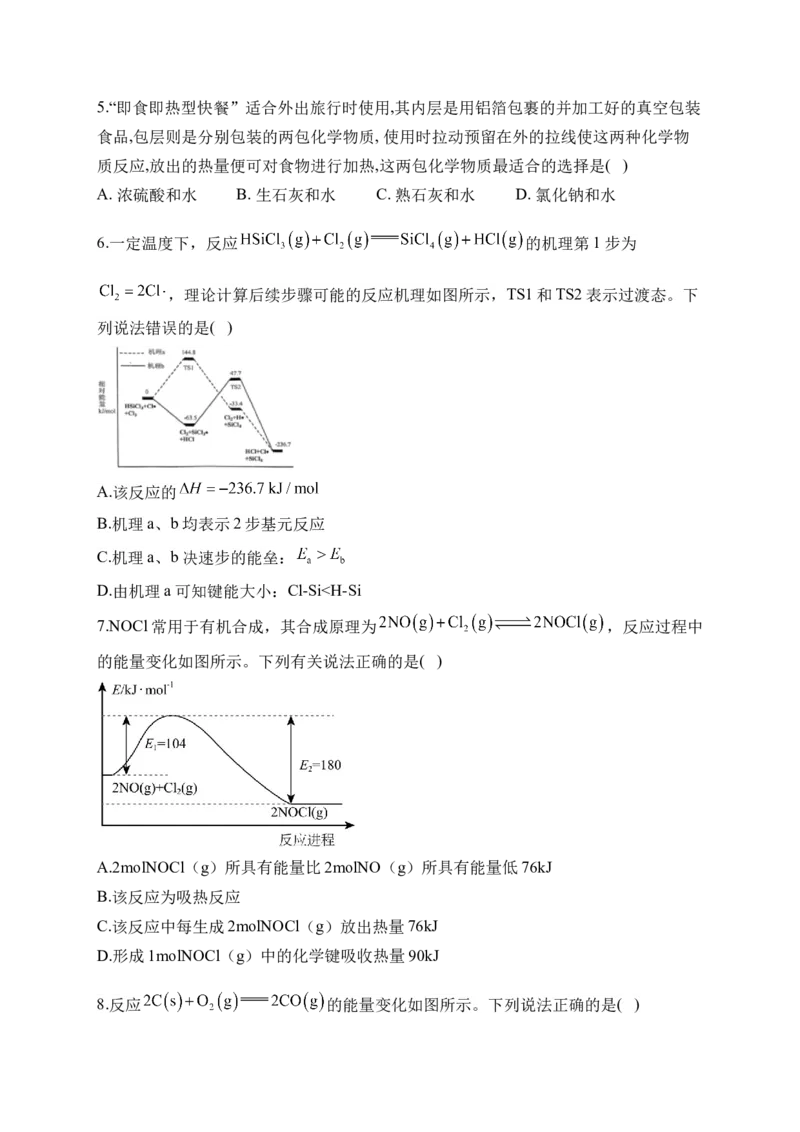
6.一定温度下,反应 的机理第1步为
,理论计算后续步骤可能的反应机理如图所示,TS1和TS2表示过渡态。下
列说法错误的是( )
A.该反应的
B.机理a、b均表示2步基元反应
C.机理a、b决速步的能垒:
D.由机理a可知键能大小:Cl-Si反应Ⅱ,故A错误;
B.能量越低越稳定,产物的稳定性:1-丁烯<2-丁烯,故B错误;
C.1-丁烯的能量大于2-丁烯,所以相同条件下完全燃烧放出的热量:1-丁烯>2-丁烯,
故C正确;
D.活化能:反应Ⅰ>反应Ⅱ,反应Ⅱ速率快,选择相对较短的反应时间,及时分离可获
得高产率的2-丁烯,故D错误;
选C。
5.答案:B
解析: A、浓硫酸溶于水放热,但浓硫酸具有极强的腐蚀性,且是液态物质,不易使
用,故A错误; B、生石灰与水反应放出大量的热,故B正确; C、熟石灰溶解于水
放热,但其溶解度极小,因此放出的热量有限,故不能达到加热的效果,故C错误;
D、氯化钠与水不反应,不能产生热量,故D错误。故选B。
6.答案:D
7.答案:C
解析:2molNOCl(g)所具有的能量比2molNO(g)和 所具有的总能量低
,A错误;
由图可知,反应物的能量总和大于生成物的能量总和,则该反应为放热反应,B错
误;
2molNO(g)和 完全反应生成2molNOCl(g),放出热量
,C正确;
形成化学键放出能量,D错误。
8.答案:C
解析:A.根据图示,12gC(s)与一定量氧气反应生成28gCO(g)放出的热量为110.5kJ,A
错误;
B. 的单位为kJ/mol,该反应的热化学方程式是2C(s)+O (g)=2CO(g)
2△H=-221KJ/mol,
B错误;
C.2molC(s)与 反应生成CO(g)放出的热量为221kJ,由于CO(g)与 反应生成
放热,因此2molC(s)与足量 反应生成 放出的热量大于221kJ,C
正确;
D.该反应的反应热等于 分子和C中化学键断裂时所吸收的总能量与CO分子中化学
键形成时所释放的总能量的差,D错误;
答案选C。
9.答案:A
解析:设O-H化学键的键能为akJ/mol,则该反应的反应热 =436kJ/mol+498kJ/
mol×0.5-2×akJ/mol=-286kJ/mol,解得a=485.5kJ/mol,A符合题意;
故答案为:A
10.答案:A
解析:已知反应的 ,即
,解得 的键能为
,2个氧原子结合生成氧气的过程需要释放能量,因此
,故选A。
11.答案:B
解析:图a中反应物总能量高于生成物总能量,故为放热反应,选项A错误;
图a中生成物总能量低,生成物更稳定,选项B正确;
图b中反应物总能量低于生成物总能量,可以表示吸热反应,而甲烷燃烧反应为放热
反应,选项C错误;
图b表示的是吸热反应,吸热反应的发生不一定需要加热,如氢氧化钡晶体和氯化铵
固体的反应在常温下就可发生,选项D错误。
12.答案:(1)①高温
②增大
③1.56;
(2)①②放热; 和
③ 或
;
解析:(1)②由图示可知,700℃以后, 的转化已基本完全,但 的转化率较
低,随着温度的升高反应Ⅱ继续正向进行,平衡产物中 的体积分数增大。③
1000℃时, 几乎已完全转化,CO 的转化率为 ,设起始时充入了
2
1mol CH 、3mol CO ,则平衡时 在反应Ⅰ中消耗1mol,总共消粍60%,所以反应
4 2
Ⅱ中消耗 ,可以计算出达到平衡时,CO 为 ,H 为 ,CO
2 2
为 ,H O为 ,反应Ⅱ的平衡常数为1.56,此时CO的体积百分数为
2
46.7%。
(2)① 与 反应生成 ,反应的化学方程式为
。②由图示可以看出, 的过程是一个放热过程。
乙酸中甲基碳原子为 杂化,而羧基碳原子为 杂化。③甲醇的碱性燃料电池类似
燃料燃烧得到 和 ,再被碱吸收,所以最终产物是碳酸钾和水,该燃料电池的
总反应为, 或
,负极是燃料发生 氧化反应,即甲酕失去电
子生成 ,同时生成水,根据电荷守恒可写出负极反应式: