文档内容
参考答案
1.【答案】A
【考点】物质的分类
【解析】氧化物是指氧元素与另外一种元素组成的二元化合物,B是碱;C是酸;D是盐。
只有A正确。
2.【答案】B
【考点】仪器名称
【解析】A为(球形)分液漏斗;B为蒸馏烧瓶;C为容量瓶;D为烧杯。
3.【答案】C
【考点】电解质
【解析】电解质是指溶于水或熔融状态下能导电的化合物,包括酸、碱、盐、部分金属氧
化物和水。A为金属单质,既不是电解质,也不是非电解质;B为有机物,属于非电解质;
C为盐类,是电解质;D为混合物,既不是电解质,也不是非电解质。
4.【答案】C
【考点】分散系
【解析】分散系中,分散质粒子直径小于1 nm的称为溶液,介于1~100 nm之间的称为胶
体,大于100 nm的称为浊液。四个选项中,A、D属于胶体;B为溶液;C为悬浊液。
5.【答案】D
【考点】能源
【解析】三大化石燃料包括:煤、石油、天然气,D不是化石燃料。
6.【答案】C
【考点】常见化合物的用途
【解析】发酵粉的主要成分是碳酸氢钠,俗称小苏打,故C错误。
7.【答案】D
【考点】反应类型判断
【解析】置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,
故D正确。
8.【答案】A
【考点】化学用语
第1页 | 共10页【解析】A选项中氯原子结构示意图应为 ,故A错误。
9.【答案】C
【考点】溶液酸碱性判断
【解析】A项,氢氧化钠的水溶液显碱性,能使酚酞变红;B项,碳酸钠水溶液中碳酸根
离子水解显碱性,能使酚酞变红;C项,氯化钠水溶液显中性,不能使酚酞变红;D项,
氨气与水反应生成氨水,氨水显碱性,能使酚酞变红;故选C。
10.【答案】D
【考点】物质鉴别
【解析】A项,CO不能使澄清石灰水变浑浊,CO 可以使澄清石灰水变浑浊;B项,苯的
2
密度比水小,在上层,四氯化碳的密度比水大,在下层;C项,氢氧化钡与NH Cl混合加
4
热产生有刺激性气味的气体,与(NH )SO 反应加热产生白色沉淀硫酸钡,同时产生有刺激
4 2 4
性气味的气体,与KSO 反应只产生白色沉淀,故可鉴别;D项,碘水中有碘单质,溴水
2 4
可以氧化淀粉碘化钾试纸中的碘离子,生成碘单质,都可以使淀粉碘化钾试纸变蓝,故无
法鉴别,选D。
11.【答案】A
【考点】五同
【解析】核素是具有一定数目质子和一定数目中子的一种原子,氧的质子数为 8,该原子
的质量数为18,那么中子数为10,故A正确;金刚石和石墨可以互相转化,B错误;乙酸
和乙酸甲酯的官能团不同,不是同系物,C错误;己烷有5种同分异构体,D错误。
12.【答案】B
【考点】离子方程式的书写
【解析】氢氧化钡是强电解质,书写离子方程式时应写成离子形式,故正确的离子方程式
为CO+Ba2+===BaCO ↓。
3
13.【答案】D
【考点】元素推断
【解析】可推出X、Y、Q、Z分别为N、O、Si、Cl,同周期元素从左到右原子半径逐渐
减小,A错误;Si的非金属性弱于Cl,所以HSiO 的酸性比HClO 的酸性弱,B错误;
2 3 4
N、O与H元素可形成NH NO ,含有离子键,C错误;Si是良好的半导体材料,与Cl可
4 3
形成化合物SiCl ,D正确。
4
第2页 | 共10页14.【答案】A
【考点】烷烃取代物的种类,乙烯、乙醇、乙醛的化学性质
【解析】苯虽然能与H 发生加成反应,但并没有碳碳双键,而是一种介于单键与双键之间
2
的特殊共价键,B错误;水与钠的反应比乙醇与钠的反应剧烈,C错误;乙醛易被氧化成
乙酸,D错误。
15.【答案】C
【考点】糖类、脂类、蛋白质
【解析】高级脂肪酸甘油酯不是高分子化合物,A错误;同种氨基酸之间也可以形成多肽,
B错误;鸡蛋清是一种蛋白质,向其中加入硫酸钠产生沉淀是发生了盐析,这是一种物理
变化,是可逆的,因此加水后沉淀又会溶解,C正确;用新制氢氧化铜检验葡萄糖时需在
碱性环境下,应先加NaOH中和硫酸,再加氢氧化铜,故D错误。
16.【答案】B
【考点】化学反应速率与转化率
【解析】正反应速率与反应物的浓度有关,且反应物浓度越大反应速率越快,而 NH 是产
3
物,故A错误;N 和H 的物质的量之比为1∶3,反应消耗也是1∶3,故N 和H 的转化
2 2 2 2
率相同,故B正确;当1 mol N 参与反应时放出的热量为92.4 kJ,而题目中没有确定反应
2
的量,故C错误;由表格可知600 ℃、30 MPa下反应达到平衡时,NH 的物质的量分数相
3
对于500 ℃、30 MPa时减小,故D错误。
17.【答案】B
【考点】原电池(电极判断、电极方程式书写)
【解析】金属(M)空气电池中M失电子作负极,故A正确;根据传递M2+和OH-,可知电
解质是熔融的 M(OH) ,故 B 错误;空气得电子作正极,电极反应为 O +4e-+
2 2
2HO===4OH-,故C正确;电池总反应为2M+O+2HO===2M(OH) ,故D正确。
2 2 2 2
18.【答案】B
【考点】弱电解质
【解析】25 ℃时,pH<7的溶液呈酸性,但温度未知,所以pH<7的溶液不一定呈酸性,
故A正确;在相同温度下,一水合氨部分电离,NaOH完全电离,物质的量浓度相等的氨
水、NaOH溶液,NaOH溶液中c(OH-)更大,故B错误;在相同温度下,盐酸、CHCOOH
3
溶液中分别存在电荷守恒:c(Cl-)+c(OH-)=c(H+),c(CHCOO-)+c(OH-)=c(H+),又因
3
为pH相等,所以c(Cl-)=c(CHCOO-),故C正确;氨水和盐酸反应后的溶液中存在c(Cl
3
-)+c(OH-)=c(NH)+c(H+),若c(Cl-)=c(NH),则c(OH-)=c(H+),溶液呈中性,故D正
第3页 | 共10页确。
19.【答案】D
【考点】热化学
【解析】根据气态水变为液态水放热,故A错误;由转化关系图可知ΔH +ΔH≠0,故B
1 2
错误;由转化关系图可知ΔH≠ΔH +ΔH ,故C错误;由转化关系图可知,经过一个循环
3 4 5
之后回到原始状态,ΔH+ΔH+ΔH+ΔH+ΔH=0,故D正确。
1 2 3 4 5
20.【答案】D
【考点】微粒间作用力和物质结构
【解析】S和Mg的最外电子层分别得、失2个电子后都形成了8个电子的稳定结构,故A
选项正确;石英和金刚石是原子晶体,原子间通过共价键结合,故 B选项正确;浓硫酸与
水混合时,浓硫酸发生电离,破坏了共价键,属于微粒间作用力,故C选项正确;HO 分
2 2
解破坏共价键,不属于分子间作用力,故D选项错误。
21.【答案】A
【考点】反应转化率与选择性
【解析】由图像可知,当乙醇进料量一定,随乙醇转化率增大,乙烯选择性先升高后减小
故A选项错误;由图像可知,当乙醇进料量一定,随温度的升高,乙烯选择性先升高后减
小,故B选项正确;由图像可知,当温度一定,随乙醇进料量增大,乙醇转化率减小,故
C选项正确;由图像可知,当温度一定,随乙醇进料量增大,乙烯选择性增大,故D选项
正确。
22.【答案】B
【考点】N
A
【解析】浓硫酸与镁反应产物是二氧化硫和硫酸镁,浓硫酸变稀之后与镁反应产物是氢气
和硫酸镁,若0.2 mol HSO 反应产物全为二氧化硫,转移电子数为0.2N ,若产物全为氢气
2 4 A
转移电子数为0.4N ,所以转移电子数应介于0.2N 和0.4N 之间,故A选项正确;pH=3
A A A
的醋酸溶液中c(H+)=10-3 mol·L-1,在1 L的溶液中,含H+的数目等于0.001N ,故B选
A
项错误;1个苯中含有6个C—H键,1 mol苯中含有C—H键的数目一定为6N ,故C选项
A
正确;R2+的核外电子数为(A-N-2),a mol的R2+的核外电子数为a(A-N-2)N ,故D选
A
项正确。
23.【答案】C
【考点】溶液中的离子平衡
【解析】根据图像可知在pH>3时,加入少量NaOH固体,α(HA-)在减小,故A选项错误;
第4页 | 共10页根据图像的交点可知HA-的电离平衡常数近似为10-4,A2-的水解平衡常数近似为10-10,
将等物质的量的NaHA和NaA混合物溶于水,所得的溶液中α(HA-)<α(A2-),故B选项
2
错误;根据图像可知NaHA溶液为酸性溶液,故HA-的电离能力大于HA-的水解能力,故
C选项正确;D选项不确定是否含别的阳离子,若含别的阳离子则α(H A)和α(HA-)不相等,
2
故D选项错误。
24.【答案】B
【考点】气体的除杂问题
【解析】题干中要求逐一吸收相应组分,即一种溶液吸收一种气体,连苯三酚的碱性溶液
除了能吸收O 之外,还能与CO 反应;CuCl的盐酸溶液除了能吸收CO之外,还能被O
2 2 2
氧化;为满足题意,吸收O 前需要先吸收CO ,吸收CO前需吸收O ,所以气体被逐一吸
2 2 2
收的顺序应该是CO 、O 和CO,所以A、C正确;若用灼热的铜网代替连苯三酚的碱性溶
2 2
液,会发生2Cu+O=====2CuO,CO+CuO=====CO +Cu,又产生了CO ,故B错误;
2 2 2
由于盐酸易挥发,最后一个吸收液为CuCl的盐酸溶液,导出气体中可能含有HCl,故D正
确。
25.【答案】C
【考点】离子推断
【解析】KSO 、Ba(OH) 、NaCO 混合物溶于水,滤渣中含有不溶于盐酸的BaSO ,不符
2 4 2 2 3 4
合③的结果,故A错误;NaCO 、AgNO 、KNO 混合物溶于水,碳酸银为滤渣,其和盐
2 3 3 3
酸反应生成二氧化碳气体和氯化银沉淀,不符合③的结果,故B错误;KCO 、NaCl、
2 3
Ba(NO ) 混合物溶于水,碳酸钡为滤渣,可以完全溶于盐酸,生成二氧化碳气体,符合③
3 2
的结果,滤液中可能是碳酸根离子剩余,也可能是钡离子剩余,若碳酸根离子有剩余,加
入氯化钡会有白色沉淀,符合②的结果,故C正确;KNO 、MgCl 、NaOH混合物溶于水,
3 2
氢氧化镁为滤渣,其溶于盐酸无气体产生,不符合③的结果,故D错误。
26.【答案】(1)CH≡CH
(2)加成反应
(3)CH CHCOOH+CHOH CHCHCOOCH +HO
3 2 3 3 2 3 2
(4)ACD
【考点】简单有机推断及有机物的性质
【解析】B的化学式为C HO ,依据A与CO、HO以物质的量1∶1∶1的比例形成B可
3 4 2 2
知A的化学式为C H ,故A为乙炔,结构简式为CH≡CH。依据转化关系以及E是有芳香
2 2
第5页 | 共10页气味、不易溶于水的油状液体可知E为酯,根据E的化学式为C HO 可知E为饱和酯,
4 8 2
B→D→E先发生酯化反应再发生加成反应,由B→C→E的反应条件可知是先发生加成反应
再 发 生 酯 化 反 应 , 故 C 为 CHCHCOOH , D 为 CH===CHCOOCH , E 为
3 2 2 3
CHCHCOOCH 。
3 2 3
(1)A为乙炔,结构简式为CH≡CH。
(2)D→E的反应类型为加成反应。
(3)C→E的化学方程式为CHCHCOOH+CHOH CHCHCOOCH +HO。
3 2 3 3 2 3 2
(4)B与C都含有羧基,都可与金属钠反应,故不可用金属钠鉴别 B和C,A项错误;A中
含有碳碳叁键,可与氯化氢发生加成反应,B项正确;E为丙酸甲酯,不可由乙醇和乙酸
加热反应生成,C项错误;与A的最简式相同,相对分子质量为78的烃的化学式为C H,
6 6
C H 不一定是苯,也有可能是含碳碳双键与碳碳叁键的烃,故可能使酸性KMnO 溶液褪色,
6 6 4
D项错误。
27.【答案】(1)HSH BaSO (2)4Na SO =====NaS+3NaSO (3)2S2-+SO+6H+
4 2 3 2 2 4
===3S↓+3HO
2
【考点】无机推断、氧化还原反应
【解析】亚硫酸钠隔绝空气加热分解质量并没改变,说明并没有生成气体,应该是分解成
了几种固体,加入盐酸后产生气体Y,根据密度算出气体Y的摩尔质量为34 g·mol-1,结合
题目以及元素守恒,推断气体Y为HS。那么NaSO 的分解生成物中一定有S2-(Na S),同
2 2 3 2
时这是一个氧化还原反应,+4价的S有降价必然还有升价,只能生成+6价,所以另一分
解产物应该是含有硫酸根的NaSO ,再配平即可。(3)X与亚硫酸钠混合,在酸性环境下产
2 4
生了淡黄色沉淀,根据题目环境以及我们学过的淡黄色沉淀推知生成S单质,显然这是一
个S2-与SO的归中反应,反应物还有H+。
28.【答案】(1)乙 铜丝变红色,试管壁有水珠生成
(2)不正确,剩余的铁将生成的三价铁还原成了二价铁离子:Fe+2Fe3+===3Fe2+
【考点】气体的收集;CuO的还原反应;Fe3+和Fe2+的转化:Fe3+的检验
【解析】(1)氢气的密度小于空气,所以用向下排空气法收集,选乙;氧化铜和氢气发生反
应CuO+H===HO+Cu,所以铜丝变红色,试管壁有水珠出现。
2 2
(2)已知3Fe+4HO(g)=====Fe O +4H ,Fe O 中含有三价铁,但是剩余的铁单质会和三价
2 3 4 2 3 4
铁离子反应生成二价铁离子,若剩余铁单质足量,将所有铁离子反应完全,那么加入硫氰
化钾溶液,就不会出现血红色。
第6页 | 共10页29.【答案】(1)60%(或0.60) (2)0.095 mol
【考点】氧化还原反应、电子守恒计算
【解析】(1)KMnO 的分解率=。题目已知KMnO 共7.90 g,物质的量为0.05 mol。加热分
4 4
解后剩余固体为7.42 g,损失的质量为O 的质量0.48 g,说明O 的物质的量为0.015 mol。
2 2
由2KMnO =====KMnO +MnO +O↑,可知消耗KMnO 0.03 mol。所以KMnO 的分解
4 2 4 2 2 4 4
率为×100%=60.0%。
(2)在整个反应过程前后,锰元素从+7价全部转化为+2价,说明整个反应过程中转移了
0.05 mol×5=0.25 mol电子。剩余固体与浓盐酸反应生成气体A,则A应为氯气。所以整个
反应过程中只有氧元素和氯元素失电子。氧元素失电子产生氧气,转移了 0.015 mol×4=
0.06 mol电子。根据电子守恒得知,氯元素必然转移0.19 mol电子。每产生1 mol氯气就转
移2 mol电子,所以一定会产生0.19 mol÷2=0.095 mol氯气。
30.【答案】(一)(1)C
(2)温度升高加快反应速率;反应吸热,平衡正向移动,温度升高使平衡正向移动的作用大
于压强增大使平衡逆向移动的作用
(3)①1.951 ②反应2的活化能比反应1的小,催化剂显著降低了反应2的活化能,反应生
成的C H 很快转变成C H,故x 显著低于x
10 12 10 8 1 2
③
(二)Fe O+6e-+3HO===2Fe+6OH-
2 3 2
【考点】热化学、电化学、化学平衡
【解析】(一)(1)提高平衡转化率即平衡正向移动,应该升温、降压。所以选择高温低压,
选C。
(3)①该反应可以直接看作十氢萘分别分解为四氢萘和萘,则生成氢气的物质的量:0.374
mol×5+0.027 mol×3=1.951 mol。
(二)根据阴极的另一个方程式以及题干信息可知,Fe O 参与阴极反应,生成Fe。电解质为
2 3
熔融NaOH—KOH,则电极方程式为Fe O+6e-+3HO===2Fe+6OH-。
2 3 2
31.【答案】(1)2Al+2NaOH+2HO===2NaAlO +3H↑ AlO+CO +2HO===Al(OH) ↓
2 2 2 2 2 3
第7页 | 共10页+HCO
(2)BCD
(3)⑥⑤④
(4)①降低AlCl 的溶解度,使其以AlCl ·6H O晶体形式析出
3 3 2
②强酸性环境会腐蚀滤纸 饱和氯化铝溶液
③用滤纸吸干
【考点】方程式书写、实验仪器操作与注意事项、制备明矾晶体、AlCl ·6H O晶体
3 2
【解析】(2)Al(OH) 加热失去水生成固体Al O ,涉及的仪器是坩埚、坩埚钳、三脚架、酒
3 2 3
精灯等,此题重点考查的是坩埚和坩埚钳的使用注意事项。坩埚洗净后,需要缓慢加热到
500 ℃以上才可以使用,故A项错;称量灼烧前后的质量不再发生变化说明坩埚内固体只
有Al O ,故B正确;使用坩埚钳移动坩埚时,需预热坩埚钳,故C正确;坩埚取下后不
2 3
能直接放在实验台上冷却,应放在石棉网上冷却待用,故D正确;加热后的固体应先冷却
后再称量,测定结果更准确,且灼烧过的Al O 不吸潮,故不需要趁热称量,故E错。
2 3
(3)由表格可知,考查影响晶体大小的因素,以及明矾晶体的制备过程。明矾晶体的溶解度
随着温度升高而增大,选用低温下明矾饱和溶液,再用规则明矾小晶体悬挂在溶液中央,
自然冷却,故选⑥⑤④。
(4)此装置的目的是制备AlCl ·6H O,通入HCl后在冰水浴作用下晶体析出,故HCl的作用
3 2
除了抑制AlCl 水解,还能促进AlCl ·6H O晶体析出;大量HCl溶解使溶液呈强酸性,会
3 3 2
腐蚀滤纸,故采用玻璃纤维代替滤纸;干燥晶体时为了防止失去结晶水,一般用滤纸吸干
即可。
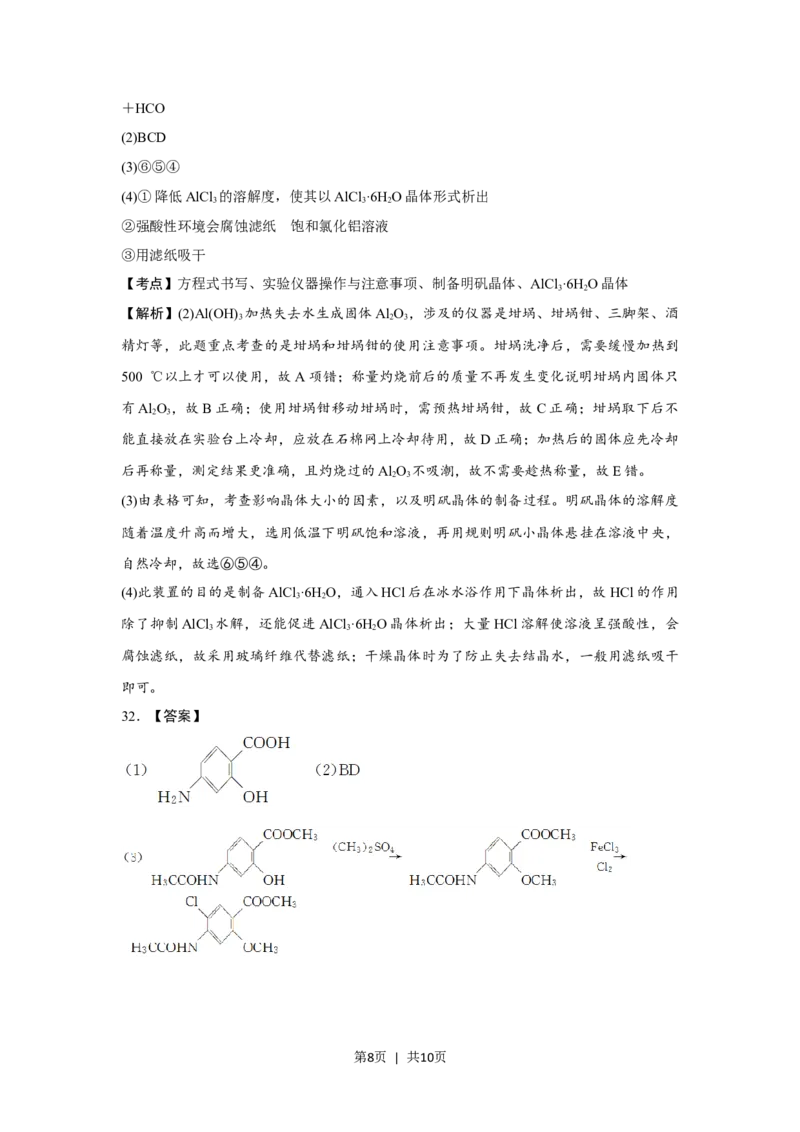
32.【答案】
第8页 | 共10页【考点】有机推断
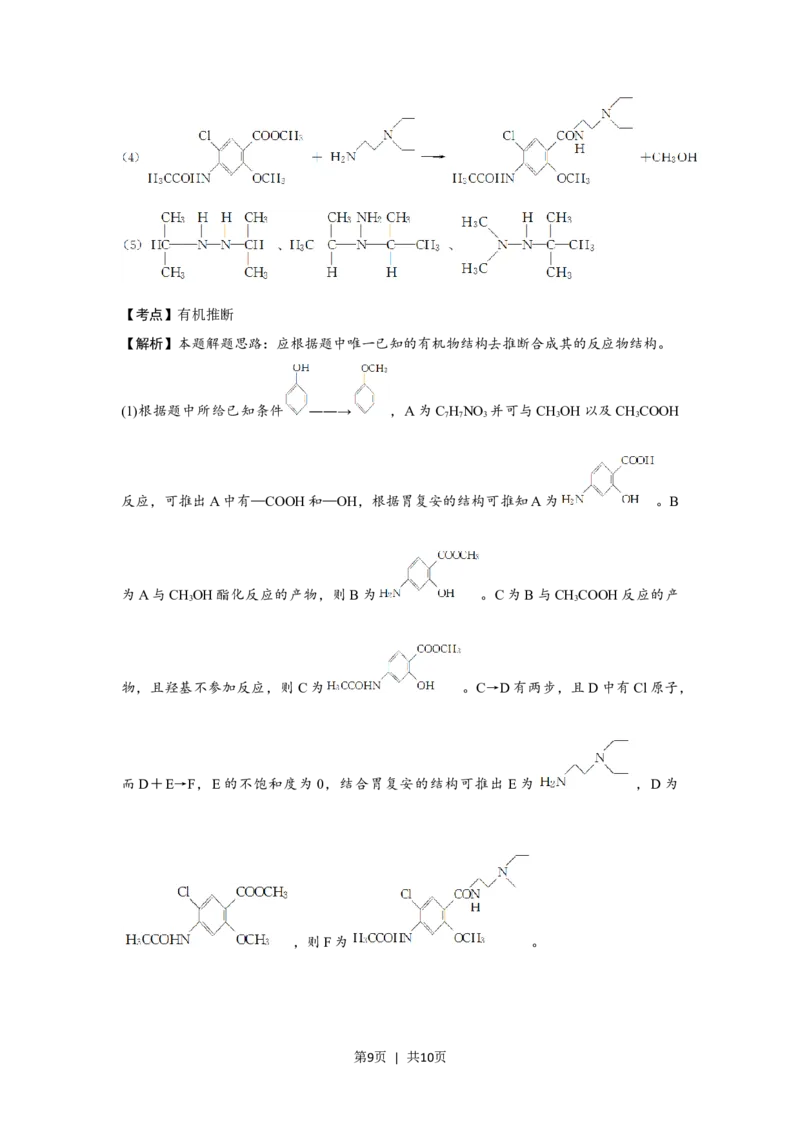
【解析】本题解题思路:应根据题中唯一已知的有机物结构去推断合成其的反应物结构。
(1)根据题中所给已知条件 ――→ ,A为C HNO 并可与CHOH以及CHCOOH
7 7 3 3 3
反应,可推出A中有—COOH和—OH,根据胃复安的结构可推知A为 。B
为A与CHOH酯化反应的产物,则B为 。C为B与CHCOOH反应的产
3 3
物,且羟基不参加反应,则C为 。C→D有两步,且D中有Cl原子,
而D+E→F,E的不饱和度为 0,结合胃复安的结构可推出 E为 ,D为
,则F为 。
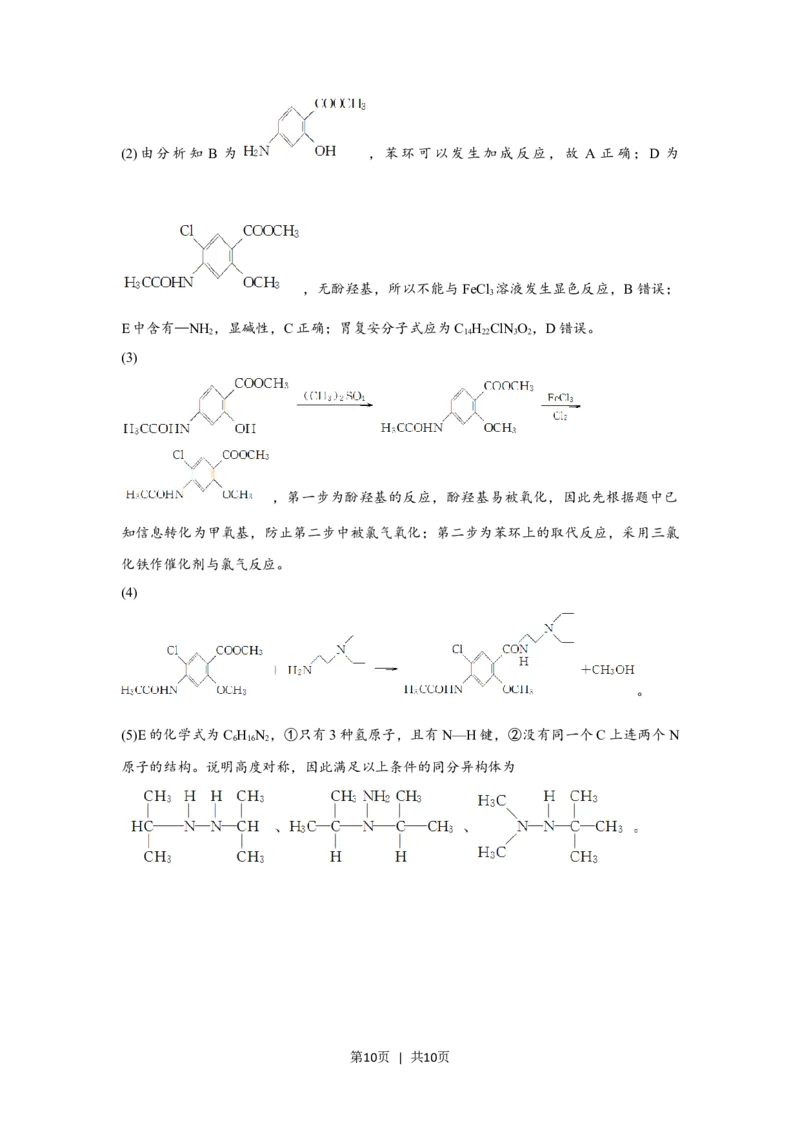
第9页 | 共10页(2)由分析知 B 为 ,苯环可以发生加成反应,故 A 正确;D 为
,无酚羟基,所以不能与FeCl 溶液发生显色反应,B错误;
3
E中含有—NH ,显碱性,C正确;胃复安分子式应为C H ClN O,D错误。
2 14 22 3 2
(3)
,第一步为酚羟基的反应,酚羟基易被氧化,因此先根据题中已
知信息转化为甲氧基,防止第二步中被氯气氧化;第二步为苯环上的取代反应,采用三氯
化铁作催化剂与氯气反应。
(4)
。
(5)E的化学式为C H N ,①只有3种氢原子,且有N—H键,②没有同一个C上连两个N
6 16 2
原子的结构。说明高度对称,因此满足以上条件的同分异构体为
第10页 | 共10页