文档内容
第3讲 电解池 金属的腐蚀与防护
[考纲要求]
1.了解电解池的工作原理,能写出电极反应和电解反应方程式。
2.了解金属发生电化学腐蚀的原因,金属腐蚀的危害,防止金属腐蚀的措施。
考点一 电解原理
1知识梳理
1.电解
使电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引起 的过程。
在此过程中, 能转化为 能。
2.电解池
(1)电解池的构成条件
①有与 相连的两个电极。
②两个电极插入 或 中。
③形成 。
(2)电极名称及电极反应式(如图)
(3)电子和离子的移动方向
3.阴、阳两极的放电顺序
(1)阳极放电顺序活性电极(Zn、Fe、Cu等):电极材料失电子;
惰性阳极(Pt、Au、石墨等): >OH->含氧酸根>F-。
(2)阴极放电顺序
>H+(酸中)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+。
[思考]
根据对电解规律的理解,用惰性电极电解3 mol·L-1 NaCl和1 mol·L-1 CuSO 的混
4
合溶液,可看作三个电解阶段。
( 1 ) 第 一 阶 段 : 相 当 于 电 解 溶 液 , 电 解 总 反 应
________________________________________________________________________;
( 2 ) 第 二 阶 段 : 相 当 于 电 解 溶 液 , 电 解 总 反 应
________________________________________________________________________;
( 3 ) 第 三 阶 段 : 相 当 于 电 解 溶 液 , 电 解 总 反 应
________________________________________________________________________。
[判断] (正确的打“√”,错误的打“×”)
(1)电解质溶液的导电过程就是电解质溶液被电解的过程( )
(2)某些不能自发进行的氧化还原反应,通过电解可以实现( )
(3)电解CuCl 溶液,阴极逸出的气体能够使湿润的淀粉碘化钾试纸变蓝色( )
2
(4)电解盐酸、硫酸等溶液,H+放电,溶液的pH逐渐增大( )
(5)电解时,电解液中阳离子移向阳极,发生还原反应( )
(6)用惰性电极电解CuSO 溶液一段时间后,加入Cu(OH) 一定可使电解质溶液恢
4 2
复到电解前的情况( )
[提醒]
常见的电解类型(惰性电极)
电解质 电解质溶
类型 实例 电极反应特点 pH
浓度 液复原
NaOH 阴:4H++4e- 增大 增大 加水
===2H↑
电解 HSO 2 增大 减小 加水
2 4
阳:4OH--4e
水型
-===2HO+
NaSO 2 增大 不变 加水
2 4
O↑
2
HCl 电解质电离出 减小 增大 通氯化氢
电解电 的阴、阳离子
解质型 CuCl 分别在两极放 减小 加氯化铜
2
电阴极:HO放
2
放H H 生碱 生成新
2 2
NaCl 增大 通氯化氢
生碱型 阳极:电解质 电解质
阴离子放电
阴极:电解质
放O 阳离子放电 生成新
2
CuSO 减小 加氧化铜
4
生酸型 阳极:HO放 电解质
2
O 生酸
2
2对点速练
练点一 电极的判断与电极反应式书写
1.按要求书写电极反应式和总反应方程式:
(1)用惰性电极电解AgNO 溶液
3
阳 极 反 应 式
________________________________________________________________________;
阴 极 反 应 式
________________________________________________________________________;
总 反 应 离 子 方 程 式
________________________________________________________________________。
(2)用惰性电极电解MgCl 溶液
2
阳 极 反 应 式
________________________________________________________________________;
阴 极 反 应 式
________________________________________________________________________;
总 反 应 离 子 方 程 式
________________________________________________________________________。
(3)用铁作电极电解NaCl溶液
阳 极 反 应 式
________________________________________________________________________;
阴 极 反 应 式
________________________________________________________________________;
总 反 应 化 学 方 程 式
________________________________________________________________________。
(4)用Al作电极电解NaOH溶液阳 极 反 应 式
________________________________________________________________________;
阴 极 反 应 式
________________________________________________________________________;
总 反 应 离 子 方 程 式
________________________________________________________________________。
(5)用Al作阳极,电解HSO 溶液,铝材表面形成氧化膜
2 4
阳 极 反 应 式
________________________________________________________________________;
阴 极 反 应 式
________________________________________________________________________;
总 反 应 化 学 方 程 式
________________________________________________________________________。
练后归纳
电解时电极反应书写“四注意”
1.书写电解池中电极反应式时,如果氢离子来自于水,那电极反应式写水或氢离子都
可以,但书写电解总反应方程式时,要写水分子。
2.阴极材料主要作用是导电,电极本身一般不反应,是溶液(或熔融电解质)中的阳
离子放电。
3.要确保两极电子转移数目相同,且总反应方程式中注明条件“电解”。
4.电解水溶液时,应注意放电顺序中H+、OH-之后的离子一般不参与放电。
练点二 电解原理分析判断
2.以石墨为电极分别电解水和饱和食盐水,关于两个电解池反应的说法正确的是(
)
A.阳极反应式相同
B.电解结束后所得液体的pH相同
C.阴极反应式相同
D.通过相同电量时生成的气体总体积相等(同温同压)
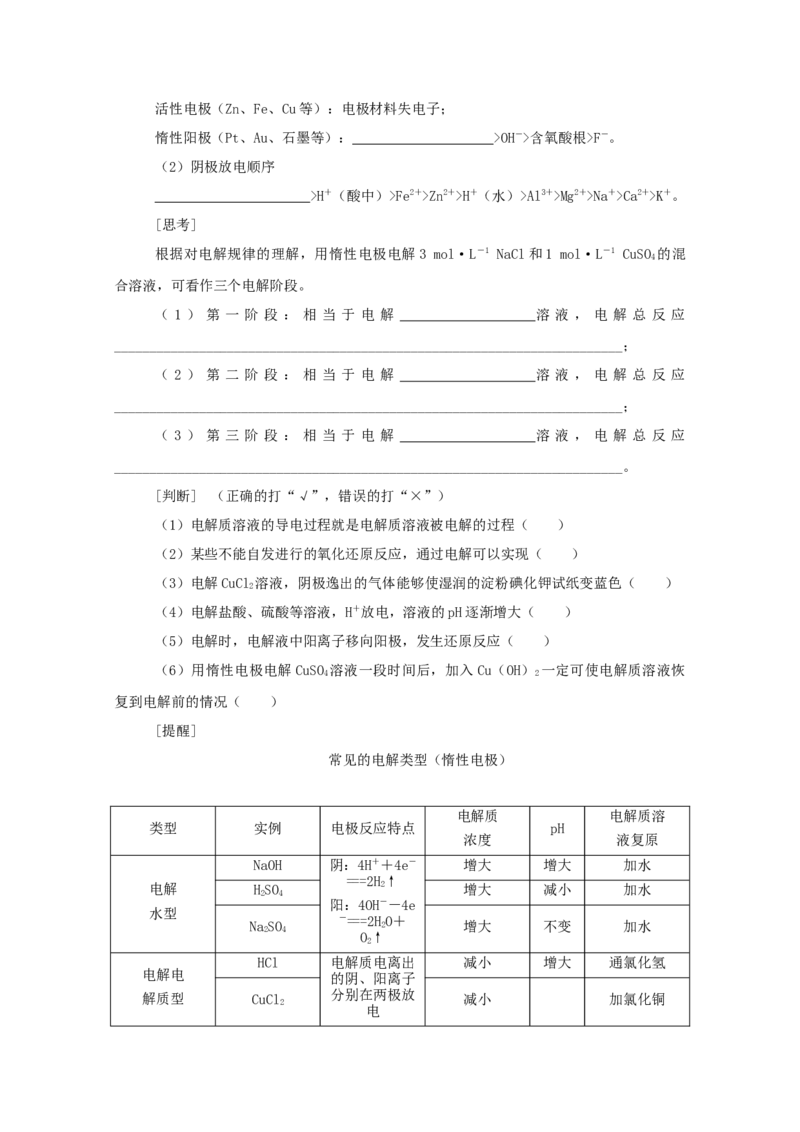
3.纳米级CuO由于具有优良的催化性能而受到关注。采用离子交换膜控制电解液中OH
2-的浓度制备纳米级CuO的装置如图所示,发生的反应为:2Cu+HO=====CuO+H↑。下列
2 2 2 2
说法正确的是( )
A.钛电极发生氧化反应
B.阳极附近溶液的pH逐渐增大
C.离子交换膜应采用阳离子交换膜
D.阳极反应式是:2Cu+2OH--2e-===CuO+HO
2 2
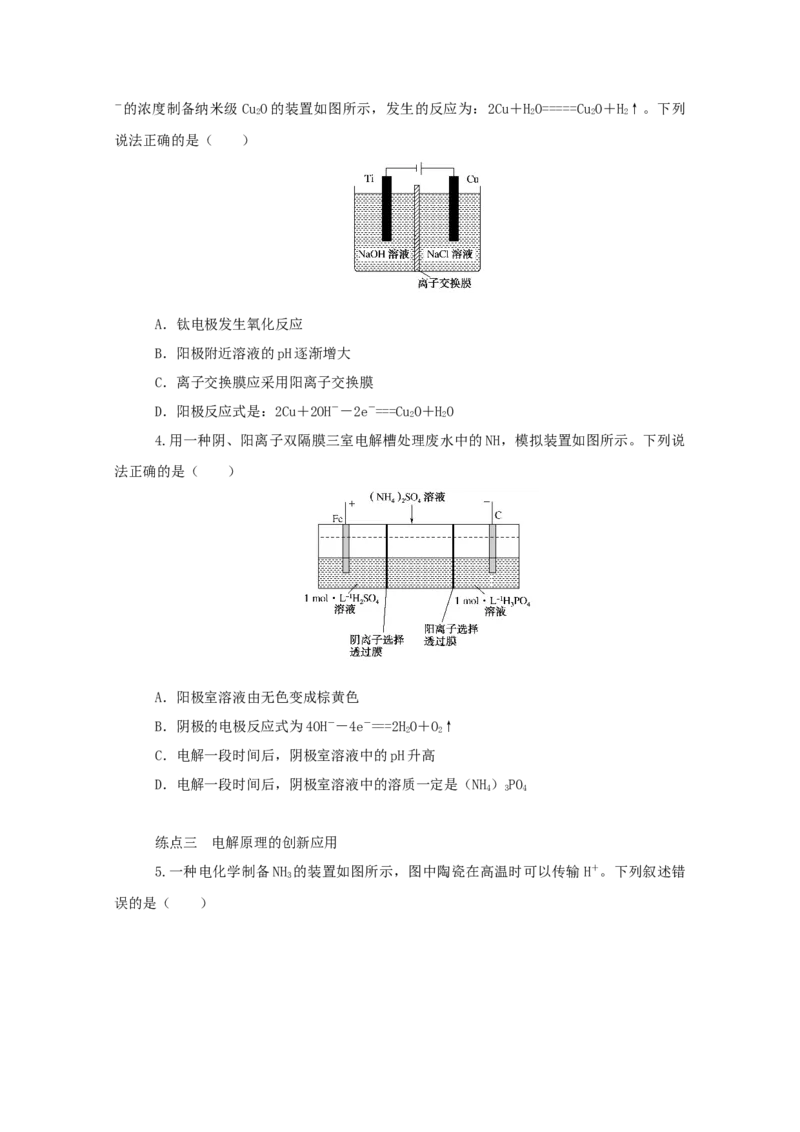
4.用一种阴、阳离子双隔膜三室电解槽处理废水中的NH,模拟装置如图所示。下列说
法正确的是( )
A.阳极室溶液由无色变成棕黄色
B.阴极的电极反应式为4OH--4e-===2HO+O↑
2 2
C.电解一段时间后,阴极室溶液中的pH升高
D.电解一段时间后,阴极室溶液中的溶质一定是(NH)PO
4 3 4
练点三 电解原理的创新应用
5.一种电化学制备NH 的装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错
3
误的是( )A.Pd电极b为阴极
B.阴极的反应式为:N+6H++6e-===2NH
2 3
C.H+由阳极向阴极迁移
D.陶瓷可以隔离N 和H
2 2
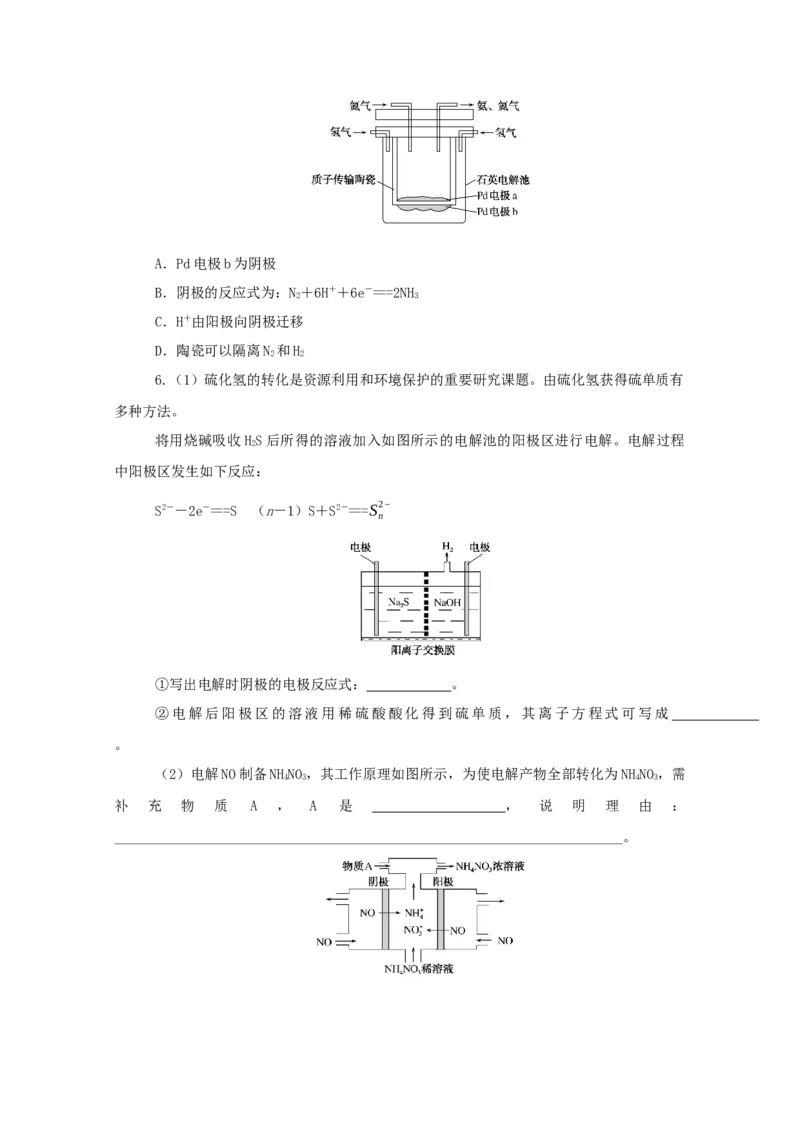
6.(1)硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有
多种方法。
将用烧碱吸收HS后所得的溶液加入如图所示的电解池的阳极区进行电解。电解过程
2
中阳极区发生如下反应:
S2--2e-===S (n-1)S+S2-===S2−
n
①写出电解时阴极的电极反应式: 。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成
。
(2)电解NO制备NHNO ,其工作原理如图所示,为使电解产物全部转化为NHNO ,需
4 3 4 3
补 充 物 质 A , A 是 , 说 明 理 由 :
________________________________________________________________________。考点二 电解原理的应用
1知识梳理
1.电解饱和食盐水
(1)电极反应
阳极反应式: ( 反应)
阴极反应式: ( 反应)
(2)总反应方程式
2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
离子反应方程式:2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2
2.电解精炼铜
(1)电极材料:阳极为 ;阴极为 。
(2)电解质溶液:含Cu2+的盐溶液。
(3)电极反应:
阳极: 、 、 、
;
阴极: 。
3.电镀
右图为金属表面镀银的工作示意图,据此回答下列问题:
(1)镀件作 极,镀层金属银作 极。
(2)电解质溶液是 。
(3)电极反应:
阳 极 :
________________________________________________________________________;
阴 极 :
________________________________________________________________________。(4)特点: 极溶解, 极沉积,电镀液的浓度 。
4.电冶金
利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。
(1)冶炼钠
2NaCl(熔融)=====2Na+Cl↑
2
电极反应:
阳 极 :
________________________________________________________________________;
阴 极 :
________________________________________________________________________。
(2)冶炼铝
2AlO(熔融)=====4Al+3O↑
2 3 2
电极反应:
阳 极 :
________________________________________________________________________;
阴 极 :
________________________________________________________________________。
(3)冶炼Mg、Ca与钠相似都是电解氯化物,因AlCl 是共价化合物,故电解AlO 制
3 2 3
Al。
[判断] (正确的打“√”,错误的打“×”)
(1)电解铜和电解精炼铜时,电解质溶液中的c(Cu2+)均保持不变( )
(2)电解冶炼镁、铝通常电解MgCl 和AlO,也可电解MgO和AlCl( )
2 2 3 3
(3)若把Cu+HSO===CuSO+H↑设计成电解池,应用Cu作阳极( )
2 4 4 2
(4)电解饱和食盐水时,两个电极均不能用金属材料( )
(5)在镀件上电镀铜时,镀件应连接电源的正极( )
(6)电解精炼时,阳极泥可以作为提炼贵重金属的原料( )
2对点速练
练点一 氯碱工业分析与拓展
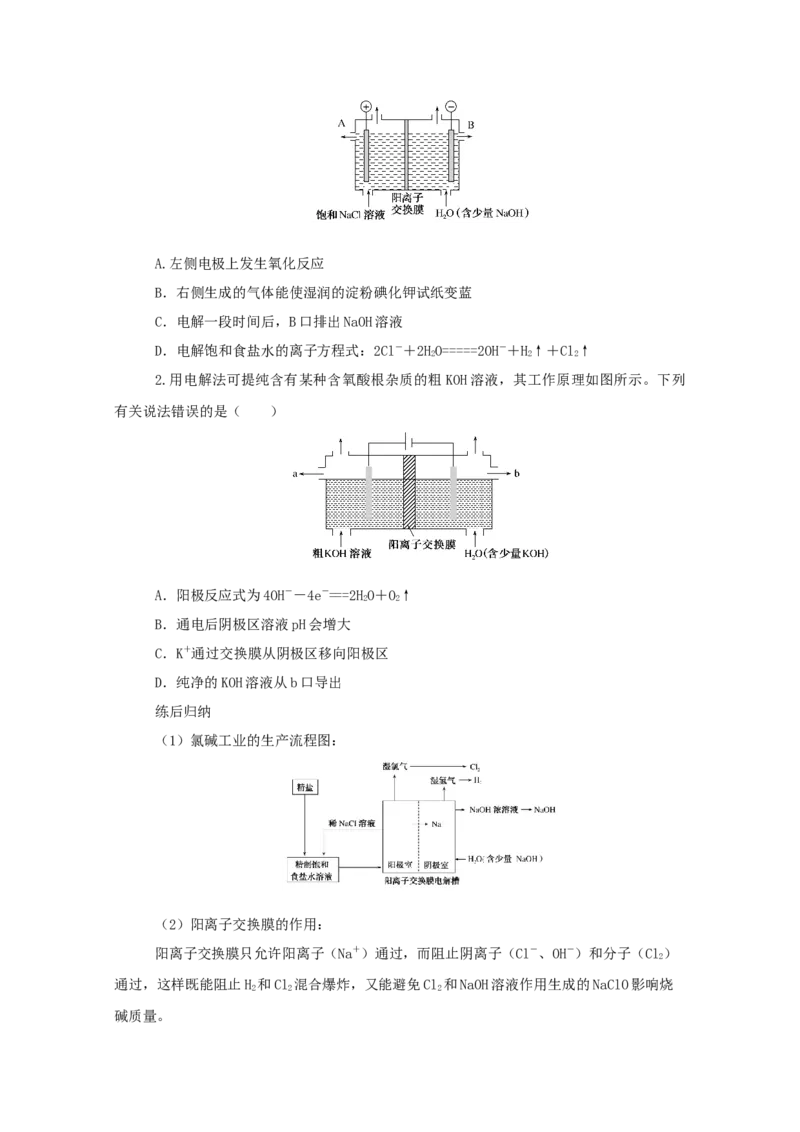
1.如图为电解饱和食盐水装置,下列有关说法不正确的是( )A.左侧电极上发生氧化反应
B.右侧生成的气体能使湿润的淀粉碘化钾试纸变蓝
C.电解一段时间后,B口排出NaOH溶液
D.电解饱和食盐水的离子方程式:2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2
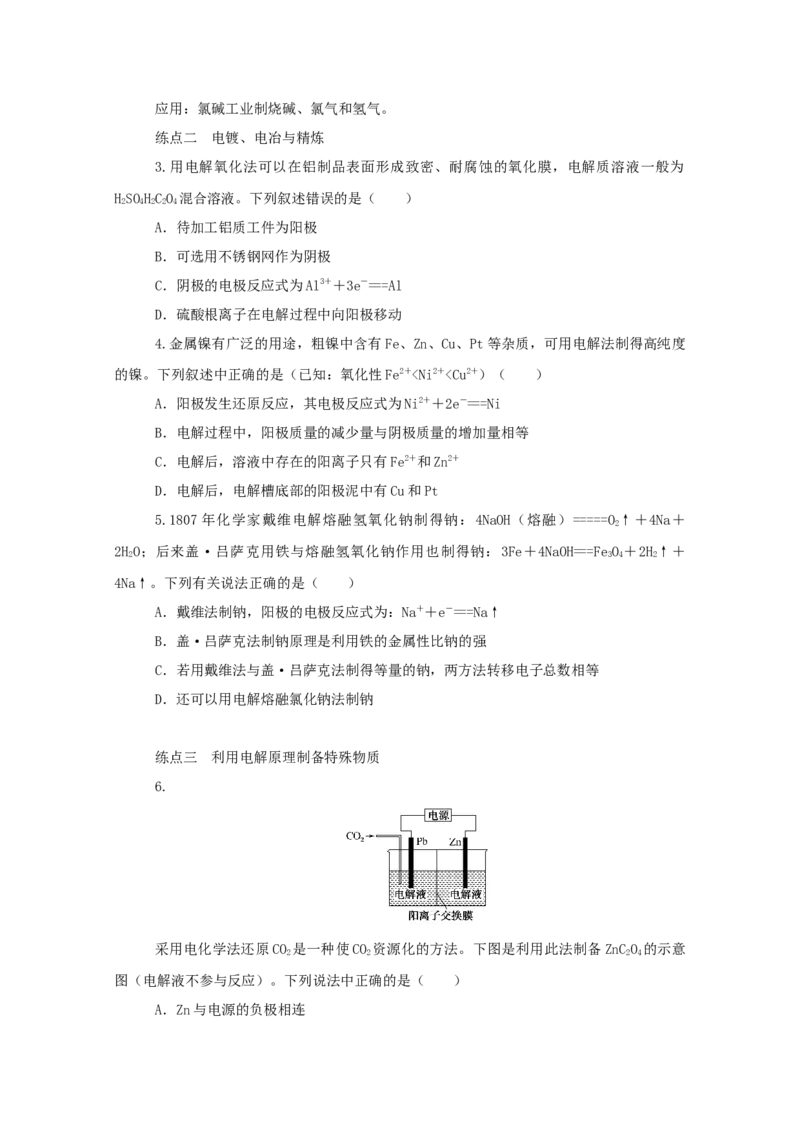
2.用电解法可提纯含有某种含氧酸根杂质的粗KOH溶液,其工作原理如图所示。下列
有关说法错误的是( )
A.阳极反应式为4OH--4e-===2HO+O↑
2 2
B.通电后阴极区溶液pH会增大
C.K+通过交换膜从阴极区移向阳极区
D.纯净的KOH溶液从b口导出
练后归纳
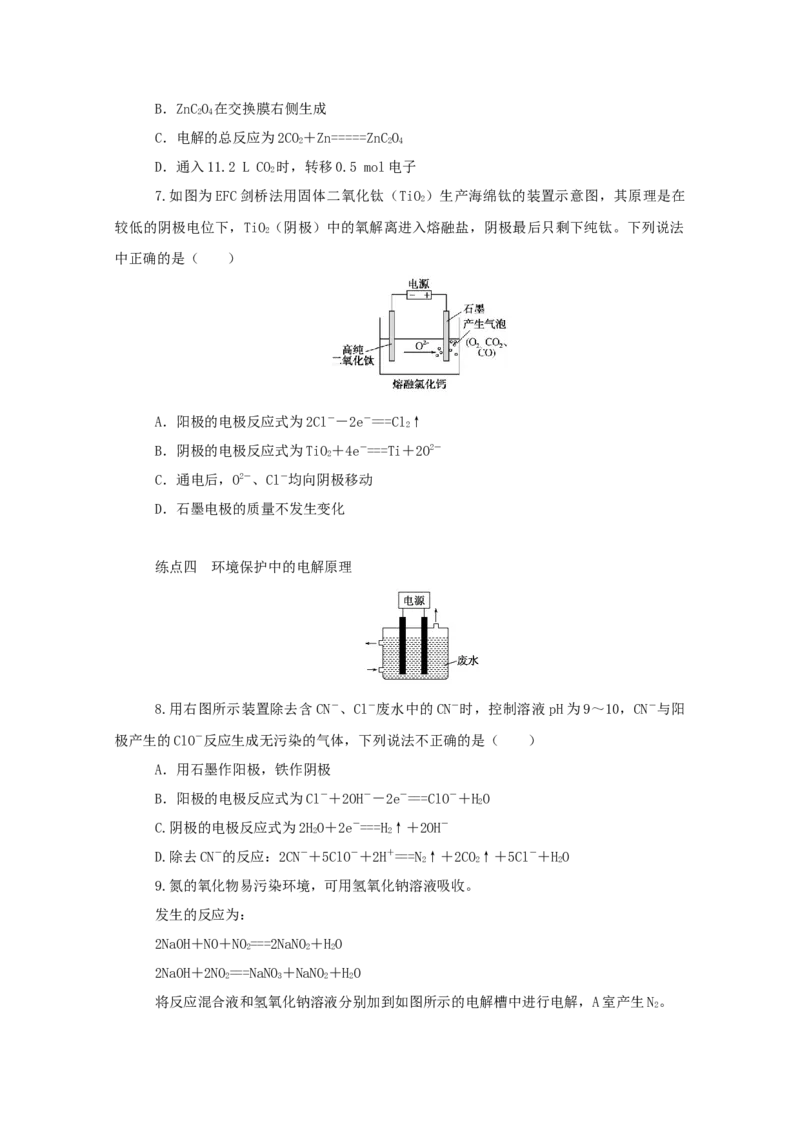
(1)氯碱工业的生产流程图:
(2)阳离子交换膜的作用:
阳离子交换膜只允许阳离子(Na+)通过,而阻止阴离子(Cl-、OH-)和分子(Cl)
2
通过,这样既能阻止H 和Cl 混合爆炸,又能避免Cl 和NaOH溶液作用生成的NaClO影响烧
2 2 2
碱质量。应用:氯碱工业制烧碱、氯气和氢气。
练点二 电镀、电冶与精炼
3.用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般为
HSOHCO 混合溶液。下列叙述错误的是( )
2 4 2 2 4
A.待加工铝质工件为阳极
B.可选用不锈钢网作为阴极
C.阴极的电极反应式为Al3++3e-===Al
D.硫酸根离子在电解过程中向阳极移动
4.金属镍有广泛的用途,粗镍中含有Fe、Zn、Cu、Pt等杂质,可用电解法制得高纯度
的镍。下列叙述中正确的是(已知:氧化性Fe2+原电池原理引起
的腐蚀>化学腐蚀>有防护措施的腐蚀。
(2)对同一金属来说,腐蚀的快慢:强电解质溶液中>弱电解质溶液中>非电解质溶液
中(浓度相同)。
(3)活泼性不同的两种金属,活泼性差异越大,腐蚀越快。
(4)对同一种电解质溶液来说,电解质浓度越大,金属腐蚀速率越快。
练点二 金属的腐蚀与防护措施
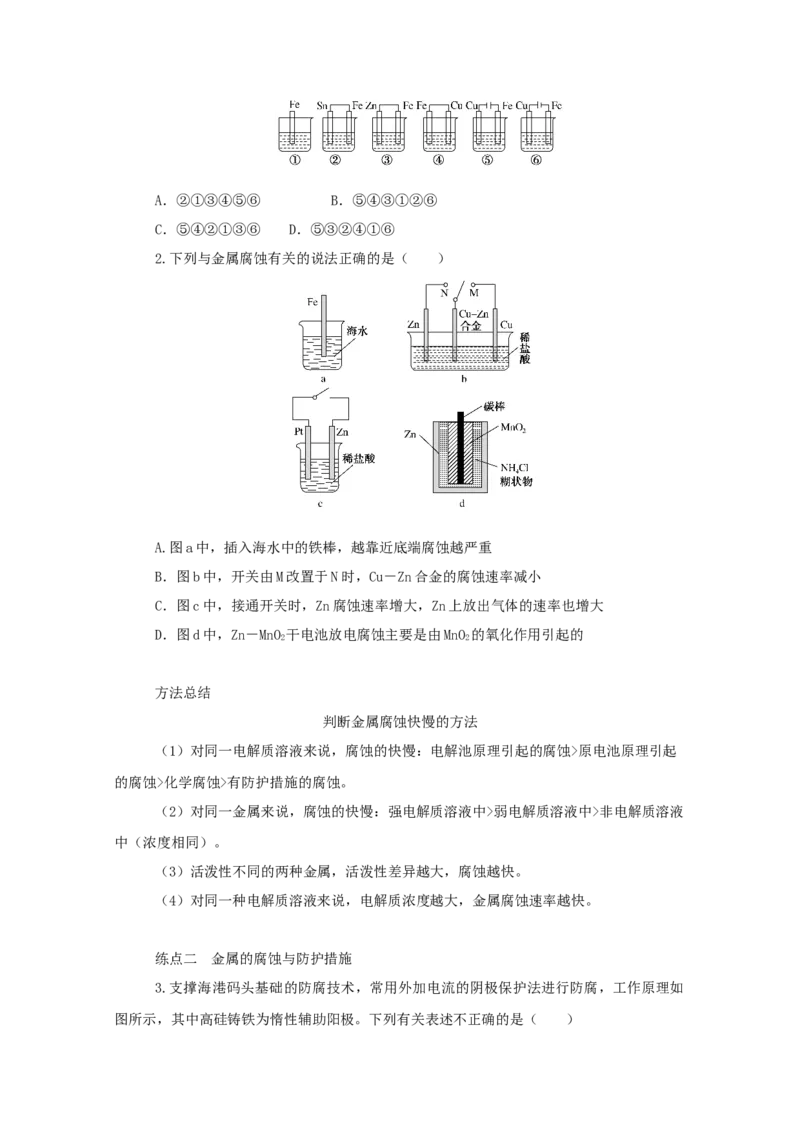
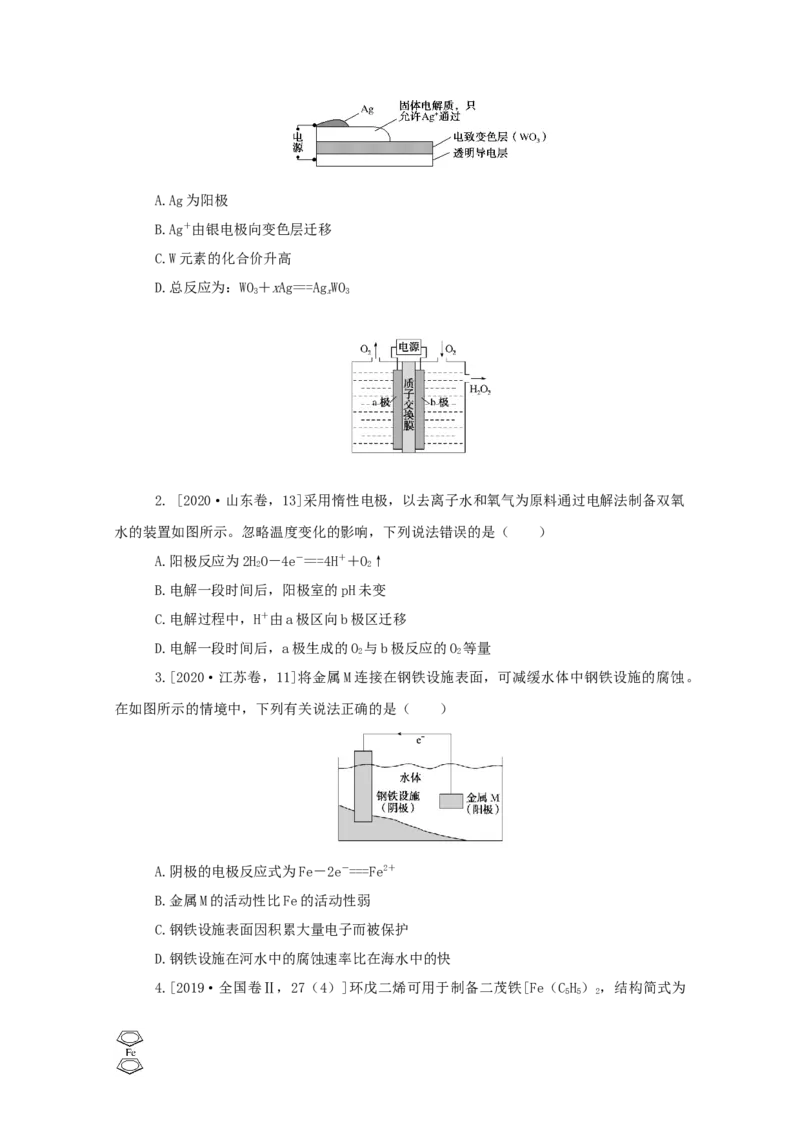
3.支撑海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如
图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
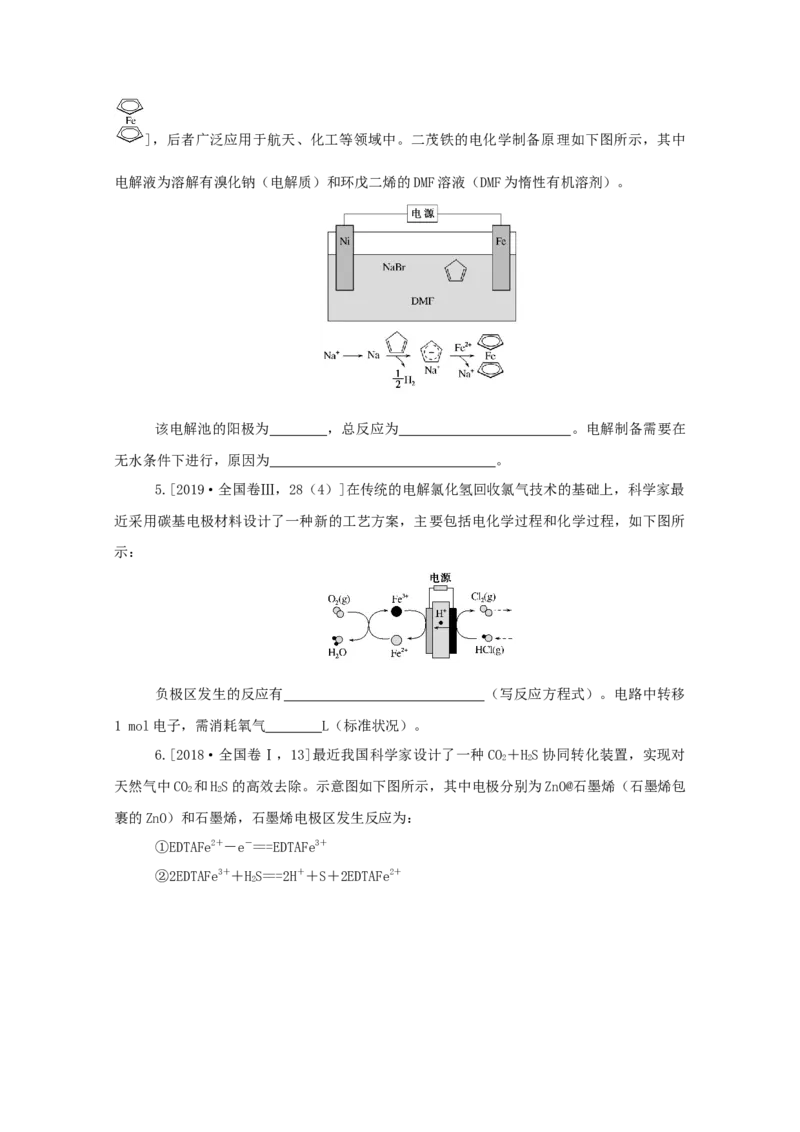
4.我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象,在铁帽上加锌环能有效防
止铁帽的腐蚀,防护原理如图所示。下列说法错误的是( )
A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应为2HO+2e-===H↑+2OH-
2 2
C.断电时,锌环上的电极反应为Zn2++2e-===Zn
D.断电时,仍能防止铁帽被腐蚀
练后归纳
影响金属腐蚀的因素包括金属本身的性质和外界环境两个方面:
(1)就金属本身的性质来说,金属越活泼,就越容易失去电子而被腐蚀。
(2)外界环境对金属腐蚀的影响也很大,如果金属在潮湿的空气中,接触腐蚀性气体
或电解质溶液,都容易被腐蚀。
由于在通常情况下,金属表面不会遇到酸性较强的溶液,所以吸氧腐蚀是金属腐蚀的
主要形式,而且析氢腐蚀最终也会被吸氧腐蚀所代替。
本讲真题研练
1.[2020·全国卷Ⅱ,12]电致变色器件可智能调控太阳光透过率,从而实现节能。下
图是某电致变色器件的示意图。当通电时,Ag+注入到无色WO 薄膜中,生成AgWO ,器件呈
3 x 3
现蓝色,对于该变化过程,下列叙述错误的是( )A.Ag为阳极
B.Ag+由银电极向变色层迁移
C.W元素的化合价升高
D.总反应为:WO+xAg===AgWO
3 x 3
2. [2020·山东卷,13]采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧
水的装置如图所示。忽略温度变化的影响,下列说法错误的是( )
A.阳极反应为2HO-4e-===4H++O↑
2 2
B.电解一段时间后,阳极室的pH未变
C.电解过程中,H+由a极区向b极区迁移
D.电解一段时间后,a极生成的O 与b极反应的O 等量
2 2
3.[2020·江苏卷,11]将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。
在如图所示的情境中,下列有关说法正确的是( )
A.阴极的电极反应式为Fe-2e-===Fe2+
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
4.[2019·全国卷Ⅱ,27(4)]环戊二烯可用于制备二茂铁[Fe(CH ) ,结构简式为
5 5 2],后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如下图所示,其中
电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。
该电解池的阳极为 ,总反应为 。电解制备需要在
无水条件下进行,原因为 。
5.[2019·全国卷Ⅲ,28(4)]在传统的电解氯化氢回收氯气技术的基础上,科学家最
近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所
示:
负极区发生的反应有 (写反应方程式)。电路中转移
1 mol电子,需消耗氧气 L(标准状况)。
6.[2018·全国卷Ⅰ,13]最近我国科学家设计了一种CO +HS协同转化装置,实现对
2 2
天然气中CO 和HS的高效去除。示意图如下图所示,其中电极分别为ZnO@石墨烯(石墨烯包
2 2
裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTAFe2+-e-===EDTAFe3+
②2EDTAFe3++HS===2H++S+2EDTAFe2+
2该装置工作时,下列叙述错误的是( )
A.阴极的电极反应:CO+2H++2e-===CO+HO
2 2
B.协同转化总反应:CO+HS===CO+HO+S
2 2 2
C.石墨烯上的电势比ZnO@石墨烯上的低
D.若采用Fe3+/Fe2+取代EDTAFe3+/EDTAFe2+,溶液需为酸性
7.[2018·北京卷,12]验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化
的3%NaCl溶液)。
① ② ③
在Fe表面生
试管内无明显变化 试管内生成蓝色沉淀
成蓝色沉淀
下列说法不正确的是( )
A.对比②③,可以判定Zn保护了Fe
B.对比①②, K[Fe(CN)]可能将Fe氧化
3 6
C.验证Zn保护Fe时不能用①的方法
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼第3讲 电解池 金属的腐蚀与防护
考点一
1知识梳理
1.氧化还原反应 电 化学
2.(1)直流电源 电解质溶液 熔融盐 闭合回路 (2)阳极 氧化 2Cl--2e-
===Cl↑ 阴极 还原 Cu2++2e-===Cu
2
3.(1)S2->I->Br->Cl- (2)Ag+>Fe3+>Cu2+
思考 答案:(1)1 mol·L-1 CuCl
2
CuCl=====Cu+Cl↑
2 2
(2)1 mol·L-1 NaCl 2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
(3)1 mol·L-1 NaOH 2HO=====O↑+2H↑
2 2 2
判断 答案:(1)√ (2)√ (3)× (4)× (5)× (6)×
2对点速练
1.答案:(1)4OH--4e-===O↑+2HO(或2HO-4e-===O↑+4H+)
2 2 2 2
4Ag++4e-===4Ag
4Ag++2HO=====4Ag+O↑+4H+
2 2
(2)2Cl--2e-===Cl↑
2
2H++2e-===H↑(或2HO+2e-===H↑+2OH-)
2 2 2
Mg2++2Cl-+2HO=====Mg(OH)↓+Cl↑+H↑
2 2 2 2
(3)Fe-2e-===Fe2+
2H++2e-===H↑(或2HO+2e-===H↑+2OH-)
2 2 2
Fe+2HO=====Fe(OH)↓+H↑
2 2 2
(4)2Al-6e-+8OH-===2AlO−
+4HO
2 2
6HO+6e-===3H↑+6OH-(或6H++6e-===3H↑)
2 2 2
2Al+2HO+2OH-=====2AlO−
+3H↑
2 2 2
(5)2Al-6e-+3HO===AlO+6H+
2 2 3
6H++6e-===3H↑
2
2Al+3HO=====AlO+3H↑
2 2 3 2
2.解析:A项,以石墨为电极电解水,阳极:4OH--4e-===2HO+O↑,以石墨为电
2 2极电解饱和食盐水,阳极:2Cl--2e-===Cl↑,二者阳极电极反应式不同,故A错误;B项,
2
电解水溶液的pH不变,电解饱和氯化钠溶液生成氢氧化钠、氯气和氢气,pH变大,所以电
解结束后所得液体的pH不相同,故B错误;C项,以石墨为电极分别电解水和饱和食盐水阴
极上都是2H++2e-===H↑,所以阴极电极反应式相同,故C正确;D项,设转移电子数为4
2
mol,则依据电解方程式:2HO=====2H↑+O↑~4e-,电解水生成3 mol气体,依据电解方
2 2 2
程式2NaCl+2HO=====2NaOH+Cl↑+H↑~2e-,电解饱和食盐水生成4 mol气体,故D错
2 2 2
误。
答案:C
3.解析:钛电极为阴极,发生还原反应,A项错误;铜作阳极,阳极上铜发生失电子
的氧化反应,电极反应式为2Cu+2OH--2e-===CuO+HO,OH-由阴极区迁移到阳极区参与反
2 2
应,离子交换膜应为阴离子交换膜,C项错误,D项正确;由阴极区迁移过来的OH-在阳极全
部参与反应,消耗OH-,pH值减小,B项错误。
答案:D
4.解析:阳极上Fe发生氧化反应,溶液由无色变为浅绿色,A项错误;阴极上H+发
生还原反应:2H++2e-===H↑,B项错误;根据阴极上电极反应,阴极消耗H+,电解一段时
2
间后,阴极室溶液pH升高,C项正确;电解一段时间后,阴极室溶液中溶质除(NH)PO 外,
4 3 4
还可能有NHHPO、(NH)HPO 等,D项错误。
4 2 4 4 2 4
答案:C
5.解析:A.此装置为电解池,总反应是N +3H===2NH ,Pd电极b上是氢气发生反应,
2 2 3
即氢气失去电子化合价升高,Pd电极b为阳极,故A说法错误;B.根据A选项分析,Pd电极
a为阴极,反应式为N +6H++6e-===2NH ,故B说法正确;C.根据电解池的原理,阳离子在
2 3
阴极上放电,即由阳极移向阴极,故C说法正确;D.根据装置图,陶瓷隔离N 和H ,故D说
2 2
法正确。
答案:A
6.解析:(1)①电解时,阴极区溶液中的阳离子放电,即水溶液中的H+放电生成H 。
2
②由题给反应可知,阳极区生成了S2− ,S2− 可以理解为(n-1)S+S2-,加入稀硫酸生成S单
n n
质和HS气体。
2
(2)根据电解NO制备NHNO 的工作原理示意图知:阴极反应式为 3NO+15e-+18H+
4 3===3NH+ +3HO,阳极反应式为 5NO-15e-+10HO===5NO− +20H+,总反应式为 8NO+
4 2 2 3
7HO=====3NHNO+2HNO,为了使电解产生的HNO 全部转化为NHNO,应补充NH。
2 4 3 3 3 4 3 3
答案:(1)①2HO+2e-===H↑+2OH-
2 2
②S2− +2H+===(n-1)S↓+HS↑
n 2
(2)NH 根据总反应:8NO+7HO=====3NHNO+2HNO,电解产生的HNO 多,应补充NH
3 2 4 3 3 3 3
考点二
1知识梳理
1.(1)2Cl--2e-===Cl↑ 氧化 2H++2e-===H↑ 还原
2 2
2.(1)粗铜 纯铜 (3)Zn-2e-===Zn2+ Fe-2e-===Fe2+ Ni-2e-===Ni2+ Cu-2e
-===Cu2+ Cu2++2e-===Cu
3.(1)阴 阳 (2)AgNO 溶液等含镀层金属阳离子的盐溶液
3
(3)Ag-e-===Ag+ Ag++e-===Ag (4)阳 阴 不变
4.(1)2Cl--2e-===Cl↑ 2Na++2e-===2Na (2)6O2--12e-===3O↑ 4Al3++12e-
2 2
===4Al
判断 答案:(1)× (2)× (3)√ (4)× (5)× (6)√
2对点速练
1.答案:B
2.解析:阳极区为粗KOH溶液,阳极上OH-失电子发生氧化反应:4OH--4e-===2HO
2
+O↑,A项正确;阴极上HO得电子发生还原反应:2HO+2e-===H↑+2OH-,阴极区附近
2 2 2 2
溶液中c(OH-)增大,pH增大,B项正确;电解时阳离子向阴极移动,故K+通过阳离子交换膜
从阳极区移向阴极区,C项错误;阴极区生成KOH,故纯净的KOH溶液从b口导出,D项正确。
答案:C
3.解析:A对:铝制品表面氧化形成致密的氧化膜,所以待加工铝质工件应为阳极,
阳极电极反应为2Al-6e-+3HO===AlO +6H+。B对,C错:阴极发生的电极反应为2H++2e
2 2 3
-===H↑,阴极可选用不锈钢网作电极。D对:电解质溶液中的阴离子向阳极移动。
2
答案:C
4.解析:电解时,阳极Zn、Fe、Ni失去电子,发生氧化反应,A项错误;因氧化性
Ni2+>Fe2+>Zn2+,故阴极反应式为Ni2++2e-===Ni,可见,阳极质量减少是因为Zn、Fe、Ni溶解,而阴极质量增加是因为Ni析出,B项错误;电解后溶液中的阳离子除Fe2+和Zn2+外,
还有Ni2+和H+,C项错误。
答案:D
5.解析:A项,阳极应发生氧化反应;B项,盖·吕萨克法制钠原理是根据钠的沸点
较低、易从反应混合物中分离出来,从而使化学平衡向正向移动;C项,根据反应方程式可
知用戴维法制取金属钠,每反应产生4 mol Na转移电子的物质的量是4 mol,而用盖·吕萨
克法制得4 mol的钠转移电子的物质的量是8 mol,因此制取等量的金属钠,转移电子的物
质的量不相等;D项,由于NaCl是离子化合物,可用电解熔融氯化钠的方法制金属钠。
答案:D
6.解析:电解过程中Zn被氧化,作阳极,所以Zn与电源的正极相连,A错误;Zn2+
透过阳离子交换膜到达左侧与生成的CO2−
形成ZnCO ,B错误;没有给出气体所处的温度和
2 4 2 4
压强,D错误。
答案:C
7.解析:电解质中的阴离子 O2-、Cl-向阳极移动,由图示可知阳极生成 O 、CO、
2
CO ,所以电极反应为2O2--4e-===O↑,O 与石墨反应生成CO、CO ,A、C、D项错误,只有
2 2 2 2
B项正确。
答案:B
8.解析:阳极产生ClO-,发生的反应为Cl-+2OH--2e-===ClO-+HO,所以阳极一
2
定是石墨电极而不是铁电极,A、B两项正确;阴极是HO得电子产生H ,C项正确;溶液的
2 2
pH为9~10,显碱性,因而除去CN-的反应为2CN-+5ClO-+2OH-===N↑+2CO2− +5Cl-+
2 3
HO,D项错误。
2
答案:D
9.解析:由A室产生N ,可知A室的电解质溶液为NaNO 和NaNO
的混合溶液,NO−
在
2 3 2 2
电极Ⅰ上放电生成N ,则电极Ⅰ为阴极,电极Ⅱ为阳极,B室的电解质溶液为NaOH溶液,OH
2
-在电极Ⅱ上放电生成O。
2
答案:①阳 O ②2NO− +6e-+4HO===8OH-+N↑
2 2 2 2考点三
1知识梳理
1.失去电子 金属阳离子 氧化
2.(1)非金属单质直接 电解质溶液 无 有微弱 氧化 氧化 电化学 (2)水膜酸
性较强(pH≤4.3) 水膜酸性很弱或呈中性 Fe-2e-===Fe2+ 2H++2e-===H↑ O +2HO+
2 2 2
4e-===4OH- Fe+2H+===Fe2++H↑ 2Fe+O+2HO===2Fe(OH) 吸氧腐蚀
2 2 2 2
3.(1)负 正 阴 阳
思考 答案:铁锅中含有的Fe、C和电解质溶液构成原电池,活泼金属作负极,Fe为
负极,C作正极。具体电极反应如下:
负极:2Fe-4e-===2Fe2+
正极:O+4e-+2HO===4OH-
2 2
2Fe+O+2HO===2Fe(OH)
2 2 2
4Fe(OH)+O+2HO===4Fe(OH)
2 2 2 3
2Fe(OH)===FeO·xHO(铁锈)+(3-x)HO
3 2 3 2 2
判断 答案:(1)× (2)√ (3)× (4)× (5)× (6)√ (7)√
2对点速练
1.解析:①是Fe为负极,杂质为正极的原电池腐蚀,是钢铁的吸氧腐蚀,腐蚀较慢。
②、③、④实质均为原电池装置。③中Fe为正极,被保护;②、④中Fe为负极,均被腐蚀,
但Fe和Cu的金属活泼性差别比Fe和Sn的大,故Fe-Cu原电池中Fe被腐蚀较快;⑤是Fe
接电源正极作阳极,Cu接电源负极作阴极的电解腐蚀,加快了Fe的腐蚀;⑥Fe接电源负极
作阴极,Cu接电源正极作阳极,防止了Fe的腐蚀。根据以上分析可知:铁在其中被腐蚀由
快到慢的顺序为⑤>④>②>①>③>⑥。
答案:C
2.解析:图a中,海水的液面与空气的交界处腐蚀最严重,A项错误;图b中,开关
由M改置于N时,形成原电池,Zn为负极,Cu-Zn合金为正极,腐蚀速率减小,B项正确;
图c中,接通开关时,形成原电池,Zn为原电池的负极,Zn腐蚀速率增大,Pt电极上放出
气体的速率也增大,C项错误;Zn-MnO 干电池中Zn作负极,干电池放电腐蚀主要是由Zn的
2
还原作用引起的,D项错误。
答案:B
3.解析:钢管桩接电源的负极,高硅铸铁接电源的正极,通电后,外电路中的电子从高硅铸铁(阳极)流向正极,从负极流向钢管桩(阴极),A、B正确;C项,题给信息高硅铸铁
为“惰性辅助阳极”不损耗,错误。
答案:C
4.解析:锌环与电源的正极相连,为阳极,A项正确;断电时,Zn比铁活泼,做负极,
电极反应为Zn-2e-===Zn2+,C项错误。
答案:C
本讲真题研练
1.解析:本题重点考查电解原理及其应用。根据题给装置图可知,该装置有外接电源,
为电解池,且Ag电极作阳极,故A项正确;通电时,阳极反应式为Ag-e-===Ag+,生成的
Ag+通过固体电解质进入电致变色层,与WO 结合得到AgWO ,W的化合价降低,阴极反应式
3 x 3
为WO+xe-===WOx−
,总反应为xAg+WO===AgWO,故B、D项正确,C项错误。
3 3 3 x 3
答案:C
2.解析:结合题图,可知a极上产生O ,发生的反应为水被氧化生成O 的反应,即a
2 2
极为阳极,b极为阴极,电极反应式如表:
电极名称 电极反应式
a极(阳极) 2HO-4e-===4H++O↑
2 2
b极(阴极) 2H++O+2e-===HO
2 2 2
结合上述分析可知,A项正确;电解一段时间后,溶液中H+浓度未变,即阳极室的pH
未变,B项正确;电解过程中H+通过质子交换膜,从a极区向b极区迁移,C项正确;由阴、
阳极的电极反应式,可知电解一段时间后,b极消耗O 的量是a极生成O 的量的2倍,即a
2 2
极生成的O 与b极反应的O 的量不相等,D项错误。
2 2
答案:D
3.解析:本题考查金属的腐蚀与防护,考查的化学学科核心素养是科学态度与社会责
任。该装置中阴极发生还原反应,A项错误;金属M被氧化,即金属活动性:M>Fe,B项错误;钢铁设施为原电池的正极,表面积累大量电子而被保护,C项正确;海水中含有大量的NaCl
等电解质,而河水中电解质较少,故钢铁设施在河水中的腐蚀速率比在海水中的慢,D项错
误。
答案:C
4.解析:根据反应历程可知,铁电极溶解生成了 Fe2+,故应让Fe电极作电解池的阳
极;由反应历程可知,反应物为Fe与环戊二烯,生成物为二茂铁和H,再根据原子守恒写出
2
总反应式;根据反应历程中有Na生成,水会与Na反应,从而中止反应,且电解过程中水会
在阴极生成OH-,进一步与Fe2+反应生成Fe(OH)。
2
答案:Fe电极
Fe+2 === +H↑[Fe+2CH===Fe(CH)+H↑]
2 5 6 5 5 2 2
水会阻碍中间物Na的生成;水会电解生成OH-,进一步与Fe2+反应生成Fe(OH)
2
5.解析:负极区发生的是得电子的还原反应,故负极区的反应有Fe3++e-===Fe2+、
4Fe2++O+4H+===4Fe3++2HO;根据得失电子守恒得出关系式:
2 2
1
Fe3+~e-~Fe2+~ O
4 2
1 mol 0.25 mol
n(O)=0.25 mol,标准状况下体积为5.6 L。
2
答案:Fe3++e-===Fe2+,4Fe2++O+4H+===4Fe3++2HO 5.6
2 2
6.解析:阴极发生还原反应,氢离子由交换膜右侧向左侧迁移,阴极的电极反应式为
CO+2e-+2H+===CO+HO,A项正确;结合阳极区发生的反应,可知协同转化总反应为 CO+
2 2 2
HS===S+CO+HO,B项正确;石墨烯作阳极,其电势高于ZnO@石墨烯的,C项错误;Fe3+、
2 2
Fe2+在碱性或中性介质中会生成沉淀,它们只稳定存在于酸性较强的介质中,D项正确。
答案:C
7.解析:②中Zn作负极,发生氧化反应生成Zn2+,Fe作正极被保护,所以取出的少
量Fe附近的溶液中滴入铁氰化钾溶液,试管内无明显变化。但③中没有 Zn保护Fe,Fe在酸
性环境中发生析氢腐蚀,Fe作负极被氧化生成Fe2+,所以取出的少量Fe附近的溶液中滴入
铁氰化钾溶液,生成蓝色沉淀,对比②③可知Zn保护了Fe,A项正确;①与②的区别在于:
前者是将铁氰化钾溶液直接滴入烧杯中,而后者是在取出的少量Fe附近的溶液中滴加铁氰化
钾溶液,①中出现了蓝色沉淀,说明有Fe2+生成。对比分析可知,可能是铁氰化钾氧化Fe生
成了Fe2+,B项正确;通过上述分析可知,验证Zn保护Fe时不能用①的方法,C项正确;若将Zn换成Cu,铁氰化钾仍会将Fe氧化为Fe2+,在铁的表面同样会生成蓝色沉淀,所以无法
判断Fe2+是不是负极产物,即无法判断Fe与Cu的活泼性,D项错误。
答案:D