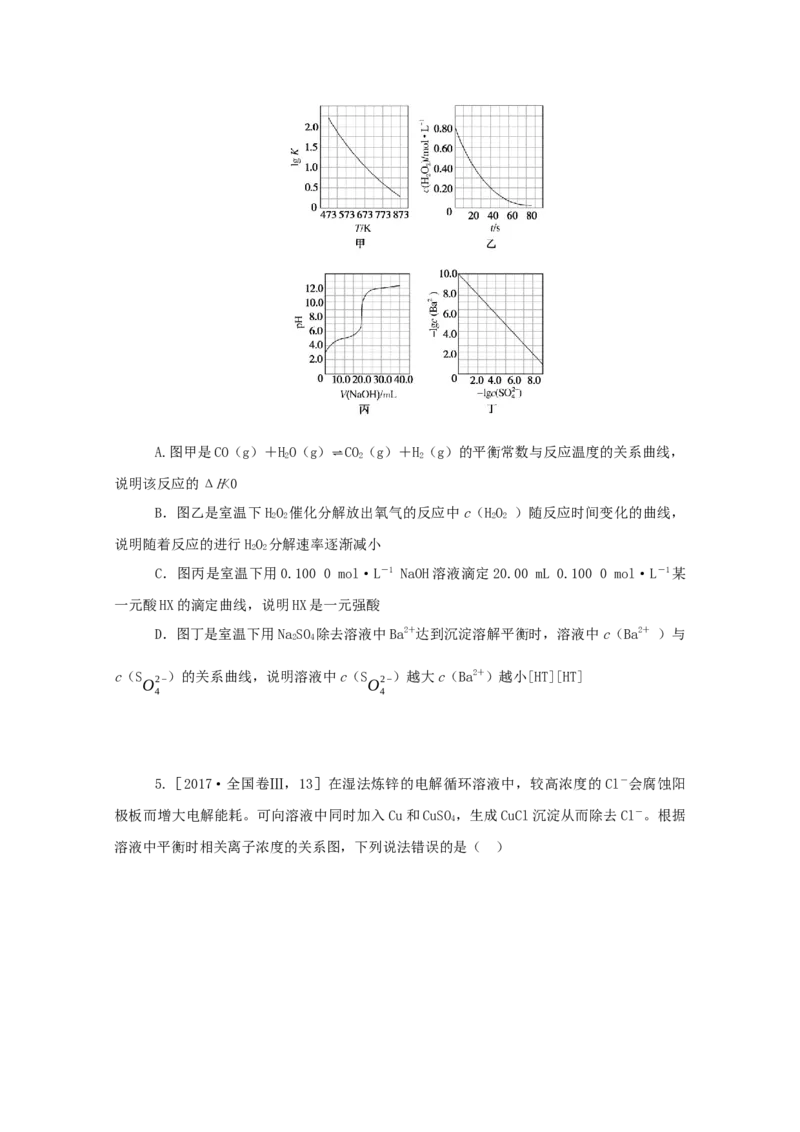
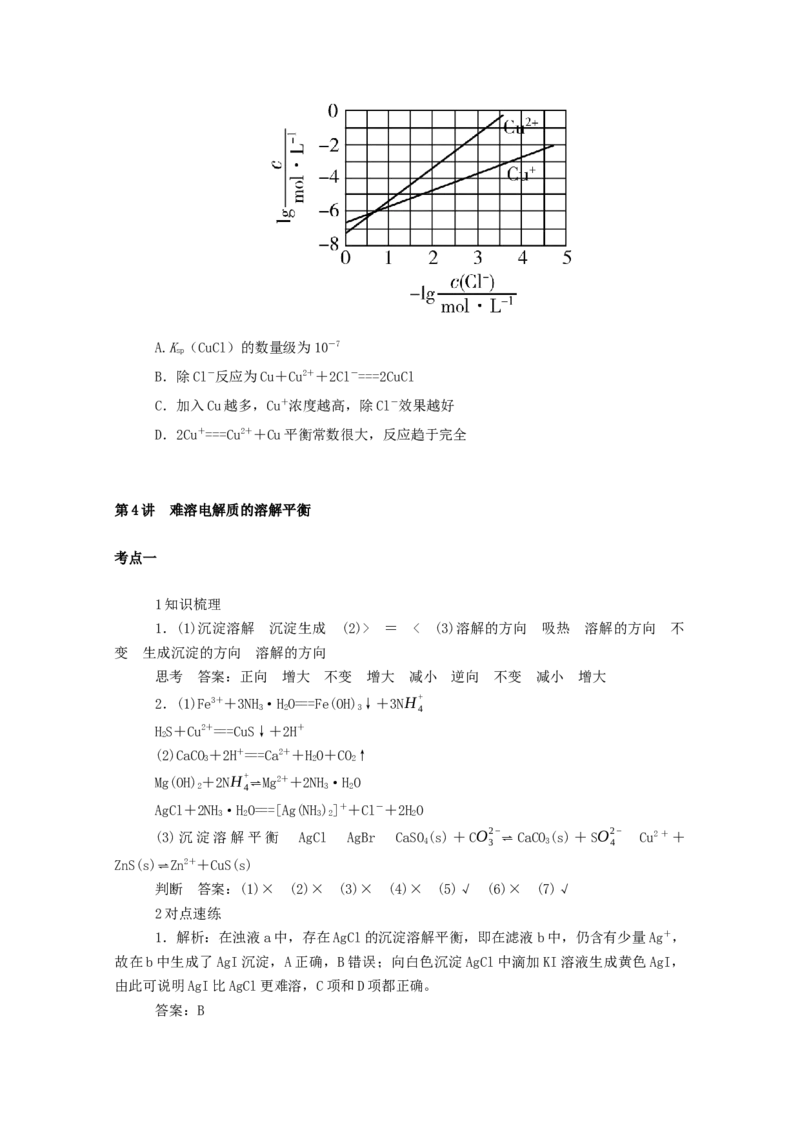
文档内容
第4讲 难溶电解质的溶解平衡
[考纲要求]
1.了解难溶电解质的沉淀溶解平衡。
2.理解溶度积的含义,能进行相关的计算。
3.了解沉淀溶解平衡的应用。
考点一 沉淀溶解平衡及应用
1知识梳理
1.沉淀的溶解平衡
(1)沉淀溶解平衡的概念
在一定温度下,当难溶强电解质溶于水形成饱和溶液时, 和 速率相
等的状态。
(2)沉淀溶解平衡的建立
(3)沉淀溶解平衡的影响因素[思考]
以AgCl为例:AgCl(s) Ag+(aq)+Cl-(aq)
⇌
平衡后 平衡后
外界条件 移动方向 K
sp
c(Ag+) c(Cl-)
升高温度 增大 增大
加水稀释 正向 不变 不变
加入少量
逆向 不变
AgNO
3
通入HCl 减小 增大
通入HS 正向 不变
2
[提醒]
难溶、可溶、易溶界定
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
2.沉淀溶解平衡的应用
(1)沉淀的生成
①调节pH法
如除去 NHCl 溶液中的 FeCl 杂质,可加入氨水调节 pH 至 3~4,离子方程式为
4 3
________________________________________________________________________
。
②沉淀剂法。
如用HS沉淀Cu2+,离子方程式为 。
2
(2)沉淀的溶解
①酸溶解法如CaCO 溶于盐酸,离子方程式为 。
3
②盐溶液溶解法
如Mg(OH) 溶于NHCl溶液,离子方程式为 。
2 4
③氧化还原溶解法
如不溶于盐酸的硫化物AgS溶于稀HNO。
2 3
④配位溶解法
如AgCl溶于氨水,离子方程式为 。
(3)沉淀的转化
在难溶物质的饱和溶液中,溶解度小的沉淀会转化成溶解度更小的沉淀。
①实质: 的移动。
②举例:AgNO 溶液――→ ――→ 则K[AgCl]>K[AgBr]。
3 sp sp
③应用:
a.锅炉除垢:将CaSO 转化为CaCO,离子方程式为 。
4 3
b.矿物转化:CuSO 溶液遇ZnS转化为CuS,离子方程式为 。
4
[判断] (正确的打“√”,错误的打“×”)
(1)沉淀达到溶解平衡状态,溶液中各离子浓度一定相等( )
(2)升高温度,沉淀溶解平衡一定正向移动( )
(3)某物质的溶解性为难溶,则该物质不溶于水( )
(4)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度( )
(5)AgCl沉淀易转化为AgI沉淀且K(AgX)=c(Ag+)·c(X-),故K(AgI)K:溶液过饱和,有 析出
c sp
应用
②Q=K:溶液饱和,处于 状态
c sp
③QCaF
3 2
B.T ℃时,两饱和溶液等体积混合,会析出CaF 固体
2
C.T ℃时,CaCO 固体在稀盐酸中的K 比在纯水中的K 大
3 sp sp
D.T ℃时,向CaCO 悬浊液中加NaF固体,可能析出CaF 固体
3 2
3.已知K (AgCl) =1.56×10-10 ,K (AgBr)=7.7×10-13,K (AgCrO )=
sp sp sp 2 4
9.0×10-12。某溶液中含有Cl-、Br-和Cr ,浓度均为0.010 mol·L-1,向该溶液中逐滴
O2−
4
加入 0.010 mol·L -1 的 AgNO 溶液时, 三种阴 离子 产生沉淀的 先后顺序 为
3
。练点二 沉淀溶解平衡曲线分析
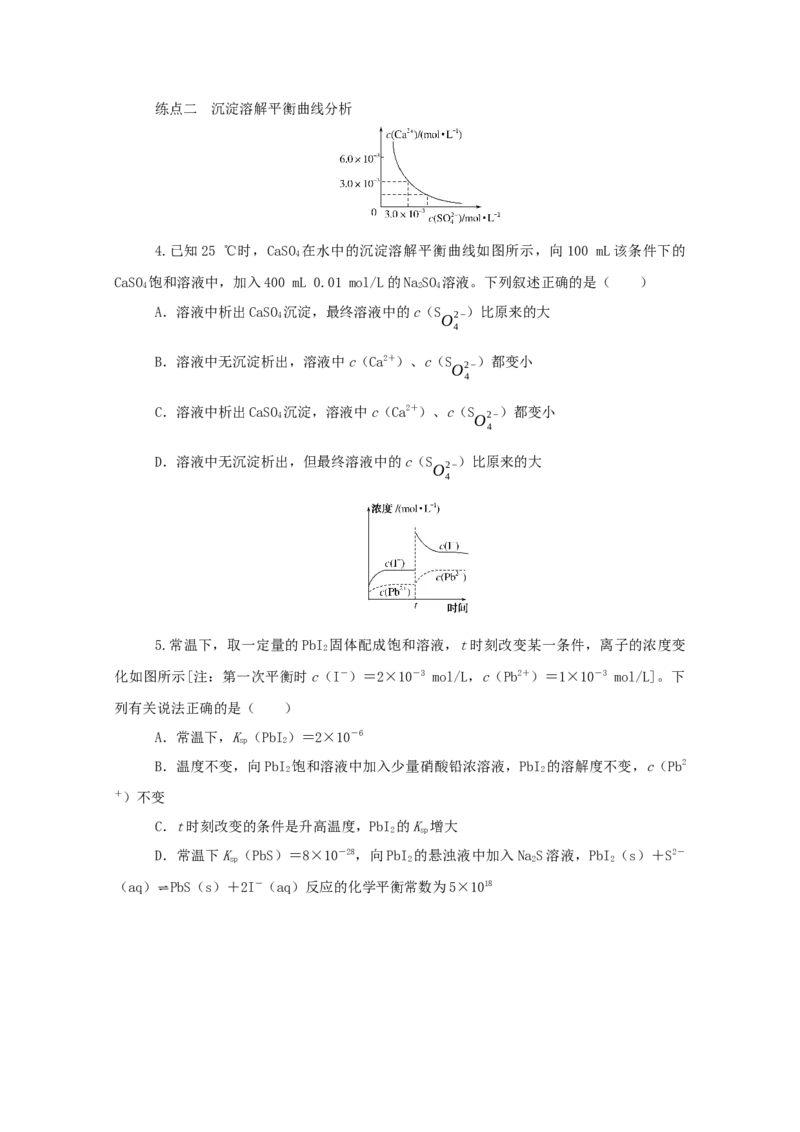
4.已知25 ℃时,CaSO 在水中的沉淀溶解平衡曲线如图所示,向100 mL该条件下的
4
CaSO 饱和溶液中,加入400 mL 0.01 mol/L的NaSO 溶液。下列叙述正确的是( )
4 2 4
A.溶液中析出CaSO 沉淀,最终溶液中的c(S )比原来的大
4 O2−
4
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(S )都变小
O2−
4
C.溶液中析出CaSO 沉淀,溶液中c(Ca2+)、c(S )都变小
4 O2−
4
D.溶液中无沉淀析出,但最终溶液中的c(S )比原来的大
O2−
4
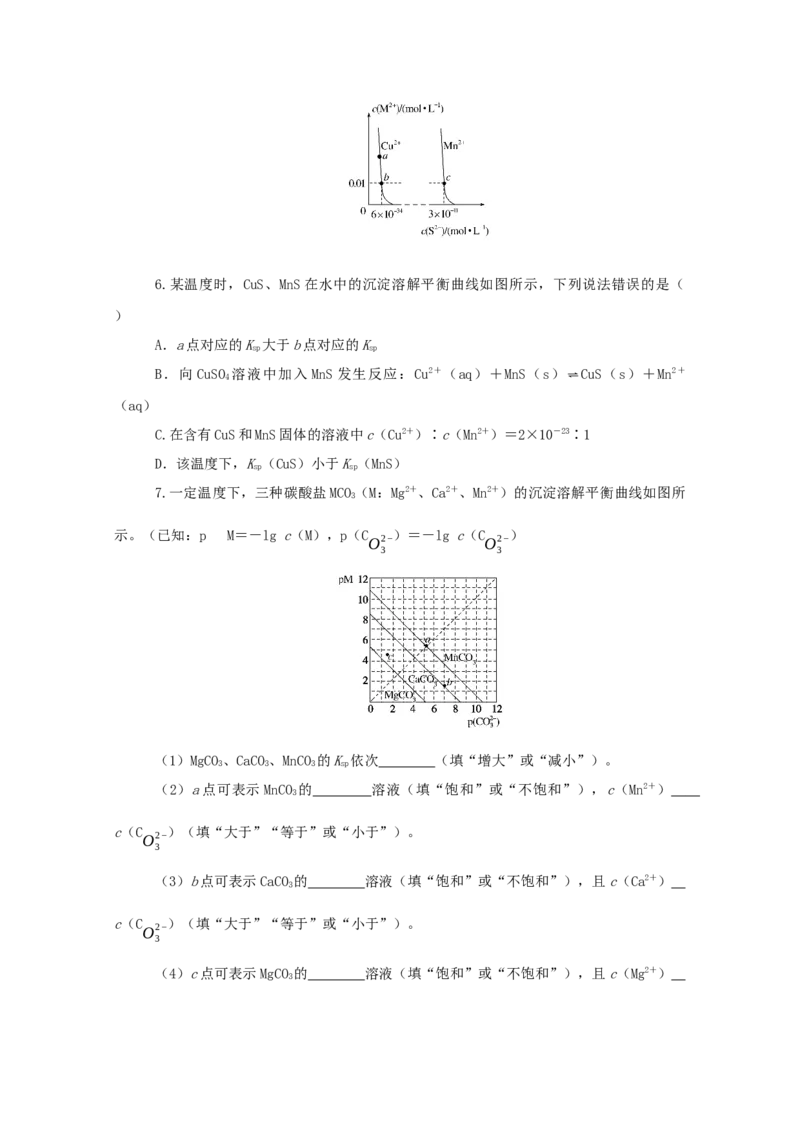
5.常温下,取一定量的PbI 固体配成饱和溶液,t时刻改变某一条件,离子的浓度变
2
化如图所示[注:第一次平衡时c(I-)=2×10-3 mol/L,c(Pb2+)=1×10-3 mol/L]。下
列有关说法正确的是( )
A.常温下,K(PbI)=2×10-6
sp 2
B.温度不变,向PbI 饱和溶液中加入少量硝酸铅浓溶液,PbI 的溶解度不变,c(Pb2
2 2
+)不变
C.t时刻改变的条件是升高温度,PbI 的K 增大
2 sp
D.常温下K (PbS)=8×10-28,向PbI 的悬浊液中加入NaS溶液,PbI (s)+S2-
sp 2 2 2
(aq) PbS(s)+2I-(aq)反应的化学平衡常数为5×1018
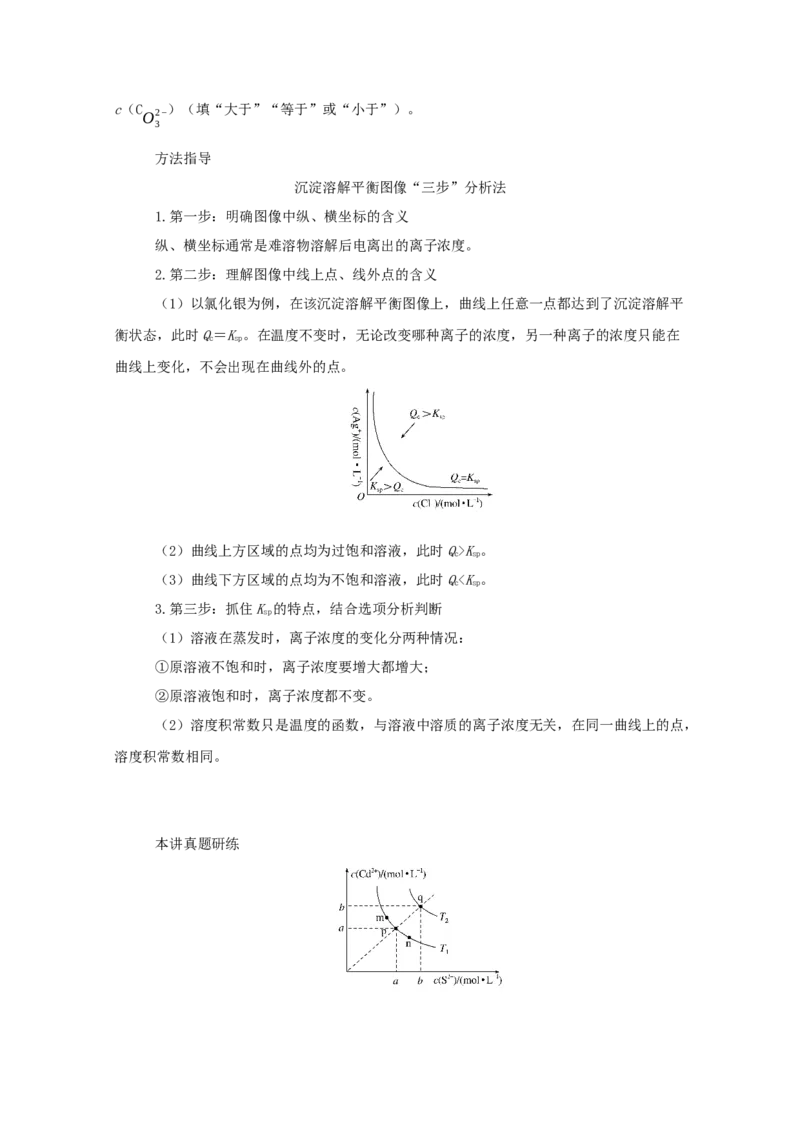
⇌6.某温度时,CuS、MnS在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是(
)
A.a点对应的K 大于b点对应的K
sp sp
B.向 CuSO 溶液中加入 MnS 发生反应:Cu2+(aq)+MnS(s) CuS(s)+Mn2+
4 ⇌
(aq)
C.在含有CuS和MnS固体的溶液中c(Cu2+)∶c(Mn2+)=2×10-23∶1
D.该温度下,K(CuS)小于K(MnS)
sp sp
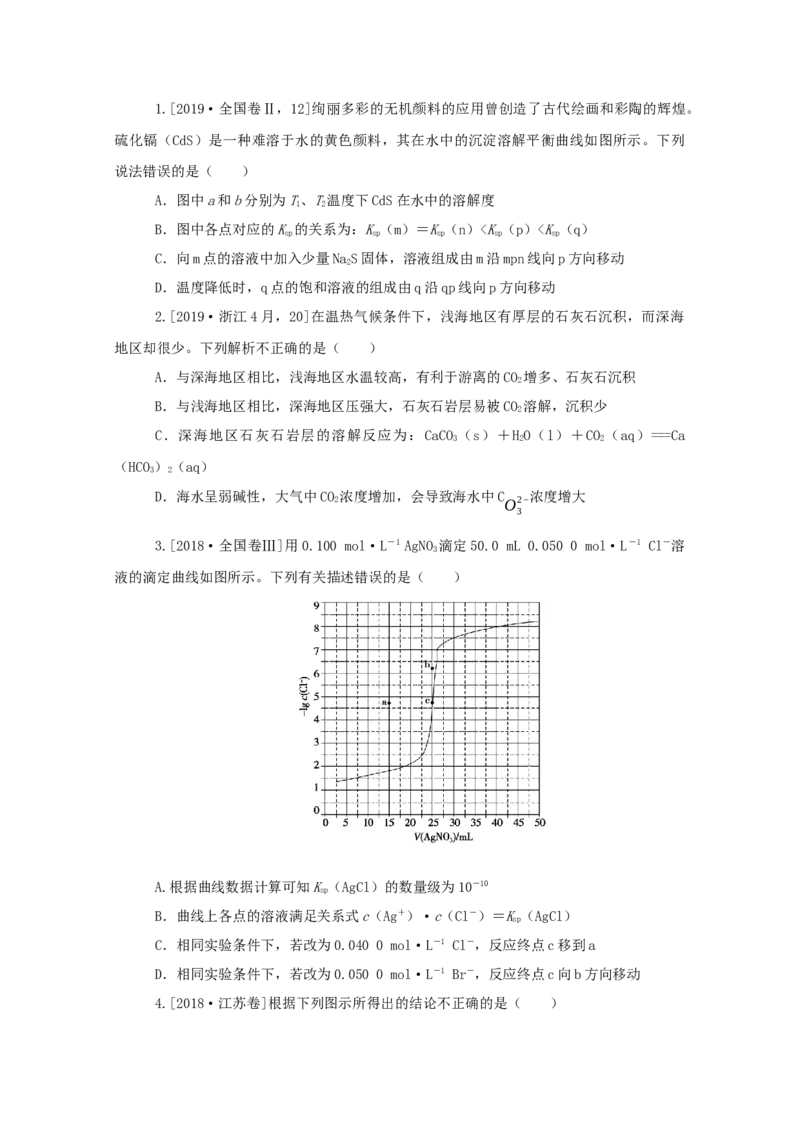
7.一定温度下,三种碳酸盐MCO (M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所
3
示。(已知:p M=-lg c(M),p(C )=-lg c(C )
O2− O2−
3 3
(1)MgCO、CaCO、MnCO 的K 依次 (填“增大”或“减小”)。
3 3 3 sp
(2)a点可表示MnCO 的 溶液(填“饱和”或“不饱和”),c(Mn2+)
3
c(C )(填“大于”“等于”或“小于”)。
O2−
3
(3)b点可表示CaCO 的 溶液(填“饱和”或“不饱和”),且c(Ca2+)
3
c(C )(填“大于”“等于”或“小于”)。
O2−
3
(4)c点可表示MgCO 的 溶液(填“饱和”或“不饱和”),且c(Mg2+)
3c(C )(填“大于”“等于”或“小于”)。
O2−
3
方法指导
沉淀溶解平衡图像“三步”分析法
1.第一步:明确图像中纵、横坐标的含义
纵、横坐标通常是难溶物溶解后电离出的离子浓度。
2.第二步:理解图像中线上点、线外点的含义
(1)以氯化银为例,在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解平
衡状态,此时Q=K。在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在
c sp
曲线上变化,不会出现在曲线外的点。
(2)曲线上方区域的点均为过饱和溶液,此时Q>K。
c sp
(3)曲线下方区域的点均为不饱和溶液,此时Q = < (3)溶解的方向 吸热 溶解的方向 不
变 生成沉淀的方向 溶解的方向
思考 答案:正向 增大 不变 增大 减小 逆向 不变 减小 增大
2.(1)Fe3++3NH·HO===Fe(OH)↓+3NH+
3 2 3 4
HS+Cu2+===CuS↓+2H+
2
(2)CaCO+2H+===Ca2++HO+CO↑
3 2 2
Mg(OH)+2NH+
Mg2++2NH·HO
2 4⇌ 3 2
AgCl+2NH·HO===[Ag(NH)]++Cl-+2HO
3 2 3 2 2
(3)沉淀溶解平衡 AgCl AgBr CaSO(s)+CO2− CaCO(s)+SO2− Cu2++
4 3 ⇌ 3 4
ZnS(s) Zn2++CuS(s)
⇌
判断 答案:(1)× (2)× (3)× (4)× (5)√ (6)× (7)√
2对点速练
1.解析:在浊液a中,存在AgCl的沉淀溶解平衡,即在滤液b中,仍含有少量Ag+,
故在b中生成了AgI沉淀,A正确,B错误;向白色沉淀AgCl中滴加KI溶液生成黄色AgI,
由此可说明AgI比AgCl更难溶,C项和D项都正确。
答案:B2.解析:酚酞显红色的溶液呈碱性,说明Mg(OH) 在水中有一定的溶解度,电离使溶
2
液呈碱性,A项正确;同浓度NHCl溶液酸性比盐酸弱,B项错误;NH+
结合Mg(OH) 溶液中
4 4 2
的OH-,促使Mg(OH) 沉淀溶解,C项正确;盐酸能够与Mg(OH) 发生中和反应,促使Mg(OH)
2 2 2
的溶解,D项正确。
答案:B
3.答案:①⑥
4.解析:①碳酸钠是强碱弱酸盐,因为水解使其溶液呈碱性,加热促进水解,碱能促
进油脂水解,所以热纯碱溶液洗涤油污的能力更强,应用了盐类水解原理,不符合题意;②
钡离子有毒,所以可溶性的钡盐有毒,钡离子和硫酸根离子反应生成不溶于酸和水的硫酸钡,
即易溶性的物质向难溶性的物质转化,所以可以用沉淀溶解平衡原理来解释;③石灰岩里不
溶性的碳酸钙在水和二氧化碳的作用下转化为微溶性的碳酸氢钙,长时间反应,形成溶洞,
可以用沉淀溶解平衡原理来解释;④碳酸钡能和盐酸反应生成氯化钡、二氧化碳和水,硫酸
钡和盐酸不反应,所以碳酸钡不能作“钡餐”而硫酸钡可以,可以用沉淀溶解平衡原理来解
释;⑤碳酸氢钠水解使其溶液呈碱性,硫酸铝水解使其溶液呈酸性,氢离子和氢氧根离子反
应生成水,则碳酸氢钠和硫酸铝相互促进水解,从而迅速产生二氧化碳,所以可以用盐类水
解原理来解释泡沫灭火器灭火的原理,不符合题意。
答案:A
5.解析:根据一般情况下沉淀转化向溶度积小的方向进行可知,K(MnS)>K(CuS),
sp sp
A项正确;该反应达平衡时c(Mn2+)、c(Cu2+)保持不变,但不一定相等,B项错误;往平衡体
系中加入少量CuSO 固体后,平衡向正反应方向移动,c(Mn2+)变大,C项正确;该反应的平
4
衡常数K===,D项正确。
答案:B
6.解析:沉淀工业废水中的Pb2+时,生成沉淀的反应进行得越完全越好,由于PbS的
溶解度最小,故选硫化物作为沉淀剂。
答案:A
考点二
1知识梳理
1.cm(An+)·cn(Bm-) cm(An+)·cn(Bm-) 沉淀 平衡 未饱和
2.(2)温度
思考 答案:a、b、d
判断 答案:(1)× (2)√ (3)× (4)× (5)√
2对点速练
1.解析:根据题意,M(OH) 开始沉淀时,OH-的最小浓度为 ,代入数值,可以计算出
n
四种离子浓度相同时,Fe3+开始沉淀时所需溶液中的c(OH-)最小,溶液的pH最小。
答案:A
2.解析:T ℃时,饱和CaCO 溶液中c(Ca2+)=c(CO2− )=10-5 mol/L,饱和CaF 溶液
3 3 21 √4.0×10-12
中c(Ca2+)·c2(F-)=4.0×10-12,c(Ca2+)= c(F-),c(Ca2+)=3 mol/L=10-4
2 4
mol/L,所以饱和CaCO 溶液和饱和CaF 溶液中,饱和CaF 溶液中的c(Ca2+)较大,A项错误;
3 2 2
等体积混合后,混合溶液中c(Ca2+)远大于饱和CaCO 溶液中的c(Ca2+),而c(CO2− )只减少
3 3
到原来的一半,此时溶液中c(Ca2+)×c(CO2−
)>K(CaCO),所以会析出CaCO 固体,B项错误;
3 sp 3 3
T ℃时,CaCO 固体在稀盐酸中的K 与在纯水中的K 相同,因为CaCO 的K 只随温度的变化
3 sp sp 3 sp
而变化,C项错误;T ℃时,向CaCO 悬浊液中加入NaF固体,当c(Ca2+)·c2(F-)≥K(CaF)
3 sp 2
时,会析出CaF 固体,D项正确。
2
答案:D
3.解析:当溶液中c(Cl-)为0. 01 mol·L-1时,产生沉淀AgCl时所需Ag+的浓度为
c(Ag+)==mol·L-1=1. 56×10-8mol·L-1,同理含Br-溶液中所需c(Ag+)==mol·L-1=
7.7×10-11mol·L-1,含CrO2− 溶液中所需c(Ag+)==mol·L-1=3×10-5 mol·L-1,所需
4
c(Ag+)越小,则越先生成沉淀,所以三种阴离子产生沉淀的先后顺序为Br-、Cl-、CrO2−
。
4
答案:Br-、Cl-、CrO2−
4
4.解析:由图示可知,该条件下CaSO 饱和溶液中,c(Ca2+)=c(SO2− )=3.0×10-3
4 4
mol/L,K(CaSO)=9.0×10-6。当向100 mL该条件下的CaSO 饱和溶液中加入400 mL 0.01
sp 4 4
mol/L 的 NaSO 溶液后,混合溶液中c(Ca2+)=6.0×10-4 mol/L,c(SO2− )=8.6×10-3
2 4 4
mol/L,溶液中Q=c(Ca2+)·c(SO2− )=5.16×10-6