文档内容
第 3 讲 物质的量及相关概念
复习目标 1.了解物质的量、摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗常数
的含义。2.能准确使用“=n===c(B)·V(aq)”进行一定量某物质与所含指定微粒的数目换
算。3.正确使用阿伏加德罗定律及推论解答气体的体积、压强与物质的量、微粒数目相关问
题。4.掌握气体(平均)摩尔质量的计算方法。
考点一 物质的量 摩尔质量
1.物质的量
(1)概念:物质的量是国际单位制中的七个基本物理量之一,用来表示一定数目微粒的集合
体。符号为n,单位是摩尔(mol)。
(2)物质的量的规范表示方法
(3)使用范围:适用于微观粒子或微观粒子的特定组合。
2.阿伏加德罗常数
(1)国际上规定,1 mol粒子集合体所含的粒子数约为 6.02 × 10 23 ,1 mol任何物质所含的粒子
数叫做阿伏加德罗常数,符号为N ,N ≈ 6.02 × 10 23 mol - 1 。
A A
(2)物质的量、阿伏加德罗常数与微粒数目的关系
(背会公式和字母含义)
n=⇒
3.摩尔质量
(1)概念:单位物质的量的物质所具有的质量称为该物质的摩尔质量。符号为M。
(2)常用单位: g·mol - 1 。
(3)数值:当粒子的摩尔质量以 g·mol - 1 为单位时,在数值上等于该粒子的相对分子(或原子)
质量。
(4)公式(背会):n=⇒
(1)物质的量是表示微粒数目多少的物理量(×)
错因:物质的量是表示含有一定数目粒子的集合体的物理量。
(2)1 mol任何物质都含有6.02×1023个分子(×)
错因:离子化合物不存在分子。(3)硫酸的摩尔质量为98 g(×)
错因: 摩尔质量的单位是 g·mo l - 1。
(4)2 mol H O的摩尔质量是1 mol H O的摩尔质量的2倍(×)
2 2
错因:物质的摩尔质量与物质的量的多少无关。
(5)1 mol O 的质量与它的相对分子质量相等(×)
2
错因:1 mol物质的质量以g为单位时,在数值上等于其相对分子质量。
题组一 准确理解物质的量、摩尔质量的概念
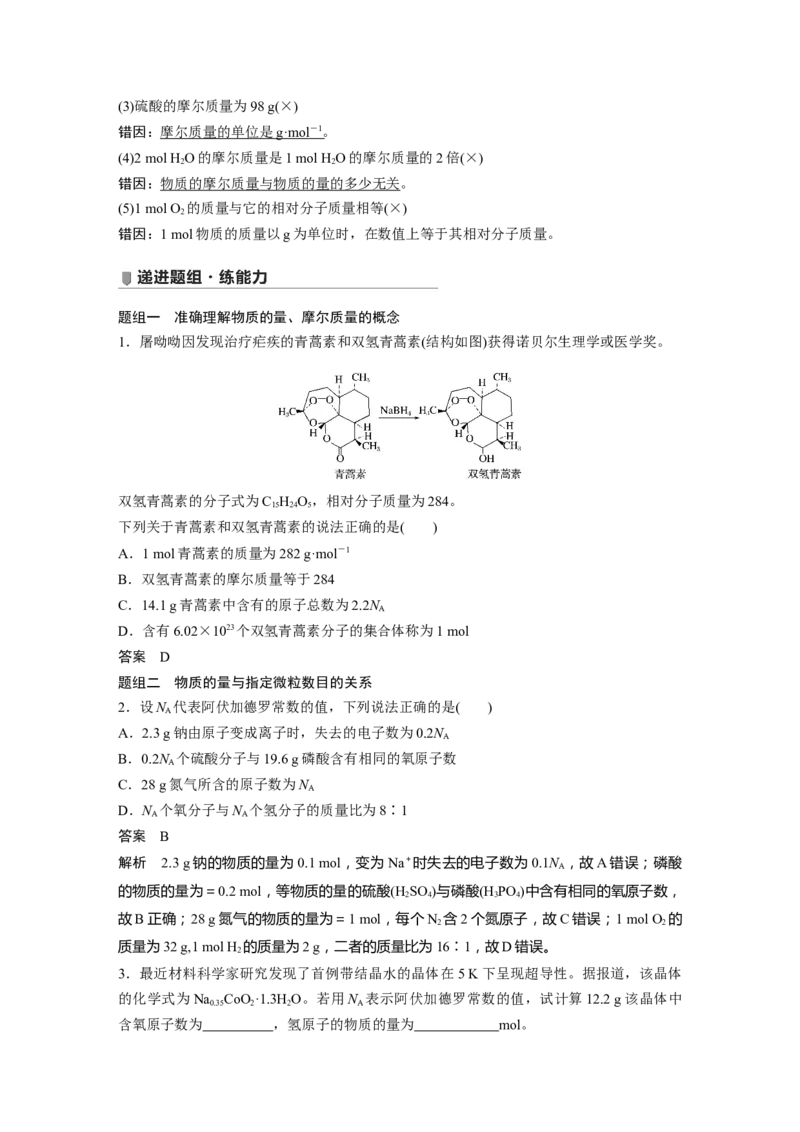
1.屠呦呦因发现治疗疟疾的青蒿素和双氢青蒿素(结构如图)获得诺贝尔生理学或医学奖。
双氢青蒿素的分子式为C H O,相对分子质量为284。
15 24 5
下列关于青蒿素和双氢青蒿素的说法正确的是( )
A.1 mol青蒿素的质量为282 g·mol-1
B.双氢青蒿素的摩尔质量等于284
C.14.1 g青蒿素中含有的原子总数为2.2N
A
D.含有6.02×1023个双氢青蒿素分子的集合体称为1 mol
答案 D
题组二 物质的量与指定微粒数目的关系
2.设N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.2.3 g钠由原子变成离子时,失去的电子数为0.2N
A
B.0.2N 个硫酸分子与19.6 g磷酸含有相同的氧原子数
A
C.28 g氮气所含的原子数为N
A
D.N 个氧分子与N 个氢分子的质量比为8∶1
A A
答案 B
解析 2.3 g钠的物质的量为0.1 mol,变为Na+时失去的电子数为0.1N ,故A错误;磷酸
A
的物质的量为=0.2 mol,等物质的量的硫酸(H SO )与磷酸(H PO )中含有相同的氧原子数,
2 4 3 4
故B正确;28 g氮气的物质的量为=1 mol,每个N 含2个氮原子,故C错误;1 mol O 的
2 2
质量为32 g,1 mol H 的质量为2 g,二者的质量比为16∶1,故D错误。
2
3.最近材料科学家研究发现了首例带结晶水的晶体在5 K下呈现超导性。据报道,该晶体
的化学式为Na CoO·1.3H O。若用N 表示阿伏加德罗常数的值,试计算12.2 g该晶体中
0.35 2 2 A
含氧原子数为 ,氢原子的物质的量为 mol。答案 0.33N 0.26
A
计算判断物质中所含指定微粒数目的技巧
弄清楚微粒与所给物质的关系:原子(电子)的物质的量=分子(或特定组合)物质的量×1个
分子(或特定组合)中所含这种原子(电子)个数。如:
第2题A项中N 表示Na原子失去的电子数目,Na―――→Na+;
A
第3题中,Na CoO·1.3H O是整体,计算对象氧原子、氢原子为部分,它们的关系为:
0.35 2 2
Na CoO·1.3H O~3.3O~2.6H
0.35 2 2
考点二 气体摩尔体积 阿伏加德罗定律
1.气体摩尔体积
(1)概念:一定温度和压强下单位物质的量的气体所占的体积,符号为V 。
m
(2)常用单位: L/mol( 或 L·mol - 1 ) 。
(3)公式(背会):n=⇒
(4)计算时常用标准状况下的气体摩尔体积
标准状况下(0 ℃、101 kPa),V ≈ 22.4 L·mol - 1 。
m
(5)注意事项
标准状况是特定条件,不是常温常压,计量对象在该条件下必须为气态。
2.阿伏加德罗定律及其推论
(1)阿伏加德罗定律内容
在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子。
(2)阿伏加德罗定律的推论
公式 语言叙述(背会)
= 同温、同压下,气体的体积与其物质的量成正比
T、p相同 同温、同压下,气体的密度与其摩尔质量(或相对分
=
子质量)成正比
T、V相同 = 温度、体积相同的气体,其压强与其物质的量成正比
(3)注意事项
①适用于任何气体,包括混合气体,但不适用于非气体。
②推论可利用pV=nRT和n===推导(其中p为压强,V为气体的体积,R为常数,T为温
度)。(1)22 g CO 气体的体积为11.2 L(×)
2
错因:未指明标准状况,无法计算。
(2)在非标准状况下,气体摩尔体积一定不是22.4 L·mol-1(×)
错因: 升高温度、增大压强也可使气体摩尔体积为 22.4 L·mo l - 1。
(3)标准状况下11.2 L Br 的物质的量为0.5 mol(×)
2
错因:Br 在标准状况下是液体,无法计算。
2
(4)标准状况下,11.2 L O 和H 的混合气体所含分子数约为3.01×1023(√)
2 2
(5)相同体积的CO和N,二者含有的原子数相同(×)
2
错因:未指明温度压强是否相同,无法判断。
使用气体摩尔体积、阿伏加德罗定律时,为何要指明温度和压强?
答案 分子数目相同,气体的体积主要由分子间距离决定,气体分子间距离受温度和压强影
响。
题组一 气体摩尔体积的含义及定义式
1.下列关于阿伏加德罗常数和气体摩尔体积等的说法正确的是( )
A.1 mol O 和1 mol N 所占的体积都约为22.4 L
2 2
B.H 的气体摩尔体积约为22.4 L
2
C.在标准状况下,1 mol H 和1 mol H O所占的体积都约为22.4 L
2 2
D.标准状况下,22.4 L乙烷、丙烷的混合气体,所含的分子数为N
A
答案 D
解析 没有明确温度和压强,无法确定气体的体积,A错误;气体摩尔体积的单位不是
“L”,而是“L·mol-1”或“m3·mol-1”,另外未指明气体所处的温度和压强,H 的气体摩
2
尔体积不一定为22.4 L·mol-1,B错误;在标准状况下,水为液态,C错误。
2.已知:①6.72 L NH (标准状况下) ②1.204×1023个HS分子 ③5.6 g CH ④0.5 mol
3 2 4
HCl,下列关系正确的是( )
A.体积大小:④>③>②>①
B.原子数目:③>①>④>②
C.密度大小:④>②>③>①
D.质量大小:④>③>②>①
答案 B
题组二 气体V与n、m、N之间的换算
3.利用太阳能分解水制氢,若光解0.02 mol水,下列说法正确的是( )
A.可生成H 的质量为0.02 g
2B.可生成氢的原子数为2.408×1023个
C.可生成H 的体积为0.224 L(标准状况)
2
D.生成H 的量理论上等于0.04 mol Na与水反应产生H 的量
2 2
答案 D
4.设N 为阿伏加德罗常数的值,如果a g某气态双原子分子的分子数为p,则b g该气体
A
在标准状况下的体积V(L)是( )
A. B. C. D.
答案 D
解析 解法一 公式法:
a g双原子分子的物质的量= mol,
双原子分子的摩尔质量== g·mol-1,
所以b g气体在标准状况下的体积为
×22.4 L·mol-1= L。
解法二 比例法:
同种气体的分子数与质量成正比,设b g气体的分子数为N
a g ~ p
b g ~ N
则:N=,双原子分子的物质的量为mol,
所以b g该气体在标准状况下的体积为 L。
题组三 阿伏加德罗定律的应用
5.下列说法不正确的是( )
A.温度相同、体积相同的O(g)和N(g)所含的分子数一定相同
2 2
B.同温同压下,SO 气体与CO 气体的密度之比等于16∶11
2 2
C.温度和容积相同的两容器分别盛有5 mol O (g)和2 mol N (g),则压强之比为5∶2
2 2
D.同温同压条件下,5 mol O 和2 mol H (g)的体积之比等于5∶2
2 2
答案 A
解析 压强未知,无法判断温度相同、体积相同的O(g)和N(g)所含分子数是否相同,A错
2 2
误;同温同压下,气体的密度之比等于其摩尔质量之比,B正确;同温同体积的气体的压强
之比等于物质的量之比,C正确;同温同压下,气体的体积之比等于物质的量之比,D正确。
6.一个密闭容器,中间有一可自由滑动的隔板(厚度不计),将容器分成两部分,当左侧充
入1 mol N ,右侧充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确
2
的是( )A.右侧与左侧分子数之比为4∶1
B.右侧CO的质量为5.6 g
C.右侧气体密度是相同条件下氢气密度的14倍
D.若改变右侧CO的充入量而使隔板处于容器正中间,保持温度不变,则应充入0.2 mol
CO
答案 C
解析 左右两侧气体温度、压强相同,相同条件下,体积之比等于物质的量之比,左右体积
之比为4∶1,则左右气体物质的量之比为4∶1,所以右侧气体物质的量为0.25 mol。相同
条件下密度之比与摩尔质量成正比,则右侧气体密度是相同条件下氢气密度的=14倍。
(1)解答有关气体摩尔体积、阿伏加德罗定律判断题时要注意三看:
一看物质的状态是否是气体,二看温度、压强是否是标准状况,三看气体分子组成。
(2)有关阿伏加德罗定律及其推论题的分析思路
第一步,分析“条件”:分析题干中的条件,找出相同与不同。
第二步,明确“要求”:分析题目要求,明确所要求的比例关系。
第三步,利用“规律”:利用阿伏加德罗定律及其推论,根据条件和要求进行判断。
题组四 气体(平均)摩尔质量的计算
7.按要求解答问题
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为 ,
可能是 气体。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为 。
(3)CO和CO 的混合气体18 g,完全燃烧后测得CO 体积为11.2 L(标准状况),则
2 2
①混合气体在标准状况下的密度是 g·L-1。
②混合气体的平均摩尔质量是 g·mol-1。
答案 (1)64 SO (2)64 (3)①1.61 ②36
2
解析 (1)M=ρ×22.4 g·mol-1≈64 g·mol-1。(2)M==64 g·mol-1。(3)CO燃烧发生反应:
2CO+O=====2CO,CO的体积与生成CO 的体积相等,燃烧后CO 的总体积为11.2 L,故
2 2 2 2
18 g CO和CO 的混合气体的总体积为11.2 L,在标准状况下,18 g CO和CO 的混合气体的
2 2
物质的量为0.5 mol,设CO的物质的量为x mol,CO 的物质的量为y mol,
2
则,解得x=0.25,y=0.25。①原混合气体的密度=≈1.61 g·L-1。
②解法一:=ρ·22.4 L·mol-1=1.61 g·L-1×22.4 L·mol-1≈36 g·mol-1;
解法二:==36 g·mol-1;
解法三:=28 g·mol-1×50%+44 g·mol-1×50%=36 g·mol-1;
故平均摩尔质量为36 g·mol-1。
8.在一定条件下,m g NHHCO 完全分解生成NH 、CO、HO(g),按要求填空。
4 3 3 2 2
(1)若所得混合气体对 H 的相对密度为 d,则混合气体的物质的量为 。
2
NH HCO 的摩尔质量为 (用含m、d的代数式表示)。
4 3
(2)若所得混合气体的密度折合成标准状况为 ρ g·L-1,则混合气体的平均摩尔质量为
(用含ρ的代数式表示)。
(3)若在该条件下,所得NH 、CO 、HO(g)的体积分数分别为a%、b%、c%,则混合气体的
3 2 2
平均相对分子质量为 (用含a、b、c的代数式表示)。
答案 (1) mol 6d g·mol-1 (2)22.4ρ g·mol-1 (3)17a%+44b%+18c%
解析 NH HCO (s)=====NH (g)+CO(g)+HO(g)
4 3 3 2 2
(1)M(混)=2d⇒n(混)= mol,
⇒M(NH HCO )=2d×3 g·mol-1=6d g·mol-1。
4 3
(2)(混)=22.4ρ g·mol-1。
(3)n(NH )∶n(CO)∶n(H O)=a%∶b%∶c%,
3 2 2
(混)=17a%+44b%+18c%。
求气体摩尔质量M的常用方法
(1)根据物质的质量(m)和物质的量(n):M=。
(2)根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(N ):M=。
A
(3)根据标准状况下气体的密度ρ:
M=ρ×22.4 L·mol-1。
(4)根据气体的相对密度(D=):=D。
(5)对于混合气体,求其平均摩尔质量,上述计算式仍然成立;还可以用下式计算:M=
M×a%+M×b%+M×c%……,a%、b%、c%……指混合物中各成分的物质的量分数(或
1 2 3
体积分数)。
考点三 物质的量浓度及简单计算1.物质的量浓度
(1)概念(背会)
物质的量浓度表示单位体积的溶液里所含溶质B的物质的量,也称为 B 的物质的量浓度 ,
符号为c 。
B
(2)常用单位:mol/L 或 mol·L - 1 。
(3)公式(背会):n=c V⇒
B
(4)注意事项
①V是溶液的体积,不是溶剂的体积,也不是溶质与溶剂的体积之和。
②n必须是溶质B的物质的量。
2.物质的量浓度和溶质质量分数的比较
物质的量浓度c 溶质质量分数w
以单位体积溶液中所含溶质的物 以溶质的质量与溶液的质量比
概念
质的量来表示溶液组成的物理量 值来表示溶液的组成的物理量
溶质的单位 mol g
溶液的单位 L g
表达式 c= w = ×100%
两者关系 w=(M:摩尔质量;单位:g·mol-1;ρ:密度,单位:g·cm-3)
(1)1 mol·L-1 NaCl溶液是指此溶液中含有1 mol NaCl(×)
错因: n = c V ,没有体积无法计算物质的量 。
B
(2)1 mol Na O溶于水,配成1 L溶液所得溶液的物质的量浓度为1 mol·L-1(×)
2
错因:1 mol Na O――――→2 mol NaOH,溶质NaOH物质的量浓度为2 mol·L-1。
2
(3)用100 mL水吸收0.1 mol HCl气体所得溶液的物质的量浓度恰好是1 mol·L-1(×)
错因: 100 mL 水吸收 HCl 后体积不再是 100 mL 。
题组一 对物质的量浓度的含义的理解
1.下列方法所得溶液中溶质的物质的量浓度为1 mol·L-1的是( )
A.将40 g NaOH固体溶解于1 L水中
B.将80 g SO 溶于水并配成1 L的溶液
3
C.将1 L 10 mol·L-1的浓盐酸与9 L水混合
D.向1 mol的硫酸钡固体中加水至1 L
答案 B
2.(2020·哈尔滨六中检测)4 ℃时,在100 mL水中溶解22.4 L(标准状况下)HCl气体形成溶液。下列说法正确的是( )
A.该溶液的物质的量浓度为10 mol·L-1
B.由于溶液的密度未知,故该溶液的物质的量浓度无法求得
C.由于溶液的密度未知,故该溶液中溶质的质量分数无法求得
D.所得溶液的体积为22.5 L
答案 B
题组二 定义式c =的相关计算
B
3.(1)用14.2 g无水硫酸钠配制成500 mL溶液,其物质的量浓度为 mol·L-1。
(2)若从中取出 50 mL 溶液,其物质的量浓度为 mol·L-1;溶质的质量为
g。
(3)若将这50 mL溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为 mol·L-
1,SO的物质的量浓度为 mol·L-1。
答案 (1)0.2 (2)0.2 1.42 (3)0.2 0.1
解析 (1)n(Na SO )==0.1 mol,
2 4
c(Na SO )==0.2 mol·L-1。
2 4
(2)从中取出50 mL溶液,浓度仍为0.2 mol·L-1,
溶质的质量m=n·M=c·V·M=0.2 mol·L-1×0.05 L×142 g·mol-1=1.42 g。
(3)50 mL溶液用水稀释到100 mL,根据c(浓)·V(浓)=c(稀)·V(稀),稀溶液中NaSO 的物质
2 4
的量浓度变为原来的,即0.1 mol·L-1,故所得溶液中Na+的物质的量浓度为0.2 mol·L-1,
SO的物质的量浓度为0.1 mol·L-1。
4.在标准状况下,将V L氨气溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此氨水的
物质的量浓度为 mol·L-1。
答案
解析 n(NH )= mol,
3
溶液体积:V=×10-3 L
c= mol·L-1= mol·L-1。
(1)注意物质溶于水后溶质是否改变,如:
NaO、NaO―→NaOH,
2 2 2
SO ―→HSO ,
3 2 4
CuSO ·5H O―→CuSO
4 2 4
(2)混淆溶液的体积和溶剂的体积
①不能用水的体积代替溶液的体积,尤其是固体、气体溶于水,一般根据溶液的密度进行计
算:
V=。②两溶液混合液的体积不是两种溶液的体积和。
(3)电解质与所含离子间c的换算
注意整体与部分的关系,如第3题中,
0.2 mol·L-1的NaSO 溶液中―→
2 4
1.(2020·全国卷Ⅲ,9)N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.22.4 L(标准状况)氮气中含有7N 个中子
A
B.1 mol重水比1 mol水多N 个质子
A
C.12 g石墨烯和12 g金刚石均含有N 个碳原子
A
D.1 L 1 mol·L-1 NaCl溶液含有28N 个电子
A
答案 C
解析 标准状况下22.4 L氮气的物质的量是1 mol,1个N 中有14个中子,则1 mol氮气有
2
14N 个中子,A错误;重水和水中的质子数相同,B错误;石墨烯和金刚石是碳元素的同素
A
异形体,是由碳元素组成的不同单质,12 g石墨烯和12 g金刚石均含有1 mol碳原子,即
N 个碳原子,C正确;1 L 1 mol·L-1 NaCl溶液中含有1 mol NaCl(含有28N 个电子)和大量
A A
的水(水分子也含有电子),D错误。
2.(2019·全国卷Ⅱ,8)已知N 是阿伏加德罗常数的值,下列说法错误的是( )
A
A.3 g 3He含有的中子数为1N
A
B.1 L 0.1 mol·L-1磷酸钠溶液含有的PO数目为0.1N
A
C.1 mol K Cr O 被还原为Cr3+转移的电子数为6N
2 2 7 A
D.48 g正丁烷和10 g异丁烷的混合物中共价键数目为13N
A
答案 B
解析 3 g 3He的物质的量为1 mol,每个3He含1个中子,则1 mol 3He含1 mol中子,A项
正确;该溶液中含0.1 mol Na PO ,由于部分PO水解,故溶液中PO的数目小于0.1N ,B
3 4 A
项错误;KCr O 中Cr元素为+6价,1 mol K Cr O 被还原成Cr3+时,得到6 mol电子,C
2 2 7 2 2 7
项正确;正丁烷和异丁烷互为同分异构体,每个分子中均含10个C—H键和3个C—C键,
即每个分子中含13个共价键,则48 g正丁烷和10 g异丁烷的混合物中含13 mol 共价键,D
项正确。
3.(2018·全国卷Ⅰ,10)N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.16.25 g FeCl 水解形成的Fe(OH) 胶体粒子数为0.1N
3 3 A
B.22.4 L(标准状况)氩气含有的质子数为18N
A
C.92.0 g甘油(丙三醇)中含有羟基数为1.0N
A
D.1.0 mol CH 与Cl 在光照下反应生成的CHCl分子数为1.0N
4 2 3 A
答案 B解析 氩气是单原子分子,标准状况下,22.4 L氩气的物质的量为1 mol,含有的质子数为
18N ,B项正确;Fe(OH) 胶体粒子是若干个Fe(OH) 分子的集合体,A项错误;92.0 g甘油
A 3 3
的物质的量为1 mol,每个甘油分子含有3个羟基,所以1 mol甘油含有的羟基数为3.0N ,
A
C项错误;CH 与Cl 发生取代反应生成的有机物除了CHCl以外,还有CHCl 、CHCl 和
4 2 3 2 2 3
CCl ,生成的CHCl分子数小于1.0N ,D项错误。
4 3 A
4.(2018·全国卷Ⅱ,11)N 代表阿伏加德罗常数的值。下列说法正确的是( )
A
A.常温常压下,124 g P 中所含P—P键数目为4N
4 A
B.100 mL 1 mol·L-1FeCl 溶液中所含Fe3+的数目为0.1N
3 A
C.标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2N
A
D.密闭容器中,2 mol SO 和1 mol O 催化反应后分子总数为2N
2 2 A
答案 C
解析 标准状况下,11.2 L甲烷和乙烯混合物的物质的量为0.5 mol,每个甲烷和乙烯分子
都含有4个氢原子,所以含有氢原子数目为2N ,C项正确;124 g P 的物质的量为1 mol,
A 4
每个P 分子中含有6个P—P键,所以含有P—P键数目为6N ,A项错误;Fe3+在水溶液中
4 A
能发生水解,100 mL 1 mol·L-1FeCl 溶液中所含Fe3+的数目小于0.1N ,B项错误;SO 和
3 A 2
O 的化合反应为可逆反应,2 mol SO 和1 mol O 催化反应后,混合气体的物质的量大于2
2 2 2
mol,即分子总数大于2N ,D项错误。
A
5.(2020·浙江7月选考,19)N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.4MnO+5HCHO+12H+===4Mn2++5CO↑+11HO,1 mol [4MnO+5HCHO]完全反应转
2 2
移的电子数为20N
A
B.用电解粗铜的方法精炼铜,当电路中通过的电子数为N 时,阳极应有32 g Cu转化为Cu2
A
+
C.常温下,pH=9的CHCOONa溶液中,水电离出的H+数为10-5N
3 A
D.1 L浓度为0.100 mol·L-1的NaCO 溶液中,阴离子数为0.100N
2 3 A
答案 A
解析 Mn元素由+7价降低到+2价,C元素由 0价升高到+4价,则 1 mol [4MnO+
5HCHO]完全反应转移的电子数为20N ,A正确;电解精炼铜时,开始阶段阳极上比Cu活
A
泼的金属杂质也会放电,故电路中通过的电子数为 N 时,阳极上被氧化的Cu的质量小于
A
32 g,B错误;题目未指明pH=9的CHCOONa溶液的体积,无法确定水电离出的H+数,
3
C错误;1 L浓度为0.100 mol·L-1的NaCO 溶液中含有0.100 mol Na CO ,CO水解生成
2 3 2 3
HCO和OH-,阴离子数目增加,故溶液中阴离子数大于0.100N ,D错误。
A
1.(2020·天津市第一中学高三月考)双酚基丙烷(BPA)的分子式为C H O 。下列有关判断不
15 16 2
正确的是( )A.BPA的摩尔质量是228 g·mol-1
B.1 mol BPA中含有6.02×1023个分子
C.BPA属于有机化合物
D.1 mol BPA在标准状况下的体积约为22.4 L
答案 D
2.下列叙述中错误的是( )
A.阿伏加德罗常数的符号为N ,其近似为6.02×1023 mol-1
A
B.等物质的量的O 和O,所含氧原子数相同
2 3
C.在0.5 mol Na SO 中,含有的Na+数约是6.02×1023
2 4
D.摩尔是物质的量的单位
答案 B
3.(2021·天津市静海区第一次月考)下列说法中正确的是( )
A.2 mol CH 的质量和O 的摩尔质量都是32 g
4 2
B.1 mol任何气体中都含有相同的原子数
C.0.5 mol NaCl约含有6.02×1023个离子
D.1 mol·L-1 KCl溶液中含有溶质1 mol
答案 C
解析 O 的摩尔质量为32 g·mol-1,A项不正确;气体有单原子分子如He,双原子分子如
2
O ,三原子分子如O ,五原子分子如CH 等,B项不正确;每个NaCl中有两个离子,0.5
2 3 4
mol NaCl中含离子总数为N ,C项正确;未指明溶液的体积,无法确定,D项不正确。
A
4.在150 ℃时碳酸铵可受热完全分解,则其完全分解后所产生的气态混合物的密度是相同
条件下氢气密度的( )
A.96倍 B.48倍 C.12倍 D.32倍
答案 C
解析 150 ℃时碳酸铵受热完全分解的化学方程式为(NH )CO===2NH ↑+HO↑+
4 2 3 3 2
CO↑。根据质量守恒定律,反应前1 mol即96 g碳酸铵受热完全分解,则反应后所生成混
2
合气体的质量应为96 g。所以,反应后生成混合气体的摩尔质量为 M(混)===24 g·mol-
1。根据密度之比等于摩尔质量之比,则有:===12。
5.(2020·山东省临沂市莒南第二中学月考)在甲、乙两个体积不同的密闭容器中,分别充入
质量相等的CO、CO 气体时,两容器的温度和压强均相同,则下列说法正确的是( )
2
A.充入的CO分子数比CO 分子数少
2
B.甲容器的体积比乙容器的体积小
C.CO的摩尔体积比CO 的摩尔体积小
2
D.甲中CO的密度比乙中CO 的密度小
2
答案 D解析 质量相等的CO和CO 的物质的量之比为11∶7,在温度和压强相同时体积之比为
2
11∶7,但摩尔体积相同。
6.现有两份体积相同的混合溶液,其组成如下:
KCl KSO ZnSO ZnCl
2 4 4 2
① 0.4 mol 0.1 mol 0.3 mol 0.1 mol
② 0.2 mol 0.2 mol 0.1 mol 0.1 mol
则两份溶液中各离子浓度( )
A.仅c(K+)相同 B.仅c(Cl-)相同
C.完全相同 D.完全不同
答案 A
解析 ①溶液中离子物质的量分别为:K+:0.4 mol+2×0.1 mol=0.6 mol,Zn2+:0.3 mol+
0.1 mol=0.4 mol,Cl-:0.4 mol+2×0.1 mol=0.6 mol,SO:0.1 mol+0.3 mol=0.4 mol;②
溶液中离子物质的量分别为:K+:0.2 mol+2×0.2 mol=0.6 mol,Zn2+:0.1 mol+0.1 mol
=0.2 mol,Cl-:0.2 mol+2×0.1 mol=0.4 mol,SO:0.2 mol+0.1 mol=0.3 mol,所以只有
c(K+)相同,A项正确。
7.下列所得溶液的物质的量浓度为0.1 mol·L-1的是( )
A.将0.1 mol氨充分溶解在1 L水中
B.将10 g质量分数为98%的硫酸与990 g水混合
C.将25.0 g胆矾溶于水配成1 L溶液
D.将10 mL 1 mol·L-1的盐酸与90 mL水充分混合
答案 C
解析 将0.1 mol氨充分溶解在1 L水中,所得溶液的体积不是1 L,故不能得到0.1 mol·L-1
的溶液,A错误;将10 g质量分数为98%的硫酸与990 g水混合,不知所配溶液的密度,无
法求算其物质的量浓度,B错误;25.0 g胆矾的物质的量为0.1 mol,将其溶于水配成1 L溶
液,所得溶液的物质的量浓度为 0.1 mol·L-1,C正确;将10 mL 1 mol·L-1的盐酸与90 mL
水充分混合,不同液体混合后的体积不等于两液体体积在数值上的简单加和,D错误。
8.(2019·烟台期中)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.400 mL 1 mol·L-1稀硝酸与Fe完全反应(还原产物只有NO),转移电子的数目为0.3N
A
B.1 mol·L-1的AlCl 溶液中含有Cl-的个数为3N
3 A
C.0.2 mol HO和DO的混合物中含有中子的数目为2N
2 2 A
D.标准状况下,2.24 L Cl 溶于水所得氯水中含氯的微粒总数为0.2N
2 A
答案 A
解析 400 mL 1 mol·L-1稀硝酸中HNO 物质的量为0.4 L×1 mol·L-1=0.4 mol,铁与稀硝酸
3
反应可以生成硝酸亚铁:3Fe+8HNO(稀)===3Fe(NO ) +2NO↑+4HO或生成硝酸铁:Fe
3 3 2 2+4HNO(稀)===Fe(NO ) +NO↑+2HO,每反应 4 mol HNO 转移电子 3 mol,0.4 mol
3 3 3 2 3
HNO 与Fe完全反应(还原产物只有NO),转移电子的数目为0.3N ,A项正确;没有给出溶
3 A
液的体积,不能计算出1 mol·L-1的AlCl 溶液中含有Cl-的个数,B项错误;1个HO中含
3 2
8个中子,而1个DO中含10个中子,所以0.2 mol H O和DO中含有中子的数目为1.6N
2 2 2 A
~2N 之间,C项错误;标准状况下,2.24 L Cl 的物质的量为0.1 mol,Cl 溶于水后仍有部
A 2 2
分以Cl 的形式存在于水中,则所得氯水中含氯的微粒总数小于0.2N ,D项错误。
2 A
9.(2021·北京市人大附中月考)下列说法不正确的是( )
A.常温常压下,3.2 g O 和O 的混合气体中含有氧原子的数目约为0.2×6.02×1023
2 3
B.一定条件下,1 mol N 和3 mol H 充分反应转移电子数小于6N
2 2 A
C.标准状况下,1.12 L HCl气体中含有电子的数目约为0.9×6.02×1023
D.0.1 mol环氧乙烷( )中含有共价键的总数约为0.3×6.02×1023
答案 D
解析 氧气和臭氧均由氧原子构成,故 3.2 g混合物中含有的氧原子的物质的量为=0.2
mol,故含氧原子的数目约为0.2×6.02×1023,故A正确;一定条件下N 和H 发生反应:
2 2
N +3H2NH ,1 mol N 和3 mol H 参与反应时转移电子数为6N ,由于该反应为可逆反
2 2 3 2 2 A
应,1 mol N 和3 mol H 充分反应转移电子数小于6N ,故B正确;标况下1.12 L HCl的物
2 2 A
质的量为 0.05 mol,而 HCl 中含 18 个电子,故 0.05 mol HCl 中含电子的数目约为
0.9×6.02×1023,故C正确;环氧乙烷中含7个共价键,故0.1 mol环氧乙烷中含共价键的总
数约为0.7×6.02×1023,故D错误。
10.(1)30 g 12C18O和28 g 14N 所含的分子数之比为 。
2
(2)同温同压下,12C18O和14N 两种气体的密度之比为 。
2
(3)同温同压同体积的12C18O和14N 具有电子数之比为 。
2
(4)28 g14N 所含的原子数为 N 。
2 A
(5)将乙烯、CO、N 三种气体分别盛放在三个相同容器中,若三个容器的温度和质量相等,
2
则三个容器的气体压强之比为 。
答案 (1)1∶1 (2)15∶14 (3)1∶1 (4)2
(5)1∶1∶1
解析 (1)M(12C18O)=30 g·mol-1,30 g 12C18O的n(12C18O)=1 mol,M(14N)=28 g·mol-1,28 g
2
14N 的n(14N)=1 mol,n(12C18O)=n(14N),N(12C18O)=N(14N),分子数之比为1∶1。(2)同温
2 2 2 2
同压下,密度之比等于摩尔质量之比,M(12C18O)∶M(14N)=30∶28=15∶14。(3)同温同压
2
同体积,则n(12C18O)=n(14N),1 mol 12C18O中n(e-)=14 mol,1 mol 14N 中n(e-)=14 mol,
2 2
所以电子数之比为1∶1。(4)M(14N)=28 g·mol-1,n(14N)=1 mol,n(原子)=2 mol,所以
2 2
N(原子)=2N 。(5)乙烯、CO、N 的质量相等,三者的摩尔质量相等,所以 n(乙烯)=n(CO)
A 2
=n(N ),同温同体积时,压强之比等于物质的量之比,所以气体压强之比为1∶1∶1。
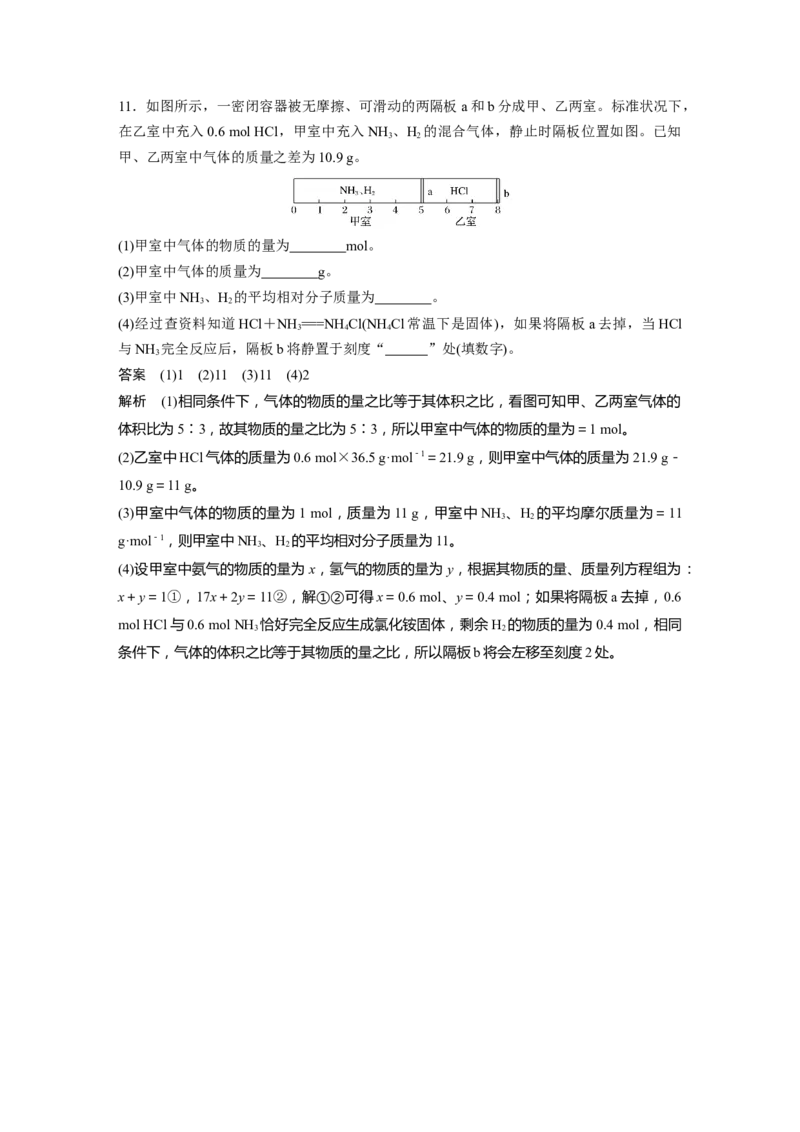
211.如图所示,一密闭容器被无摩擦、可滑动的两隔板a和b分成甲、乙两室。标准状况下,
在乙室中充入0.6 mol HCl,甲室中充入NH 、H 的混合气体,静止时隔板位置如图。已知
3 2
甲、乙两室中气体的质量之差为10.9 g。
(1)甲室中气体的物质的量为 mol。
(2)甲室中气体的质量为 g。
(3)甲室中NH 、H 的平均相对分子质量为 。
3 2
(4)经过查资料知道HCl+NH ===NH Cl(NHCl常温下是固体),如果将隔板a去掉,当HCl
3 4 4
与NH 完全反应后,隔板b将静置于刻度“ ”处(填数字)。
3
答案 (1)1 (2)11 (3)11 (4)2
解析 (1)相同条件下,气体的物质的量之比等于其体积之比,看图可知甲、乙两室气体的
体积比为5∶3,故其物质的量之比为5∶3,所以甲室中气体的物质的量为=1 mol。
(2)乙室中HCl气体的质量为0.6 mol×36.5 g·mol-1=21.9 g,则甲室中气体的质量为21.9 g-
10.9 g=11 g。
(3)甲室中气体的物质的量为1 mol,质量为11 g,甲室中NH 、H 的平均摩尔质量为=11
3 2
g·mol-1,则甲室中NH 、H 的平均相对分子质量为11。
3 2
(4)设甲室中氨气的物质的量为x,氢气的物质的量为y,根据其物质的量、质量列方程组为:
x+y=1①,17x+2y=11②,解①②可得x=0.6 mol、y=0.4 mol;如果将隔板a去掉,0.6
mol HCl与0.6 mol NH 恰好完全反应生成氯化铵固体,剩余H 的物质的量为0.4 mol,相同
3 2
条件下,气体的体积之比等于其物质的量之比,所以隔板b将会左移至刻度2处。