文档内容
专项提能特训 1 从氧化还原反应的视角分析“化工生产”
中的物质变化
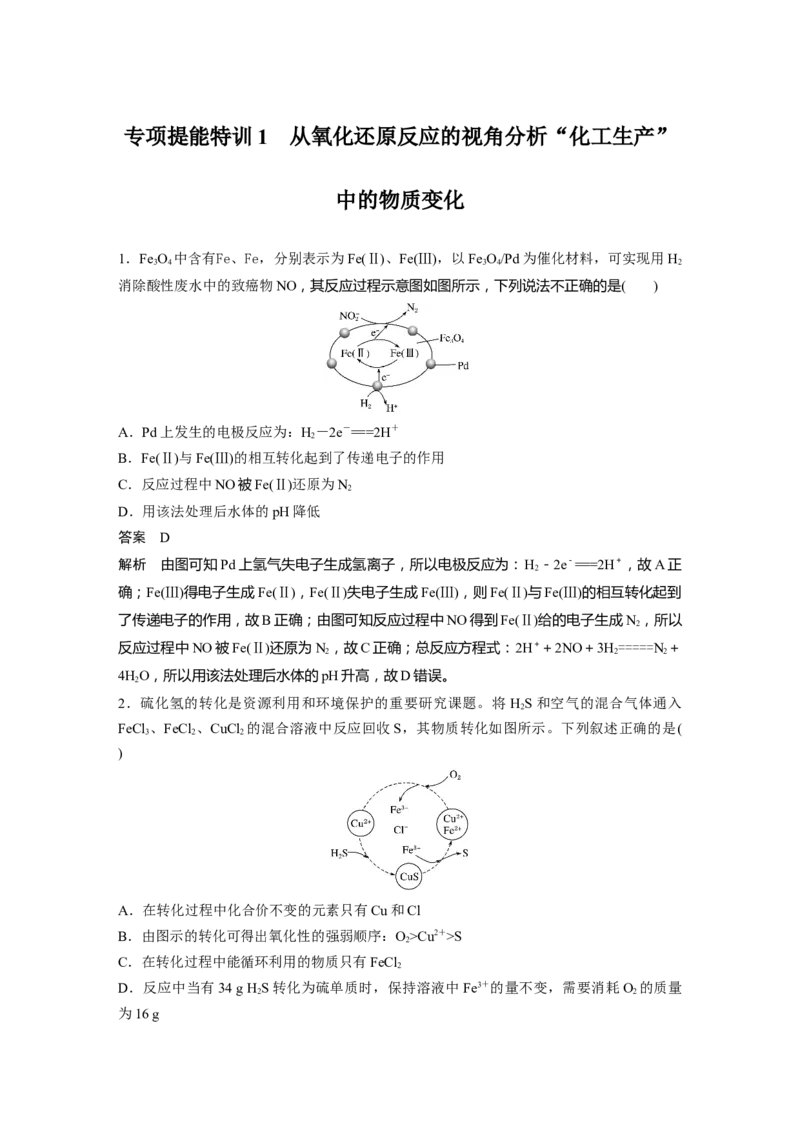
1.Fe O 中含有Fe、Fe,分别表示为Fe(Ⅱ)、Fe(Ⅲ),以Fe O/Pd为催化材料,可实现用H
3 4 3 4 2
消除酸性废水中的致癌物NO,其反应过程示意图如图所示,下列说法不正确的是( )
A.Pd上发生的电极反应为:H-2e-===2H+
2
B.Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传递电子的作用
C.反应过程中NO被Fe(Ⅱ)还原为N
2
D.用该法处理后水体的pH降低
答案 D
解析 由图可知Pd上氢气失电子生成氢离子,所以电极反应为:H -2e-===2H+,故A正
2
确;Fe(Ⅲ)得电子生成Fe(Ⅱ),Fe(Ⅱ)失电子生成Fe(Ⅲ),则Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到
了传递电子的作用,故B正确;由图可知反应过程中NO得到Fe(Ⅱ)给的电子生成N,所以
2
反应过程中NO被Fe(Ⅱ)还原为N ,故C正确;总反应方程式:2H++2NO+3H=====N +
2 2 2
4HO,所以用该法处理后水体的pH升高,故D错误。
2
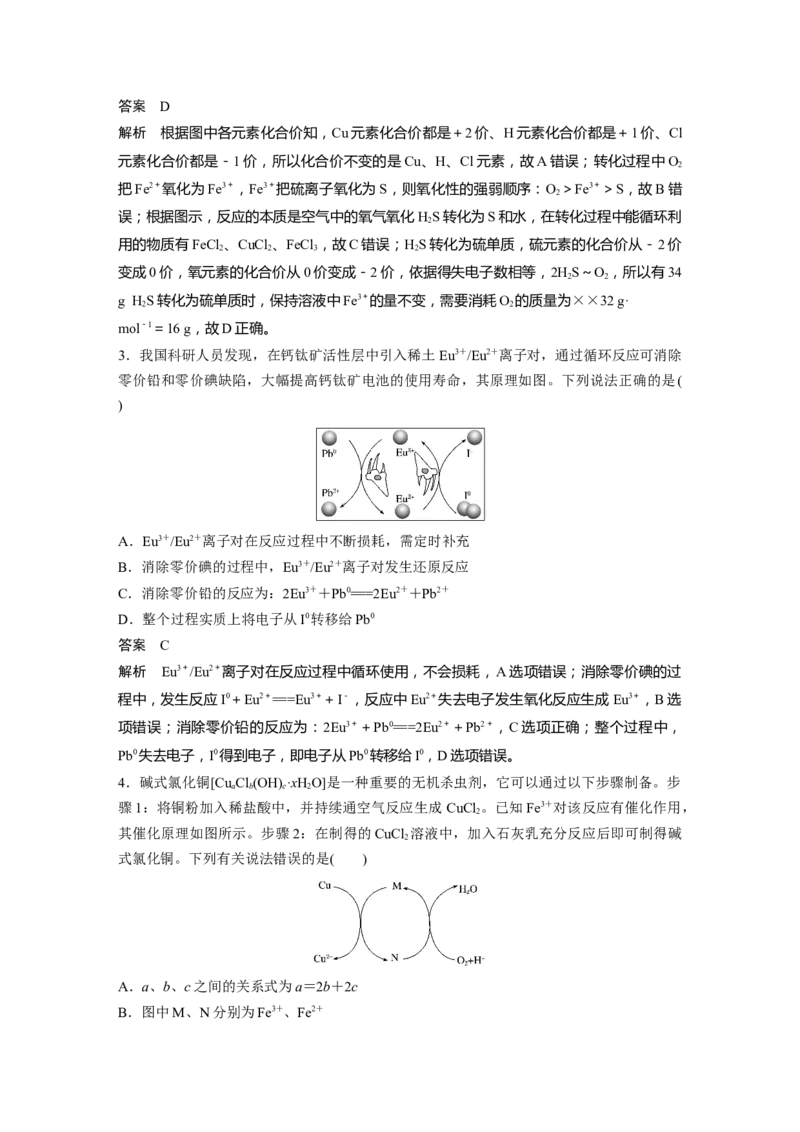
2.硫化氢的转化是资源利用和环境保护的重要研究课题。将 HS和空气的混合气体通入
2
FeCl 、FeCl 、CuCl 的混合溶液中反应回收S,其物质转化如图所示。下列叙述正确的是(
3 2 2
)
A.在转化过程中化合价不变的元素只有Cu和Cl
B.由图示的转化可得出氧化性的强弱顺序:O>Cu2+>S
2
C.在转化过程中能循环利用的物质只有FeCl
2
D.反应中当有34 g H S转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O 的质量
2 2
为16 g答案 D
解析 根据图中各元素化合价知,Cu元素化合价都是+2价、H元素化合价都是+1价、Cl
元素化合价都是-1价,所以化合价不变的是Cu、H、Cl元素,故A错误;转化过程中O
2
把Fe2+氧化为Fe3+,Fe3+把硫离子氧化为S,则氧化性的强弱顺序:O >Fe3+>S,故B错
2
误;根据图示,反应的本质是空气中的氧气氧化HS转化为S和水,在转化过程中能循环利
2
用的物质有FeCl 、CuCl 、FeCl ,故C错误;HS转化为硫单质,硫元素的化合价从-2价
2 2 3 2
变成0价,氧元素的化合价从0价变成-2价,依据得失电子数相等,2HS~O ,所以有34
2 2
g HS转化为硫单质时,保持溶液中Fe3+的量不变,需要消耗O 的质量为××32 g·
2 2
mol-1=16 g,故D正确。
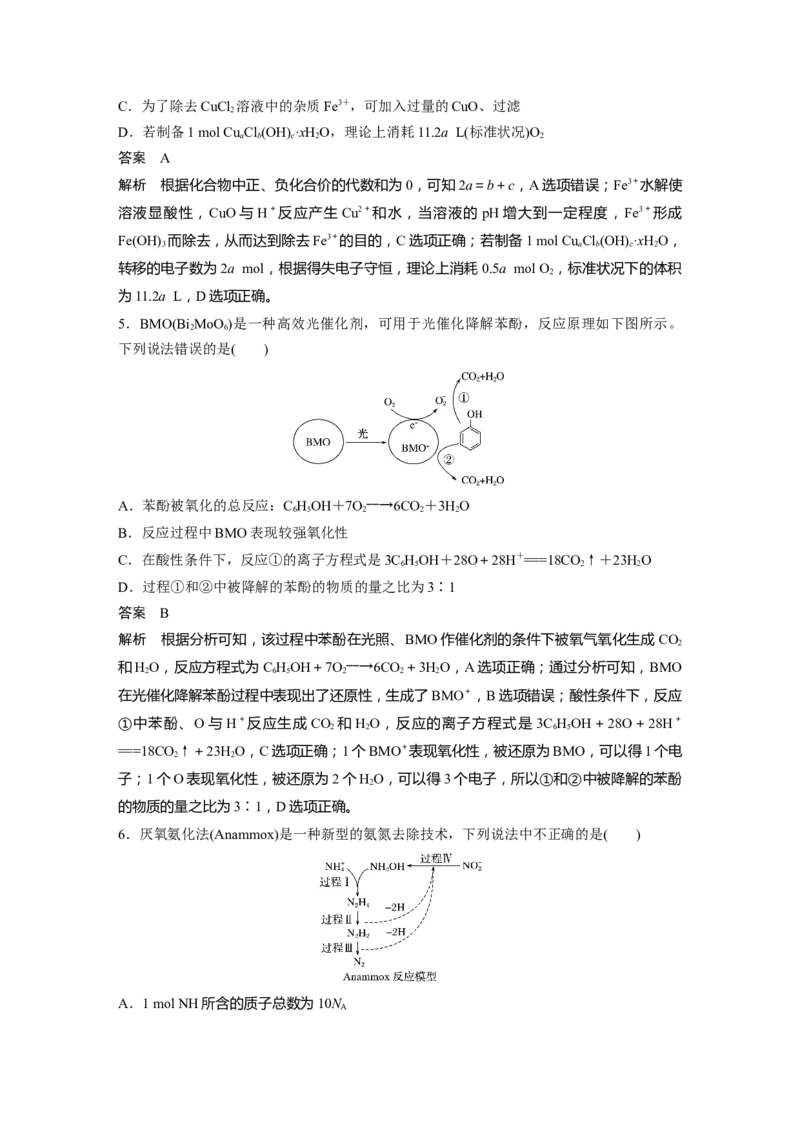
3.我国科研人员发现,在钙钛矿活性层中引入稀土Eu3+/Eu2+离子对,通过循环反应可消除
零价铅和零价碘缺陷,大幅提高钙钛矿电池的使用寿命,其原理如图。下列说法正确的是(
)
A.Eu3+/Eu2+离子对在反应过程中不断损耗,需定时补充
B.消除零价碘的过程中,Eu3+/Eu2+离子对发生还原反应
C.消除零价铅的反应为:2Eu3++Pb0===2Eu2++Pb2+
D.整个过程实质上将电子从I0转移给Pb0
答案 C
解析 Eu3+/Eu2+离子对在反应过程中循环使用,不会损耗,A选项错误;消除零价碘的过
程中,发生反应I0+Eu2+===Eu3++I-,反应中Eu2+失去电子发生氧化反应生成Eu3+,B选
项错误;消除零价铅的反应为:2Eu3++Pb0===2Eu2++Pb2+,C选项正确;整个过程中,
Pb0失去电子,I0得到电子,即电子从Pb0转移给I0,D选项错误。
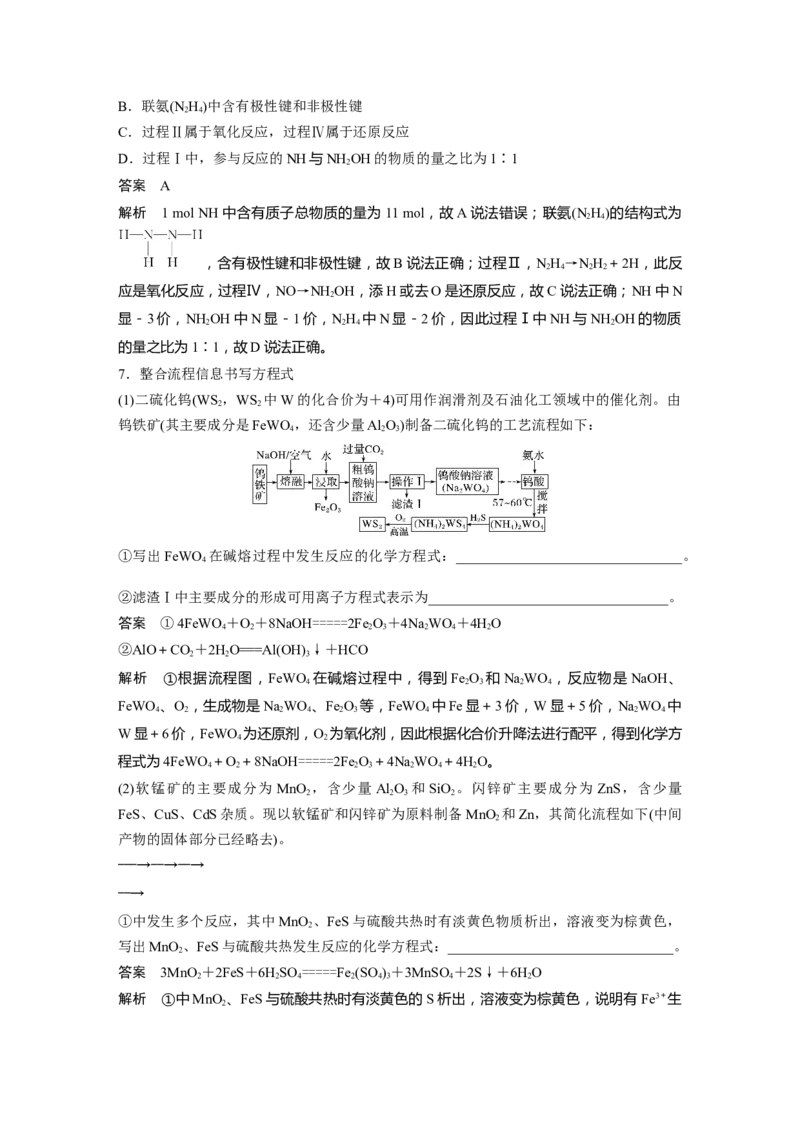
4.碱式氯化铜[Cu Cl(OH)·xHO]是一种重要的无机杀虫剂,它可以通过以下步骤制备。步
a b c 2
骤1:将铜粉加入稀盐酸中,并持续通空气反应生成 CuCl 。已知Fe3+对该反应有催化作用,
2
其催化原理如图所示。步骤2:在制得的CuCl 溶液中,加入石灰乳充分反应后即可制得碱
2
式氯化铜。下列有关说法错误的是( )
A.a、b、c之间的关系式为a=2b+2c
B.图中M、N分别为Fe3+、Fe2+C.为了除去CuCl 溶液中的杂质Fe3+,可加入过量的CuO、过滤
2
D.若制备1 mol Cu Cl(OH)·xHO,理论上消耗11.2a L(标准状况)O
a b c 2 2
答案 A
解析 根据化合物中正、负化合价的代数和为0,可知2a=b+c,A选项错误;Fe3+水解使
溶液显酸性,CuO与H+反应产生Cu2+和水,当溶液的 pH增大到一定程度,Fe3+形成
Fe(OH) 而除去,从而达到除去Fe3+的目的,C选项正确;若制备1 mol Cu Cl(OH)·xHO,
3 a b c 2
转移的电子数为2a mol,根据得失电子守恒,理论上消耗0.5a mol O ,标准状况下的体积
2
为11.2a L,D选项正确。
5.BMO(Bi MoO )是一种高效光催化剂,可用于光催化降解苯酚,反应原理如下图所示。
2 6
下列说法错误的是( )
A.苯酚被氧化的总反应:C HOH+7O――→6CO+3HO
6 5 2 2 2
B.反应过程中BMO表现较强氧化性
C.在酸性条件下,反应①的离子方程式是3C HOH+28O+28H+===18CO↑+23HO
6 5 2 2
D.过程①和②中被降解的苯酚的物质的量之比为3∶1
答案 B
解析 根据分析可知,该过程中苯酚在光照、BMO作催化剂的条件下被氧气氧化生成 CO
2
和HO,反应方程式为C HOH+7O――→6CO +3HO,A选项正确;通过分析可知,BMO
2 6 5 2 2 2
在光催化降解苯酚过程中表现出了还原性,生成了BMO+,B选项错误;酸性条件下,反应
①中苯酚、O与H+反应生成 CO 和HO,反应的离子方程式是 3C HOH+28O+28H+
2 2 6 5
===18CO↑+23HO,C选项正确;1个BMO+表现氧化性,被还原为BMO,可以得1个电
2 2
子;1个O表现氧化性,被还原为2个HO,可以得3个电子,所以①和②中被降解的苯酚
2
的物质的量之比为3∶1,D选项正确。
6.厌氧氨化法(Anammox)是一种新型的氨氮去除技术,下列说法中不正确的是( )
A.1 mol NH所含的质子总数为10N
AB.联氨(N H)中含有极性键和非极性键
2 4
C.过程Ⅱ属于氧化反应,过程Ⅳ属于还原反应
D.过程Ⅰ中,参与反应的NH与NH OH的物质的量之比为1∶1
2
答案 A
解析 1 mol NH中含有质子总物质的量为11 mol,故A说法错误;联氨(N H)的结构式为
2 4
,含有极性键和非极性键,故B说法正确;过程Ⅱ,NH→NH +2H,此反
2 4 2 2
应是氧化反应,过程Ⅳ,NO→NH OH,添H或去O是还原反应,故C说法正确;NH中N
2
显-3价,NH OH中N显-1价,NH 中N显-2价,因此过程Ⅰ中NH与NH OH的物质
2 2 4 2
的量之比为1∶1,故D说法正确。
7.整合流程信息书写方程式
(1)二硫化钨(WS ,WS 中W的化合价为+4)可用作润滑剂及石油化工领域中的催化剂。由
2 2
钨铁矿(其主要成分是FeWO,还含少量Al O)制备二硫化钨的工艺流程如下:
4 2 3
①写出FeWO 在碱熔过程中发生反应的化学方程式:________________________________。
4
②滤渣Ⅰ中主要成分的形成可用离子方程式表示为__________________________________。
答案 ①4FeWO+O+8NaOH=====2Fe O+4NaWO+4HO
4 2 2 3 2 4 2
②AlO+CO+2HO===Al(OH) ↓+HCO
2 2 3
解析 ①根据流程图,FeWO 在碱熔过程中,得到Fe O 和NaWO ,反应物是NaOH、
4 2 3 2 4
FeWO 、O ,生成物是NaWO 、Fe O 等,FeWO 中Fe显+3价,W显+5价,NaWO 中
4 2 2 4 2 3 4 2 4
W显+6价,FeWO 为还原剂,O 为氧化剂,因此根据化合价升降法进行配平,得到化学方
4 2
程式为4FeWO+O+8NaOH=====2Fe O+4NaWO+4HO。
4 2 2 3 2 4 2
(2)软锰矿的主要成分为 MnO ,含少量 Al O 和SiO 。闪锌矿主要成分为 ZnS,含少量
2 2 3 2
FeS、CuS、CdS杂质。现以软锰矿和闪锌矿为原料制备MnO 和Zn,其简化流程如下(中间
2
产物的固体部分已经略去)。
―――→――→――→
――→
①中发生多个反应,其中MnO 、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,
2
写出MnO 、FeS与硫酸共热发生反应的化学方程式:________________________________。
2
答案 3MnO +2FeS+6HSO =====Fe (SO )+3MnSO +2S↓+6HO
2 2 4 2 4 3 4 2
解析 ①中MnO 、FeS与硫酸共热时有淡黄色的S析出,溶液变为棕黄色,说明有Fe3+生
2成,发生反应的化学方程式为 3MnO +2FeS+6HSO =====Fe (SO ) +3MnSO +2S↓+
2 2 4 2 4 3 4
6HO。
2
(3)含FeS 的燃煤可用氧化亚铁硫杆菌(T.f)、氧化亚铁微螺菌(L.f)、氧化硫硫杆菌(T.t)进行脱
2
硫,其脱硫过程如图所示:
已知:脱硫总反应为FeS+14Fe3++8HO===2SO+15Fe2++16H+;
2 2
Ⅰ反应的离子方程式为FeS+6Fe3++3HO===SO+7Fe2++6H+。
2 2 2
写出Ⅱ反应的离子方程式:________________________________________________________。
答案 8Fe3++SO+5HO===2SO+8Fe2++10H+
2 2
解析 反应Ⅱ是Fe3+和SO反应生成亚铁离子和硫酸根离子。
2
8.(1)高锰酸钾纯度的测定:称取1.080 0 g样品,溶解后定容于100 mL容量瓶中,摇匀。
取浓度为0.200 0 mol·L-1的HC O 标准溶液20.00 mL,加入稀硫酸酸化,用KMnO 溶液平
2 2 4 4
行 滴 定 三 次 , 平 均 消 耗 的 体 积 为 24.48 mL , 该 样 品 的 纯 度 为
__________________________(保留小数点后两位)。
答案 95.62%
解析 根据离子方程式2MnO+5HC O+6H+===2Mn2++10CO↑+8HO可知KMnO 与草
2 2 4 2 2 4
酸反应的关系式是:2KMnO ~5HC O 。配制的溶液的浓度为:c= mol·L-1。则1.080 0 g样
4 2 2 4
品中含KMnO 的物质的量为:n= L×mol·L-1≈0.006 536 mol,KMnO 的质量为:m=
4 4
0.006 536 mol×158 g·mol-1=1.032 688 g。故其纯度为:w=×100%≈95.62%。
(2)为测定产品中KCr O 的含量,某兴趣小组将m g产品溶于水配制为500 mL溶液,准确
2 2 7
量取50.00 mL,加入稀硫酸酸化,然后加入过量的KI充分还原,加________作指示剂,到
达终点消耗30.00 mL 0.050 0 mol·L-1的NaSO 溶液。则该次生产的样品中KCr O 含量为
2 2 3 2 2 7
________%。(已知:Cr O+6I-+14H+===2Cr3++3I +7HO,2Na SO +I===NaSO +
2 2 2 2 2 3 2 2 4 6
2NaI)
答案 淀粉溶液
解析 有碘单质存在,可以选用淀粉溶液作指示剂;根据化学反应:Cr O+6I-+14H+
2
===2Cr3++3I +7HO和I +2SO===2I-+SO,可得Cr O~3I ~6SO,m g产品最终消耗
2 2 2 2 4 2 2 2
n(S O)=0.050 0 mol·L-1×30.00×10-3L×=0.015 0 mol,则n(CrO)=0.015 0 mol×=0.002
2 2
50 mol,则样品中KCr O 含量为×100%=%。
2 2 7