文档内容
第 41 讲 溶液中“粒子”浓度关系
复习目标 1.理解电解质溶液中的电离平衡和水解平衡。2.掌握溶液中各组分之间的守恒
关系与大小比较。3.学会分析不同类型图像中各离子浓度之间的关系。
考点一 “粒子”浓度关系判断
1.熟悉两大理论,构建思维基点
(1)电离理论
①弱电解质的电离是微弱的,电离产生的微粒都非常少,同时还要考虑水的电离,如氨水溶
液中:NH ·H O、NH、OH-浓度的大小关系是c(NH ·H O)>c(OH-)>c(NH)。
3 2 3 2
②多元弱酸的电离是分步进行的,其主要是第一步电离(第一步电离程度远大于第二步电离)。
如在HS溶液中:HS、HS-、S2-、H+的浓度大小关系是c(H S)>c(H+)>c(HS-)>c(S2-)。
2 2 2
(2)水解理论
①弱电解质离子的水解损失是微量的(双水解除外),但由于水的电离,故水解后酸性溶液中
c(H+)或碱性溶液中c(OH-)总是大于水解产生的弱电解质的浓度。如NH Cl溶液中:NH、
4
Cl-、NH ·H O、H+的浓度大小关系是c(Cl-)>c(NH)>c(H+)>c(NH ·H O)。
3 2 3 2
②多元弱酸酸根离子的水解是分步进行的,其主要是第一步水解,如在 NaCO 溶液中:
2 3
CO、HCO、HCO 的浓度大小关系应是c(CO)>c(HCO)>c(H CO)。
2 3 2 3
2.把握三种守恒,明确等量关系
(1)电荷守恒规律
电解质溶液中,无论存在多少种离子,溶液都呈电中性,即阴离子所带负电荷总数一定等于
阳离子所带正电荷总数。如NaHCO 溶液中存在着Na+、H+、HCO、CO、OH-,存在如下
3
关系:c(Na+)+c(H+)=c(HCO)+c(OH-)+2c(CO)。
(2)物料守恒规律
电解质溶液中,由于某些离子能够水解,离子种类增多,但元素总是守恒的。如KS溶液中
2
S2-、HS-都能水解,故S元素以S2-、HS-、HS三种形式存在,它们之间有如下守恒关系:
2
c(K+)=2c(S2-)+2c(HS-)+2c(H S)。
2
(3)质子守恒规律
如NaS水溶液中的质子转移情况图示如下:
2由图可得NaS水溶液中质子守恒式可表示:c(H O+)+2c(H S)+c(HS-)=c(OH-)或c(H+)+
2 3 2
2c(H S)+c(HS-)=c(OH-)。质子守恒的关系式也可以由电荷守恒式与物料守恒式推导得到。
2
(1)弱酸、弱碱的电离和盐的水解是微弱的,但水的电离程度远远小于弱酸、弱碱的电离和
盐的水解。所以在稀醋酸溶液中:c(CHCOOH)>c(H+)>c(CHCOO-)>c(OH-);在
3 3
CHCOONa溶液中:c(Na+)>c(CHCOO-)>c(OH-)>c(CHCOOH)>c(H+)。
3 3 3
(2)电荷守恒式中不只是各离子浓度的简单相加,如2c(CO)的化学计量数2代表一个CO带2
个负电荷,不可漏掉;物料守恒式中,离子浓度系数不能漏写或颠倒,如 NaS溶液中的物
2
料守恒式中,“2”表示c(Na+)是溶液中各种硫元素存在形式的硫原子总浓度的2倍。
1.粒子种类的判断
(1)NaHCO 溶液中:_____________________________________________________________。
3
(2)向NaOH溶液中通入CO 气体(任意量):_________________________________________。
2
答案 (1)(2)粒子种类都是离子:Na+、CO、HCO、OH-、H+;分子:HCO、HO
2 3 2
2.0.1 mol·L-1的NaCO 溶液中各离子浓度的关系
2 3
(1)大小关系:__________________________________________________________________。
(2)物料守恒:__________________________________________________________________。
(3)电荷守恒:__________________________________________________________________。
(4)质子守恒:__________________________________________________________________。
答案 (1)c(Na+)>c(CO)>c(OH-)>c(HCO)>c(H+)
(2)c(Na+)=2[c(CO)+c(HCO)+c(H CO)]
2 3
(3)c(Na+)+c(H+)=c(HCO)+c(OH-)+2c(CO)
(4)c(OH-)=c(H+)+2c(H CO)+c(HCO)
2 3
解析 NaCO===2Na++CO(完全电离),
2 3
CO+HOHCO+OH-(主要),
2
HCO+HOHCO+OH-(次要),
2 2 3
HOH++OH-(极微弱)。
2
3.等浓度的NaOH和CHCOOH按1∶2体积比混合后pH<7
3
(1)离子浓度大小顺序为_________________________________________________________。
(2)电荷守恒式:_______________________________________________________________。(3)物料守恒式:_______________________________________________________________。
答案 (1)c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
(2)c(CHCOO-)+c(OH-)=c(Na+)+c(H+)
3
(3)2c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
解析 中和反应后,溶质为等量的CHCOONa、CHCOOH,且CHCOOH的电离程度大于
3 3 3
CHCOONa的水解程度,c(CHCOO-)与c(CHCOOH)浓度之和等于c(Na+)的2倍。
3 3 3
4.25 ℃时,相同物质的量浓度的下列溶液中:
①NH Cl、②CHCOONH 、③NH HSO 、④(NH )SO 、⑤(NH )Fe(SO ) ,c(NH)由大到小
4 3 4 4 4 4 2 4 4 2 4 2
的顺序为___________________________。
答案 ⑤>④>③>①>②
解析 分析流程为
分组―――――→
题组一 单一溶液中离子浓度大小的比较
1室温下,下列指定溶液中微粒的浓度关系正确的是( )
A.0.1 mol·L-1(NH )SO 溶液:c(SO)>c(NH)>c(H+)>c(OH-)
4 2 4
B.0.1 mol·L-1NaCO 溶液:c(OH-)=c(H+)+c(HCO)+c(H CO)
2 3 2 3
C.0.1 mol·L-1明矾溶液:c(SO)>c(K+)>c(Al3+)>c(H+)>c(OH-)
D.0.1 mol·L-1的NaHCO 溶液:c(Na+)=c(HCO)+c(H CO)+2c(CO)
3 2 3
答案 C
解析 0.1 mol·L-1(NH )SO 溶液中铵根离子水解,溶液显酸性,但水解程度不大,则c(NH)
4 2 4
>c(SO)>c(H+)>c(OH-),A 错误;根据质子守恒,应是 c(OH-)=c(H+)+c(HCO)+
2c(H CO),B错误;明矾溶液中Al3+发生水解,C正确;由物料守恒知,c(CO)不应乘以
2 3
2,D错误。
2.HA为酸性略强于醋酸的一元弱酸,在0.1 mol·L-1NaA溶液中,离子浓度关系正确的是(
)
A.c(Na+)>c(A-)>c(H+)>c(OH-)
B.c(Na+)>c(OH-)>c(A-)>c(H+)
C.c(Na+)+c(OH-)=c(A-)+c(H+)
D.c(Na+)+c(H+)=c(A-)+c(OH-)
答案 D
解析 由题意可知,NaA溶液水解显碱性,则c(Na+)>c(A-)>c(OH-)>c(H+)。水解是微
弱的反应,因此水解生成的OH-浓度远小于未水解的A-浓度,A、B项错;电荷守恒表达
式应为c(Na+)+c(H+)=c(OH-)+c(A-),C项错。3.常温下,浓度均为0.1 mol·L-1的下列溶液中,粒子的物质的量浓度关系正确的是( )
A.氨水中,c(NH)=c(OH-)=0.1 mol·L-1
B.NH Cl溶液中,c(NH)>c(Cl-)
4
C.NaSO 溶液中,c(Na+)>c(SO)>c(OH-)=c(H+)
2 4
D.NaSO 溶液中,c(Na+)=2c(SO)+c(HSO)+c(H SO )
2 3 2 3
答案 C
解析 氨水为弱碱溶液,只能部分电离出OH-,结合电荷守恒c(NH)+c(H+)=c(OH-),可
得c(NH)<c(OH-)<0.1 mol·L-1,A错误;NH Cl溶液中,NH部分水解、Cl-浓度不变,则
4
溶液中c(NH)<c(Cl-),B错误;NaSO 溶液显中性,c(OH-)=c(H+),结合电荷守恒可得
2 4
c(Na+)=2c(SO),溶液中离子浓度大小为 c(Na+)>c(SO)>c(OH-)=c(H+),C正确;根据
NaSO 溶液中的物料守恒可得c(Na+)=2c(SO)+2c(HSO)+2c(H SO ),D错误。
2 3 2 3
题组二 混合溶液中离子浓度大小的比较
4.用物质的量都是 0.1 mol 的 CHCOOH 和 CHCOONa 配成 1 L 混合溶液,已知其中
3 3
c(CHCOO-)>c(Na+),对该溶液的下列判断正确的是( )
3
A.c(H+)>c(OH-)
B.c(CHCOO-)=0.1 mol·L-1
3
C.c(CHCOOH)>c(CHCOO-)
3 3
D.c(CHCOO-)+c(OH-)=0.1 mol·L-1
3
答案 A
解析 由电荷守恒:c(CHCOO-)+c(OH-)=c(Na+)+c(H+),因c(CHCOO-)>c(Na+),则
3 3
c(H + )
>c(OH-);由物料守恒:c(CHCOOH)+c(CHCOO-)=0.2 mol·L-1,因c(CHCOO-)>c(Na
3 3 3
+)=0.1 mol·L-1,则c(CHCOO-)>c(CHCOOH)。
3 3
5.25 ℃时,在10 mL浓度均为0.1 mol·L-1 的NaOH和NH ·H O混合溶液中滴加0.1 mol·L-
3 2
1的盐酸。下列有关溶液中粒子浓度关系正确的是( )
A.未加盐酸时:c(OH-)>c(Na+)=c(NH ·H O)
3 2
B.加入10 mL盐酸时:c(NH)+c(H+)=c(OH-)
C.加入盐酸至溶液pH=7时:c(Cl-)=c(Na+)
D.加入20 mL盐酸时: c(Cl-)=c(NH)+c(Na+)
答案 B
解析 A项,NH ·H O是弱电解质,能部分电离,溶液中c(Na+)>c(NH ·H O);B项,当加
3 2 3 2
入10 mL盐酸时,恰好将NaOH中和完,溶液中c(Na+)=c(Cl-),根据电荷守恒:c(Na+)+
c(NH)+c(H+)=c(Cl-)+c(OH-)可知,c(NH)+c(H+)=c(OH-);C项,溶液pH=7时,溶液
中c(H+)=c(OH-) ,根据电荷守恒可知c(Na+)+c(NH)=c(Cl-);D项,加入20 mL盐酸时,
恰好将NaOH和NH ·H O中和完,根据物料守恒有c(Na+)+c(NH)+c(NH ·H O)=c(Cl-)。
3 2 3 26.(2019·浙江4月选考,21)室温下,取20 mL 0.1 mol·L-1某二元酸HA,滴加0.2 mol·L-1
2
NaOH溶液。
已知:HA===H++HA-,HA-H++A2-。下列说法不正确的是( )
2
A.0.1 mol·L-1 HA溶液中有c(H+)-c(OH-)-c(A2-)=0.1 mol·L-1
2
B.当滴加至中性时,溶液中c(Na+)=c(HA-)+2c(A2-),用去NaOH溶液的体积小于10 mL
C.当用去NaOH溶液体积10 mL时,溶液的pH<7,此时溶液中有c(A2-)=c(H+)-c(OH
-)
D.当用去NaOH溶液体积20 mL时,此时溶液中有c(Na+)=2c(HA-)+2c(A2-)
答案 B
解析 0.1 mol·L-1HA溶液存在电荷守恒,其关系为c(H+)=c(OH-)+2c(A2-)+c(HA-),因
2
而c(H+)-c(OH-)-c(A2-)=c(A2-)+c(HA-)=0.1 mol·L-1,A项正确;若NaOH用去10
mL,反应得到NaHA溶液,由于HA-H++A2-,溶液显酸性,因而滴加至中性时,需要
加入超过10 mL的NaOH溶液,B项错误;当用去NaOH溶液体积10 mL时,得到NaHA溶
液,溶液的pH<7,存在质子守恒,其关系为c(A2-)=c(H+)-c(OH-),C项正确;当用去
NaOH溶液体积20 mL时,得到NaA溶液,根据物料守恒有c(Na+)=2c(HA-)+2c(A2-),D
2
项正确。
题组三 不同溶液中同一离子浓度大小的比较
7.下列5种混合溶液,分别由0.1 mol·L-1的两种溶液等体积混合而成:①CHCOONa与
3
NaHSO ,② CHCOONa 与 NaOH,③ CHCOONa 与 NaCl,④ CHCOONa 与 NaHCO ,
4 3 3 3 3
⑤CHCOONa与NaHSO。下列各项排序正确的是( )
3 3
A.pH:②>④>⑤>③>①
B.c(CHCOOH):①>③>⑤>④>②
3
C.c(CHCOO-):②>③>④>⑤>①
3
D.:①>⑤>③>④>②
答案 D
解析 A项中pH的大小关系为②>④>③>⑤>①;B项中c(CHCOOH)的大小关系为①
3
>⑤>③>④>②;C项中c(CHCOO-)的大小关系为②>④>③>⑤>①;D项中的大小
3
关系为①>⑤>③>④>②,故正确。
8.比较下列几组溶液中指定离子浓度的大小。
(1)浓度均为0.1 mol·L-1的①HS、②NaHS、③NaS、④HS和NaHS混合液,溶液pH从
2 2 2
大到小的顺序是______________。
(2)相同浓度的下列溶液中:①CHCOONH 、②CHCOONa、③CHCOOH,c(CHCOO-)
3 4 3 3 3
由大到小的顺序是_____________________________________________________。
(3)c(NH)相等的①(NH )SO 溶液、②NH HSO 溶液、③(NH )CO 溶液、④NH Cl溶液,其
4 2 4 4 4 4 2 3 4
物质的量浓度由大到小的顺序为________________________________________________。答案 (1)③>②>④>① (2)②>①>③ (3)④>②>③>①
比较电解质溶液中粒子浓度相对大小的解题思路
考点二 离子浓度与曲线关系图
滴定过程中,离子浓度动态分析
关键点 溶液中溶质成分及粒子浓度大小关系
溶质是CHCOOH
3
V(NaOH)=0(0点) 粒子浓度大小关系: c (CH COOH) > c (H
3
常温下,用0.100 0 mol·L- + ) > c (CH COO - ) > c (OH - )
3
1 NaOH溶液滴定20.00 溶质是等物质的量的CHCOOH 和
3
mL 0.100 0 mol·L- V(NaOH)=10 mL CHCOONa
3
1CHCOOH溶液 (点①) 粒子浓度大小关系: c (CH COO - ) > c (Na
3 3
+ ) > c (CH COOH) > c (H + ) > c (OH - )
3
溶质是CHCOONa 和少量的CHCOOH
3 3
pH=7(点②) 粒子浓度大小关系: c (Na + ) = c (CH COO
3
- ) > c (H + ) = c (OH - )
溶质是CHCOONa
3
V(NaOH)=20 mL
粒子浓度大小关系: c (Na + ) > c (CH COO
3
(点③)
- ) > c (OH - ) > c (H + )溶质是等物质的量的CHCOONa 和
3
NaOH
V(NaOH)=40 mL
粒子浓度大小关系: c (Na + ) > c (OH - ) >
c (CH COO - ) > c (H + )
3
题组一 一元弱酸(或弱碱)中和反应过程中曲线分析
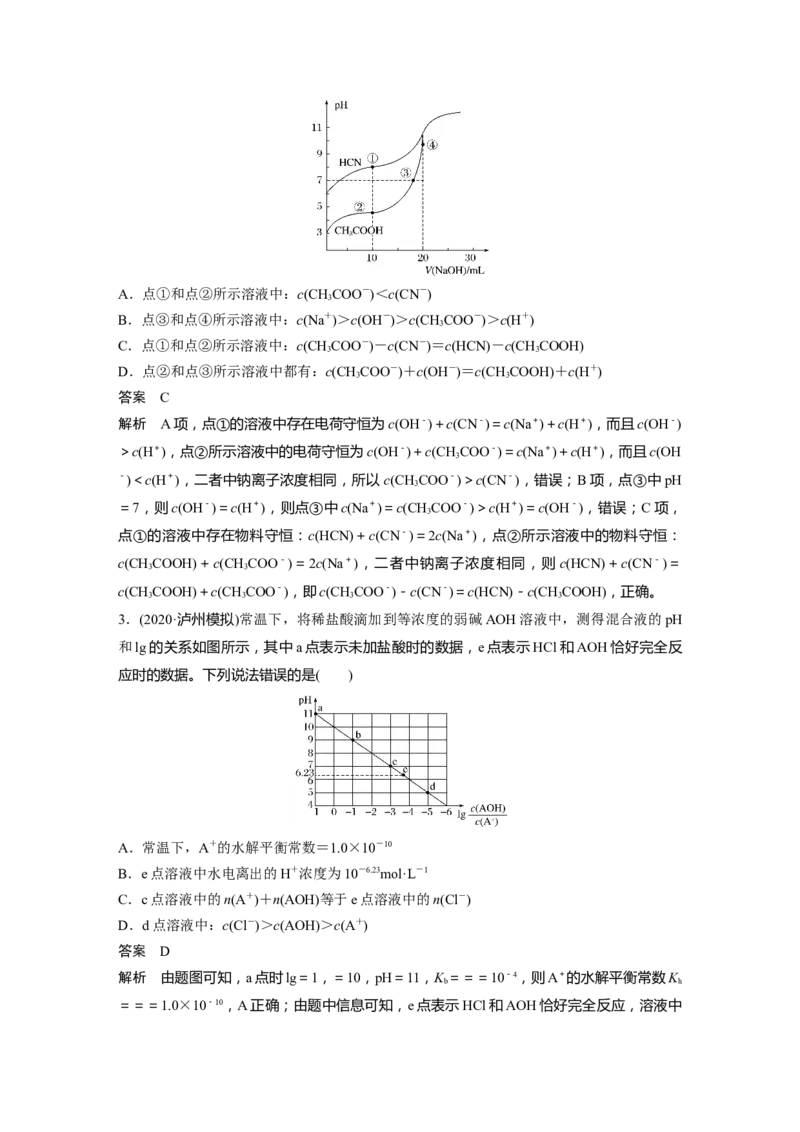
1.常温下,在10 mL 0.1 mol·L-1MOH溶液中滴加pH=1的盐酸,溶液中AG(AG=lg)与盐
酸体积(V)之间的关系如图所示。
下列说法错误的是( )
A.常温下,MOH的电离常数约为1×10-5
B.E、F、G和P点中,G点水电离程度最大
C.G点对应的溶液中:c(Cl-)>c(M+)>c(H+)>c(OH-)
D.P点溶液中:c(Cl-)=2c(MOH)+2c(M+)
答案 C
解析 E点表示未滴定时MOH溶液中lg=8,c(OH-)=1×10-3mol·L-1,MOH的电离常数
K =≈1×10-5,故A正确;G点接近酸和碱恰好完全反应,在E、F、G和P点中,G点水
b
电离程度最大,故B正确;G点对应的溶液pH=7,c(M+)=c(Cl-)>c(H+)=c(OH-),故C
错误;P点,加入盐酸体积是MOH溶液的2倍,pH=1的盐酸浓度为0.1 mol·L-1,根据物
料守恒知,c(Cl-)=2c(MOH)+2c(M+),故D正确。
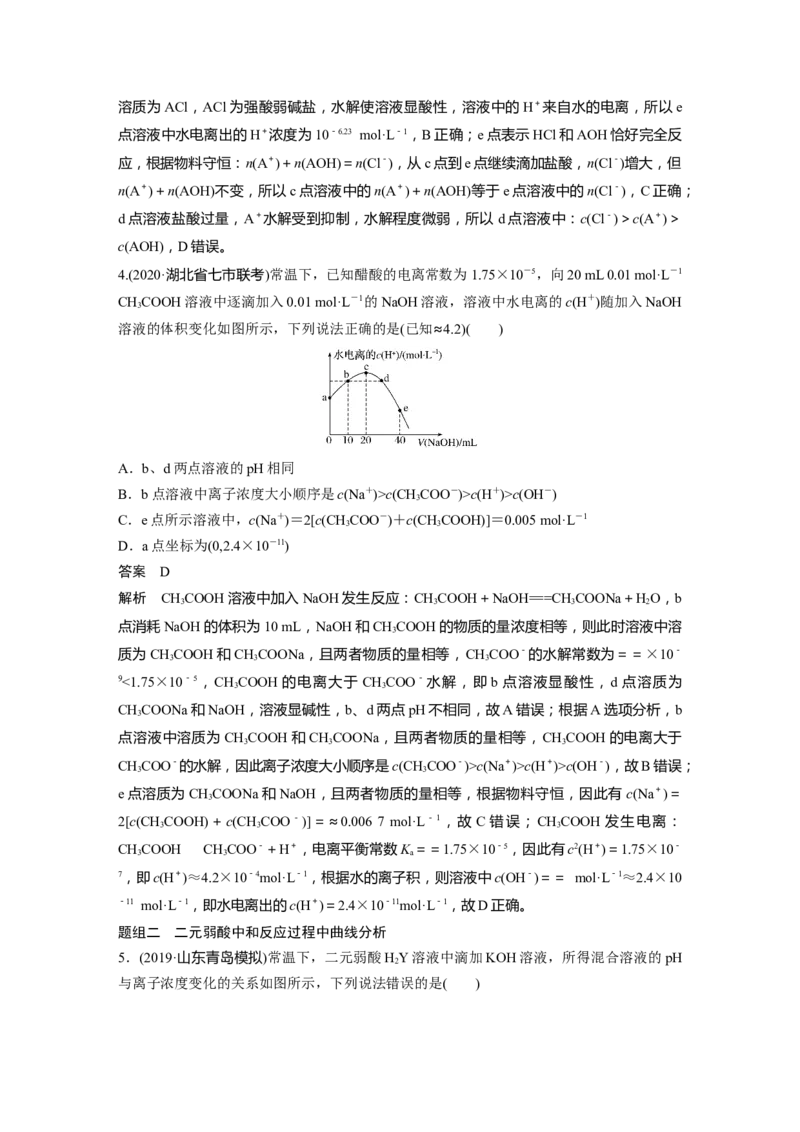
2.(2020·石家庄模拟)常温下,用 0.10 mol·L-1 NaOH溶液分别滴定 20.00 mL浓度均为
0.10 mol·L-1 CHCOOH溶液和HCN溶液所得滴定曲线如下图。下列说法正确的是( )
3A.点①和点②所示溶液中:c(CHCOO-)<c(CN-)
3
B.点③和点④所示溶液中:c(Na+)>c(OH-)>c(CHCOO-)>c(H+)
3
C.点①和点②所示溶液中:c(CHCOO-)-c(CN-)=c(HCN)-c(CHCOOH)
3 3
D.点②和点③所示溶液中都有:c(CHCOO-)+c(OH-)=c(CHCOOH)+c(H+)
3 3
答案 C
解析 A项,点①的溶液中存在电荷守恒为c(OH-)+c(CN-)=c(Na+)+c(H+),而且c(OH-)
>c(H+),点②所示溶液中的电荷守恒为c(OH-)+c(CHCOO-)=c(Na+)+c(H+),而且c(OH
3
-)<c(H+),二者中钠离子浓度相同,所以 c(CHCOO-)>c(CN-),错误;B项,点③中pH
3
=7,则c(OH-)=c(H+),则点③中c(Na+)=c(CHCOO-)>c(H+)=c(OH-),错误;C项,
3
点①的溶液中存在物料守恒:c(HCN)+c(CN-)=2c(Na+),点②所示溶液中的物料守恒:
c(CHCOOH)+c(CHCOO-)=2c(Na+),二者中钠离子浓度相同,则 c(HCN)+c(CN-)=
3 3
c(CHCOOH)+c(CHCOO-),即c(CHCOO-)-c(CN-)=c(HCN)-c(CHCOOH),正确。
3 3 3 3
3.(2020·泸州模拟)常温下,将稀盐酸滴加到等浓度的弱碱AOH溶液中,测得混合液的pH
和lg的关系如图所示,其中a点表示未加盐酸时的数据,e点表示HCl和AOH恰好完全反
应时的数据。下列说法错误的是( )
A.常温下,A+的水解平衡常数=1.0×10-10
B.e点溶液中水电离出的H+浓度为10-6.23mol·L-1
C.c点溶液中的n(A+)+n(AOH)等于e点溶液中的n(Cl-)
D.d点溶液中:c(Cl-)>c(AOH)>c(A+)
答案 D
解析 由题图可知,a点时lg=1,=10,pH=11,K ===10-4,则A+的水解平衡常数K
b h
===1.0×10-10,A正确;由题中信息可知,e点表示HCl和AOH恰好完全反应,溶液中溶质为ACl,ACl为强酸弱碱盐,水解使溶液显酸性,溶液中的H+来自水的电离,所以e
点溶液中水电离出的H+浓度为10-6.23 mol·L-1,B正确;e点表示HCl和AOH恰好完全反
应,根据物料守恒:n(A+)+n(AOH)=n(Cl-),从c点到e点继续滴加盐酸,n(Cl-)增大,但
n(A+)+n(AOH)不变,所以c点溶液中的n(A+)+n(AOH)等于e点溶液中的n(Cl-),C正确;
d点溶液盐酸过量,A+水解受到抑制,水解程度微弱,所以 d点溶液中:c(Cl-)>c(A+)>
c(AOH),D错误。
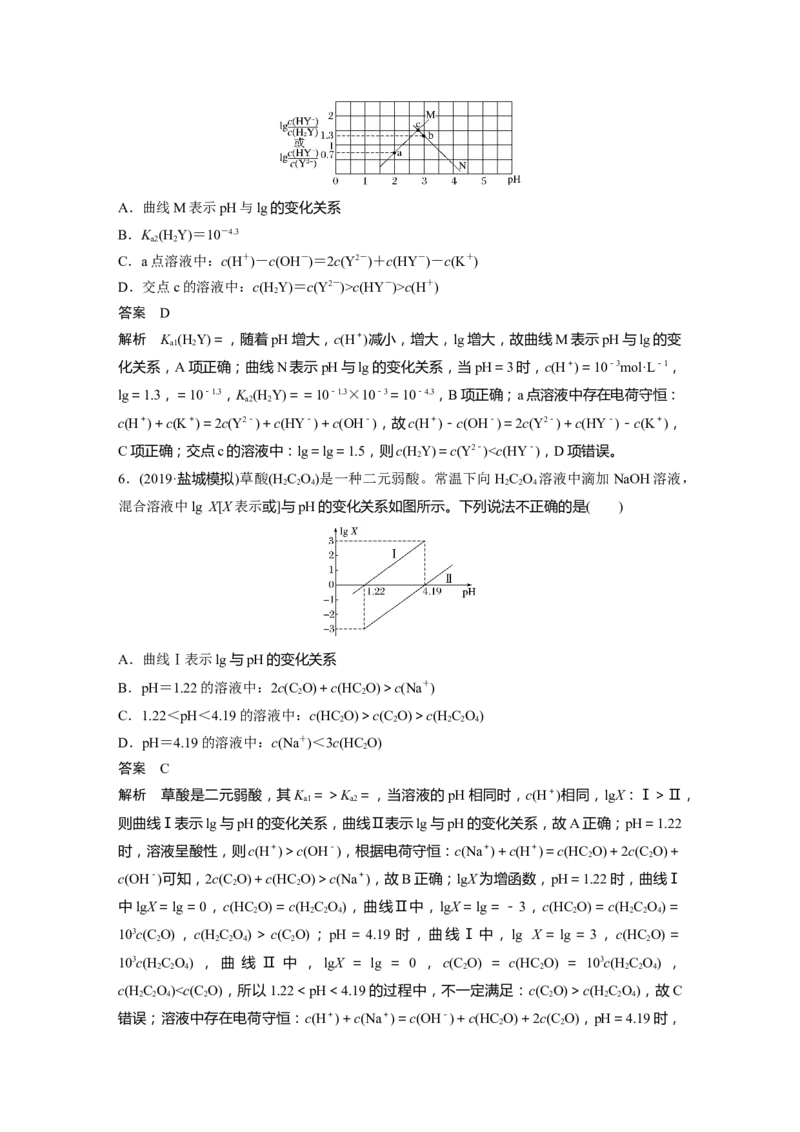
4.(2020·湖北省七市联考)常温下,已知醋酸的电离常数为1.75×10-5,向20 mL 0.01 mol·L-1
CHCOOH溶液中逐滴加入0.01 mol·L-1的NaOH溶液,溶液中水电离的c(H+)随加入NaOH
3
溶液的体积变化如图所示,下列说法正确的是(已知≈4.2)( )
A.b、d两点溶液的pH相同
B.b点溶液中离子浓度大小顺序是c(Na+)>c(CHCOO-)>c(H+)>c(OH-)
3
C.e点所示溶液中,c(Na+)=2[c(CHCOO-)+c(CHCOOH)]=0.005 mol·L-1
3 3
D.a点坐标为(0,2.4×10-11)
答案 D
解析 CHCOOH溶液中加入NaOH发生反应:CHCOOH+NaOH===CHCOONa+HO,b
3 3 3 2
点消耗NaOH的体积为10 mL,NaOH和CHCOOH的物质的量浓度相等,则此时溶液中溶
3
质为CHCOOH和CHCOONa,且两者物质的量相等,CHCOO-的水解常数为==×10-
3 3 3
9<1.75×10-5,CHCOOH 的电离大于 CHCOO-水解,即 b 点溶液显酸性,d 点溶质为
3 3
CHCOONa和NaOH,溶液显碱性,b、d两点pH不相同,故A错误;根据A选项分析,b
3
点溶液中溶质为CHCOOH和CHCOONa,且两者物质的量相等,CHCOOH的电离大于
3 3 3
CHCOO-的水解,因此离子浓度大小顺序是c(CHCOO-)>c(Na+)>c(H+)>c(OH-),故B错误;
3 3
e点溶质为CHCOONa和NaOH,且两者物质的量相等,根据物料守恒,因此有 c(Na+)=
3
2[c(CHCOOH)+c(CHCOO-)]=≈0.006 7 mol·L-1,故 C 错误;CHCOOH 发生电离:
3 3 3
CHCOOHCHCOO-+H+,电离平衡常数K==1.75×10-5,因此有c2(H+)=1.75×10-
3 3 a
7,即c(H+)≈4.2×10-4mol·L-1,根据水的离子积,则溶液中c(OH-)== mol·L-1≈2.4×10
-11 mol·L-1,即水电离出的c(H+)=2.4×10-11mol·L-1,故D正确。
题组二 二元弱酸中和反应过程中曲线分析
5.(2019·山东青岛模拟)常温下,二元弱酸HY溶液中滴加KOH溶液,所得混合溶液的pH
2
与离子浓度变化的关系如图所示,下列说法错误的是( )A.曲线M表示pH与lg的变化关系
B.K (H Y)=10-4.3
a2 2
C.a点溶液中:c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(K+)
D.交点c的溶液中:c(H Y)=c(Y2-)>c(HY-)>c(H+)
2
答案 D
解析 K (H Y)=,随着pH增大,c(H+)减小,增大,lg增大,故曲线M表示pH与lg的变
a1 2
化关系,A项正确;曲线N表示pH与lg的变化关系,当pH=3时,c(H+)=10-3mol·L-1,
lg=1.3,=10-1.3,K (H Y)==10-1.3×10-3=10-4.3,B项正确;a点溶液中存在电荷守恒:
a2 2
c(H+)+c(K+)=2c(Y2-)+c(HY-)+c(OH-),故c(H+)-c(OH-)=2c(Y2-)+c(HY-)-c(K+),
C项正确;交点c的溶液中:lg=lg=1.5,则c(H Y)=c(Y2-)c(SO)
>c(H SO )
2 3
D.直线Ⅱ中M、N点一定存在c2(HSO)>c(SO)·c(H SO )
2 3
答案 C
解析 通入少量二氧化硫的过程中,溶液的酸性增强,直线Ⅱ中的N点向M点移动;K
a1
=,则lg K =lg+lg c(H+),lg=lgK +pH,同理可得lg=lgK +pH,故α =α 一定等于
a1 a1 a2 1 2
45°;由图像可知,当对应溶液的pH处于1.810,溶液中c(H SO )、
2 3
c(SO)的大小无法确定;由于K >K ,>,则c2(HSO)>c(SO)·c(H SO )。
a1 a2 2 3
题组四 各粒子分布分数的曲线分析
9.LiH PO 是制备电池的重要原料。室温下,LiH PO 溶液的pH随c (H PO)的变化如图1
2 4 2 4 初始 2
所示,HPO 溶液中HPO的分布分数δ随pH的变化如图2所示。下列有关LiH PO 溶液的
3 4 2 2 4
叙述正确的是( )
A.溶液中存在3个平衡
B.含P元素的粒子有HPO、HPO和PO
2
C.随c (H PO)增大,溶液的pH明显变小
初始 2
D.用浓度大于1 mol·L-1的HPO 溶液溶解LiCO ,当pH达到4.66时,HPO 几乎全部转
3 4 2 3 3 4
化为LiH PO
2 4
答案 D
解析 根据图1可知:当LiH PO 的浓度大于1 mol·L-1时其pH=4.66,根据图2可知,当
2 4
pH=4.66 时 HPO 的分布分数达到 0.994,即 HPO 几乎全部转化为 LiH PO ,D 对;
2 3 4 2 4
LiH PO 溶液中存在HPO的电离平衡、HPO的电离平衡、HPO的水解平衡、HO的电离平
2 4 2 2 2
衡等至少4个平衡,A错;LiH PO 溶液中含P元素的粒子有HPO、HPO、PO和HPO ,B
2 4 2 3 4
错;LiH PO 溶液的pH随着HPO初始浓度的增大逐渐减小,但当 HPO的浓度增大到
2 4 2 2
10-1 mol·L-1时,浓度再增大,溶液的pH基本不变,C错。
10.(2020·武汉质检)亚砷酸(H AsO )可以用于治疗白血病,在溶液中存在多种微粒形态。向
3 3
1 L 0.1 mol·L-1 HAsO 溶液中逐滴加入KOH溶液,各种微粒物质的量分数与溶液的pH关
3 3
系如图所示。下列说法正确的是( )A.HAsO 的电离常数K 的数量级为10-9
3 3 a1
B.pH在8.0~10.0时,反应的离子方程式:HAsO +OH-===HAsO+HO
3 3 2 2
C.M点对应的溶液中:c(H AsO)+c(HAsO)+c(AsO)+c(H AsO )=0.1 mol·L-1
2 3 3
D.pH=12时,溶液中:c(H AsO)+2c(HAsO)+3c(AsO)+c(H AsO )>c(H+)+c(K+)
2 3 3
答案 B
解析 由图中数据可知,pH=9.3时,c(H AsO)=c(H AsO ),故HAsO 的电离常数K ==
2 3 3 3 3 a1
c(H+)=10-9.3,故K 的数量级为10-10,A项错误;由图可知,pH在8.0~10.0时,HAsO
a1 3 3
的物质的量分数逐渐减小、HAsO 的物质的量分数逐渐增大,故反应的离子方程式为
2
HAsO +OH-===HAsO+HO,B 项正确;根据物料守恒可知,M 点对应的溶液中,
3 3 2 2
n(H AsO)+n(HAsO)+n(AsO)+n(H AsO )=0.1 mol,由于不知道此时溶液的体积是多少(或
2 3 3
不知道加入KOH溶液的体积),故其总浓度小于0.1 mol·L-1,C项错误;由电荷守恒可知,
c(H AsO)+2c(HAsO)+3c(AsO)+c(OH-)=c(H+)+c(K+),pH=12时,溶液显碱性,由图可
2
知,此时HAsO 主要转化为HAsO和HAsO,说明HAsO和HAsO的电离作用小于HAsO
3 3 2 2 2
和HAsO的水解作用,HAsO和HAsO水解都产生OH-,故c(OH-)>c(H AsO ),因此,溶
2 3 3
液中c(H AsO)+2c(HAsO)+3c(AsO)+c(H AsO )<c(H+)+c(K+),D项错误。
2 3 3
对数图像的解题策略
(1)先确定图像的类型是对数图像还是负对数图像。
(2)再弄清楚图像中横坐标和纵坐标的含义,是浓度对数还是比值对数。
(3)抓住图像中特殊点:如pH=7,lg x=0,交叉点。
(4)理清图像中曲线的变化趋势及含义,根据含义判断线上、线下的点所表示的意义。
(5)将图像中数据或曲线的变化与所学知识对接,作出选项的正误判断。
1.(2020·全国卷Ⅰ,13)以酚酞为指示剂,用0.100 0 mol·L-1的NaOH溶液滴定20.00 mL未
知浓度的二元酸HA溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V 的变化关
2 NaOH
系如下图所示。[比如A2-的分布系数:δ(A2-)=]下列叙述正确的是( )
A.曲线①代表δ(H A),曲线②代表δ(HA-)
2
B.HA溶液的浓度为0.200 0 mol·L-1
2
C.HA-的电离常数K=1.0×10-2
a
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
答案 C
解析 根据图像可知,滴定终点消耗NaOH溶液40 mL,HA是二元酸,可知酸的浓度是
2
0.100 0 mol·L-1,B项错误;起点溶液pH=1.0,c(H+)=0.100 0 mol·L-1,可知HA第一步
2
电离是完全的,溶液中没有HA,所以曲线①代表δ(HA-),曲线②代表δ(A2-),A项错误;
2
由图可知,当δ(A2-)=δ(HA-)时,pH=2.0,c(H+)=1.0×10-2 mol·L-1,HA-A2-+H
+,K(HA-)==1.0×10-2,C项正确;滴定终点时,根据电荷守恒c(Na+)+c(H+)=2c(A2-)
a
+c(HA-)+c(OH-),以酚酞为指示剂,说明滴定终点时溶液呈碱性,c(OH-)>c(H+),所以
c(Na+)>2c(A2-)+c(HA-),D项错误。
2.[2020·新高考全国卷Ⅰ(山东),15改编]25 ℃时,某混合溶液中c(CHCOOH)+c(CHCOO
3 3
-)
=0.1 mol·L-1,lg c(CHCOOH)、lg c(CHCOO-)、lg c(H+)和lg c(OH-)随pH变化的关系
3 3
如下图所示。K 为CHCOOH的电离常数,下列说法正确的是( )
a 3
A.O点时,c(CHCOOH)=c(CHCOO-)
3 3
B.N点时,pH=lg K
a
C.该体系中,c(CHCOOH)= mol·L-1
3
D.pH由7到14的变化过程中,CHCOO-的水解程度始终增大
3
答案 C
解析 随着溶液碱性的增强,c(CHCOOH)减小,c(CHCOO-)增大,故 MN 线表示
3 3lgc(CHCOO-),NP线表示lgc(CHCOOH),MO线表示lgc(H+),OP线表示lgc(OH-)。O点
3 3
时,c(H+)=c(OH-),N 点时,c(CHCOOH)=c(CHCOO-),A 项错误;N 点时,
3 3
lgc(CHCOOH)与lgc(CHCOO-)相等,故c(H+)=K,pH=-lgK,B项错误;由CHCOOH
3 3 a a 3
的电离平衡常数推导可知K==c(H+)·,故c(CHCOOH)=mol·L-1,C项正确;溶液pH增
a 3
大,碱性增强,CHCOO-的水解程度减小,D项错误。
3
3.(2020·浙江7月选考,23)常温下,用0.1 mol·L-1氨水滴定10 mL浓度均为0.1 mol·L-1的
HCl和CHCOOH的混合液,下列说法不正确的是( )
3
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl-)>c(CHCOO-)
3 3
B.当滴入氨水10 mL时,c(NH)+c(NH ·H O)=c(CHCOO-)+c(CHCOOH)
3 2 3 3
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH ·H O)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)<c(Cl-)
答案 D
解析HCl是强酸,CHCOOH是弱酸,浓度均为0.1 mol·L-1时,c(Cl-)>c(CHCOO-),A正
3 3
确;滴入10 mL氨水时,NH ·H O和CHCOOH的物质的量相等,据物料守恒可得c(NH)+
3 2 3
c(NH ·H O)=c(CHCOO-)+c(CHCOOH),B正确;滴入20 mL氨水时,恰好完全反应,所
3 2 3 3
得溶液为等浓度的NH Cl和CHCOONH 的混合溶液,据电荷守恒可知c(NH)+c(H+)=c(Cl
4 3 4
-)+c(CHCOO-)+c(OH-),据物料守恒可得 c(NH)+c(NH ·H O)=c(CHCOOH)+
3 3 2 3
c(CHCOO-)+c(Cl-),联立两式可得c(CHCOOH)+c(H+)=c(NH ·H O)+c(OH-),C正确;
3 3 3 2
滴入20 mL氨水时,所得混合液呈酸性,若溶液呈中性,氨水滴入量要大于 20 mL,结合电
荷守恒关系c(NH)+c(H+)=c(Cl-)+c(CHCOO-)+c(OH-),溶液呈中性时,c(H+)=c(OH
3
-),得c(NH)=c(Cl-)+c(CHCOO-),则有c(NH)>c(Cl-),D错误。
3
4.(2020·江苏,14改编)室温下,将两种浓度均为0.10 mol·L-1的溶液等体积混合,若溶液
混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是( )
A.NaHCO —NaCO 混合溶液(pH=10.30):c(Na+)>c(CO)>c(HCO)>c(OH-)
3 2 3
B.氨水—NH Cl混合溶液(pH=9.25):c(NH)+c(H+)=c(NH ·H O)+c(OH-)
4 3 2
C.CHCOOH—CHCOONa混合溶液(pH=4.76):c(Na+)>c(CHCOOH)>c(CHCOO-)>
3 3 3 3
c(H+)
D.HC O—NaHC O 混合溶液(pH=1.68,HC O 为二元弱酸):c(H+)+c(H C O)=c(Na+)
2 2 4 2 4 2 2 4 2 2 4
+c(C O)+c(OH-)
2
答案 D
解析 A项,溶液呈碱性,说明 CO水解的程度大于 HCO电离的程度,因此 c(HCO)>
c(CO),CO的水解是微弱的,溶液中仍有大量的CO,则c(CO)>c(OH-),错误;B项,由
电荷守恒可知,c(NH)+c(H+)=c(Cl-)+c(OH-),物料守恒为c(NH ·H O)+c(NH)=2c(Cl
3 2
-),两式联立消去c(Cl-)可得:c(NH)+2c(H+)=c(NH ·H O)+2c(OH-),错误;C项,溶液
3 2呈酸性,说明CHCOOH电离的程度大于CHCOO-水解的程度,则溶液中微粒浓度关系为
3 3
c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+),错误;D项,由电荷守恒知,c(H+)+c(Na+)
3 3
=c(HC O)+2c(C O)+c(OH-),由物料守恒知,2c(Na+)=c(HC O)+c(C O)+c(H C O),两
2 2 2 2 2 2 4
式相减得c(H+)+c(H C O)=c(Na+)+c(C O)+c(OH-),正确。
2 2 4 2
5.(2017·全国卷Ⅰ,13)常温下将NaOH溶液滴加到己二酸(H X)溶液中,混合溶液的pH与
2
离子浓度变化的关系如图所示。下列叙述错误的是( )
A.K (H X)的数量级为10-6
a2 2
B.曲线N表示pH与lg的变化关系
C.NaHX溶液中c(H+)>c(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)
答案 D
解析 横坐标取0时,曲线M对应pH约为5.4,曲线N对应pH约为4.4,因为是NaOH滴
定HX溶液,所以在酸性较强的溶液中会存在c(HX-)=c(H X),所以曲线N表示pH与lg
2 2
的变化关系,B正确;=1时,即lg=0,pH≈5.4,c(H+)≈1×10-5.4 mol·L-1,K =≈1×10-
a2
5.4,A正确;NaHX溶液中,c(HX-)>c(X2-),即<1,lg<0,此时溶液呈酸性,C正确;当溶
液呈中性时,由曲线M可知lg>0,>1,即c(X2-)>c(HX-),D错误。
1.一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的HS溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1
2
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的HC O 溶液与pH=12的NaOH溶液以任意比例混合:c(Na+)+c(H+)=c(OH-)
2 2 4
+c(HC O)
2
D.pH相同的①CHCOONa,②NaHCO ,③NaClO三种溶液的c(Na+):①>②>③
3 3
答案 D
解析 A项,pH=5的HS溶液中,H+的浓度为1×10-5 mol·L-1,但是HS-的浓度会小于
2
H+的浓度,H+来自HS的第一步电离、HS-的电离和水的电离,故H+的浓度大于HS-的浓
2度,故不正确;B项,弱碱不完全电离,弱碱稀释10倍时,pH减小不到一个单位,a<b+
1,故不正确;C项,草酸是弱酸,氢氧化钠是强碱,无论怎样混合得到的溶液都符合电荷
守恒,而该等式中缺少草酸根,不符合电荷守恒,故不正确;D项,因为酸性:醋酸>碳酸
>次氯酸,根据越弱越水解的原则,pH相同的三种钠盐,浓度的大小关系为醋酸钠>碳酸氢
钠>次氯酸钠,则钠离子的浓度为①>②>③,故正确。
2.NaSO 溶液作为吸收液吸收SO 时,吸收液pH随n(SO)∶n(HSO)变化图像如图:
2 3 2
则以下离子浓度关系的判断正确的是( )
A.NaHSO 溶液中c(H+)<c(OH-)
3
B.NaSO 溶液中c(Na+)>c(SO)>c(HSO)>c(OH-)>c(H+)
2 3
C.当吸收溶液呈中性时,c(Na+)>c(SO)>c(HSO)>c(OH-)=c(H+)
D.当吸收溶液呈中性时,c(Na+)>c(HSO)+c(SO)
答案 D
解析 A项,NaHSO 溶液显酸性,c(H+)>c(OH-);B项,NaSO 溶液中,c(Na+)>c(SO)
3 2 3
>c(OH-)>c(HSO)>c(H+);C项,=1∶1时,溶液略显碱性,若使溶液显中性,则c(SO)
<c(HSO),错误;D项,根据电荷守恒,c(Na+)+c(H+)=c(OH-)+2c(SO)+c(HSO),由于
c(H+)=c(OH-),则c(Na+)=2c(SO)+c(HSO),正确。
3.(2018·浙江4月选考,23)在常温下,向10 mL浓度均为0.1 mol·L-1的NaOH和NaCO
2 3
混合溶液中滴加0.1 mol·L-1盐酸,溶液pH随盐酸加入体积的变化如图所示。下列说法正确
的是( )
A.在a点的溶液中:c(Na+ )>c(CO)>c(Cl-)>c(OH-)>c(H+)
B.在b点的溶液中:2n(CO)+n(HCO)<0.001 mol
C.在c点的溶液pH<7,是因为此时HCO的电离能力大于其水解能力D.若将 0.1 mol·L-1的盐酸换成同浓度的醋酸,当滴至溶液的 pH=7 时:c(Na+)=
c(CHCOO-)
3
答案 B
解析 向NaOH和NaCO 的混合溶液中滴加0.1 mol·L-1盐酸时,反应过程为OH-+H+
2 3
===HO,CO+H+===HCO,HCO+H+===HCO。A项,加入盐酸体积为5 mL时,溶液中
2 2 3
溶质的物质的量之比为n(NaCl)∶n(NaOH)∶n(Na CO)=1∶1∶2,溶液中离子浓度大小应
2 3
为c(Na+)>c(CO)>c(OH-)>c(Cl-)>c(H+),错误;B项,溶液的pH=7时电荷守恒:c(Na
+)+c(H+)=2c(CO)+c(HCO)+c(OH-)+c(Cl-),化简可得:2c(CO)+c(HCO)=
c(Na+)-c(Cl-),即2n(CO)+n(HCO)=n(Na+)-n(Cl-)=0.003 mol-n(Cl-),pH=7时盐酸
体积大于20 mL,故n(Cl-)>0.002 mol,所以2n(CO)+n(HCO)<0.001 mol成立,正确;C
项,c点pH小于7是因为反应生成的HCO 的电离大于HCO的水解导致,错误;D项,把
2 3
盐酸换成同浓度的醋酸,滴至溶液pH=7时,电荷守恒:c(Na+)+c(H+)=2c(CO)+c(HCO)
+c(OH-)+c(CHCOO-),c(Na+)与c(CHCOO-)不相等,错误。
3 3
4.(2019·天津质检)常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的
pH与离子浓度变化关系如下图所示[已知:p=-lg]。下列叙述不正确的是( )
A.K(HA)的数量级为10-5
a
B.滴加NaOH溶液过程中,保持不变
C.m点所示溶液中:c(H+)=c(HA)+c(OH-)-c(Na+)
D.n点所示溶液中:c(Na+)=c(A-)+c(HA)
答案 D
解析 HAH++A-,K(HA)=,p=-lg=0时,K(HA)=c(H+)=10-4.76,K(HA)的数量
a a a
级为10-5,A项正确;==,故滴加NaOH溶液过程中,保持不变,B项正确;由电荷守恒
可知,m点所示溶液中:c(H+)+c(Na+)=c(A-)+c(OH-),由A分析可知,m点时c(A-)=
c(HA),则c(H+)=c(HA)+c(OH-)-c(Na+),C项正确;n点溶液中根据电荷守恒有c(Na+)
+c(H+)=c(OH-)+c(A-),n点溶液呈酸性,c(H+)>c(OH-),则c(Na+)<c(A-),故不可能
有c(Na+)=c(A-)+c(HA),D项错误。
5.联氨(N H)是一种二元弱碱,有NH+HONH+OH- K =3×10-6
2 4 2 4 2 2 b1
NH+HONH+OH- K =7.6×10-15
2 2 2 b2
室温下,用0.01 mol·L-1 HCl溶液滴定10 mL 0.1 mol·L-1的联氨(N H)水溶液。滴定过程中
2 4
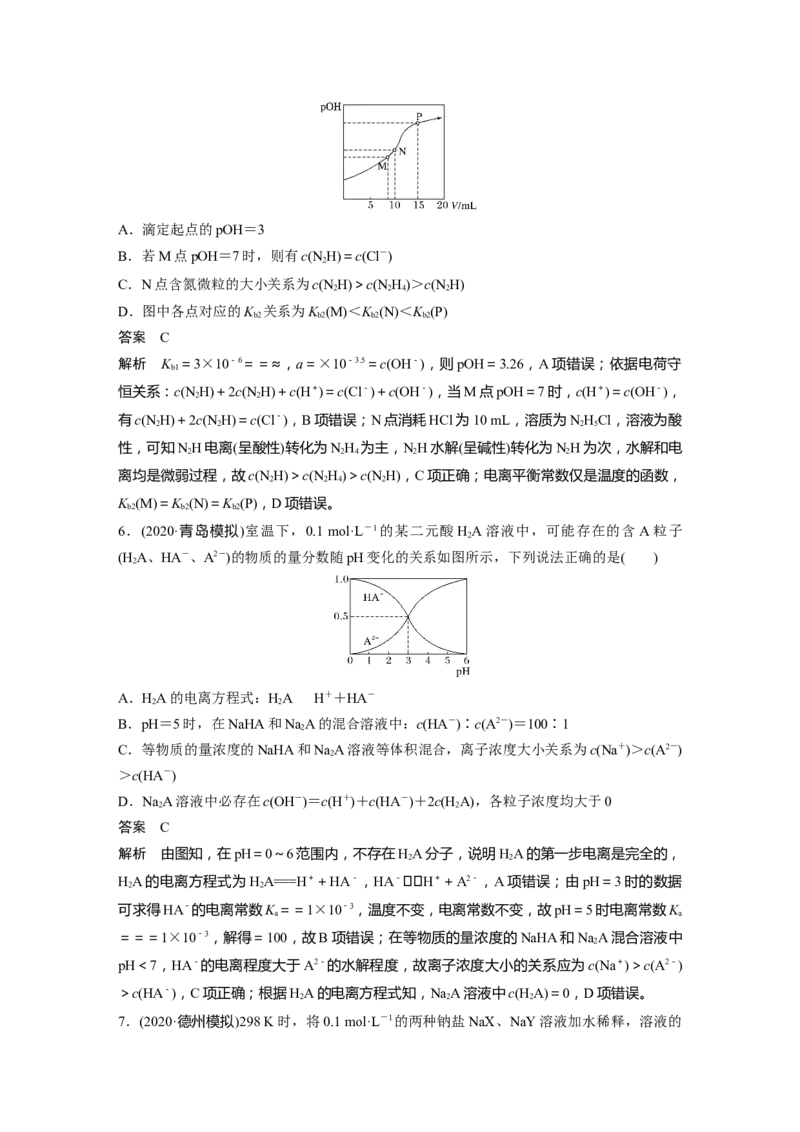
溶液的pOH变化如图所示,且M点pOH=7(已知lg3≈0.48),则下列判断正确的是( )A.滴定起点的pOH=3
B.若M点pOH=7时,则有c(N H)=c(Cl-)
2
C.N点含氮微粒的大小关系为c(N H)>c(N H)>c(N H)
2 2 4 2
D.图中各点对应的K 关系为K (M)<K (N)<K (P)
b2 b2 b2 b2
答案 C
解析 K =3×10-6==≈,a=×10-3.5=c(OH-),则pOH=3.26,A项错误;依据电荷守
b1
恒关系:c(N H)+2c(N H)+c(H+)=c(Cl-)+c(OH-),当M点pOH=7时,c(H+)=c(OH-),
2 2
有c(N H)+2c(N H)=c(Cl-),B项错误;N点消耗HCl为10 mL,溶质为NHCl,溶液为酸
2 2 2 5
性,可知NH电离(呈酸性)转化为NH 为主,NH水解(呈碱性)转化为NH为次,水解和电
2 2 4 2 2
离均是微弱过程,故c(N H)>c(N H)>c(N H),C项正确;电离平衡常数仅是温度的函数,
2 2 4 2
K (M)=K (N)=K (P),D项错误。
b2 b2 b2
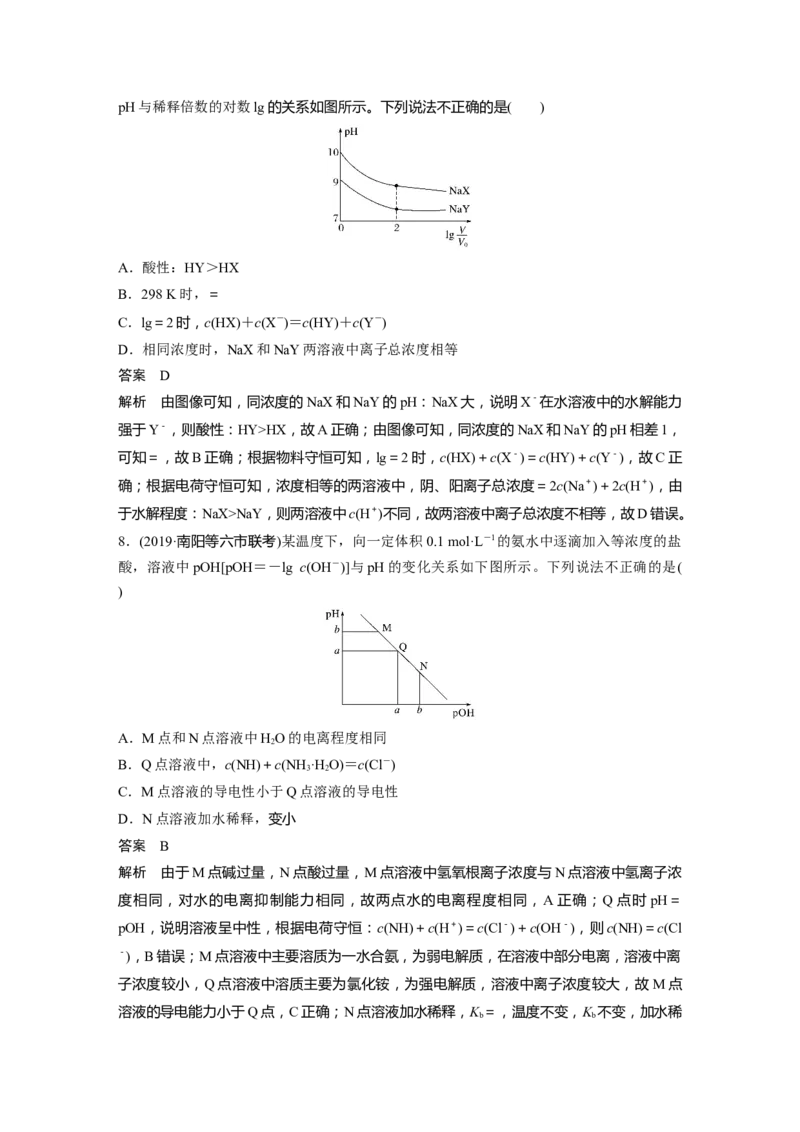
6.(2020·青岛模拟)室温下,0.1 mol·L-1的某二元酸HA溶液中,可能存在的含A粒子
2
(H A、HA-、A2-)的物质的量分数随pH变化的关系如图所示,下列说法正确的是( )
2
A.HA的电离方程式:HAH++HA-
2 2
B.pH=5时,在NaHA和NaA的混合溶液中:c(HA-)∶c(A2-)=100∶1
2
C.等物质的量浓度的NaHA和NaA溶液等体积混合,离子浓度大小关系为c(Na+)>c(A2-)
2
>c(HA-)
D.NaA溶液中必存在c(OH-)=c(H+)+c(HA-)+2c(H A),各粒子浓度均大于0
2 2
答案 C
解析 由图知,在pH=0~6范围内,不存在HA分子,说明HA的第一步电离是完全的,
2 2
HA的电离方程式为HA===H++HA-,HA-H++A2-,A项错误;由pH=3时的数据
2 2
可求得HA-的电离常数K==1×10-3,温度不变,电离常数不变,故pH=5时电离常数K
a a
===1×10-3,解得=100,故B项错误;在等物质的量浓度的NaHA和NaA混合溶液中
2
pH<7,HA-的电离程度大于A2-的水解程度,故离子浓度大小的关系应为c(Na+)>c(A2-)
>c(HA-),C项正确;根据HA的电离方程式知,NaA溶液中c(H A)=0,D项错误。
2 2 2
7.(2020·德州模拟)298 K时,将0.1 mol·L-1的两种钠盐NaX、NaY溶液加水稀释,溶液的pH与稀释倍数的对数lg的关系如图所示。下列说法不正确的是( )
A.酸性:HY>HX
B.298 K时,=
C.lg=2时,c(HX)+c(X-)=c(HY)+c(Y-)
D.相同浓度时,NaX和NaY两溶液中离子总浓度相等
答案 D
解析 由图像可知,同浓度的NaX和NaY的pH:NaX大,说明X-在水溶液中的水解能力
强于Y-,则酸性:HY>HX,故A正确;由图像可知,同浓度的NaX和NaY的pH相差1,
可知=,故B正确;根据物料守恒可知,lg=2时,c(HX)+c(X-)=c(HY)+c(Y-),故C正
确;根据电荷守恒可知,浓度相等的两溶液中,阴、阳离子总浓度=2c(Na+)+2c(H+),由
于水解程度:NaX>NaY,则两溶液中c(H+)不同,故两溶液中离子总浓度不相等,故D错误。
8.(2019·南阳等六市联考)某温度下,向一定体积0.1 mol·L-1的氨水中逐滴加入等浓度的盐
酸,溶液中pOH[pOH=-lg c(OH-)]与pH的变化关系如下图所示。下列说法不正确的是(
)
A.M点和N点溶液中HO的电离程度相同
2
B.Q点溶液中,c(NH)+c(NH ·H O)=c(Cl-)
3 2
C.M点溶液的导电性小于Q点溶液的导电性
D.N点溶液加水稀释,变小
答案 B
解析 由于M点碱过量,N点酸过量,M点溶液中氢氧根离子浓度与N点溶液中氢离子浓
度相同,对水的电离抑制能力相同,故两点水的电离程度相同,A正确;Q点时pH=
pOH,说明溶液呈中性,根据电荷守恒:c(NH)+c(H+)=c(Cl-)+c(OH-),则c(NH)=c(Cl
-),B错误;M点溶液中主要溶质为一水合氨,为弱电解质,在溶液中部分电离,溶液中离
子浓度较小,Q点溶液中溶质主要为氯化铵,为强电解质,溶液中离子浓度较大,故M点
溶液的导电能力小于Q点,C正确;N点溶液加水稀释,K =,温度不变,K 不变,加水稀
b b释氢离子浓度减小,c(OH-)增大,所以变小,故D正确。
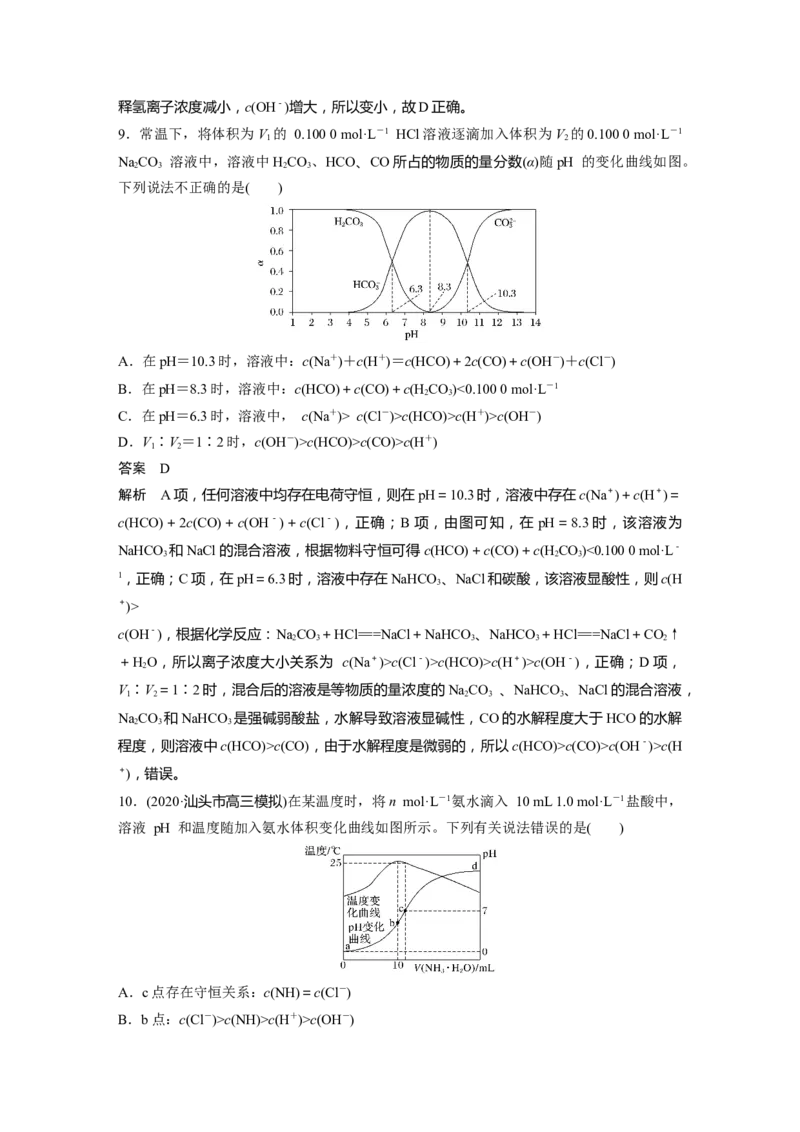
9.常温下,将体积为V 的 0.100 0 mol·L-1 HCl溶液逐滴加入体积为V 的0.100 0 mol·L-1
1 2
NaCO 溶液中,溶液中HCO 、HCO、CO所占的物质的量分数(α)随pH 的变化曲线如图。
2 3 2 3
下列说法不正确的是( )
A.在pH=10.3时,溶液中:c(Na+)+c(H+)=c(HCO)+2c(CO)+c(OH-)+c(Cl-)
B.在pH=8.3时,溶液中:c(HCO)+c(CO)+c(H CO)<0.100 0 mol·L-1
2 3
C.在pH=6.3时,溶液中, c(Na+)> c(Cl-)>c(HCO)>c(H+)>c(OH-)
D.V∶V=1∶2时,c(OH-)>c(HCO)>c(CO)>c(H+)
1 2
答案 D
解析 A项,任何溶液中均存在电荷守恒,则在pH=10.3时,溶液中存在c(Na+)+c(H+)=
c(HCO)+2c(CO)+c(OH-)+c(Cl-),正确;B项,由图可知,在 pH=8.3时,该溶液为
NaHCO 和NaCl的混合溶液,根据物料守恒可得 c(HCO)+c(CO)+c(H CO)<0.100 0 mol·L-
3 2 3
1,正确;C项,在pH=6.3时,溶液中存在NaHCO 、NaCl和碳酸,该溶液显酸性,则c(H
3
+)>
c(OH-),根据化学反应:NaCO +HCl===NaCl+NaHCO 、NaHCO +HCl===NaCl+CO↑
2 3 3 3 2
+HO,所以离子浓度大小关系为 c(Na+)>c(Cl-)>c(HCO)>c(H+)>c(OH-),正确;D项,
2
V∶V =1∶2时,混合后的溶液是等物质的量浓度的NaCO 、NaHCO 、NaCl的混合溶液,
1 2 2 3 3
NaCO 和NaHCO 是强碱弱酸盐,水解导致溶液显碱性,CO的水解程度大于HCO的水解
2 3 3
程度,则溶液中c(HCO)>c(CO),由于水解程度是微弱的,所以c(HCO)>c(CO)>c(OH-)>c(H
+),错误。
10.(2020·汕头市高三模拟)在某温度时,将n mol·L-1氨水滴入 10 mL 1.0 mol·L-1盐酸中,
溶液 pH 和温度随加入氨水体积变化曲线如图所示。下列有关说法错误的是( )
A.c点存在守恒关系:c(NH)=c(Cl-)
B.b点:c(Cl-)>c(NH)>c(H+)>c(OH-)C.水的电离程度:b>c>a>d
D.25 ℃时 ,NH Cl 水解平衡常数为(n-1)×10-7(用n表示)
4
答案 C
解析 c点溶液呈中性,c(H+)=c(OH-),由电荷守恒:c(NH)+c(H+)=c(Cl-)+c(OH-),所
以c(NH)=c(Cl-),A正确;b点溶液为NH Cl溶液,此溶液中离子浓度大小为 c(Cl-)>
4
c(NH)>c(H+)>c(OH-),B正确;b点溶液温度最高,说明此时两溶液恰好反应生成氯化铵,
铵根离子水解促进了水的电离,而a、d两点都抑制了水的电离,所以b点水的电离程度最
大;由于d点混合液的pH不知,则无法判断a、d两点水的电离程度大小,C错误;根据图
像可知,25 ℃时溶液的pH=7,则:c(H+)=c(OH-)=10-7mol·L-1,c(NH)=c(Cl-)=0.5
mol·L-1,根据物料守恒可知:c(NH ·H O)=(0.5 n-0.5) mol·L-1,则25 ℃时NH Cl水解常
3 2 4
数为K ==(n-1)×10-7,D正确。
h
11.(2020·安徽省皖南八校高三模拟)常温下向一定浓度的NaX溶液中滴入盐酸,粒子浓度
2
与混合溶液的pH变化的关系如图所示,已知:HX是二元弱酸,Y表示或,pY=-lgY。下
2
列叙述错误的是( )
A.曲线n表示p与pH的变化关系
B.K (H X)=1.0×10-10.3
a1 2
C.NaHX溶液中c(OH-)>c(H+)
D.当pH=7时,混合溶液中c(Na+)=c(HX-)+2c(X2-)+c(Cl-)
答案 B
解析 HX为二元弱酸,以第一步电离为主,则K (H X)>K (H X),则pH相同时,<,pY
2 a1 2 a2 2
=-lgY,则p>p,则m、n分别表示pH与p、p的变化关系,据此结合选项分析解答。根
据分析可知,n表示pH与p的变化关系,A选项正确;M点pH=9.3,c(H+)=10-9.3mol·L-
1,p=-lg=1,则=0.1,所以K (H X)=·c(H+)=10-9.3×0.1=1.0×10-10.3,N点pH=7.4,
a2 2
c(H+)=10-7.4mol·L-1,p=-lg=-1,则=10,所以K (H X)=·c(H+)=10-7.4×10=1.0×10
a1 2
-6.4,B选项错误;根据B可知HX-的电离平衡常数为1.0×10-10.3;曲线n表示pH与p的变
化关系,N点pH=7.4,p=-lg=-1,=10,所以HX-的水解平衡常数K ==×=1.0×10
h
-7.6>1.0×10-10.3,说明HX-的水解程度大于其电离程度,则NaHX溶液呈碱性,c(H+)<
c(OH-),C选项正确;当溶液呈中性时,c(H+)=c(OH-),根据电荷守恒可知:c(Na+)=
c(HX-)+2c(X2-)+c(Cl-),D选项正确。
12.(2020·洛阳市高三统考)25 ℃时,向NaHCO 溶液中滴入盐酸,混合溶液的pH与离子浓
3度变化的关系如图所示。下列叙述正确的是( )
A.图中a=2.6
B.25 ℃时,HCO+HOHCO+OH-的K =1.0×10-6.4
2 2 3 h
C.M点溶液中:c(H+)+c(H CO)=c(Cl-)+2c(CO)+c(OH-)
2 3
D.若要表示题目条件下pH与lg的变化关系,则曲线应该在平行于曲线x的下方
答案 A
解析 根据点N(7.4,1),lg=1,则=10,碳酸的一级电离常数K ==10×10-7.4=10-6.4,将
a1
M点c(H+)带入一级电离常数公式,解得=102.6,a=2.6,A正确;该反应的水解常数K
h
=,根据M点,=
10-2.6 ,c(H+)=10-9 mol·L-1,c(OH-)=10-5 mol·L-1,带入数值,此反应的水解平衡常数
为1×10-7.6,B错误;M点溶液中,依据电荷守恒c(H+)+c(Na+)=c(Cl-)+2c(CO)+c(OH
-)+c(HCO),此时溶液为NaHCO 和NaCl的混合溶液,c(Na+)>c(HCO)+c(H CO),所以
3 2 3
c(H+)+c(H CO)