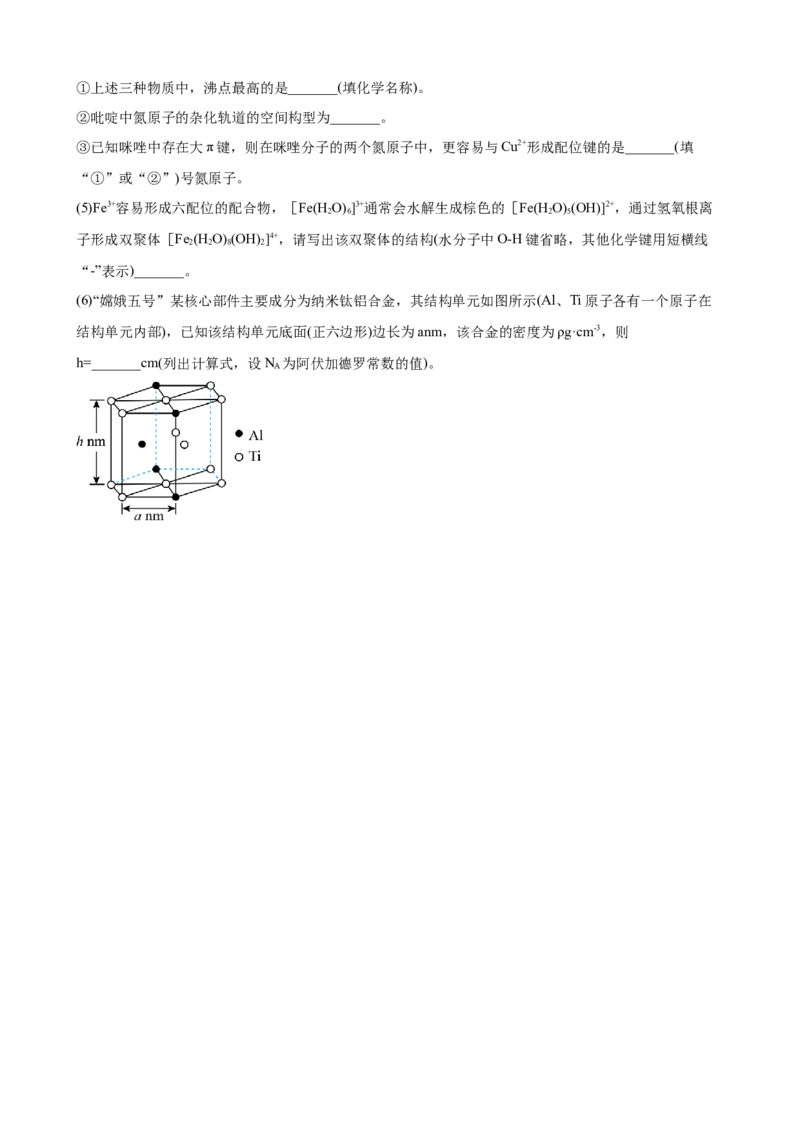文档内容
2023届高三化学高考备考一轮复习专题训练:物质结构与性质
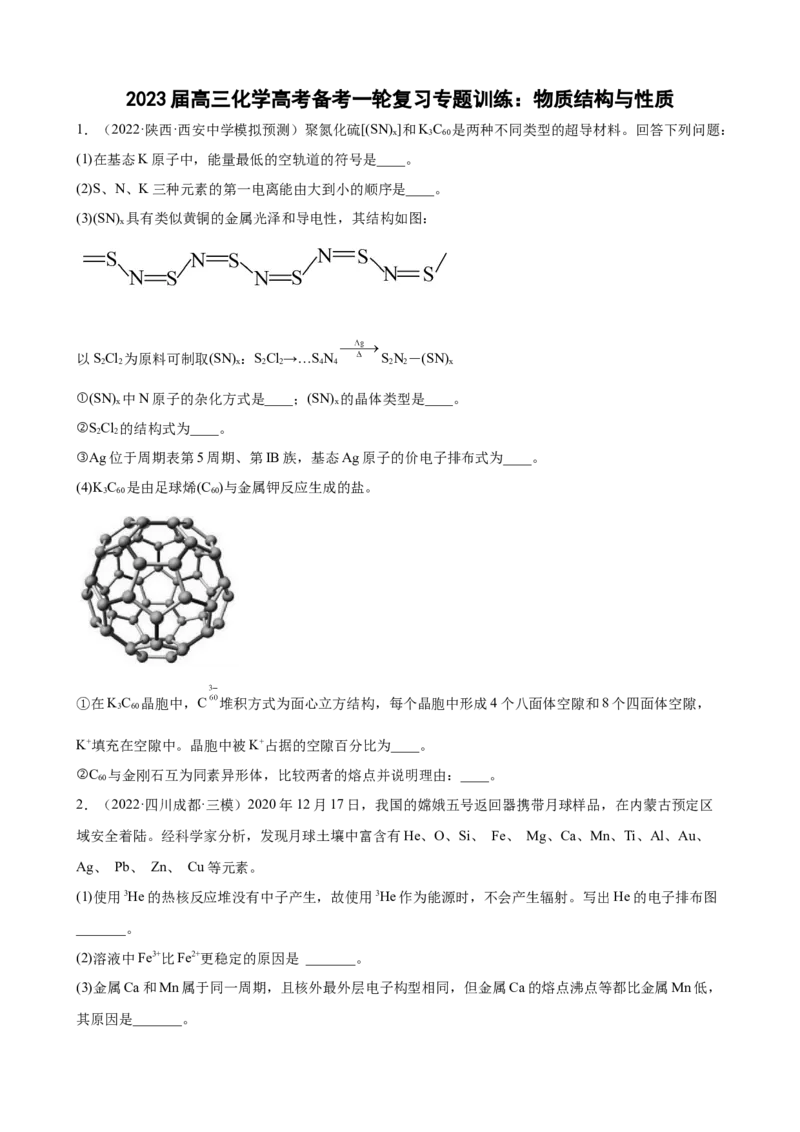
1.(2022·陕西·西安中学模拟预测)聚氮化硫[(SN) ]和KC 是两种不同类型的超导材料。回答下列问题:
x 3 60
(1)在基态K原子中,能量最低的空轨道的符号是____。
(2)S、N、K三种元素的第一电离能由大到小的顺序是____。
(3)(SN) 具有类似黄铜的金属光泽和导电性,其结构如图:
x
以SCl 为原料可制取(SN) :SCl→…SN SN-(SN)
2 2 x 2 2 4 4 2 2 x
①(SN) 中N原子的杂化方式是____;(SN) 的晶体类型是____。
x x
②S Cl 的结构式为____。
2 2
③Ag位于周期表第5周期、第IB族,基态Ag原子的价电子排布式为____。
(4)K C 是由足球烯(C )与金属钾反应生成的盐。
3 60 60
①在KC 晶胞中,C 堆积方式为面心立方结构,每个晶胞中形成4个八面体空隙和8个四面体空隙,
3 60
K+填充在空隙中。晶胞中被K+占据的空隙百分比为____。
②C 与金刚石互为同素异形体,比较两者的熔点并说明理由:____。
60
2.(2022·四川成都·三模)2020年12月17日,我国的嫦娥五号返回器携带月球样品,在内蒙古预定区
域安全着陆。经科学家分析,发现月球土壤中富含有He、O、Si、 Fe、 Mg、Ca、Mn、Ti、Al、Au、
Ag、 Pb、 Zn、 Cu等元素。
(1)使用3He的热核反应堆没有中子产生,故使用3He作为能源时,不会产生辐射。写出He的电子排布图
_______。
(2)溶液中Fe3+比Fe2+更稳定的原因是 _______。
(3)金属Ca和Mn属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点沸点等都比金属Mn低,
其原因是_______。(4)向Cu(OH) 悬浊液中通入NH ,蓝色沉淀溶解,溶液变为深蓝色,发生了如下反应:Cu(OH) + 4NH
2 3 2 3
= [Cu(NH )]2+ + 2OH—,NH 分子中N的杂化类型为_______, 比较NH 和[Cu(NH )]2+中H—N—H 键角
3 4 3 3 3 4
的大小: NH _______ [Cu(NH)]2+ (填“>”或“<”),1mol [Cu(NH )]2+中σ键的数目为_______N 。
3 3 4 3 4 A
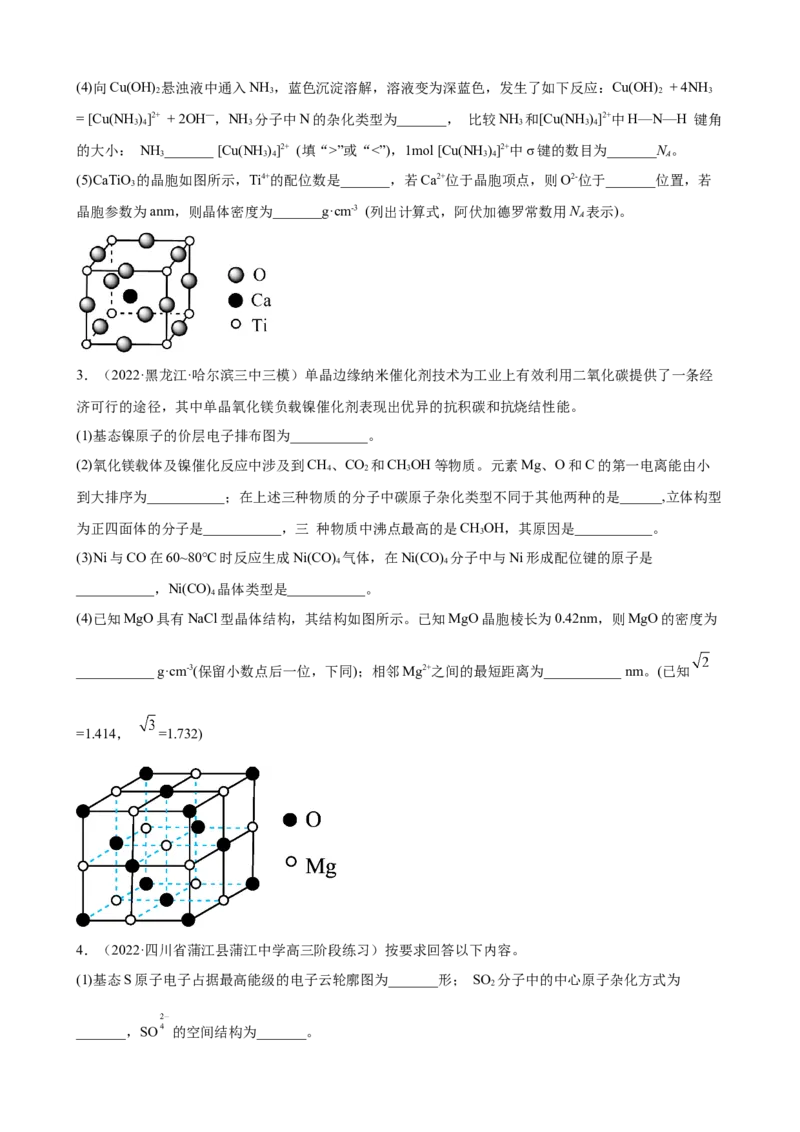
(5)CaTiO 的晶胞如图所示,Ti4+的配位数是_______,若Ca2+位于晶胞项点,则O2-位于_______位置,若
3
晶胞参数为anm,则晶体密度为_______g·cm-3 (列出计算式,阿伏加德罗常数用N 表示)。
A
3.(2022·黑龙江·哈尔滨三中三模)单晶边缘纳米催化剂技术为工业上有效利用二氧化碳提供了一条经
济可行的途径,其中单晶氧化镁负载镍催化剂表现出优异的抗积碳和抗烧结性能。
(1)基态镍原子的价层电子排布图为___________。
(2)氧化镁载体及镍催化反应中涉及到CH、CO 和CHOH等物质。元素Mg、O和C的第一电离能由小
4 2 3
到大排序为___________;在上述三种物质的分子中碳原子杂化类型不同于其他两种的是______,立体构型
为正四面体的分子是___________,三 种物质中沸点最高的是CHOH,其原因是___________。
3
(3)Ni与CO在60~80°C时反应生成Ni(CO) 气体,在Ni(CO) 分子中与Ni形成配位键的原子是
4 4
___________,Ni(CO) 晶体类型是___________。
4
(4)已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞棱长为0.42nm,则MgO的密度为
___________ g·cm-3(保留小数点后一位,下同);相邻Mg2+之间的最短距离为___________ nm。(已知
=1.414, =1.732)
4.(2022·四川省蒲江县蒲江中学高三阶段练习)按要求回答以下内容。
(1)基态S原子电子占据最高能级的电子云轮廓图为_______形; SO 分子中的中心原子杂化方式为
2
_______,SO 的空间结构为_______。(2)近期我国科学家对嫦娥五号月球土壤样品进行了分析,研究表明每吨月壤样品的钛含量是地球土壤平
均含量的6倍多。Ti 在元素周期表的位置_______; 基态Ti原子的电子排布式 _______。
(3)H O 的空间结构示意图如下。
2 2
①下列关于HO 的说法中正确的是_______(填字母)。
2 2
A.分子中有极性键 B.分子中有非极性键
C.氧原子的轨道发生了sp2 杂化 D.分子是非极性分子
②H O 可使酸性KCr O 溶液由橙黄色变为绿色,铬元素被还原为+3价,该反应的离子方程式是_______。
2 2 2 2 7
(4)铜和氧形成一种离子化合物的晶体结构如图所示,设阿伏加德罗常数的值为 ,晶胞边长a nm,则
晶体的密度为_______ 。(已知 的摩尔质量 )
5.(2022·山西吕梁·一模)铁、钴、镍等金属及其化合物在科学研究和工业生产中应用非常广泛。回答
下列问题:
(1)基态铁原子的核外电子排布式为___________。
(2)K [Fe(CN) ]溶液可以检验Fe2+。K[Fe(CN) ]中含有的σ键与π键的数目之比___________, 与CN-互
3 6 3 6
为等电子体的分子有___________(举一例,填化学式)。
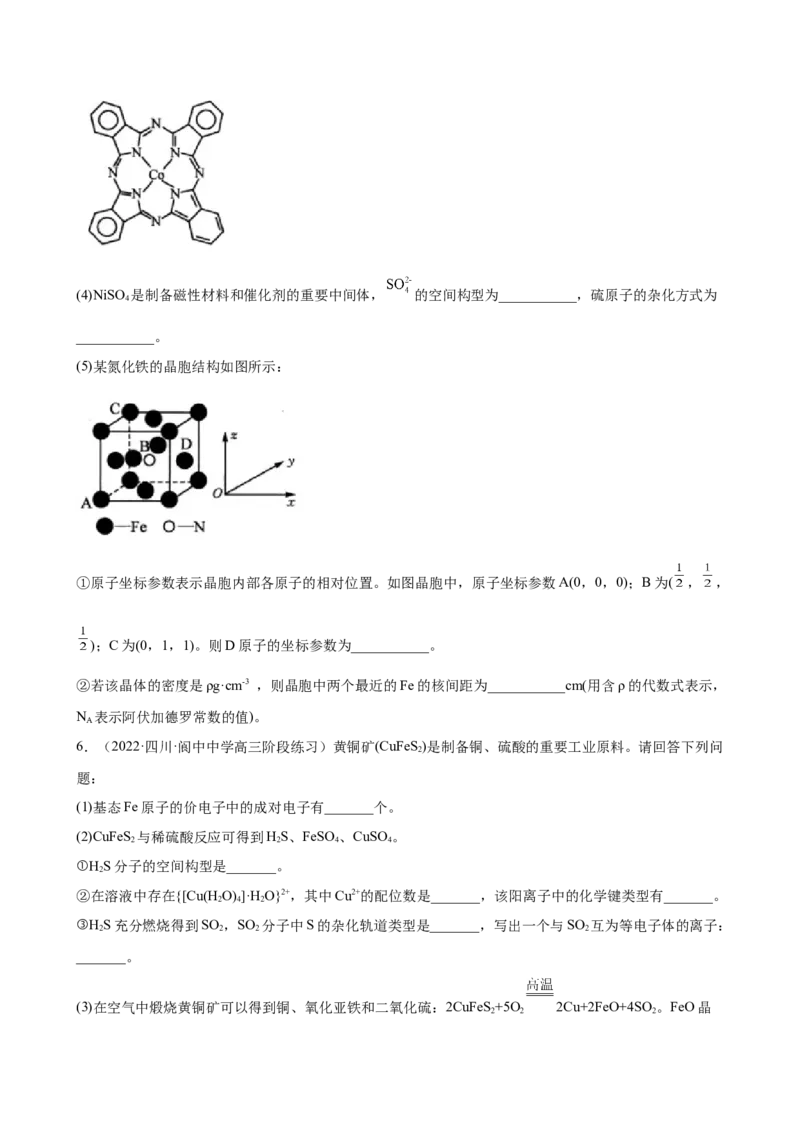
(3)酞菁钴的结构简式如图所示,其中三种非金属元素的电负性由大到小的顺序为___________。(4)NiSO 是制备磁性材料和催化剂的重要中间体, 的空间构型为___________,硫原子的杂化方式为
4
___________。
(5)某氮化铁的晶胞结构如图所示:
①原子坐标参数表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数A(0,0,0);B为( , ,
);C为(0,1,1)。则D原子的坐标参数为___________。
②若该晶体的密度是ρg·cm-3 ,则晶胞中两个最近的Fe的核间距为___________cm(用含ρ的代数式表示,
N 表示阿伏加德罗常数的值)。
A
6.(2022·四川·阆中中学高三阶段练习)黄铜矿(CuFeS)是制备铜、硫酸的重要工业原料。请回答下列问
2
题:
(1)基态Fe原子的价电子中的成对电子有_______个。
(2)CuFeS 与稀硫酸反应可得到HS、FeSO 、CuSO 。
2 2 4 4
①HS分子的空间构型是_______。
2
②在溶液中存在{[Cu(H O) ]·H O}2+,其中Cu2+的配位数是_______,该阳离子中的化学键类型有_______。
2 4 2
③HS充分燃烧得到SO ,SO 分子中S的杂化轨道类型是_______,写出一个与SO 互为等电子体的离子:
2 2 2 2
_______。
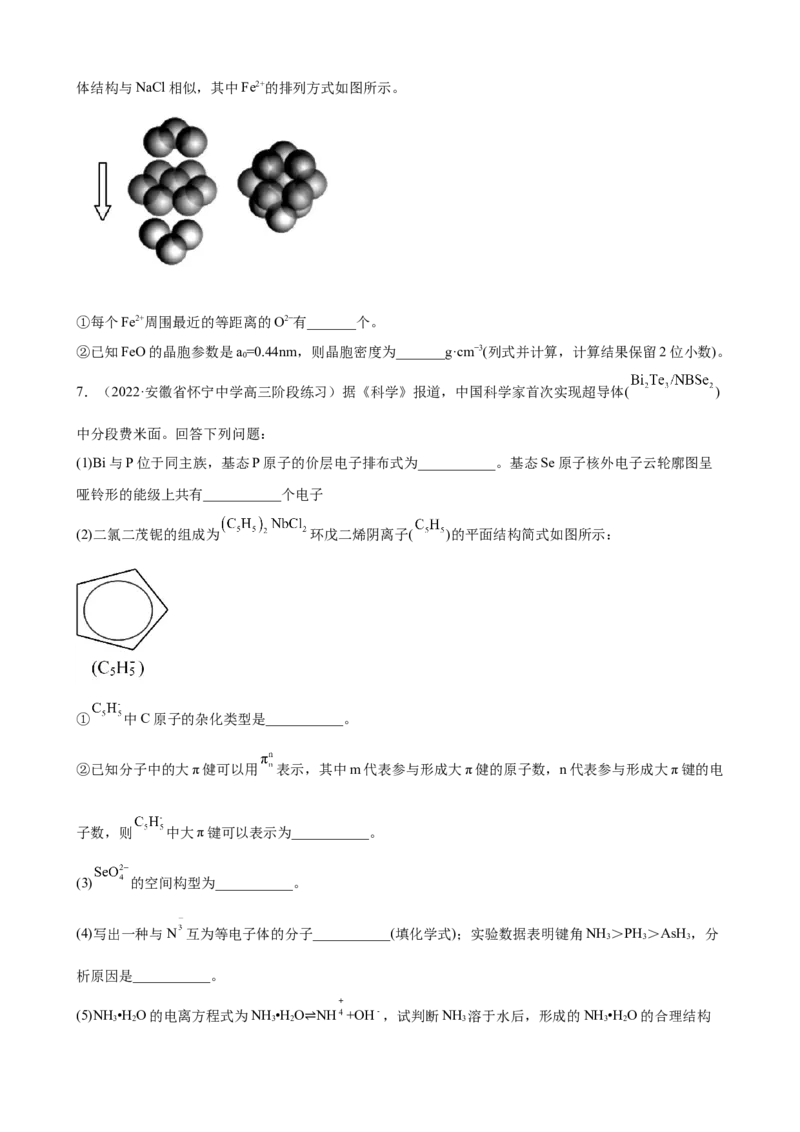
(3)在空气中煅烧黄铜矿可以得到铜、氧化亚铁和二氧化硫:2CuFeS+5O 2Cu+2FeO+4SO 。FeO晶
2 2 2体结构与NaCl相似,其中Fe2+的排列方式如图所示。
①每个Fe2+周围最近的等距离的O2−有_______个。
②已知FeO的晶胞参数是a=0.44nm,则晶胞密度为_______g·cm−3(列式并计算,计算结果保留2位小数)。
0
7.(2022·安徽省怀宁中学高三阶段练习)据《科学》报道,中国科学家首次实现超导体( )
中分段费米面。回答下列问题:
(1)Bi与P位于同主族,基态P原子的价层电子排布式为___________。基态Se原子核外电子云轮廓图呈
哑铃形的能级上共有___________个电子
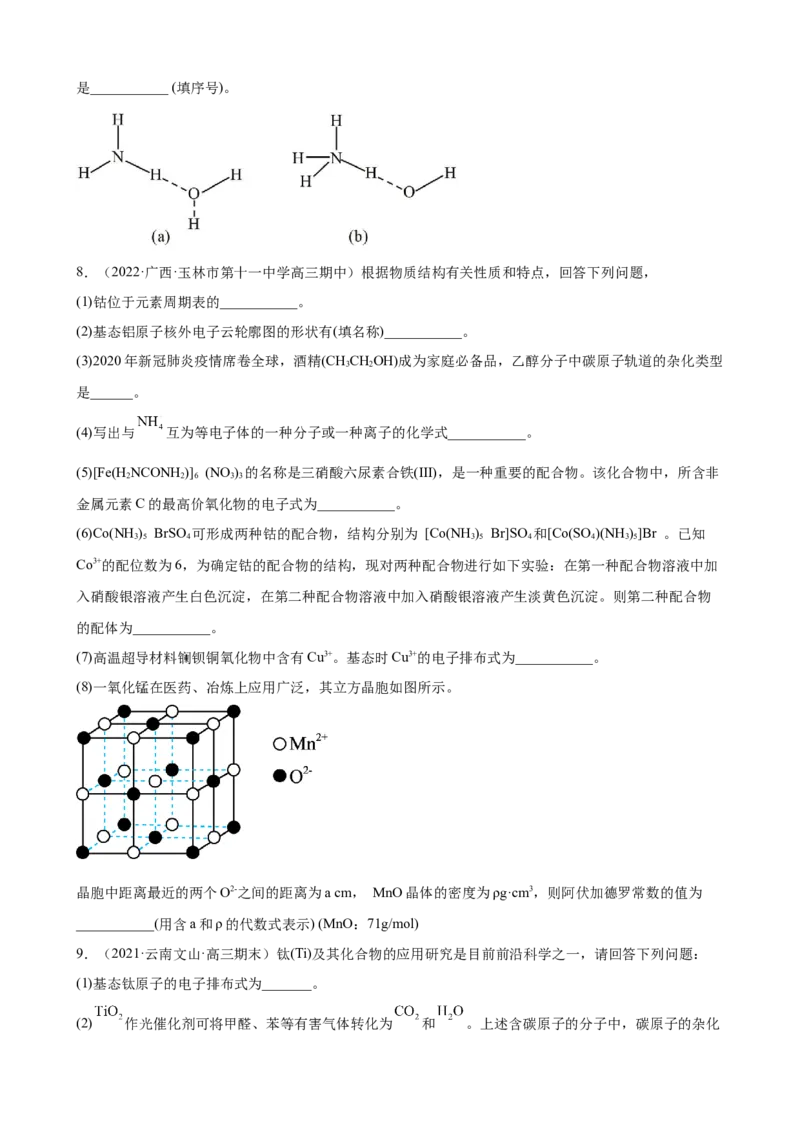
(2)二氯二茂铌的组成为 环戊二烯阴离子( )的平面结构简式如图所示:
① 中C原子的杂化类型是___________。
②已知分子中的大π健可以用 表示,其中m代表参与形成大π健的原子数,n代表参与形成大π键的电
子数,则 中大π键可以表示为___________。
(3) 的空间构型为___________。
(4)写出一种与N 互为等电子体的分子___________(填化学式);实验数据表明键角NH >PH >AsH ,分
3 3 3
析原因是___________。
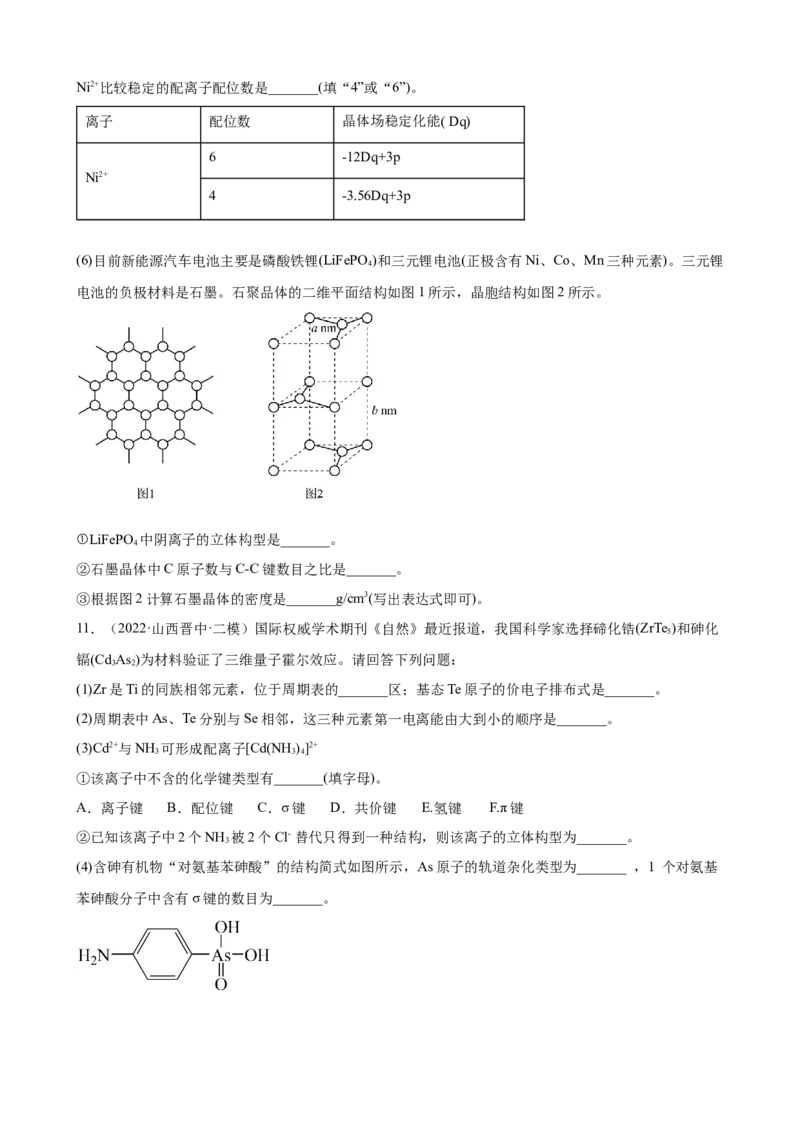
(5)NH •H O的电离方程式为NH •H O NH +OH﹣,试判断NH 溶于水后,形成的NH •H O的合理结构
3 2 3 2 3 3 2
⇌是___________ (填序号)。
8.(2022·广西·玉林市第十一中学高三期中)根据物质结构有关性质和特点,回答下列问题,
(1)钴位于元素周期表的___________。
(2)基态铝原子核外电子云轮廓图的形状有(填名称)___________。
(3)2020年新冠肺炎疫情席卷全球,酒精(CHCHOH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型
3 2
是______。
(4)写出与 互为等电子体的一种分子或一种离子的化学式___________。
(5)[Fe(H NCONH)] (NO ) 的名称是三硝酸六尿素合铁(III),是一种重要的配合物。该化合物中,所含非
2 2 6 3 3
金属元素C的最高价氧化物的电子式为___________。
(6)Co(NH ) BrSO 可形成两种钴的配合物,结构分别为 [Co(NH ) Br]SO 和[Co(SO )(NH )]Br 。已知
3 5 4 3 5 4 4 3 5
Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加
入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物
的配体为___________。
(7)高温超导材料镧钡铜氧化物中含有Cu3+。基态时Cu3+的电子排布式为___________。
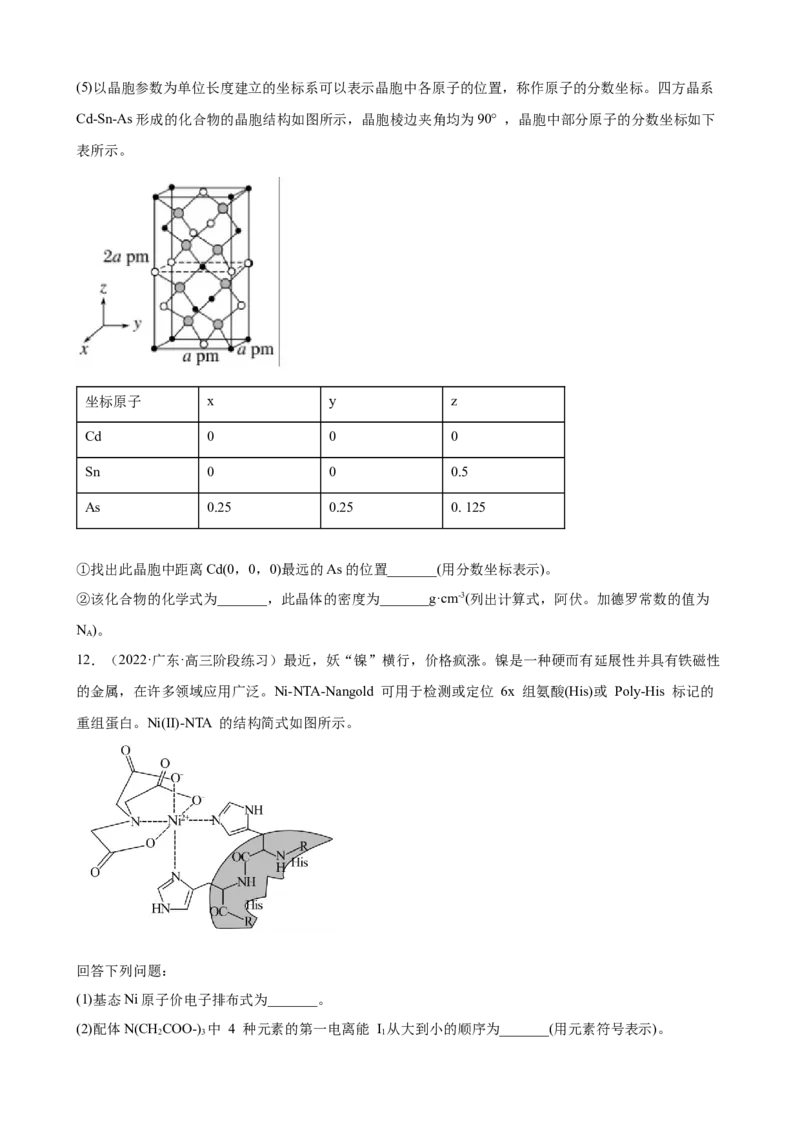
(8)一氧化锰在医药、冶炼上应用广泛,其立方晶胞如图所示。
晶胞中距离最近的两个O2-之间的距离为a cm, MnO晶体的密度为ρg·cm3,则阿伏加德罗常数的值为
___________(用含a和ρ的代数式表示) (MnO:71g/mol)
9.(2021·云南文山·高三期末)钛(Ti)及其化合物的应用研究是目前前沿科学之一,请回答下列问题:
(1)基态钛原子的电子排布式为_______。
(2) 作光催化剂可将甲醛、苯等有害气体转化为 和 。上述含碳原子的分子中,碳原子的杂化方式为 的是_______(填名称)。
(3)作为过渡元素的Fe、Cu容易形成配位化合物, 中C、N两种元素的电负性大小关系为
_______。硫酸铜稀溶液中微粒间不存在的作用力有_______(填序号)。
A.配位键 B.金属键 C.离子键 D.共价键 E.氢键 F.范德华力
(4)已知Ba、Mo的氯化物沸点信息如下表所示。二者沸点差异的原因是_______。
氯化物 沸点
1560℃
268℃
(5) 分子中H-N-H的键角为107°,在 中,H-N-H键角近似109.5°,键角变大的原因是
_______。
(6)贵金属磷化物 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图示。已知晶胞参数
为anm,晶体中与P距离最近的Rh的数目为_______,晶体的密度为_______ 。(列出计算式即可)。
10.(2022·陕西·模拟预测)第24届冬奥会于2022年2月4日在北京隆重开幕,“科技冬奥”理念体现
在方方面面。
Ⅰ.完成下列问题
(1)冬奥会采用的石墨烯(即单层石墨)材料制造户外保暖穿戴设备,该材料中的碳原子采取_______杂化。
Ⅱ.奥运会场馆使用了大量的合金。第Ⅷ族元素Fe、Co、Ni性质相似,称为铁系元素,主要用于制造合金。
(2)基态Fe2+与Fe3+的最外层电子数之比为_______,实验室常用 A离子来检验Fe3+,且又是CO 的某一种
2
等电子体写出A离子的结构式_______。
(3)Fe(CO) 是一种黄色粘稠状液体化合物,则CO作配体时,配位原子是_______ , 其原因是_______。
5
(4)写出与Ni同周期元素中,基态原子未成对电子数与Ni相同的元名素称_______。
(5)如表为Ni2+不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知,Ni2+比较稳定的配离子配位数是_______(填“4”或“6”)。
离子 配位数 晶体场稳定化能( Dq)
6 -12Dq+3p
Ni2+
4 -3.56Dq+3p
(6)目前新能源汽车电池主要是磷酸铁锂(LiFePO )和三元锂电池(正极含有Ni、Co、Mn三种元素)。三元锂
4
电池的负极材料是石墨。石聚品体的二维平面结构如图1所示,晶胞结构如图2所示。
①LiFePO 中阴离子的立体构型是_______。
4
②石墨晶体中C原子数与C-C键数目之比是_______。
③根据图2计算石墨晶体的密度是_______g/cm3(写出表达式即可)。
11.(2022·山西晋中·二模)国际权威学术期刊《自然》最近报道,我国科学家选择碲化锆(ZrTe )和砷化
5
镉(Cd As )为材料验证了三维量子霍尔效应。请回答下列问题:
3 2
(1)Zr是Ti的同族相邻元素,位于周期表的_______区;基态Te原子的价电子排布式是_______。
(2)周期表中As、Te分别与Se相邻,这三种元素第一电离能由大到小的顺序是_______。
(3)Cd2+与NH 可形成配离子[Cd(NH )]2+
3 3 4
①该离子中不含的化学键类型有_______(填字母)。
A.离子键 B.配位键 C.σ键 D.共价键 E.氢键 F.π键
②已知该离子中2个NH 被2个Cl- 替代只得到一种结构,则该离子的立体构型为_______。
3
(4)含砷有机物“对氨基苯砷酸”的结构简式如图所示,As原子的轨道杂化类型为_______ ,1 个对氨基
苯砷酸分子中含有σ键的数目为_______。(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系
Cd-Sn-As形成的化合物的晶胞结构如图所示,晶胞棱边夹角均为90° ,晶胞中部分原子的分数坐标如下
表所示。
坐标原子 x y z
Cd 0 0 0
Sn 0 0 0.5
As 0.25 0.25 0. 125
①找出此晶胞中距离Cd(0,0,0)最远的As的位置_______(用分数坐标表示)。
②该化合物的化学式为_______,此晶体的密度为_______g·cm-3(列出计算式,阿伏。加德罗常数的值为
N )。
A
12.(2022·广东·高三阶段练习)最近,妖“镍”横行,价格疯涨。镍是一种硬而有延展性并具有铁磁性
的金属,在许多领域应用广泛。Ni-NTA-Nangold 可用于检测或定位 6x 组氨酸(His)或 Poly-His 标记的
重组蛋白。Ni(II)-NTA 的结构简式如图所示。
回答下列问题:
(1)基态Ni原子价电子排布式为_______。
(2)配体N(CH COO-) 中 4 种元素的第一电离能 I 从大到小的顺序为_______(用元素符号表示)。
2 3 1(3)与 Ni2+配位的原子形成的空间构型为_______。
(4)已知 存在大π键,其结构中氮原子的杂化方式为_______。
(5)Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点Ni明显高于Ca,其原因是_______。
(6)某笼形包合物Ni(CN)(NH )(C H) 的晶胞如图所示。
a 3 b 6 6 c
①该笼形包合物溶于酸能形成一种弱酸HCN,HCN中δ键和π键个数之比为_______。
②推测该包合物中氨与苯分子数目比,即b:c为_______,氨分子极易溶于水的原因是_______。
③若此晶胞体积为V nm3,阿伏加德罗常数为N ,晶胞的摩尔质量为M g/mol,则晶体密度为_______
A
g/cm3(例出计算表达式)。
13.(2022·山东省实验中学模拟预测)神舟十三号首次采用的大面积可展收柔性太阳电池翼,具有面积
轻量化、使用寿命长等突出优点。回答下列问题:
(1)太阳电池翼的主要材料为单质硅,其基态原子具有___________种不同能量的电子;若硅原子电子排布
表示为[Ne]3s23p ,则违背了___________(填原理名称)。
(2)由于硅的价层有d轨道可以利用,而碳没有,因此化合物的结构具有较大差异:化合物N(SiH )(平面
3 3
形)和N(CH )(三角锥形)中,更易形成配合物的是___________(填化学式);已知甲基的供电子能力强于氢
3 3
原子,则N(CH )、NH 中R—N—R(R代表C或H)键角较大的是___________(填化学式);1,3—二碘四
3 3 3
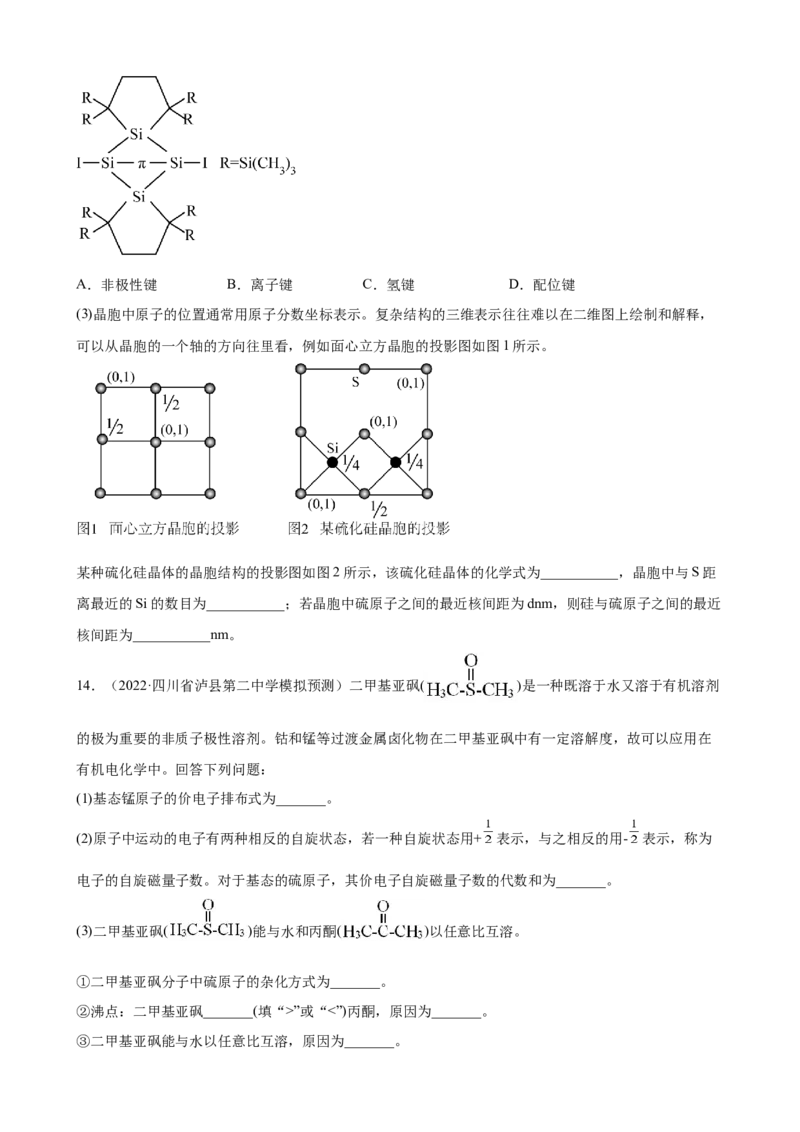
硅双环[1.1.0]丁烷分子如图所示,该分子中四个硅原子共面且其中两个硅原子间形成 电子单键(特殊
键)。该分子中硅原子的杂化形式是___________,该分子形成的晶体中不存在的化学键是___________
(填标号)。A.非极性键 B.离子键 C.氢键 D.配位键
(3)晶胞中原子的位置通常用原子分数坐标表示。复杂结构的三维表示往往难以在二维图上绘制和解释,
可以从晶胞的一个轴的方向往里看,例如面心立方晶胞的投影图如图1所示。
某种硫化硅晶体的晶胞结构的投影图如图2所示,该硫化硅晶体的化学式为___________,晶胞中与S距
离最近的Si的数目为___________;若晶胞中硫原子之间的最近核间距为dnm,则硅与硫原子之间的最近
核间距为___________nm。
14.(2022·四川省泸县第二中学模拟预测)二甲基亚砜( )是一种既溶于水又溶于有机溶剂
的极为重要的非质子极性溶剂。钴和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在
有机电化学中。回答下列问题:
(1)基态锰原子的价电子排布式为_______。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用- 表示,称为
电子的自旋磁量子数。对于基态的硫原子,其价电子自旋磁量子数的代数和为_______。
(3)二甲基亚砜( )能与水和丙酮( )以任意比互溶。
①二甲基亚砜分子中硫原子的杂化方式为_______。
②沸点:二甲基亚砜_______(填“>”或“<”)丙酮,原因为_______。
③二甲基亚砜能与水以任意比互溶,原因为_______。(4)CoCl ·4NH 有绿色和紫色两种结构,已知中心原子Co的配位数为6。将1mol绿色或紫色CoCl ·4NH
3 3 3 3
溶于水中,加入足量AgNO 溶液,均生成1molAgCl沉淀。
3
①CoCl ·4NH 中配离子的化学式为_______。
3 3
②NH 分子与钴离子形成配合物后H-N-H键角_______(填“变大”“变小”或“不变”)。
3
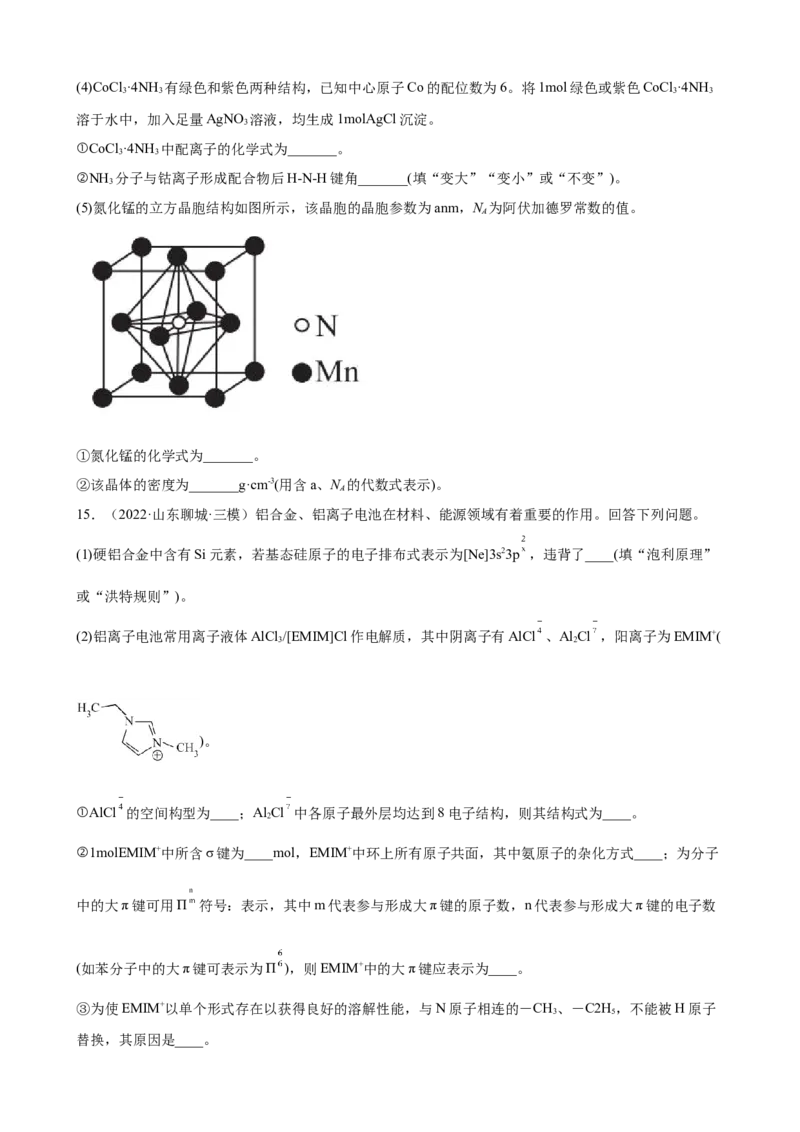
(5)氮化锰的立方晶胞结构如图所示,该晶胞的晶胞参数为anm,N 为阿伏加德罗常数的值。
A
①氮化锰的化学式为_______。
②该晶体的密度为_______g·cm-3(用含a、N 的代数式表示)。
A
15.(2022·山东聊城·三模)铝合金、铝离子电池在材料、能源领域有着重要的作用。回答下列问题。
(1)硬铝合金中含有Si元素,若基态硅原子的电子排布式表示为[Ne]3s23p ,违背了____(填“泡利原理”
或“洪特规则”)。
(2)铝离子电池常用离子液体AlCl /[EMIM]Cl作电解质,其中阴离子有AlCl 、Al Cl ,阳离子为EMIM+(
3 2
)。
①AlCl 的空间构型为____;Al Cl 中各原子最外层均达到8电子结构,则其结构式为____。
2
②1molEMIM+中所含σ键为____mol,EMIM+中环上所有原子共面,其中氨原子的杂化方式____;为分子
中的大π键可用Π 符号:表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数
(如苯分子中的大π键可表示为Π ),则EMIM+中的大π键应表示为____。
③为使EMIM+以单个形式存在以获得良好的溶解性能,与N原子相连的-CH、-C2H,不能被H原子
3 5
替换,其原因是____。(3)一种金属间化合物的晶胞结构如图所示:
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子
的分数坐标为(0,0,0),B点原子的分数坐标为( , , ),则C点Al原子在z轴方向上的分数坐标
z=___(用含c、s的代数式表示);已知:阿伏加德罗常数的值为N ,则该晶体的密度为____g•cm-3(列出计
A
算表达式)。
16.(2022·重庆一中模拟预测)氯元素成键能力强,形成的离子或化合物种类多样。研究这些化合物简
直妙不可言。
(1)氯原子的核外电子运动状态数为___________。
(2)根据VSEPR理论, 和 的空间构型分别是___________和___________,S和I分别以
___________和___________杂化轨道同氯原子形成共价键。
(3) 和 是等电子体,其S-Cl键键长___________(填“>”“=”或“<”)P-Cl键键长,原因是
___________。
(4) 的结构如图, 的配位数为___________, 可看做位于由距离最近的 所围成的
___________空隙中(填几何图形);如 的摩尔质量为M,晶胞参数为apm,密度为 ,则 与
的最近距离为___________, (阿伏加德罗常数)的计算式为___________。17.(2022·北京·北师大实验中学三模)酚和芳香胺有广泛用途。
资料:i.苯酚分子中O的杂化轨道类型是sp2,未参与杂化的p轨道中有一对电子,该p轨道正好与苯环
的π电子轨道发生侧面重叠,形成p-π共轭体系(大π键),使O的电子向苯环转移。
ii.苯胺分子结构与苯酚有相似之处,N的孤对电子占据的轨道也和苯环的π电子轨道部分重叠,形成共
轭体系。
(1)p电子云轮廓图的形状是_______。
(2)C、H、O三种元素的电负性由强到弱的顺序是_______。
(3)比较相同条件下,苯酚与氯苯在水中的溶解度并说明理由:_______。
(4)苯胺分子中的原子不在同一平面内,N的杂化轨道类型是_______。
(5)下列说法正确的是_______(填序号)。
a.第一电离能: O>N>C
b.苯酚具有酸性与分子中的p-π共轭有关
c.苯胺的碱性比氨强
d.苯胺可能与溴水发生取代反应
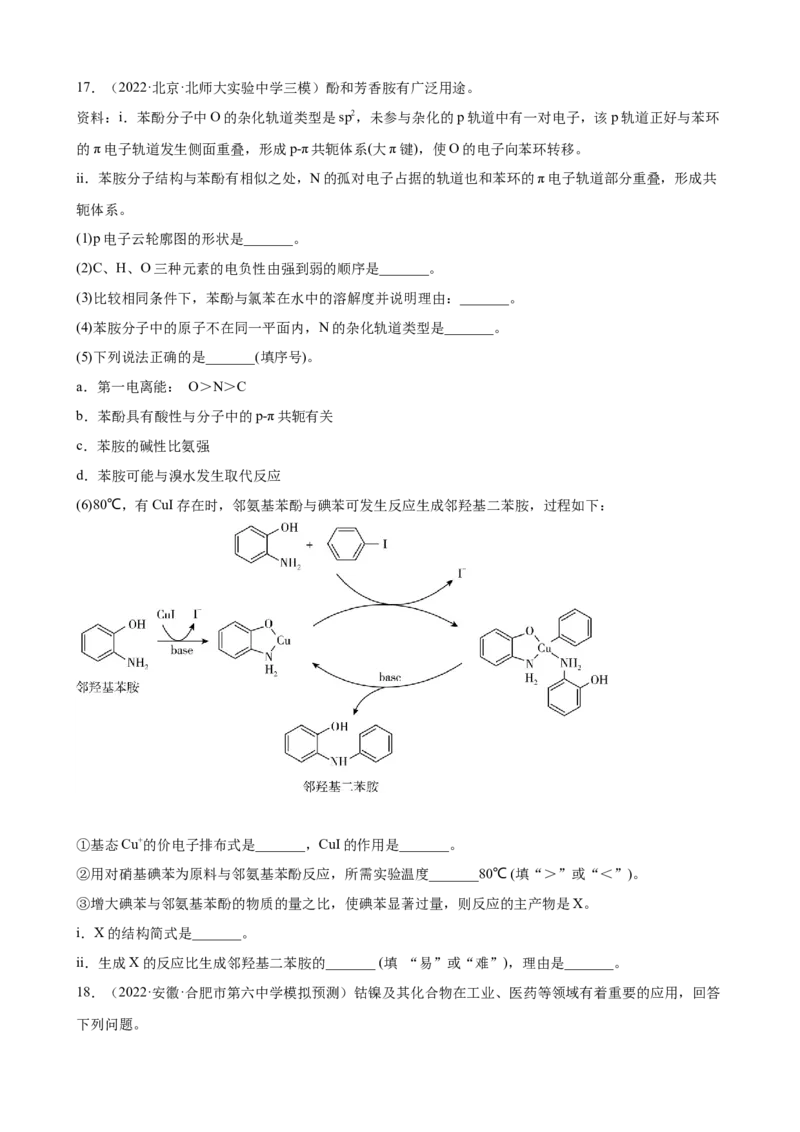
(6)80℃,有CuI存在时,邻氨基苯酚与碘苯可发生反应生成邻羟基二苯胺,过程如下:
①基态Cu+的价电子排布式是_______,CuI的作用是_______。
②用对硝基碘苯为原料与邻氨基苯酚反应,所需实验温度_______80℃ (填“>”或“<”)。
③增大碘苯与邻氨基苯酚的物质的量之比,使碘苯显著过量,则反应的主产物是X。
i.X的结构简式是_______。
ii.生成X的反应比生成邻羟基二苯胺的_______ (填 “易”或“难”),理由是_______。
18.(2022·安徽·合肥市第六中学模拟预测)钴镍及其化合物在工业、医药等领域有着重要的应用,回答
下列问题。(1)Co2+的价电子的电子排布图为____。
(2)Na [Co(NO )]常用于检验钾离子,NO 的空间构型为____,任写一个与NO 互为等电子体的分子:
3 2 6
____(填化学式),Na[Co(NO )]中存在的化学键类型有___。
3 2 6
(3)NH 可与Co2+形成[Co(NH )]2+,与游离的氨分子相比,其键角∠H—N—H变大,原因是____。
3 3 6
(4)砷化镍可用于制造发光器件,第一电离能:As____Se(填“>”或“<"),原因是___。
(5)镍钛记忆合金用于飞机外壳。已知一种镍钛合金的晶胞结构如图所示,其中Ti原子采用面心立方最密
堆积方式,该合金中与Ti原子距离最近且相等的Ni原子个数为____;若合金的密度为ρg·cm-3,设N 是
A
阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是___pm(用含ρ和N 的计算式表示,不必化简)。
A
19.(2022·海南海口·二模)工业上利用铁酸镓 、铁酸锌 为原料可以提取铁、
锌、镓,并采用MOCVD(金属有机物化学气相沉淀)技术制备砷化镓(GaAs),利用MOCVD技术制备
GaAs的反应原理为 。
回答下列问题:
(1)基态铁原子的价层电子排布式为___________。
(2)在周期表中,铜和锌相邻。电离能: ___________ (填“>”“<”或“=”,下同),
___________ 。
(3) 、 分子相同的是___________(填字母)。
A.空间构型 B.中心原子的杂化轨道类型 C.分子极性 D.化学键类型
(4)GaN、GaAs是常用的半导体材料,其晶体的熔点分别为1700℃、1238℃,前者熔点高于后者的主要原
因是___________;它们的组成元素Ga、N、As的电负性由大到小的顺序是___________。
(5)砷化镓的晶胞结构如图所示。①镓原子可以看成是填充在砷原子构成的空隙中,镓原子填充这样的空隙中构成正四面体形,这样的空
隙填充率为___________。
②设 是阿伏加德罗常数的值,晶体的密度为 。砷化镓晶胞中相邻两个面心上砷原子之间的距
离为___________pm(用含 、 的计算式表示)。
20.(2022·广西广西·模拟预测)我国科学家研究发现AgGrS 在室温下具有超离子行为(原子可在晶体中
2
自由移动)。回答下列问题:
(1)基态铬原子的核外电子排布式为___________, 基态硫原子核外有___________种不同运动状态的电子。
(2)与硫元素同族的几种元素中,电负性最大的是___________ ( 填元素符号)。常见含硫的微粒有SO 、
2
SO 、 、 、 HS等, 的空间构型为___________ ; 请写出与HS互为等电子体的一种微粒
3 2 2
的化学式___________ ;SO 、SO 杂化轨道类型相同,但键角SO 大于SO ,原因是___________。
2 3 3 2
(3)Ag+与氨水形成的二氨合银配离子[Ag(NH)]+的空间构型是直线型,则其中心原子的杂化类型是_____,
3 2
该配离子中的配位原子是___________(填元素符号),lmol该配离子中含有的σ键的数目为________。
(4)复合材料氧铬酸钙的立方晶胞如图所示。
已知A、B的原子分数坐标分别为(0,0,0)、(1,1,0),则C的原子分数坐标为___________,该物质的
化学式为___________,已 知钙和氧的最近距离为a pm。晶体的密度ρ g·cm-3,则阿伏加德罗常数
N =___________ mol-1( 用含a和ρ的式子表示,列出计算式即可)。
A
21.(2022·四川·宁南中学高三阶段练习)金属单质及其化合物是化工生产、生活中常用的材料
(1)基态Ni原子价电子排布图为_______。(2)某镍配合物由1个Ni2+与2个 形成。
①形成该镍配合物的元素中,第二周期元素的第一电离能由小到大的顺序为_______(用元素符号表示) ,
配合物中C采用的杂化类型为_______。
②已知该配合物中只有一种元素的原子与Ni2+配位,则与镍配位的原子为_______(填“C”、“N"”或“O")
(3)Ni(CO) 是常温下呈液态的镍的重要配合物,易溶于CCl 、苯等有机溶剂,则Ni(CO) 的空间构型为
4 4 4
_______,Ni(CO) 中含有的σ键与π键的数目之比为_______,与CO互为等电子的离子有_______(任写
4
一种)。
(4)MgCO 的热分解温度低于CaCO 的原因是_______。
3 3
(5)Na O的晶胞结构如图,Na+的配位数为_______。已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数为
2
N ,则两个最近的氧离子间距离为_______nm(用含ρ、N 的计算式表示)。
A A
22.(2022·陕西·西北工业大学附属中学模拟预测)“嫦娥五号”首次实现了我国地外天体采样返回,带
回的月壤中包含了H、O、N、A1、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。回答下列问题:
(1)锌(Zn)、镉(Cd)是同一副族的相邻元素,Cd的原子序数更大,则基态Cd原子的价电子轨道表示式为
_______。
(2)若配离子[Fe(CN) ](x-2)-的中心离子价电子数与配体提供的电子数之和为18,则x=_______。
x
(3)碲和硫同主族,TeO 的空间构型为_______,写出一个与TeO 互为等电子体的分子_______。
(4)咪唑、噻唑、吡啶是含N和S的有机杂环类化合物,结构如图所示:①上述三种物质中,沸点最高的是_______(填化学名称)。
②吡啶中氮原子的杂化轨道的空间构型为_______。
③已知咪唑中存在大π键,则在咪唑分子的两个氮原子中,更容易与Cu2+形成配位键的是_______(填
“①”或“②”)号氮原子。
(5)Fe3+容易形成六配位的配合物,[Fe(H O) ]3+通常会水解生成棕色的[Fe(H O) (OH)]2+,通过氢氧根离
2 6 2 5
子形成双聚体[Fe (H O) (OH) ]4+,请写出该双聚体的结构(水分子中O-H键省略,其他化学键用短横线
2 2 8 2
“-”表示)_______。
(6)“嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在
结构单元内部),已知该结构单元底面(正六边形)边长为anm,该合金的密度为ρg·cm-3,则
h=_______cm(列出计算式,设N 为阿伏加德罗常数的值)。
A参考答案:
1.(1)3d
(2)N、S、K
(3) sp2 分子晶体 4d105s1
(4) 100% 金刚石的熔点高。C 是分子晶体,金刚石是共价晶体,所以金刚石的熔点
60
较高
2.(1)
(2)Fe3+的3d能级为3d5,处于半充满状态,较稳定
(3)钙的原子半径较大且价电子数较少,金属键较弱
(4) sp3 < 16
(5) 6 面心
3.(1)
(2) Mg<C<O CO CH 甲醇为极性分子,且甲醇分子间能形成氢键
2 4
(3) C 分子晶体
(4) 3.6 0.30
4.(1) 哑铃形 sp2 正四面体
(2) 第四周期第IVB族 [Ar]3d24s2
(3) AB Cr O + 3H O+8H+=2Cr3++3O ↑+7H O
2 2 2 2 2
(4)
5.(1)1s22s22p63s23p63d64s2或[Ar]3d64s2
(2) 1:1 CO
(3)N>C>H
(4) 正四面体形 sp3(5) (1, , ) ×
6.(1)4
(2) V形 4 共价键、配位键 sp2
(3) 6 ≈5.62
7.(1) 3s23p3 16
(2) sp2
(3)正四面体
(4) CO、NO或CS(写一种即可) 三者结构相似,电负性:N>P>As,中心原子电负
2 2 2
性越大,成键电子对越靠近中心原子,成键电子对距离越小,排斥力越大,则键角越大
(5)b
8.(1)第四周期第VIII族
(2)球形、哑铃形(或哑铃状)
(3)sp3
(4)CH (或SiH、GeH 、 BH 、 AlH )
4 4 4
(5)
(6) 、NH
3
(7)[Ar]3d8 (或1s2 2s2 2p63s2 3p63d8)
(8)
9.(1) 或
(2)甲醛、苯
(3) BC
(4) 属于离子晶体, 属于分子晶体,离子晶体的沸点主要取决于离子键,分子
晶体的沸点主要取决于分子间作用力,离子键通常强于分子间作用力(合理即可)(5) 中,配位键 键的成键电子对相比 中孤电子对对 键的排斥力变
小,故 中 键角变大
(6) 8
10.(1)sp2
(2) 14:13 [S=C=N]-
(3) C C 原子的电负性比O的小,对孤电子对的吸引力更小,更容易给出孤电子对
(4)钛、锗、硒
(5)6
(6) 正四面体 2:3 或 或
11.(1) d 5s25p4
(2)As>Se> Te
(3) AF 正四面体
(4) sp3 19
(5) (0.25,0.75,0.875)、(0.75,0.25,0.875) CdSnAs
2
(合理即可)
12.(1)3d84s2
(2)N>O>H>C
(3)八面体
(4)sp2
(5)Ni与Ca同周期,Ni的原子半径比较小且价电子数多,形成的金属键比较强,熔沸点比
较高
(6) 1:1 1:1 氨分子和水分子间可以形成氢键,氨分子和水分子极性接近,溶解
度大 M×1021/(N V)
A
13.(1) 5 洪特规则
(2) N(CH ) N(CH ) sp2,sp3 BD
3 3 3 3(3) SiS 2 d
2
14.(1)3d54s2
(2)+1(或-1)
(3) sp3 > 二甲基亚砜的相对分子质量大于丙酮,因此分子间的范德华力较
大,沸点较高 二甲基亚砜能够与水分子之间形成氢键,且与水均为极性分子
(4) [Co(NH )Cl]+ 变大
3 4 2
(5) Mn N
4
15.(1)洪特规则
(2) 正四面体 19 sp2 Π 氨原子上
连氢原子易形成分子间氢键,使该离子不易以单个形式存在
(3)
16.(1)17
(2) 三角锥 平面正方形
(3) < S有较大核电荷,处于较高氧化态
(4) 8 正四面体
17.(1)纺锤形(或哑铃形)
(2)O>C>H
(3)相同条件下,苯酚在水中的溶解度大于氯苯,因为苯酚分子含有电负性较强的O原子,
和水分子之间会形成氢键,而氯苯不含O原子,不能和水分子形成氢键
(4)sp3杂化
(5)bd(6) 3d10 催化剂 < 难 中间产
物 的空间阻力较大,不易生成
18.(1)
(2) V形 SO 共价键、离子键、配位键
2
(3)氨分子与Co2+形成配位键,孤电子对变成σ键电子对,与氨分子的成键电子对间的斥力
减弱,键角增大
(4) > As原子价电子排布式为4s24p3,是半充满结构,较为稳定,难以失去电子
(5) 6 × ×1010
19.(1)
(2) < >
(3)BD
(4) 它们都是原子晶体,原子半径: ,键能:
(5) 50%
20.(1) 1s22s22p63s23p63d54s1(或[Ar]3d54s1) 16
(2) O 三角锥形 HO SO 中含有一个孤电 子对而SO 中没有孤电子对,
2 2 3孤电子对对成键电子对有较强的排斥力,导致SO 键角减小
2
(3) sp N 8mol
(4) ( ,1, ) CaCrO
3
21.(1)
(2) C