文档内容
2023届高考化学一轮备考专题强化训练题:化学反应原理综合题
1.(2022·重庆市育才中学模拟预测)元素镓( )在半导体、太阳能电池和合金材料等领域具有重要应
用。
(1)惰性气体保护下, (三乙基镓)蒸汽在紫外光照射时可分解制得高纯度的 ,同时生成乙烯
和单质___________。
(2) 和 相似, 与 溶液反应的化学方程式为___________; 能与氨水发生中和反应,
则酸性: ___________ (填“>”“<”或“=”)。
(3)一定条件下,在恒容密闭容器中加入 ,平衡后 的物质的量
分数为0.25。
① 的转化率 ___________
②计算 ___________ (设 起始浓度为 )。
③对于上述反应,下列叙述正确的是___________(填标号)。
a.平衡后
b.增加 浓度,平衡后 的转化率减小
c.除低温度,平衡后 的物质的量分数增大
d.若缩小体积,则平衡后 的转化率增大
(4)液态金属 (熔点为 )在能源储存和纳米材料等领域具有重要应用价值。如图液态 作电极经
电化学合成尺寸均匀的 晶体的示意图。回答下列问题:
①生成 晶体的电极反应式为___________。
②利用液态 电极合成出 晶体的过程是___________。
2.(2022·四川·威远中学校高三阶段练习)回答下列问题
(1)向某体积固定的密闭容器中加入0.3molA、0.1molC和一定量(未知)的B三种气体,一定条件下发生反
应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回
答:
①若t=15,则t-t 内反应速率v(C) =_______,A的转化率为_______;
1 0 1
②写出反应的化学方程式:_______。
③B的起始的物质的量是_______mol;t 后向容器中充入氦气,反应速率_______。(填增大、减小或者不
2
变)
(2)已知断裂几种化学键要吸收的能量如下:
化学键 C-H O=O C=O H-O
断裂1mol键吸收的能量/kJ 415 497 745 463
16 gCH 在O 中完全燃烧生成气态CO 和气态水时_______(填“吸收”或 “放出”)约_______kJ热量。
4 2 2
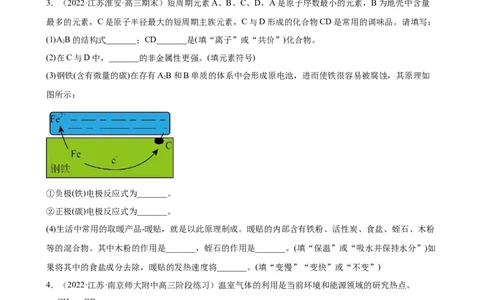
(3)燃料电池是一种高效、环境友好的供电装置,如图为乙醇燃料电池的工作原理示意图,a、b均为惰性
电极。①使用时,空气从_______口通入(填“A”或“B”);
②a极的电极反应为:_______。
3.(2022·江苏淮安·高三期末)短周期元素A、B、C、D,A是原子序数最小的元素,B为地壳中含量
最多的元素,C是原子半径最大的短周期主族元素,C与D形成的化合物CD是常用的调味品。请填写:
(1)A B的结构式_______;CD_______是(填“离子”或“共价”)化合物。
2
(2)在C与D中,_______的非金属性更强。(填元素符号)
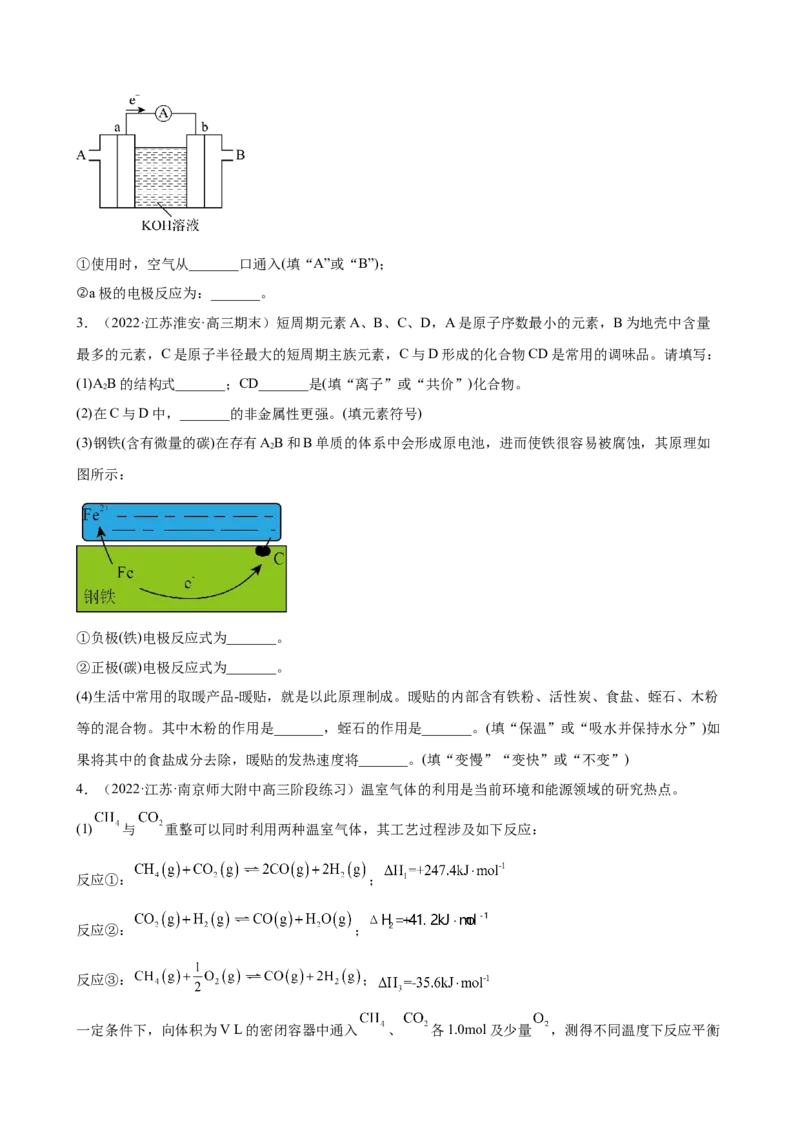
(3)钢铁(含有微量的碳)在存有AB和B单质的体系中会形成原电池,进而使铁很容易被腐蚀,其原理如
2
图所示:
①负极(铁)电极反应式为_______。
②正极(碳)电极反应式为_______。
(4)生活中常用的取暖产品-暖贴,就是以此原理制成。暖贴的内部含有铁粉、活性炭、食盐、蛭石、木粉
等的混合物。其中木粉的作用是_______,蛭石的作用是_______。(填“保温”或“吸水并保持水分”)如
果将其中的食盐成分去除,暖贴的发热速度将_______。(填“变慢”“变快”或“不变”)
4.(2022·江苏·南京师大附中高三阶段练习)温室气体的利用是当前环境和能源领域的研究热点。
(1) 与 重整可以同时利用两种温室气体,其工艺过程涉及如下反应:
反应①: ;
反应②: ;
反应③: ;
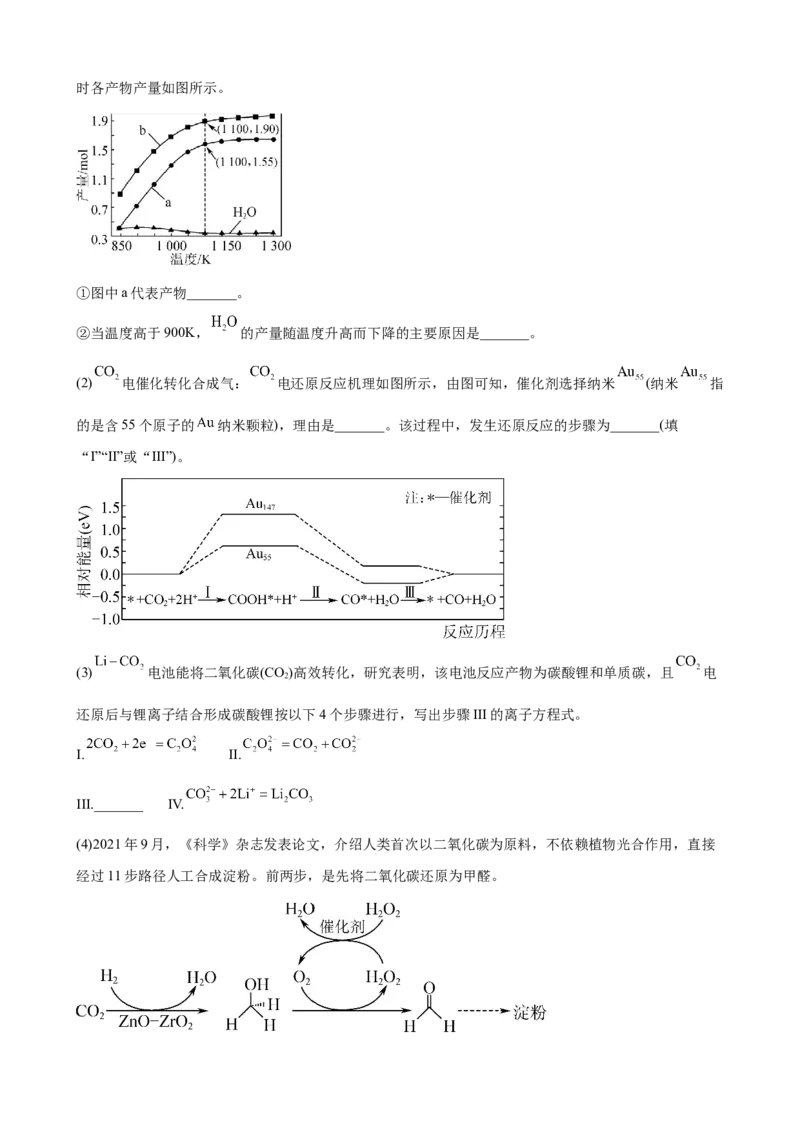
一定条件下,向体积为V L的密闭容器中通入 、 各1.0mol及少量 ,测得不同温度下反应平衡时各产物产量如图所示。
①图中a代表产物_______。
②当温度高于900K, 的产量随温度升高而下降的主要原因是_______。
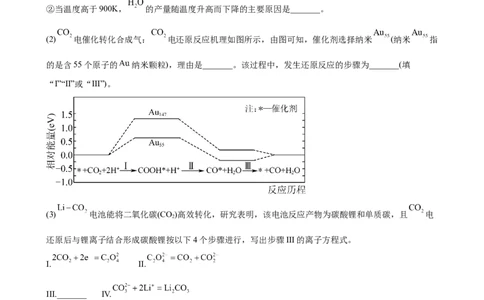
(2) 电催化转化合成气: 电还原反应机理如图所示,由图可知,催化剂选择纳米 (纳米 指
的是含55个原子的 纳米颗粒),理由是_______。该过程中,发生还原反应的步骤为_______(填
“I”“II”或“III”)。
(3) 电池能将二氧化碳(CO)高效转化,研究表明,该电池反应产物为碳酸锂和单质碳,且 电
2
还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤III的离子方程式。
I. II.
III._______ IV.
(4)2021年9月,《科学》杂志发表论文,介绍人类首次以二氧化碳为原料,不依赖植物光合作用,直接
经过11步路径人工合成淀粉。前两步,是先将二氧化碳还原为甲醛。请写出前两步总反应的化学方程式:_______。
5.(2022·四川·宁南中学高三阶段练习)回答下列问题
(1)甲烷重整是提高甲烷利用率的重要方式,
CH(g)+HO(g) CO(g)+3H(g) △H =+206kJ•mol﹣1 ①
4 2 2 1
CH(g)+CO (g) 2CO(g)+2H(g) △H =+247.2kJ•mol﹣1 ②
4 2 2 2
CO(g)+HO(g) CO(g)+H(g) △H
2 2 2 3
△H=_______kJ•mol﹣1。
3
(2)汽车尾气中含有较多的氮氧化物和不完全燃烧的CO,汽车三元催化器可以实现降低氮氧化物的排放量。
汽车尾气中的NO(g)和CO(g)在催化剂的作用下转化成两种无污染的气体,2NO(g)+2CO(g) N(g)
2
+2CO (g) △H;在体积为1L的密闭容器中充入1mol CO和1mol NO,一定条件下测得CO的平衡转化率
2
与温度、压强关系如图所示:
①△H_______0,p_______p(填><或=)
1 2
②在恒定压强为p,温度为200℃下,经过5min达到平衡时,N 的平均反应速率为_______,则该温度下
1 2
的平衡常数为_______。(保留三位有效数字)
③若在恒容的密闭容器中,充入1mol CO和1mol NO发生反应,下列选项中不能说明该反应已经达到平
衡状态的是_______。
A.CO和NO的物质的量之比不变 B.混合气体的密度保持不变
C.混合气体的压强保持不变 D.气体的平均相对分子质量保持不变
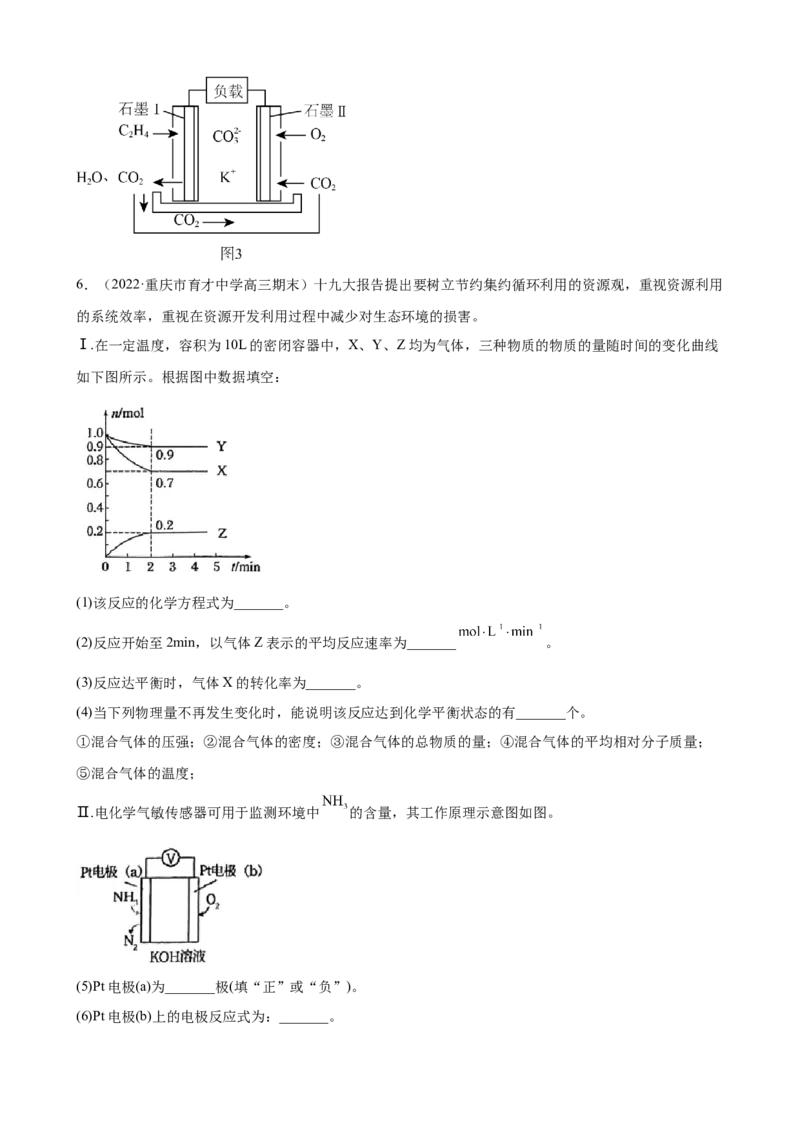
(3)某乙烯熔融碳酸盐燃料电池工作原理如图3所示,则负极上电极反应式_______。6.(2022·重庆市育才中学高三期末)十九大报告提出要树立节约集约循环利用的资源观,重视资源利用
的系统效率,重视在资源开发利用过程中减少对生态环境的损害。
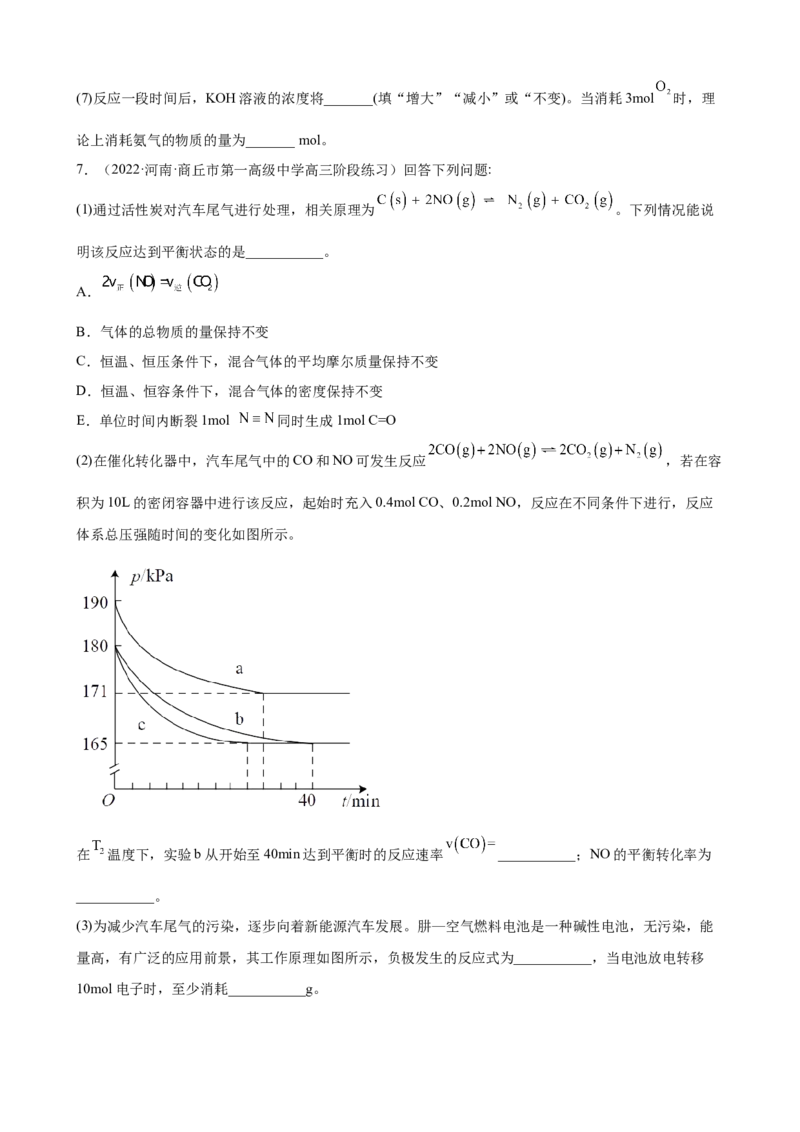
Ⅰ.在一定温度,容积为10L的密闭容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线
如下图所示。根据图中数据填空:
(1)该反应的化学方程式为_______。
(2)反应开始至2min,以气体Z表示的平均反应速率为_______ 。
(3)反应达平衡时,气体X的转化率为_______。
(4)当下列物理量不再发生变化时,能说明该反应达到化学平衡状态的有_______个。
①混合气体的压强;②混合气体的密度;③混合气体的总物质的量;④混合气体的平均相对分子质量;
⑤混合气体的温度;
Ⅱ.电化学气敏传感器可用于监测环境中 的含量,其工作原理示意图如图。
(5)Pt电极(a)为_______极(填“正”或“负”)。
(6)Pt电极(b)上的电极反应式为:_______。(7)反应一段时间后,KOH溶液的浓度将_______(填“增大”“减小”或“不变)。当消耗3mol 时,理
论上消耗氨气的物质的量为_______ mol。
7.(2022·河南·商丘市第一高级中学高三阶段练习)回答下列问题:
(1)通过活性炭对汽车尾气进行处理,相关原理为 。下列情况能说
明该反应达到平衡状态的是___________。
A.
B.气体的总物质的量保持不变
C.恒温、恒压条件下,混合气体的平均摩尔质量保持不变
D.恒温、恒容条件下,混合气体的密度保持不变
E.单位时间内断裂1mol 同时生成1mol C=O
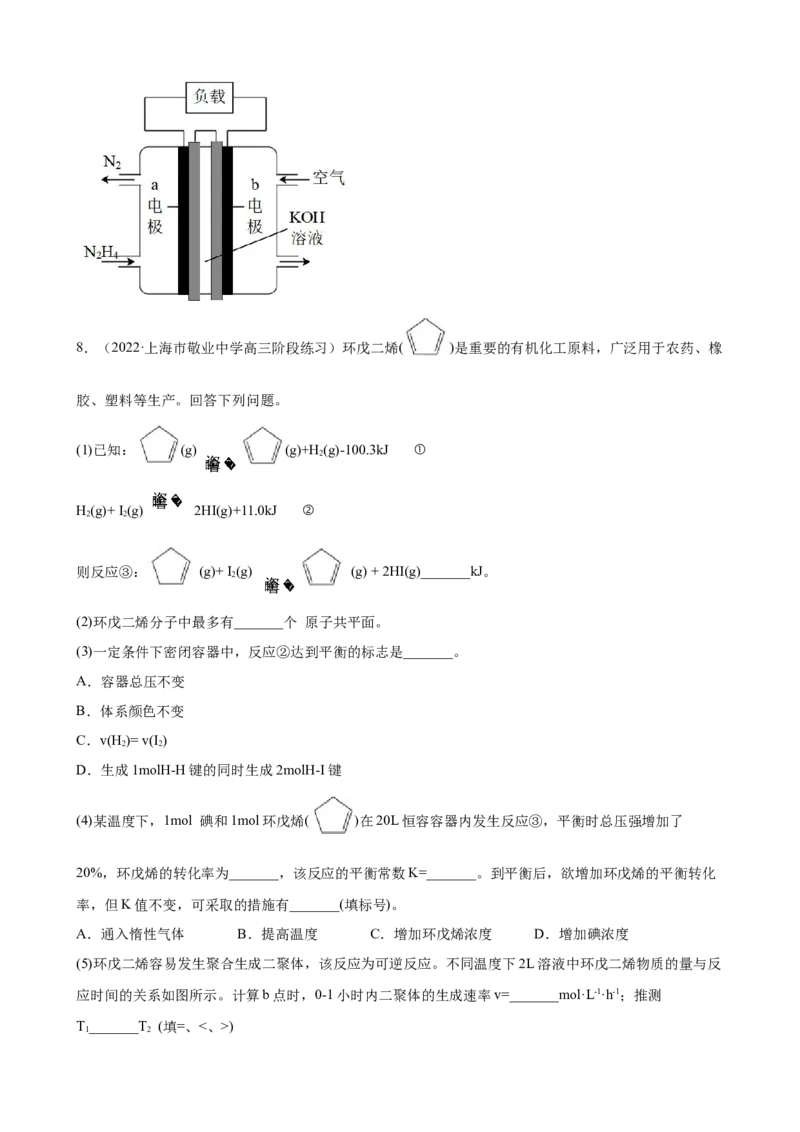
(2)在催化转化器中,汽车尾气中的CO和NO可发生反应 ,若在容
积为10L的密闭容器中进行该反应,起始时充入0.4mol CO、0.2mol NO,反应在不同条件下进行,反应
体系总压强随时间的变化如图所示。
在 温度下,实验b从开始至40min达到平衡时的反应速率 ___________;NO的平衡转化率为
___________。
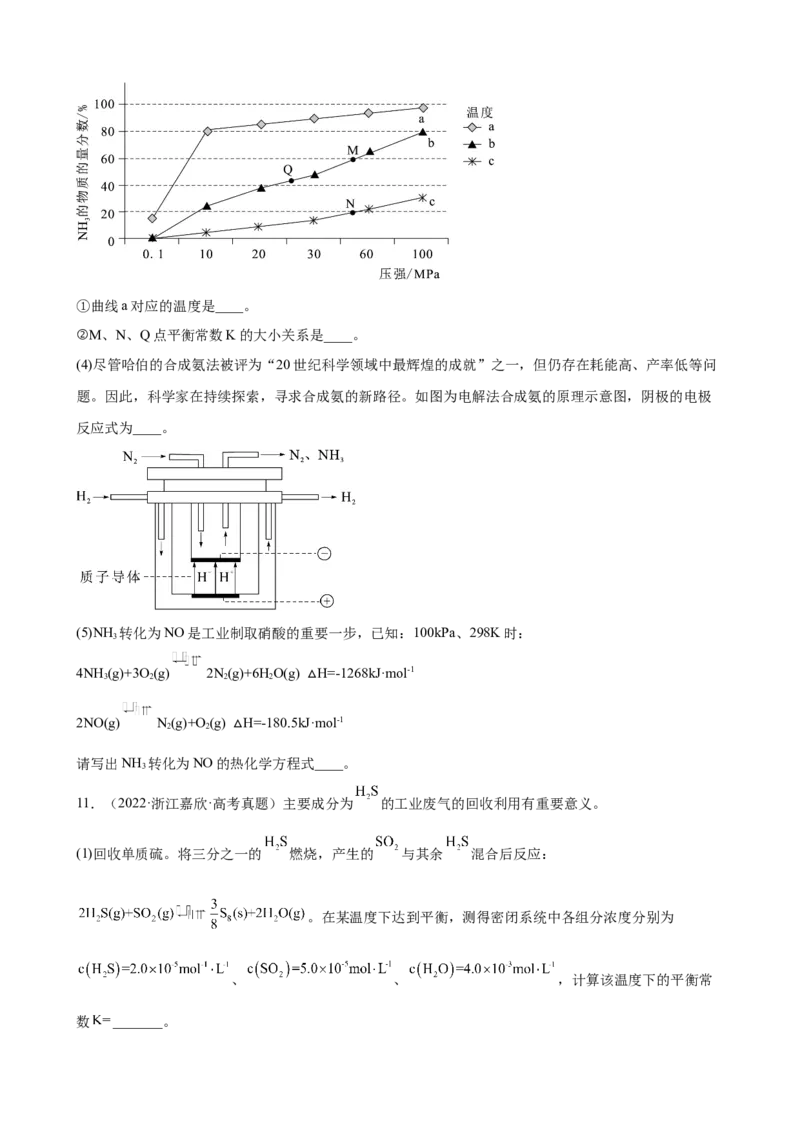
(3)为减少汽车尾气的污染,逐步向着新能源汽车发展。肼—空气燃料电池是一种碱性电池,无污染,能
量高,有广泛的应用前景,其工作原理如图所示,负极发生的反应式为___________,当电池放电转移
10mol电子时,至少消耗___________g。8.(2022·上海市敬业中学高三阶段练习)环戊二烯( )是重要的有机化工原料,广泛用于农药、橡
胶、塑料等生产。回答下列问题。
(1)已知: (g) (g)+H(g)-100.3kJ ①
2
H(g)+ I (g) 2HI(g)+11.0kJ ②
2 2
则反应③: (g)+ I (g) (g) + 2HI(g)_______kJ。
2
(2)环戊二烯分子中最多有_______个 原子共平面。
(3)一定条件下密闭容器中,反应②达到平衡的标志是_______。
A.容器总压不变
B.体系颜色不变
C.v(H )= v(I )
2 2
D.生成1molH-H键的同时生成2molH-I键
(4)某温度下,1mol 碘和1mol环戊烯( )在20L恒容容器内发生反应③,平衡时总压强增加了
20%,环戊烯的转化率为_______,该反应的平衡常数K=_______。到平衡后,欲增加环戊烯的平衡转化
率,但K值不变,可采取的措施有_______(填标号)。
A.通入惰性气体 B.提高温度 C.增加环戊烯浓度 D.增加碘浓度
(5)环戊二烯容易发生聚合生成二聚体,该反应为可逆反应。不同温度下2L溶液中环戊二烯物质的量与反
应时间的关系如图所示。计算b点时,0-1小时内二聚体的生成速率v=_______mol·L-1·h-1;推测
T_______T (填=、<、>)
1 29.(2022·黑龙江·哈尔滨三中模拟预测)乙醇在催化剂存在下受热发生脱水反应,既可分子内脱水生成
乙烯,也可分子间脱水生成乙醚,具体反应式如下:
①C HOH(g)=C H(g)+HO(g)
2 5 2 4 2
②2C HOH(g)=C HOC H(g)+HO(g)
2 5 2 5 2 5 2
已知:乙醇和乙醚的沸点分别为78.4℃和34.5℃。
试回答下列问题:
(1)若150℃时,一定量的乙醇脱水转化为7gC H,该反应吸收11.5kJ的热量,则其热化学方程式为____。
2 4
(2)反应进程与相对能量如图所示:
由图可知反应②的 H____0(填“>”“=”或“<”);要提高反应①的平衡转化率,可采取的措施为____(填选
项)。 △
A.体积不变,增大压强 B.升温
C.体积不变,增加乙醇的量 D.及时分离出乙烯
(3)已选取适当催化剂后,要缩短反应②达到平衡的时间,可采取的措施有____。
(4)如表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据(设每次实
验反应时间均相同):
反应温度(℃) 乙醇转化率(%) 乙烯选择性(%) 乙醚选择性(%)
100 25.22 4.38 94.52150 54.25 52.24 46.71
200 78.69 55.26 43.70
250 95.20 96.80 2.20
300 99.56 98.49 1.20
350 99.84 99.20 0.36
注:乙烯选择性= ;乙醚选择性=
①在该催化剂条件下制乙烯,选择合适的温度区间是____。温度不宜过低或过高的原因是____。
②250℃时,若在体积为1L的恒容密闭容器中投入1molCH CHOH进行反应,反应达平衡时,乙醇的平
3 2
衡转化率为a,乙烯的选择性为m,乙醚的选择性为m。求250℃时反应①的化学平衡常数K为____(用
1 2
含a、m、m 的代数式表示)。
1 2
10.(2022·北京市回民学校模拟预测)氨对人类的生存和发展有着重要意义,1909年哈伯在实验室中首
次利用氮气与氢气反应合成氨,实现了人工固氮。
(1)①反应N(g)+3H(g) 2NH (g)的化学平衡常数表达式为_____。
2 2 3
②实验室检验氨气的方法是____。
(2)在一定条件下氨的平衡含量如表。
温度/℃ 压强/MPa 氨的平衡含量
200 10 81.5%
550 10 8.25%
①该反应为_____(填“吸热”或“放热”)反应。
②哈伯选用的条件是550℃、10MPa,而非200℃、10MPa,可能的原因是____。
(3)实验室研究是工业生产的基石。如图中的实验数据是在其它条件不变时,不同温度(200℃、400℃、
600℃)、压强下,平衡混合物中NH 的物质的量分数的变化情况。
3①曲线a对应的温度是____。
②M、N、Q点平衡常数K的大小关系是____。
(4)尽管哈伯的合成氨法被评为“20世纪科学领域中最辉煌的成就”之一,但仍存在耗能高、产率低等问
题。因此,科学家在持续探索,寻求合成氨的新路径。如图为电解法合成氨的原理示意图,阴极的电极
反应式为____。
(5)NH 转化为NO是工业制取硝酸的重要一步,已知:100kPa、298K时:
3
4NH (g)+3O(g) 2N(g)+6HO(g) H=-1268kJ·mol-1
3 2 2 2
△
2NO(g) N(g)+O(g) H=-180.5kJ·mol-1
2 2
△
请写出NH 转化为NO的热化学方程式____。
3
11.(2022·浙江嘉欣·高考真题)主要成分为 的工业废气的回收利用有重要意义。
(1)回收单质硫。将三分之一的 燃烧,产生的 与其余 混合后反应:
。在某温度下达到平衡,测得密闭系统中各组分浓度分别为
、 、 ,计算该温度下的平衡常
数 _______。(2)热解 制 。根据文献,将 和 的混合气体导入石英管反应器热解(一边进料,另一边出料),
发生如下反应:
Ⅰ
Ⅱ
总反应:
Ⅲ
投料按体积之比 ,并用 稀释;常压,不同温度下反应相同时间后,测得 和
体积分数如下表:
温度/ 950 1000 1050 1100 1150
0.5 1.5 3.6 5.5 8.5
0.0 0.0 0.1 0.4 1.8
请回答:
①反应Ⅲ能自发进行的条件是_______。
②下列说法正确的是_______。
A.其他条件不变时,用Ar替代 作稀释气体,对实验结果几乎无影响
B.其他条件不变时,温度越高, 的转化率越高
C.由实验数据推出 中的 键强于 中的 键
D.恒温恒压下,增加 的体积分数, 的浓度升高
③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过程能量示意图
_______。④在 ,常压下,保持通入的 体积分数不变,提高投料比 , 的转化率不
变,原因是_______。
⑤在 范围内(其他条件不变), 的体积分数随温度升高发生变化,写出该变化规律并分
析原因_______。
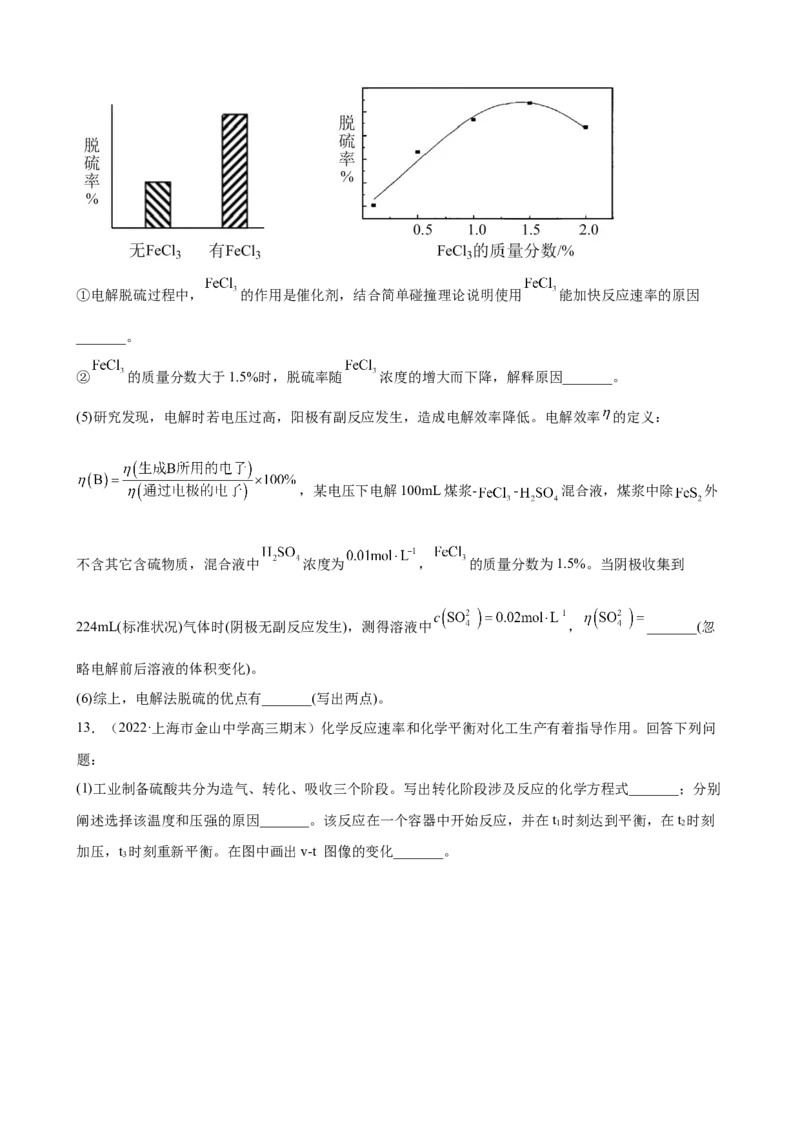
12.(2022·北京市第十七中学高三阶段练习)电化学原理被广泛应用于生产、生活的许多方面,利用电
解法脱除煤中的含硫物质(主要是 )的原理如图所示。
(1)阴极石墨棒上有无色气体产生,该气体是_______。
(2)阳极的电极反应式为_______。
(3)补全脱硫反应方程式:_______。
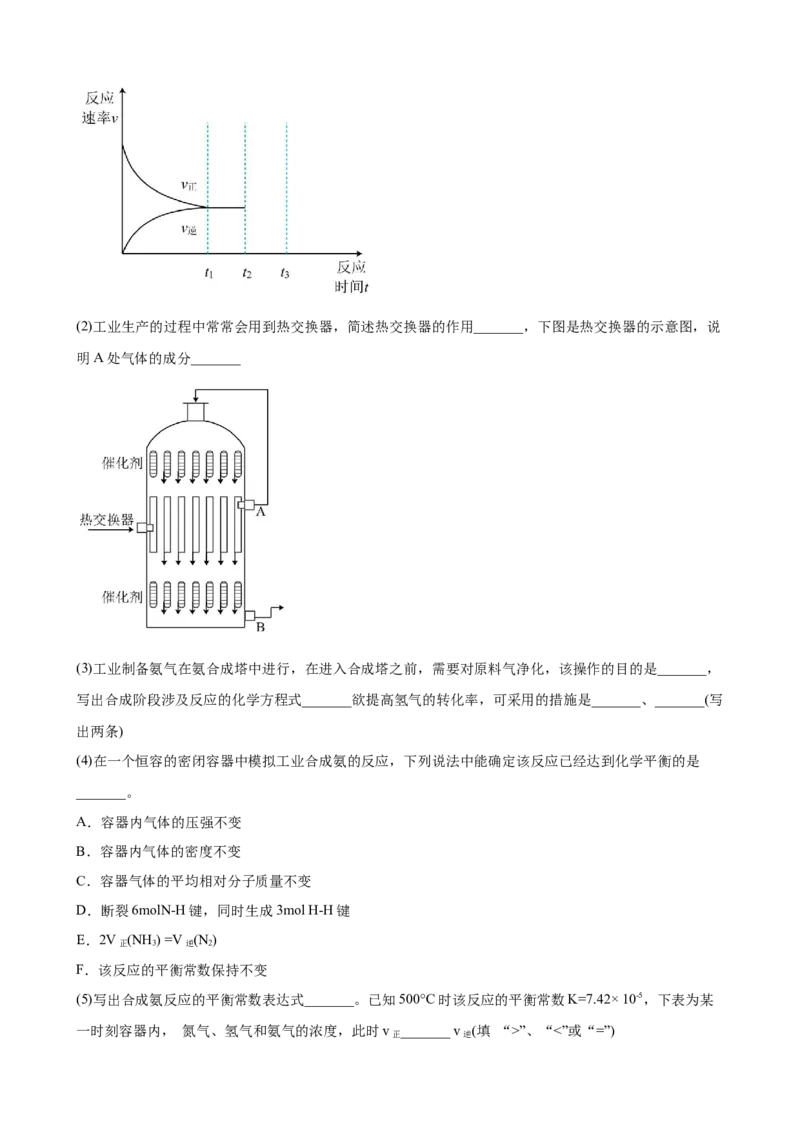
(4)相同反应时间, 对脱硫率的影响如图所示。①电解脱硫过程中, 的作用是催化剂,结合简单碰撞理论说明使用 能加快反应速率的原因
_______。
② 的质量分数大于1.5%时,脱硫率随 浓度的增大而下降,解释原因_______。
(5)研究发现,电解时若电压过高,阳极有副反应发生,造成电解效率降低。电解效率 的定义:
,某电压下电解100mL煤浆- - 混合液,煤浆中除 外
不含其它含硫物质,混合液中 浓度为 , 的质量分数为1.5%。当阴极收集到
224mL(标准状况)气体时(阴极无副反应发生),测得溶液中 , _______(忽
略电解前后溶液的体积变化)。
(6)综上,电解法脱硫的优点有_______(写出两点)。
13.(2022·上海市金山中学高三期末)化学反应速率和化学平衡对化工生产有着指导作用。回答下列问
题:
(1)工业制备硫酸共分为造气、转化、吸收三个阶段。写出转化阶段涉及反应的化学方程式_______;分别
阐述选择该温度和压强的原因_______。该反应在一个容器中开始反应,并在t 时刻达到平衡,在t 时刻
1 2
加压,t 时刻重新平衡。在图中画出v-t 图像的变化_______。
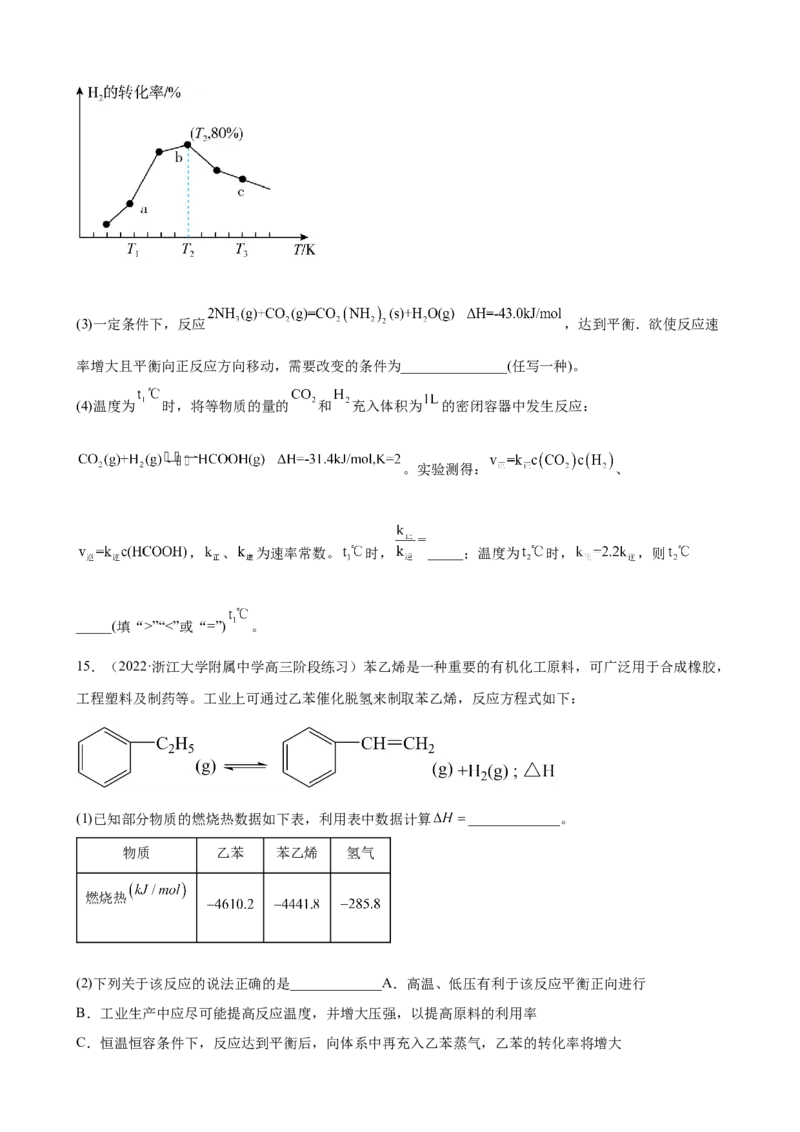
3(2)工业生产的过程中常常会用到热交换器,简述热交换器的作用_______,下图是热交换器的示意图,说
明A处气体的成分_______
(3)工业制备氨气在氨合成塔中进行,在进入合成塔之前,需要对原料气净化,该操作的目的是_______,
写出合成阶段涉及反应的化学方程式_______欲提高氢气的转化率,可采用的措施是_______、_______(写
出两条)
(4)在一个恒容的密闭容器中模拟工业合成氨的反应,下列说法中能确定该反应已经达到化学平衡的是
_______。
A.容器内气体的压强不变
B.容器内气体的密度不变
C.容器气体的平均相对分子质量不变
D.断裂6molN-H键,同时生成3mol H-H键
E.2V (NH ) =V (N )
正 3 逆 2
F.该反应的平衡常数保持不变
(5)写出合成氨反应的平衡常数表达式_______。已知500°C时该反应的平衡常数K=7.42× 10-5,下表为某
一时刻容器内, 氮气、氢气和氨气的浓度,此时v _______ v (填 “>”、“<”或“=”)
正 逆单位:mol·L-1
N H NH
2 2 3
30 10 5
14.(2022·山西·临县第一中学高三阶段练习)国家主席习近平提出了中国应对气候变化的两个目标:二
氧化碳排放力争于2030年前达到峰值,于2060年前实现碳中和。因此,科学家研发 利用技术、降低
空气中 含量成为了热点。回答下列问题:
(1) 还原 制 的部分反应如下:
①
②
反应 ______
(2)在一定条件下,向 恒容密闭容器中充入 和 发生反应
,测得在相同时间内,不同温度下 的转化率如图所示。a、b、
c点 的大小顺序为_______________; 时,若达到平衡时所用时间为 ,则 内
的平均反应速率为___________ (保留三位有效数字),若平衡时压强为 ,
_______ (保留三位有效数字, 为以分压表示的平衡常数,分压=总压×物质的量分数)。(3)一定条件下,反应 ,达到平衡.欲使反应速
率增大且平衡向正反应方向移动,需要改变的条件为_______________(任写一种)。
(4)温度为 时,将等物质的量的 和 充入体积为 的密闭容器中发生反应:
。实验测得: 、
, 、 为速率常数。 时, _____;温度为 时, ,则
_____(填“>”“<”或“=”) 。
15.(2022·浙江大学附属中学高三阶段练习)苯乙烯是一种重要的有机化工原料,可广泛用于合成橡胶,
工程塑料及制药等。工业上可通过乙苯催化脱氢来制取苯乙烯,反应方程式如下:
(1)已知部分物质的燃烧热数据如下表,利用表中数据计算 _____________。
物质 乙苯 苯乙烯 氢气
燃烧热
(2)下列关于该反应的说法正确的是_____________A.高温、低压有利于该反应平衡正向进行
B.工业生产中应尽可能提高反应温度,并增大压强,以提高原料的利用率
C.恒温恒容条件下,反应达到平衡后,向体系中再充入乙苯蒸气,乙苯的转化率将增大D.选择合适的催化剂可以缩短达到平衡的时间,但不会提高生成物中苯乙烯的含量
(3)工业上通入过热水蒸气( ),在常压的条件下发生乙苯的催化脱氢反应。
①反应中通入水蒸气的作用是____________________。
②将乙苯和水蒸气通入反应器,期末乙苯的物质的量分数为 ,在温度t、压强p下进行反应。平衡时,
乙苯的转化率为 ,该反应的平衡常数 _________(分压=总压×物质的量分数)
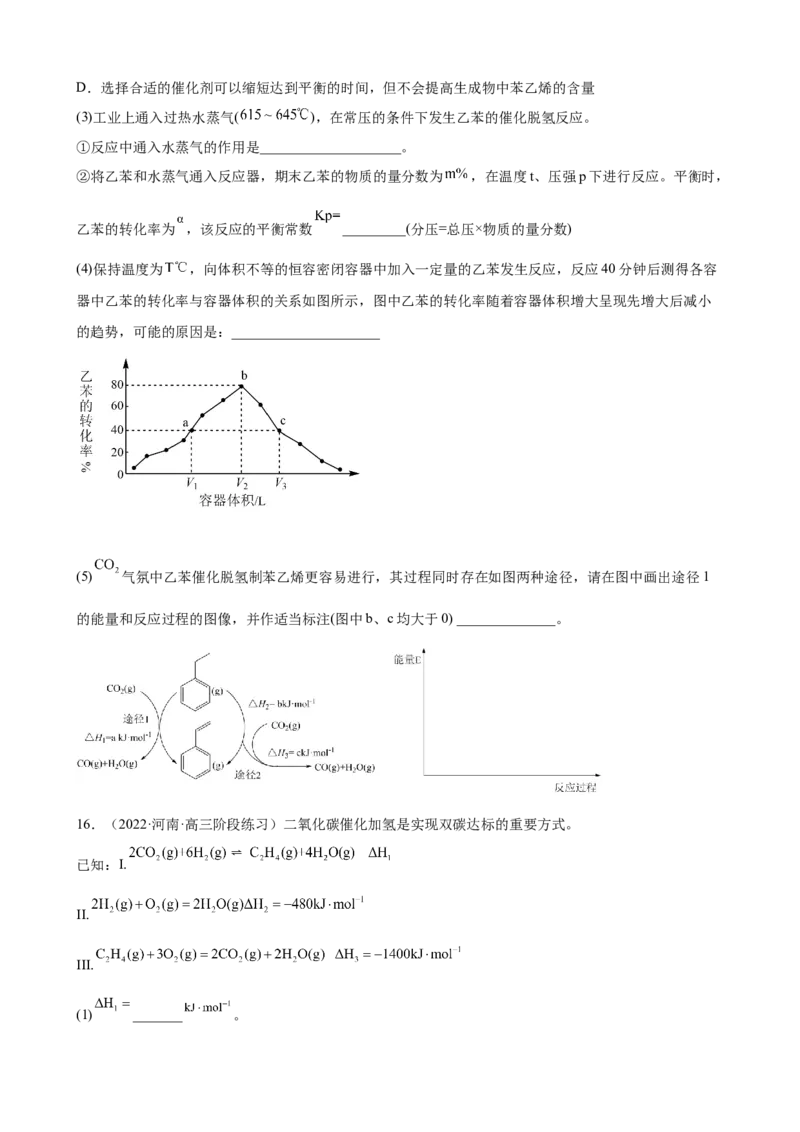
(4)保持温度为 ,向体积不等的恒容密闭容器中加入一定量的乙苯发生反应,反应40分钟后测得各容
器中乙苯的转化率与容器体积的关系如图所示,图中乙苯的转化率随着容器体积增大呈现先增大后减小
的趋势,可能的原因是:_____________________
(5) 气氛中乙苯催化脱氢制苯乙烯更容易进行,其过程同时存在如图两种途径,请在图中画出途径1
的能量和反应过程的图像,并作适当标注(图中b、c均大于0) ______________。
16.(2022·河南·高三阶段练习)二氧化碳催化加氢是实现双碳达标的重要方式。
已知:I.
II.
III.
(1) _______ 。(2) 时,向一体积为2L的恒容密闭容器中通入2molCO (g)和6molH (g),只发生反应I,测得容器内总
2 2
压强变化如图。
① 内, 的平均速率为_______。
②达到平衡时, 的转化率为_______。
③下列措施能提高 平衡转化率的是_______(填标号)。
A.使用合适的催化剂 B.充入氢气 C.升高温度 D.分离产物
(3)已知反应I的正反应速率 ( 为正、逆反应速率
常数,只与温度、催化剂有关,与浓度无关)。
① 时, ,则该温度下压强平衡常数 _______。 ,平衡时 ,则 _______(填
“>”、“<”或“=”) 。
②下列说法正确的是_______(填标号)。
A.升高温度, 增大的倍数大于 增大的倍数
B.加入高效催化剂, 增大的倍数等于 增大的倍数
C.增大压强, 增大的倍数大于 增大的倍数
D.增大 浓度, 增大的倍数大于 增大的倍数
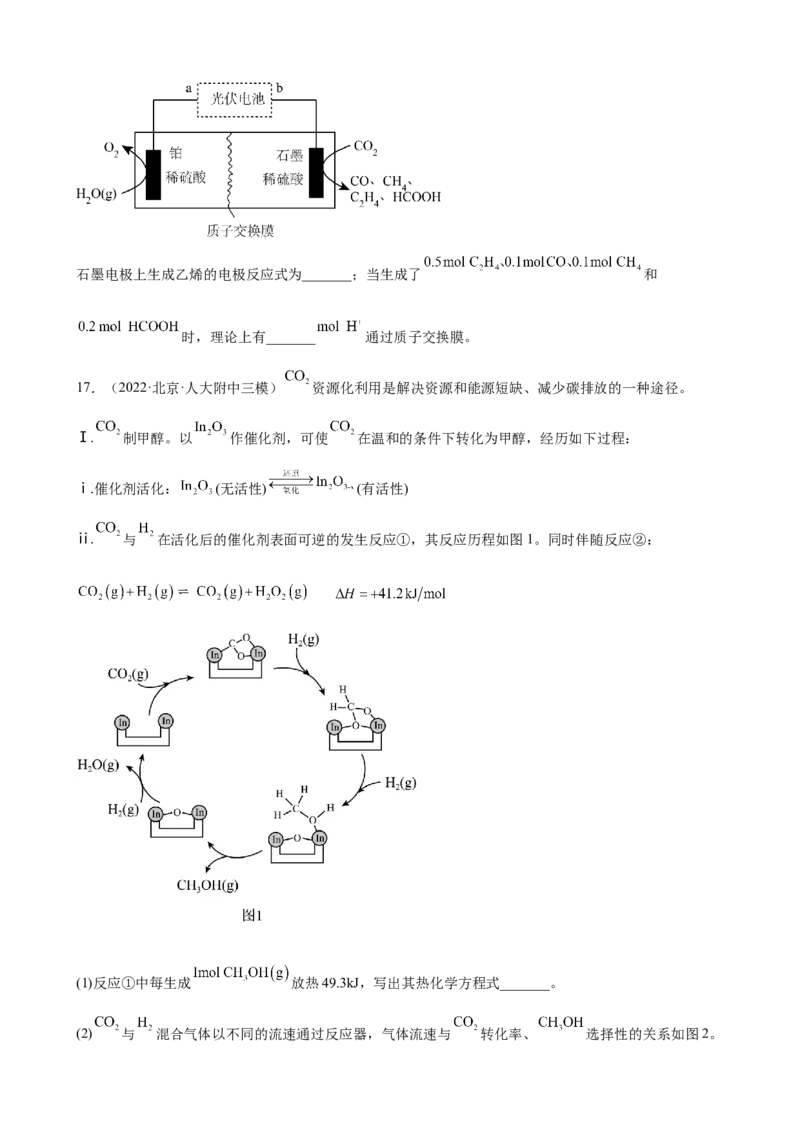
(4)工业上采用电催化法实现 还原制乙烯,除乙烯外还有副产物,装置如图所示。石墨电极上生成乙烯的电极反应式为_______;当生成了 和
时,理论上有_______ 通过质子交换膜。
17.(2022·北京·人大附中三模) 资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
Ⅰ. 制甲醇。以 作催化剂,可使 在温和的条件下转化为甲醇,经历如下过程:
ⅰ.催化剂活化: (无活性) (有活性)
ⅱ. 与 在活化后的催化剂表面可逆的发生反应①,其反应历程如图1。同时伴随反应②:
(1)反应①中每生成 放热49.3kJ,写出其热化学方程式_______。
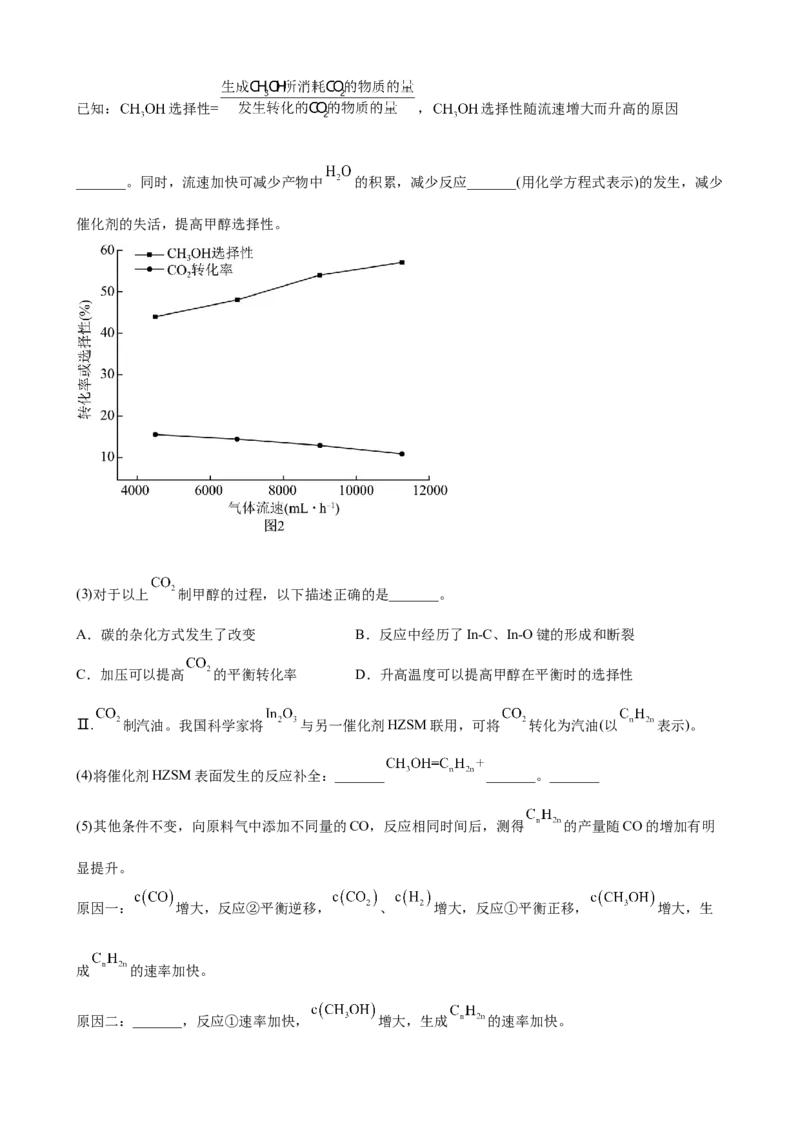
(2) 与 混合气体以不同的流速通过反应器,气体流速与 转化率、 选择性的关系如图2。已知: 选择性= , 选择性随流速增大而升高的原因
_______。同时,流速加快可减少产物中 的积累,减少反应_______(用化学方程式表示)的发生,减少
催化剂的失活,提高甲醇选择性。
(3)对于以上 制甲醇的过程,以下描述正确的是_______。
A.碳的杂化方式发生了改变 B.反应中经历了In-C、In-O键的形成和断裂
C.加压可以提高 的平衡转化率 D.升高温度可以提高甲醇在平衡时的选择性
Ⅱ. 制汽油。我国科学家将 与另一催化剂HZSM联用,可将 转化为汽油(以 表示)。
(4)将催化剂HZSM表面发生的反应补全:_______ _______。_______
(5)其他条件不变,向原料气中添加不同量的CO,反应相同时间后,测得 的产量随CO的增加有明
显提升。
原因一: 增大,反应②平衡逆移, 、 增大,反应①平衡正移, 增大,生
成 的速率加快。
原因二:_______,反应①速率加快, 增大,生成 的速率加快。补全原因二_______
18.(2022·浙江·温州中学模拟预测)乙烯、丙烯是化学工业的最基本原料,工业上可采用多种方法生产,
请回答下列问题:
方法一:利用丙烷脱氢制烯烃,反应如下。
Ⅰ
Ⅱ
Ⅲ
Ⅳ
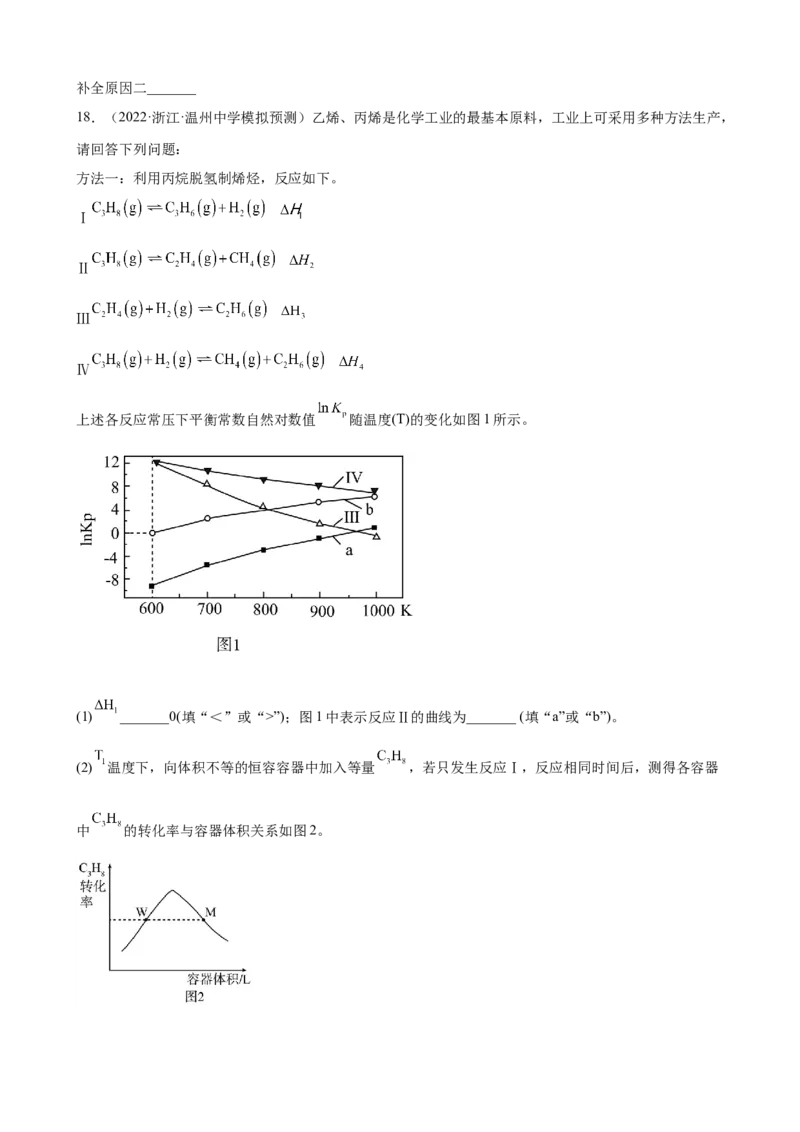
上述各反应常压下平衡常数自然对数值 随温度(T)的变化如图1所示。
(1) _______0(填“<”或“>”);图1中表示反应Ⅱ的曲线为_______ (填“a”或“b”)。
(2) 温度下,向体积不等的恒容容器中加入等量 ,若只发生反应Ⅰ,反应相同时间后,测得各容器
中 的转化率与容器体积关系如图2。①下列说法正确的是_______。
A.各容器内反应的平衡常数相同
B.体系处于W点时,加催化剂,可提高 转化率
C.体系处于W、M两点时,若升高温度,净反应速率均增加
D.反应过程中若容器内气体密度不再变化,则反应已达平衡
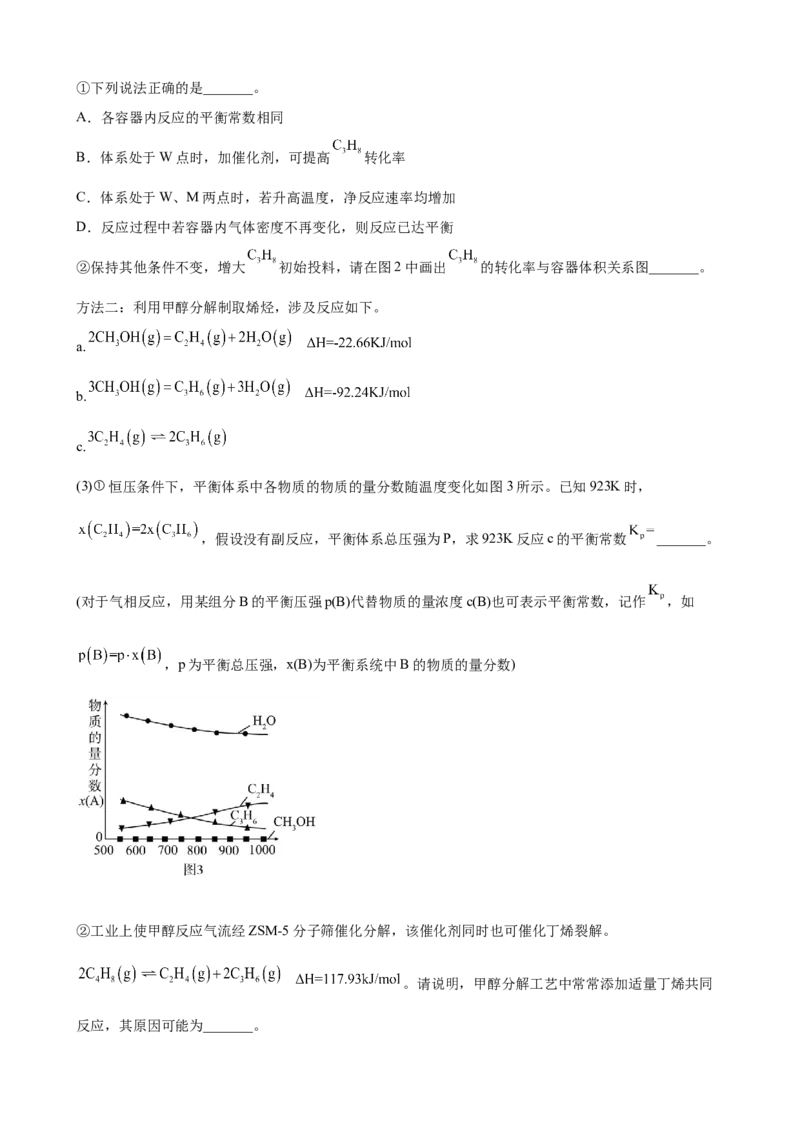
②保持其他条件不变,增大 初始投料,请在图2中画出 的转化率与容器体积关系图_______。
方法二:利用甲醇分解制取烯烃,涉及反应如下。
a.
b.
c.
(3)①恒压条件下,平衡体系中各物质的物质的量分数随温度变化如图3所示。已知923K时,
,假设没有副反应,平衡体系总压强为P,求923K反应c的平衡常数 _______。
(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作 ,如
,p为平衡总压强,x(B)为平衡系统中B的物质的量分数)
②工业上使甲醇反应气流经ZSM-5分子筛催化分解,该催化剂同时也可催化丁烯裂解。
。请说明,甲醇分解工艺中常常添加适量丁烯共同
反应,其原因可能为_______。19.(2022·上海市川沙中学高三阶段练习)废气中的 通过高温热分解可制取氢气:
。现在3L密闭容器中,控制不同温度进行 分解实验。
(1)硫化氢分子的空间构型为_______。
(2)某温度时,测得反应体系中有气体1.31mol,反应t min后,测得气体为1.37mol,则t min内 的生成
速率为_______。
(3)某温度时, 的转化率达到最大值的依据是_______(选填编号)。
a.气体的压强不发生变化 b.气体的密度不发生变化
c. 不发生变化 d.单位时间里分解的 和生成的 一样多
(4)实验结果如图,图中曲线a表示 的平衡转化率与温度关系,曲线b表示不同温度下、反应经过相同
时间且末达到化学平衡时 的转化率,该反应为_______反应(填“放热”或“吸热”);曲线b随温度
的升高,向曲线a逼近的原因是_______;在容器不变的情况下,如果要提高 的体积分数,可采取的一
种措施是_______。
(5)使1L 与20L空气(空气中 体积分数为0.2)完全反应后恢复到室温,混合气体的体积是
_______L。若2g 完全燃烧后生成二氧化硫和水蒸气,同时放出29.4kJ的热量,该反应的热化学方程
式是_______。20.(2022·江苏省响水中学高三阶段练习)合理利用资源,加强环境保护,降低碳排放,实施低碳经济
是今后经济生活的主流。回答下列问题:
(1)下列措施不利于有效减少二氧化碳的是_______(填字母)。
A.植树造林,保护森林,保护植被
B.加大对煤和石油的开采,并鼓励使用液化石油气
C.大力发展风能、水力、潮汐能发电和核电,大力推行太阳能的综合开发
D.推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
(2)科学家致力于二氧化碳的“组合转化”技术研究,如将CO 和H 以1∶4的物质的量之比混合通入反应
2 2
器,在适当条件下反应可获得一种重要能源。请完成以下化学方程式:
CO+4H _______+2H O
2 2 2
(3)用CO 合成燃料甲醇(CHOH)是碳减排的新方向。现进行如下实验:某温度下发生反应:CO(g)
2 3 2
+3H
2
(g)⇌CH
3
OH(g)+H
2
O(g),在体积为1 L的密闭容器中,充入2 mol CO
2
和6 mol H
2
。
① 能判断该反应已达化学平衡的标志是_______(填字母)。
a.CO 百分含量保持不变
2
b.容器中混合气体的质量保持不变
c.容器中H 浓度与CO 浓度之比为3∶1
2 2
d.CO 的生成速率与CHOH的生成速率相等
2 3
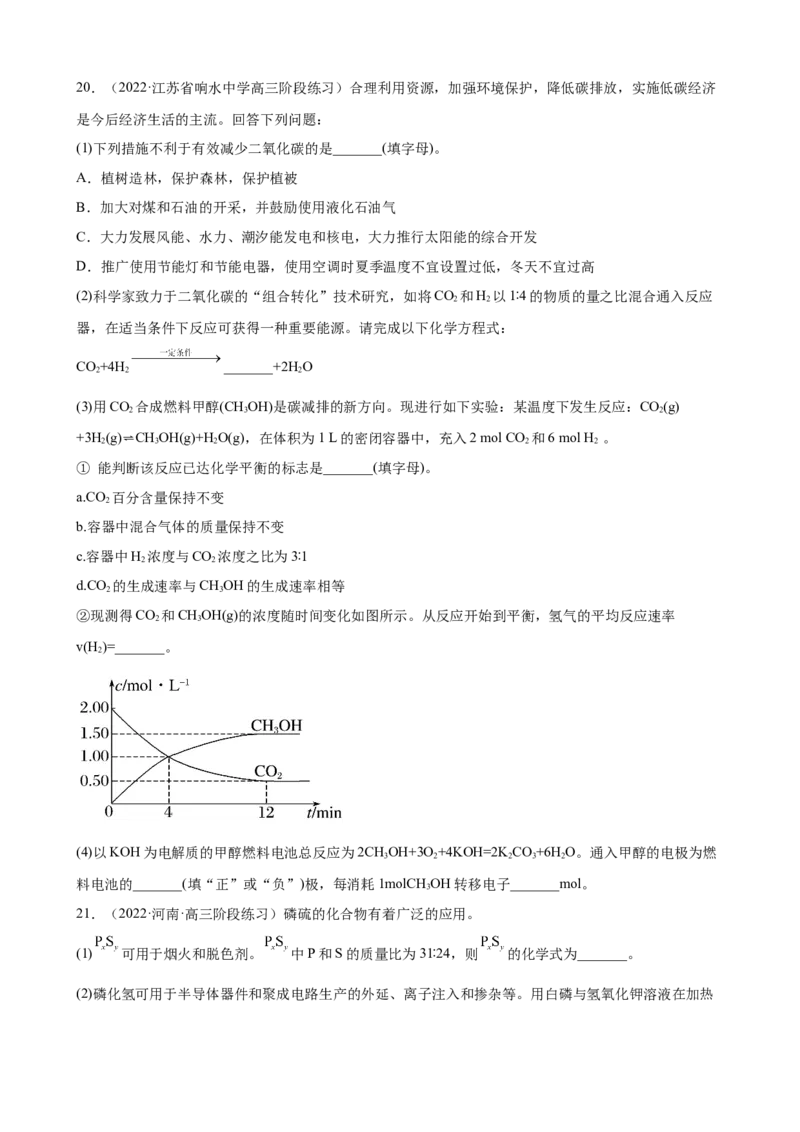
②现测得CO 和CHOH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的平均反应速率
2 3
v(H )=_______。
2
(4)以KOH为电解质的甲醇燃料电池总反应为2CHOH+3O +4KOH=2K CO+6H O。通入甲醇的电极为燃
3 2 2 3 2
料电池的_______(填“正”或“负”)极,每消耗1molCH OH转移电子_______mol。
3
21.(2022·河南·高三阶段练习)磷硫的化合物有着广泛的应用。
(1) 可用于烟火和脱色剂。 中P和S的质量比为31∶24,则 的化学式为_______。
(2)磷化氢可用于半导体器件和聚成电路生产的外延、离子注入和掺杂等。用白磷与氢氧化钾溶液在加热条件下反应制得磷化氢气体,同时产生次磷酸钾( )。
① 中磷的化合价为_______。
②写出上述反应的化学方程式:_______。
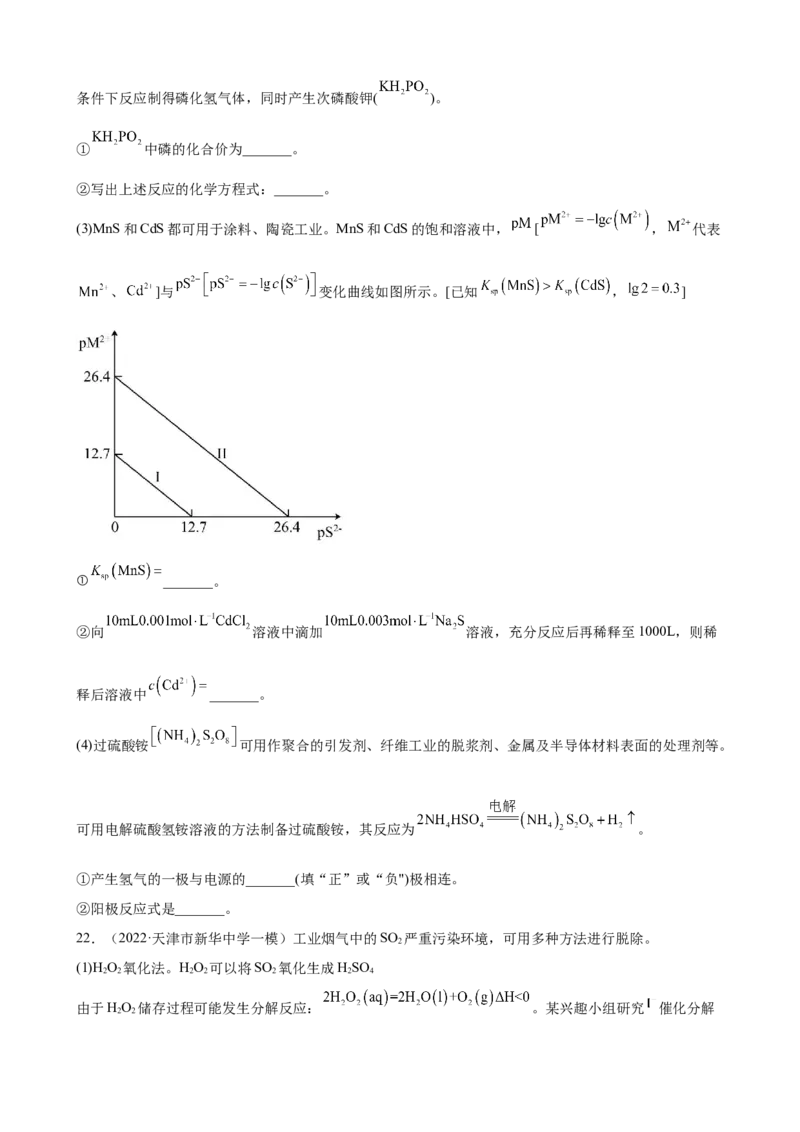
(3)MnS和CdS都可用于涂料、陶瓷工业。MnS和CdS的饱和溶液中, [ , 代表
、 ]与 变化曲线如图所示。[已知 , ]
① _______。
②向 溶液中滴加 溶液,充分反应后再稀释至1000L,则稀
释后溶液中 _______。
(4)过硫酸铵 可用作聚合的引发剂、纤维工业的脱浆剂、金属及半导体材料表面的处理剂等。
可用电解硫酸氢铵溶液的方法制备过硫酸铵,其反应为 。
①产生氢气的一极与电源的_______(填“正”或“负")极相连。
②阳极反应式是_______。
22.(2022·天津市新华中学一模)工业烟气中的SO 严重污染环境,可用多种方法进行脱除。
2
(1)H O 氧化法。HO 可以将SO 氧化生成HSO
2 2 2 2 2 2 4
由于HO 储存过程可能发生分解反应: 。某兴趣小组研究 催化分解
2 2HO 历程如下,请补全第二步反应的热化学方程式。
2 2
第一步: 慢反应
第二步:_______ _______ 快反应
请根据I-催化HO 的分解反应历程补充剩余的能量示意图_______。
2 2
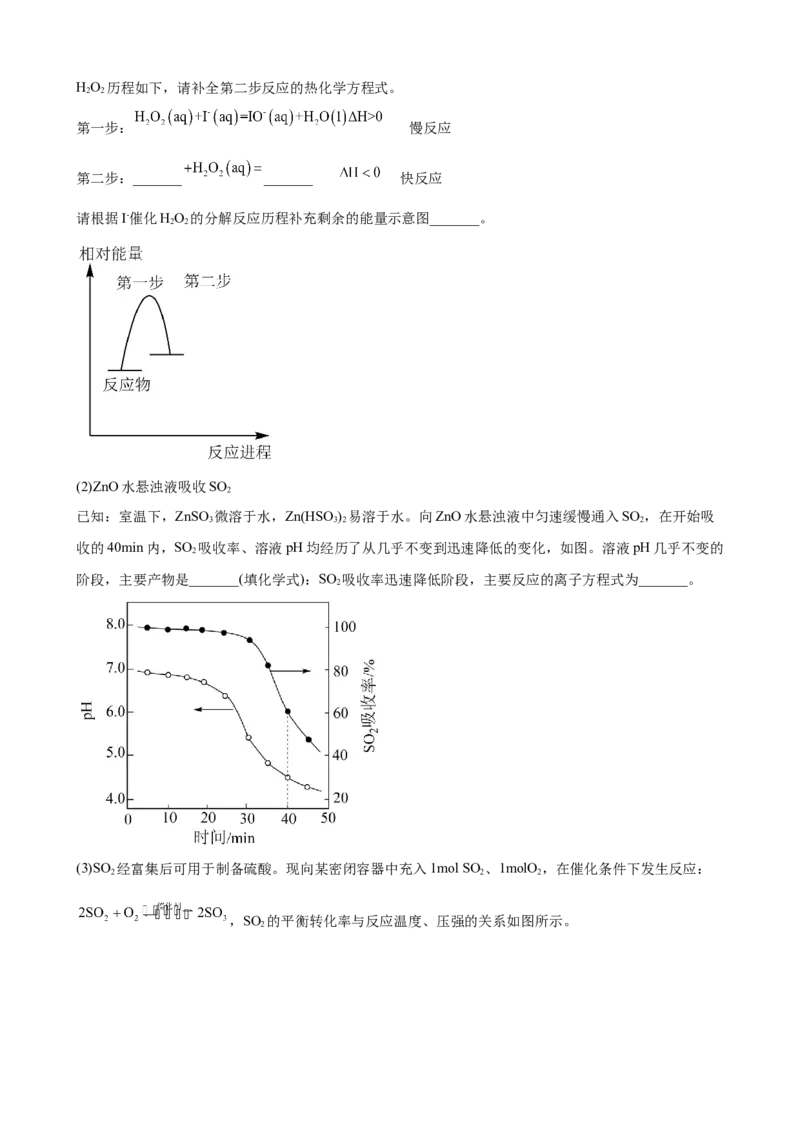
(2)ZnO水悬浊液吸收SO
2
已知:室温下,ZnSO 微溶于水,Zn(HSO ) 易溶于水。向ZnO水悬浊液中匀速缓慢通入SO ,在开始吸
3 3 2 2
收的40min内,SO 吸收率、溶液pH均经历了从几乎不变到迅速降低的变化,如图。溶液pH几乎不变的
2
阶段,主要产物是_______(填化学式):SO 吸收率迅速降低阶段,主要反应的离子方程式为_______。
2
(3)SO 经富集后可用于制备硫酸。现向某密闭容器中充入1mol SO 、1molO ,在催化条件下发生反应:
2 2 2
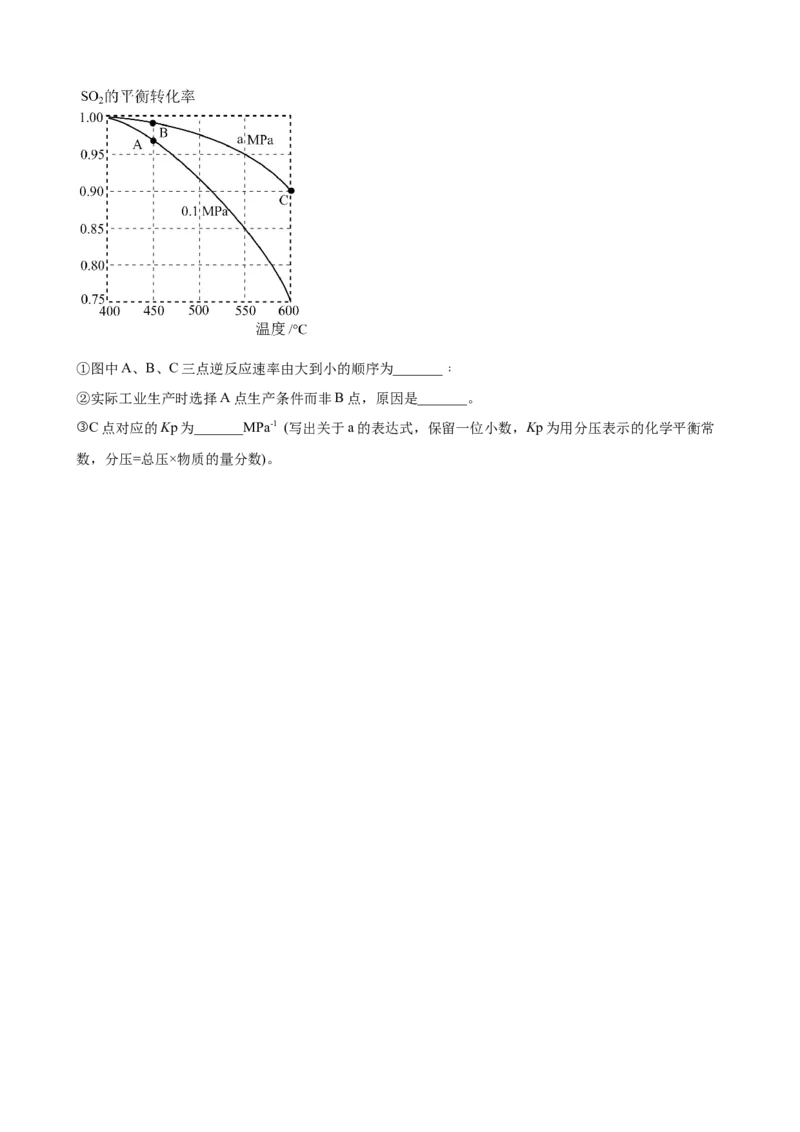
,SO 的平衡转化率与反应温度、压强的关系如图所示。
2①图中A、B、C三点逆反应速率由大到小的顺序为_______﹔
②实际工业生产时选择A点生产条件而非B点,原因是_______。
③C点对应的Kp为_______MPa-1 (写出关于a的表达式,保留一位小数,Kp为用分压表示的化学平衡常
数,分压=总压×物质的量分数)。参考答案:
1.(1)H
2
(2) 2Ga+2NaOH+2H O=2NaGaO +3H ↑ >
2 2 2
(3) 33% bc
(4) 外加直流电的阴极保护法
2.(1) 60% 0.04 mol 不变
(2) 放出 688
(3) B
3.(1) H-O-H 离子
(2)Cl
(3) 2Fe -4e-= 2Fe2+ (Fe-2e-= Fe2+也可以) HO+O +4e-= 4OH-
2 2
(4) 吸水并保持水分 保温 变慢
4.(1) H HO分解生成H 和O
2 2 2 2
(2) 活化能低 I、II
(3)
(4)
5.(1)﹣41.2
(2) < < 0.04 0.247 AB
(3)C H+6 -12e-=8CO +2H O
2 4 2 2
6.(1)
(2)
(3)
(4)3
(5)负
(6)O +4e-+2H O=4OH-
2 2(7) 减小 4
7.(1)CD
(2) 50%
(3) 80
8.(1)-89.3
(2)9
(3)BD
(4) 40% 3.56×10-2 D
(5) 0.45 <
9.(1)C HOH(g) C H(g)+HO(g) ΔH=+46kJ/mol
2 5 2 4 2
(2) < BD
(3)升高温度、增大压强
(4) 250-300℃ 温度过低,乙醇转化率较低,乙烯选择性较低;温度过高,乙醇转化率
变化不大,烯选择性变化不大,浪费能源 K=
10.(1) 用湿润的红色石蕊试纸检验,试纸变蓝证明有氨气
(2) 放热 催化剂活性最好,可以通过合成氨的反应速率
(3) 200℃ M=Q>N
(4)
(5)4NH (g)+5O(g) 4NO(g)+6H O(g) H=-907 kJ·mol-1;
3 2 2
△
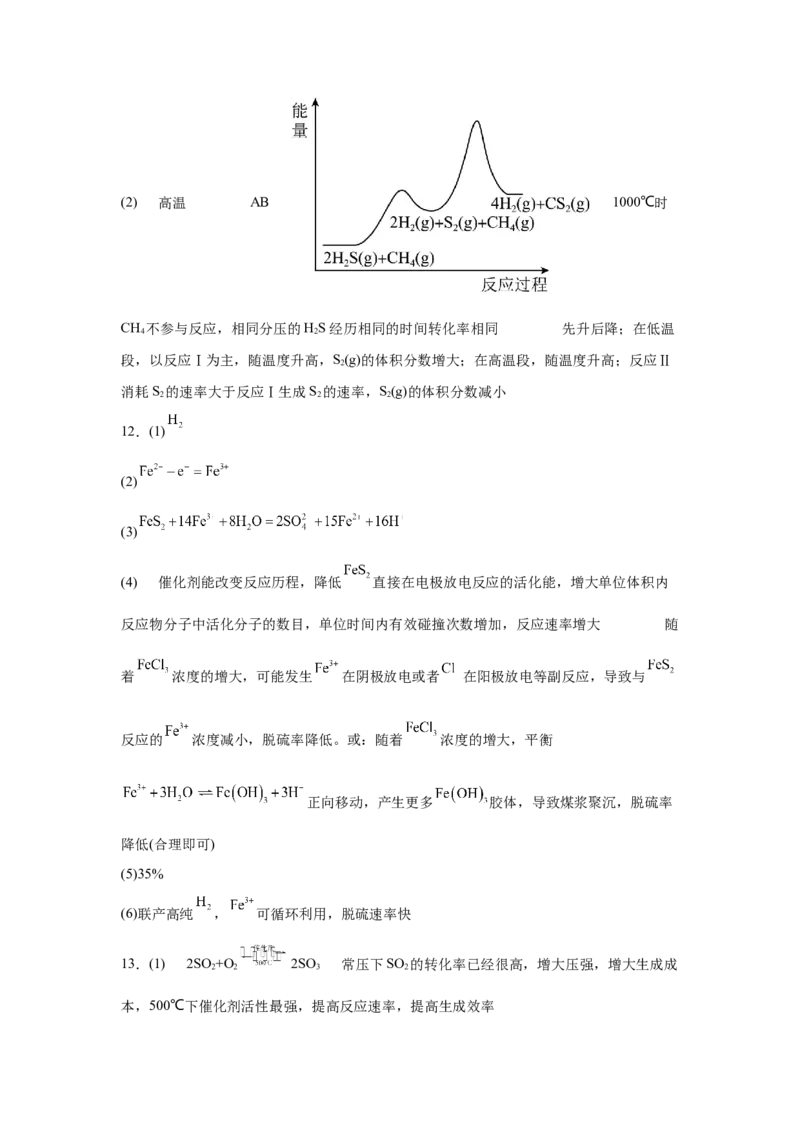
11.(1)8×108 L·mol-1(2) 高温 AB 1000℃时
CH 不参与反应,相同分压的HS经历相同的时间转化率相同 先升后降;在低温
4 2
段,以反应Ⅰ为主,随温度升高,S(g)的体积分数增大;在高温段,随温度升高;反应Ⅱ
2
消耗S 的速率大于反应Ⅰ生成S 的速率,S(g)的体积分数减小
2 2 2
12.(1)
(2)
(3)
(4) 催化剂能改变反应历程,降低 直接在电极放电反应的活化能,增大单位体积内
反应物分子中活化分子的数目,单位时间内有效碰撞次数增加,反应速率增大 随
着 浓度的增大,可能发生 在阴极放电或者 在阳极放电等副反应,导致与
反应的 浓度减小,脱硫率降低。或:随着 浓度的增大,平衡
正向移动,产生更多 胶体,导致煤浆聚沉,脱硫率
降低(合理即可)
(5)35%
(6)联产高纯 , 可循环利用,脱硫速率快
13.(1) 2SO +O 2SO 常压下SO 的转化率已经很高,增大压强,增大生成成
2 2 3 2
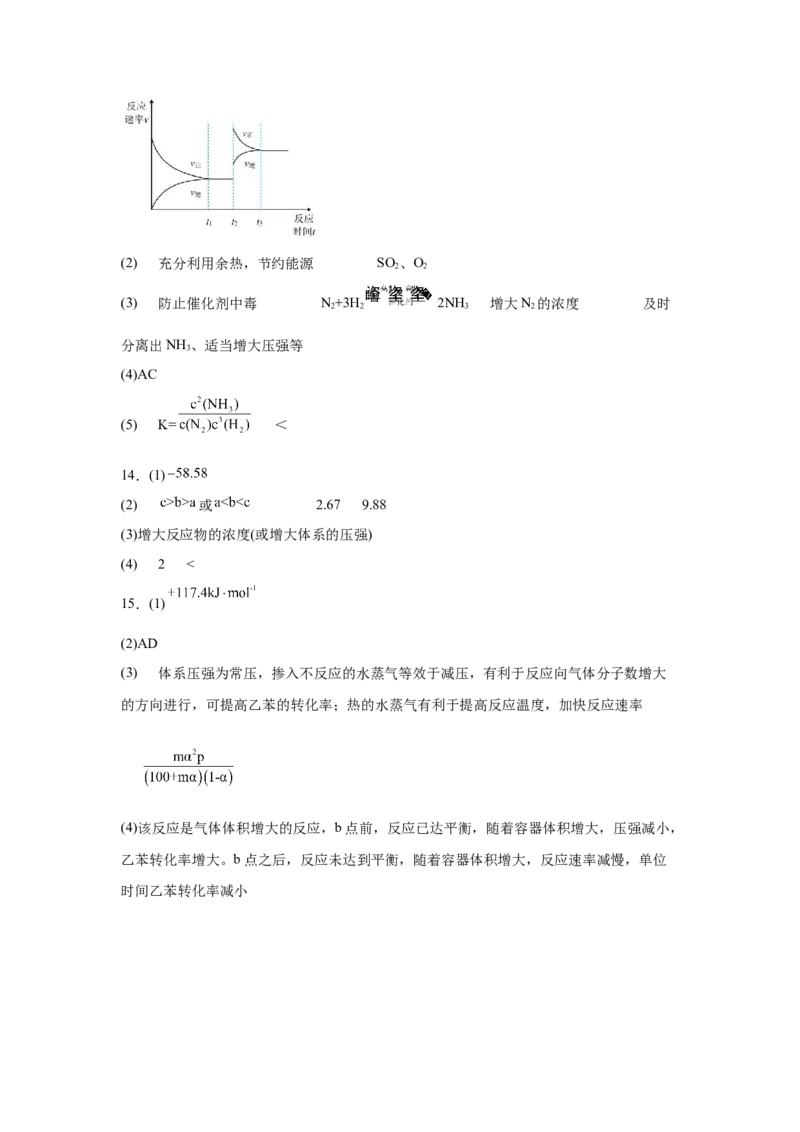
本,500℃下催化剂活性最强,提高反应速率,提高生成效率(2) 充分利用余热,节约能源 SO 、O
2 2
(3) 防止催化剂中毒 N+3H 2NH 增大N 的浓度 及时
2 2 3 2
分离出NH 、适当增大压强等
3
(4)AC
(5) K= <
14.(1)
(2) 或 2.67 9.88
(3)增大反应物的浓度(或增大体系的压强)
(4) 2 <
15.(1)
(2)AD
(3) 体系压强为常压,掺入不反应的水蒸气等效于减压,有利于反应向气体分子数增大
的方向进行,可提高乙苯的转化率;热的水蒸气有利于提高反应温度,加快反应速率
(4)该反应是气体体积增大的反应,b点前,反应已达平衡,随着容器体积增大,压强减小,
乙苯转化率增大。b点之后,反应未达到平衡,随着容器体积增大,反应速率减慢,单位
时间乙苯转化率减小(5)
16.(1)-40
(2) 80% D
(3) 2 > B
(4) 7.4
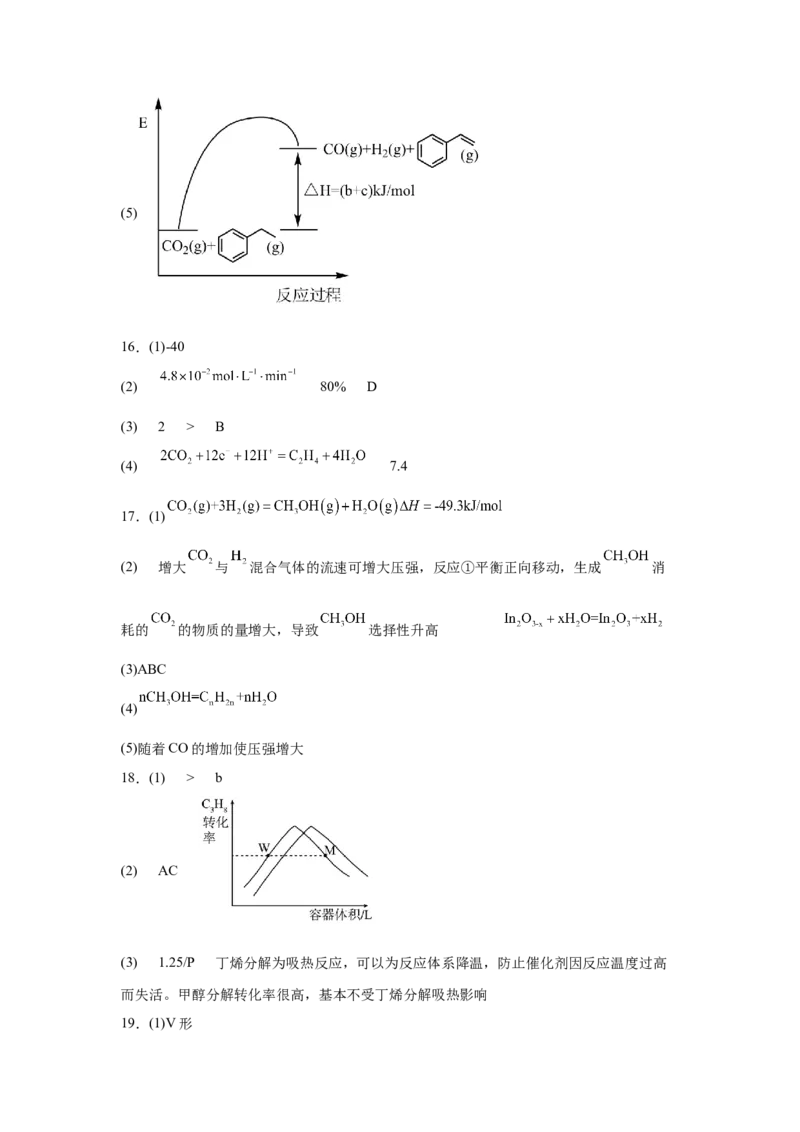
17.(1)
(2) 增大 与 混合气体的流速可增大压强,反应①平衡正向移动,生成 消
耗的 的物质的量增大,导致 选择性升高
(3)ABC
(4)
(5)随着CO的增加使压强增大
18.(1) > b
(2) AC
(3) 1.25/P 丁烯分解为吸热反应,可以为反应体系降温,防止催化剂因反应温度过高
而失活。甲醇分解转化率很高,基本不受丁烯分解吸热影响
19.(1)V形(2) mol/(L·min)
(3)ac
(4) 吸热 随着温度升高,反应速率加快,达到平衡所需要的时间变短
升高温度或及时分离S 气体
2
(5) 19.5 2HS(g)+3O(g)=2SO(g)+2HO(g) △H=—999.6kJ/mol
2 2 2 2
20.(1)B
(2)CH
4
(3) ad 0.375mol∙L-1∙min-1
(4) 负 6
21.(1)
(2) +1 P+3KOH+3H O PH ↑+3
4 2 3
(3) 10-12.7 mol/L
(4) 负 2 -2e-═
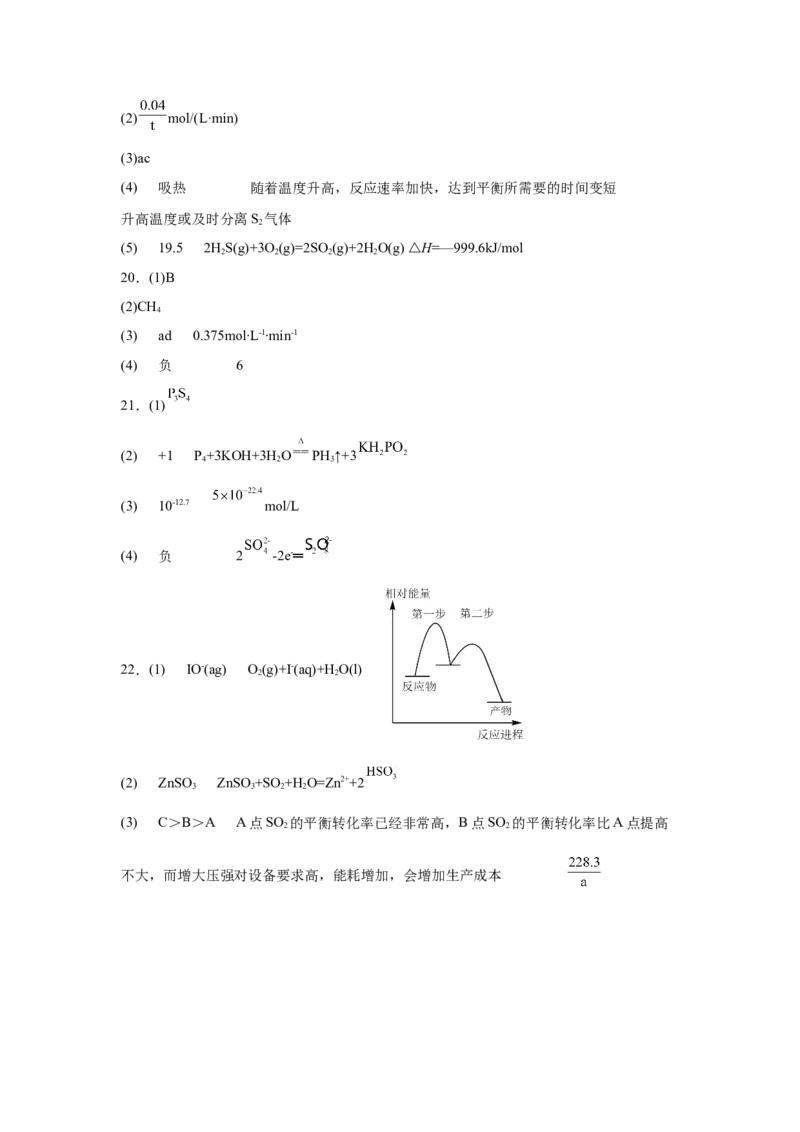
22.(1) IO-(ag) O(g)+I-(aq)+H O(l)
2 2
(2) ZnSO ZnSO+SO+H O=Zn2++2
3 3 2 2
(3) C>B>A A点SO 的平衡转化率已经非常高,B点SO 的平衡转化率比A点提高
2 2
不大,而增大压强对设备要求高,能耗增加,会增加生产成本