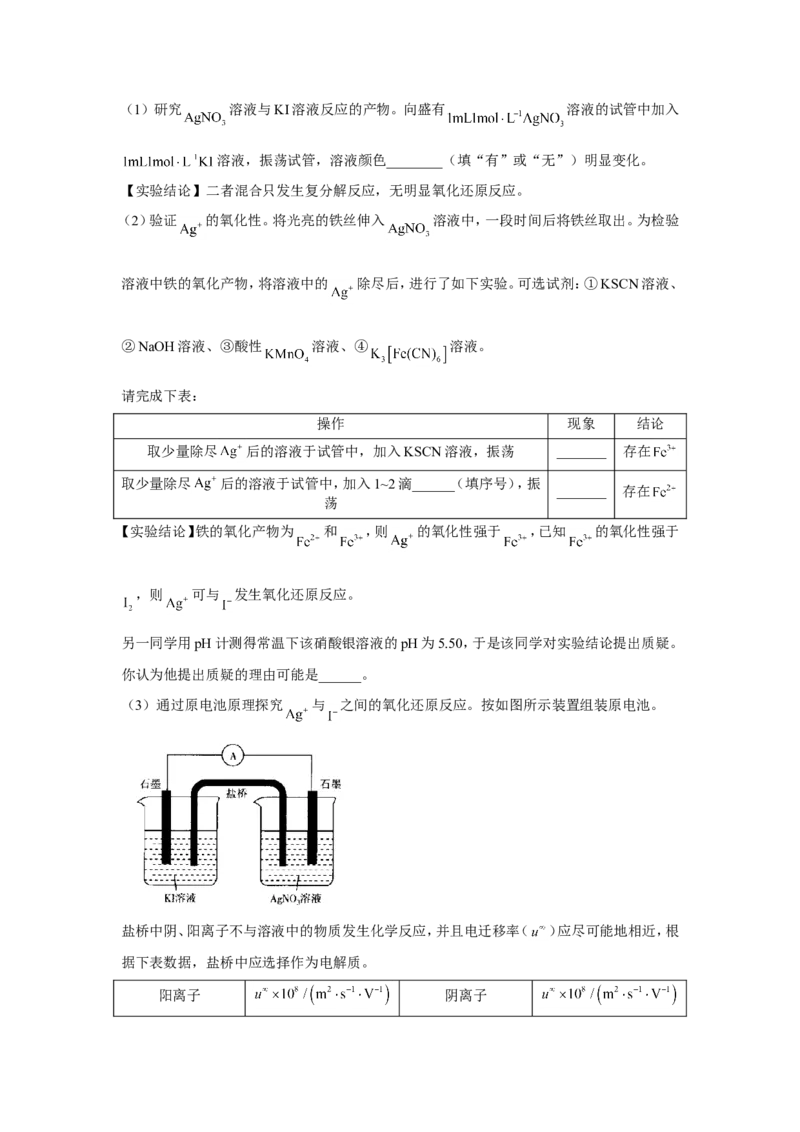文档内容
化学实验设计与探究 训练题
一、选择题
1.下列实验设计正确的是( )
A.将 通入溴水中证明 具有漂白性
B.将铁屑放入稀 中证明Fe比 活泼
C.将澄清石灰水滴入某溶液证明其中存在
D.将乙烯通入 酸性溶液证明乙烯具有还原性
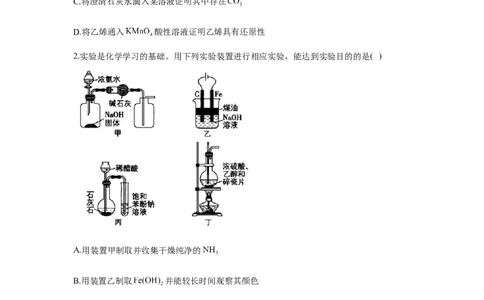
2.实验是化学学习的基础。用下列实验装置进行相应实验,能达到实验目的的是( )
A.用装置甲制取并收集干燥纯净的
B.用装置乙制取 并能较长时间观察其颜色
C.用装置丙完成醋酸、碳酸和苯酚的酸性强弱验证实验
D.用装置丁实验室制取少量乙烯
3.根据下列实验操作和现象所得到的结论正确的是( )
选项 实验操作和现象 结论
向淀粉溶液中加适量20% 溶液,加热,冷却后加NaOH
A 淀粉未水解
溶液至中性,再滴加少量碘水,溶液变蓝
室温下,向 溶液中加入少量镁粉,产生大量气 镁与盐酸反应放
B
泡,测得溶液温度上升 热室温下,向浓度均为 的 和 混合溶液中 白色沉淀是
C
加入 溶液,出现白色沉淀
向 溶液中滴加 溶液,溶液
D 具有氧化性
褪色
4.下列实验设计正确的是( )
A.用乙醇萃取碘水中的碘
B.用氢氧化钠溶液除去乙酸乙酯中的乙酸
C.向乙醇和乙酸中分别加入钠,比较其官能团的活泼性
D.向蔗糖和稀硫酸共热后的溶液中加入少量银氨溶液,检验生成的葡萄糖
5. 溶液是实验室中常用试剂。下列与 溶液有关实验的操作和结论都一定正确
的是( )
选项 A B C D
实验
操作
收集
前者产生气泡更快 蒸发 溶液
能用排空法
结论 催化效果好于 可获得胆矾晶体
收集
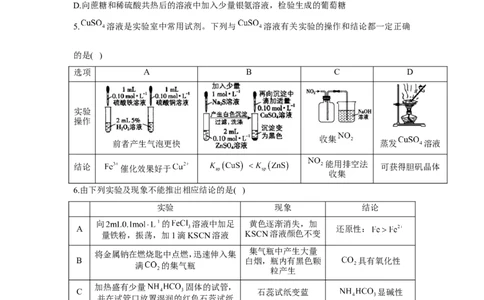
6.由下列实验及现象不能推出相应结论的是( )
实验 现象 结论
向 的 溶液中加足 黄色逐渐消失,加
A 还原性:
量铁粉,振荡,加1滴KSCN溶液 KSCN溶液颜色不变
集气瓶中产生大量
将金属钠在燃烧匙中点燃,迅速伸入集
B 白烟,瓶内有黑色颗 具有氧化性
满 的集气瓶
粒产生
加热盛有少量 固体的试管,
C 石蕊试纸变蓝 显碱性
并在试管口放置湿润的红色石蕊试纸
向2支盛有2mL相同浓度银氨溶液的 一支试管中产生黄
D 试管中分别加入2滴相同浓度的NaCl 色沉淀,另一支中无
和NaI溶液 明显现象
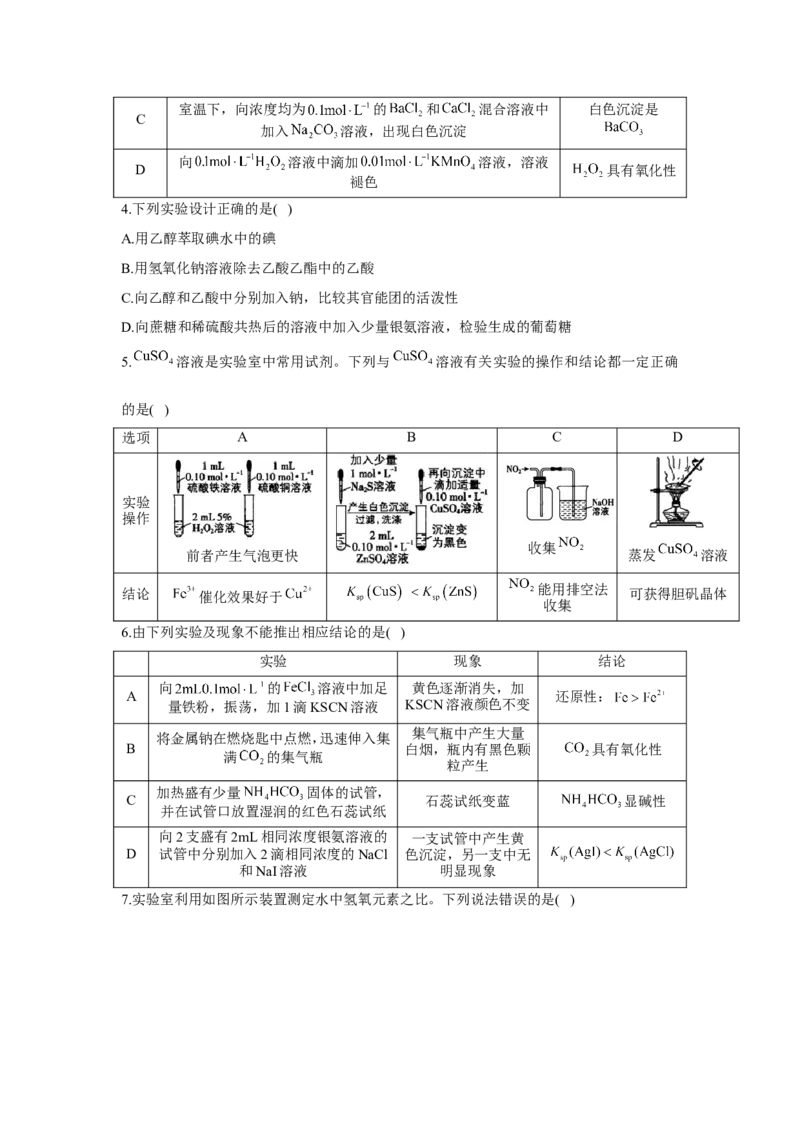
7.实验室利用如图所示装置测定水中氢氧元素之比。下列说法错误的是( )A.①、③、④中依次盛装无水 、碱石灰、碱石灰
B.需测定实验前后装置②和装置③的质量差
C.结束反应时,应先移走酒精灯,待装置②的玻璃管冷至室温,再关闭活塞K
D.实验后装置②的玻璃管中CuO未全部变红,对实验结果无影响
8.下列实验现象与实验操作不相匹配的是( )
实验操作 实验现象
向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯 溶液的紫色逐渐褪去,静置
A
后静置 后溶液分层
集气瓶中产生浓烟并有黑色
B 将镁条点燃后迅速伸入集满 的集气瓶
颗粒产生
有刺激性气味气体产生,溶
C 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸
液变浑浊
向盛有 溶液的试管中加过量铁粉,充分振荡后 黄色逐渐消失,加KSCN后
D
加1 滴KSCN溶液 溶液颜色不变
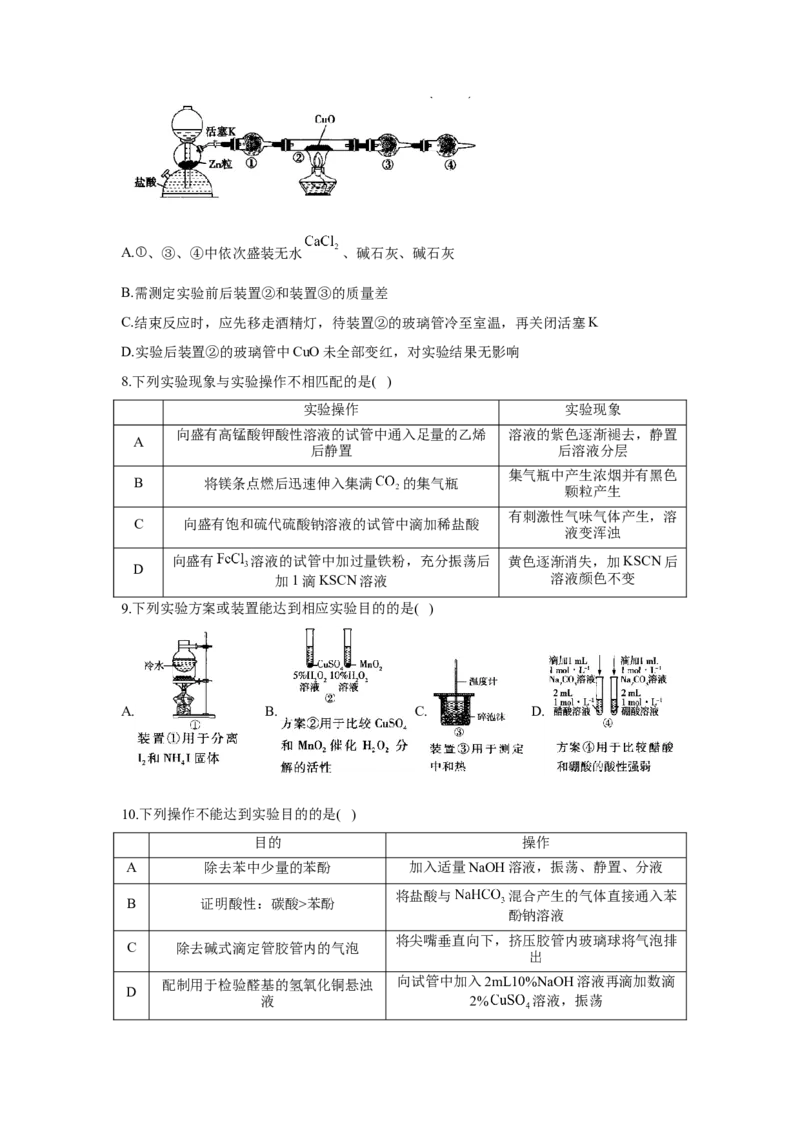
9.下列实验方案或装置能达到相应实验目的的是( )
A. B. C. D.
10.下列操作不能达到实验目的的是( )
目的 操作
A 除去苯中少量的苯酚 加入适量NaOH溶液,振荡、静置、分液
将盐酸与 混合产生的气体直接通入苯
B 证明酸性:碳酸>苯酚
酚钠溶液
将尖嘴垂直向下,挤压胶管内玻璃球将气泡排
C 除去碱式滴定管胶管内的气泡
出
配制用于检验醛基的氢氧化铜悬浊 向试管中加入2mL10%NaOH溶液再滴加数滴
D
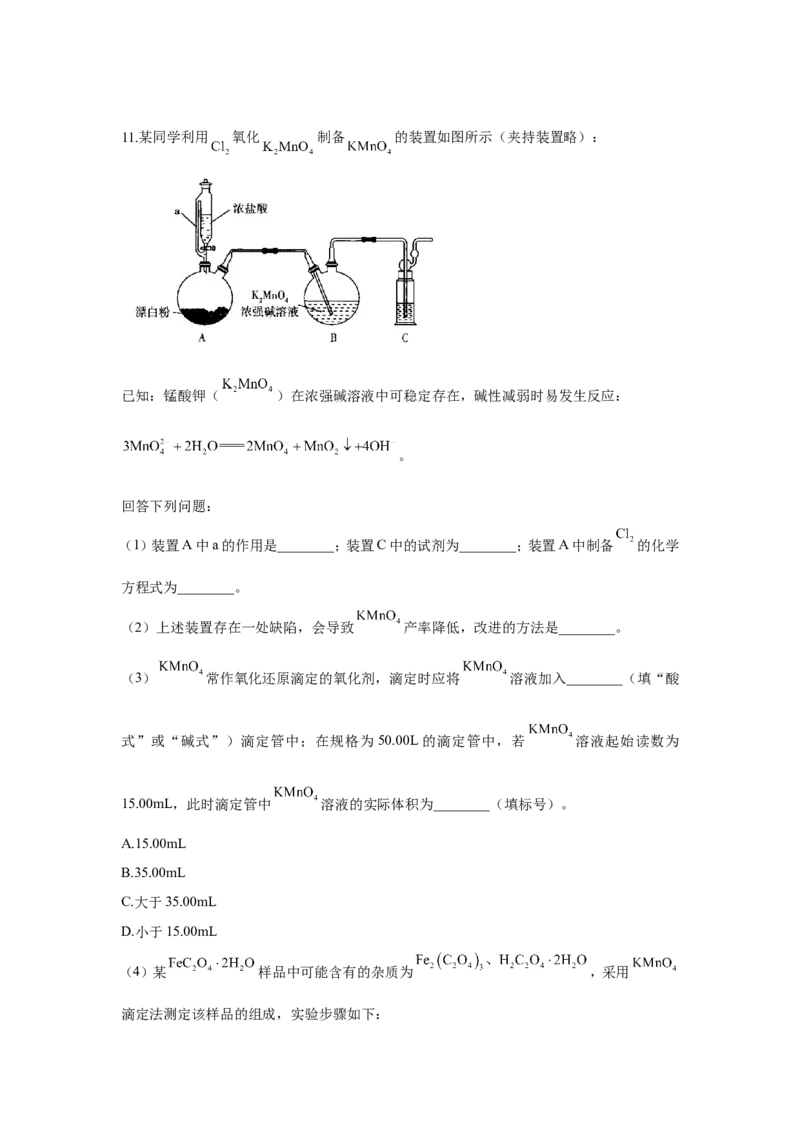
液 2% 溶液,振荡11.某同学利用 氧化 制备 的装置如图所示(夹持装置略):
已知:锰酸钾( )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
。
回答下列问题:
(1)装置A中a的作用是________;装置C中的试剂为________;装置A中制备 的化学
方程式为________。
(2)上述装置存在一处缺陷,会导致 产率降低,改进的方法是________。
(3) 常作氧化还原滴定的氧化剂,滴定时应将 溶液加入________(填“酸
式”或“碱式”)滴定管中;在规格为50.00L的滴定管中,若 溶液起始读数为
15.00mL,此时滴定管中 溶液的实际体积为________(填标号)。
A.15.00mL
B.35.00mL
C.大于35.00mL
D.小于15.00mL
(4)某 样品中可能含有的杂质为 ,采用
滴定法测定该样品的组成,实验步骤如下:Ⅰ.称取 样品于锥形瓶中,加入稀 溶解,水浴加热至75℃。用 的 溶
液趁热滴定至溶液出现粉红色且30s内不褪色,消耗 溶液 。
Ⅱ.向上述溶液中加入适量还原剂将 完全还原为 ,加入稀 酸化后,在75℃继
续用 溶液滴定至溶液出现粉红色且30s内不褪色,又消耗 溶液 。
样品中所含 的质量分数表达式为________。
下列关于样品组成分析的说法,正确的是________(填标号)。
A. 时,样品中一定不含杂质
B. 越大,样品中 含量一定越高
C.若步骤I中滴入 溶液不足,则测得样品中Fe元素含量偏低
D.若所用 溶液实际浓度偏低,则测得样品中Fe元素含量偏高
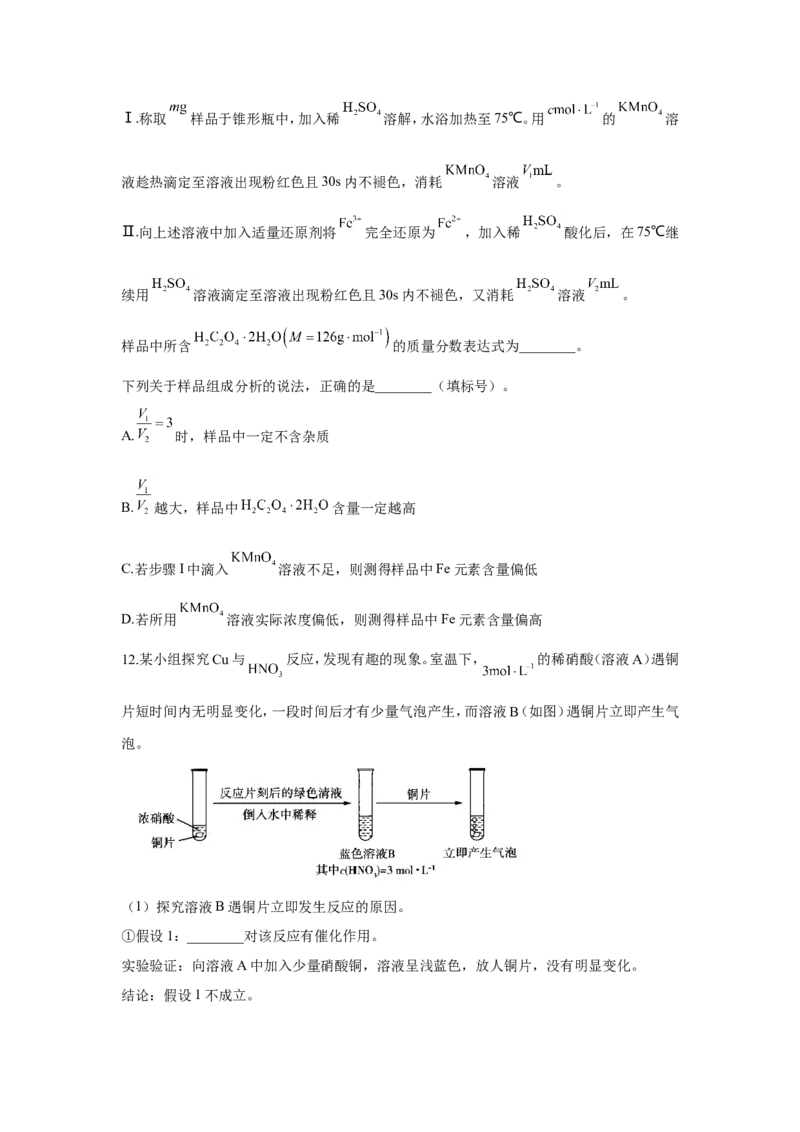
12.某小组探究Cu与 反应,发现有趣的现象。室温下, 的稀硝酸(溶液A)遇铜
片短时间内无明显变化,一段时间后才有少量气泡产生,而溶液B(如图)遇铜片立即产生气
泡。
(1)探究溶液B遇铜片立即发生反应的原因。
①假设1:________对该反应有催化作用。
实验验证:向溶液A中加入少量硝酸铜,溶液呈浅蓝色,放人铜片,没有明显变化。
结论:假设1不成立。②假设2: 对该反应有催化作用。
方案I:向盛有铜片的溶液A中通入少量 ,铜片表面立即产生气泡,反应持续进行。有同
学认为应补充对比实验:向盛有铜片的溶液A中加入几滴 的硝酸,没有明显变化。
补充该实验的目的是________。
方案Ⅱ:向溶液B中通入氮气数分钟得溶液C。
相同条件下,铜片与A、B、C三份溶液的反应速率:B>C>A,该实验能够证明假设2成立的理
由是________。
③查阅资料: 溶于水可以生成 和________。
向盛有铜片的溶液A中加入________,铜片上立即产生气泡,实验证明 对该反应也有
催化作用。
结论: 和 均对Cu与 的反应有催化作用。
(2)Cu与稀硝酸反应中 参与的可能催化过程如下。将ii补充完整。
ⅰ.
ⅱ._____________________________
ⅲ.
(3)探究 的性质。
将一定质量的 放在坩埚中加热,在不同温度阶段进行质量分析,当温度升
至 时,剩余固体质量变为原来的24.33%,则剩余固体的化学式可能为_________。
13.在学习氧化还原反应时,某同学提出 具有较强氧化性, 具有较强还原性,二者也可
发生氧化还原反应。该同学设计下列实验进行验证。(1)研究 溶液与KI溶液反应的产物。向盛有 溶液的试管中加入
溶液,振荡试管,溶液颜色________(填“有”或“无”)明显变化。
【实验结论】二者混合只发生复分解反应,无明显氧化还原反应。
(2)验证 的氧化性。将光亮的铁丝伸入 溶液中,一段时间后将铁丝取出。为检验
溶液中铁的氧化产物,将溶液中的 除尽后,进行了如下实验。可选试剂:①KSCN溶液、
②NaOH溶液、③酸性 溶液、④ 溶液。
请完成下表:
操作 现象 结论
取少量除尽 后的溶液于试管中,加入KSCN溶液,振荡 _______ 存在
取少量除尽 后的溶液于试管中,加入1~2滴______(填序号),振
_______ 存在
荡
【实验结论】铁的氧化产物为 和 ,则 的氧化性强于 ,已知 的氧化性强于
,则 可与 发生氧化还原反应。
另一同学用pH计测得常温下该硝酸银溶液的pH为5.50,于是该同学对实验结论提出质疑。
你认为他提出质疑的理由可能是______。
(3)通过原电池原理探究 与 之间的氧化还原反应。按如图所示装置组装原电池。
盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率( )应尽可能地相近,根
据下表数据,盐桥中应选择作为电解质。
阳离子 阴离子4.07 4.16
5.19 7.40
6.59 7.91
7.62 8.27
实验开始后,电流表指针发生偏转,正极电极表面有光亮的银析出,则该原电池负极的电极
反应式为__________。
【实验结论】__________。
( 4 ) 查 阅 资 料 可 知 常 温 下 : ;
。试从反应速率与化学平衡两个角度
解释 溶液与KI溶液混合只发生复分解反应而无明显氧化还原反应的可能原因:
________。
14.为测定 溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
Ⅰ.甲方案
实验原理:
实验步骤:
(1)判断 沉淀完全的操作为_______。
(2)步骤②判断沉淀是否洗净所选用的试剂为_______。
(3)步骤③灼烧时盛装样品的仪器名称为_______。
(4)固体质量为 ,则 =____ 。
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得 _______(填“偏高”“偏
低”或“无影响”)。Ⅱ.乙方案
实验原理:
实验步骤:
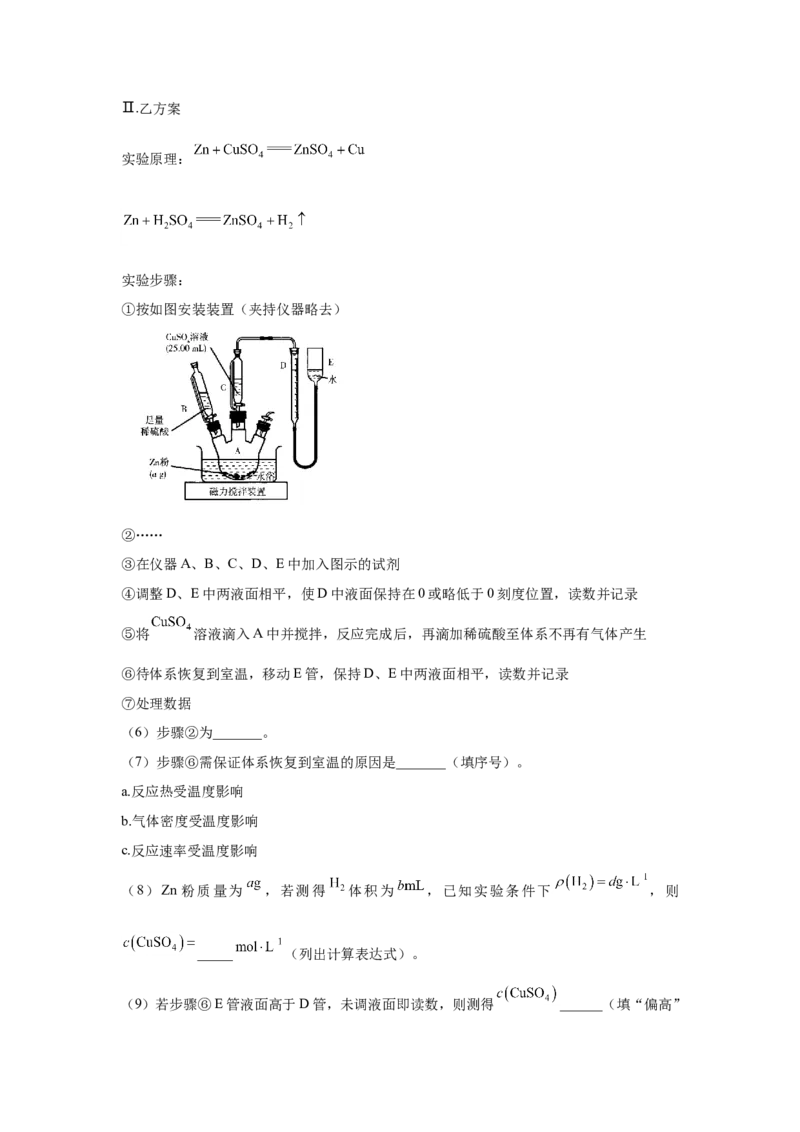
①按如图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录
⑤将 溶液滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为_______。
(7)步骤⑥需保证体系恢复到室温的原因是_______(填序号)。
a.反应热受温度影响
b.气体密度受温度影响
c.反应速率受温度影响
(8)Zn 粉质量为 ,若测得 体积为 ,已知实验条件下 ,则
_____ (列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得 ______(填“偏高”“偏低”或“无影响”)。
(10)是否能用同样的装置和方法测定 溶液的浓度:______(填“是”或“否”)。
15.某化学小组研究HCl被氧化的条件,进行如下实验。
(1)研究HCl被 氧化
实验 操作 现象
Ⅰ 常温下将 和 浓盐酸混合 溶液呈浅棕色,有刺激性气味
Ⅱ 将Ⅰ中混合物过滤,加热滤液 生成大量黄绿色气体
Ⅲ 加热 和 稀盐酸混合物 无明显现象
①已知 呈弱碱性。Ⅰ中溶液呈浅棕色是由于 与浓盐酸发生了复分解反应,化学
方程式是_____________________。
②Ⅱ中发生了分解反应,反应的化学方程式是____________________。
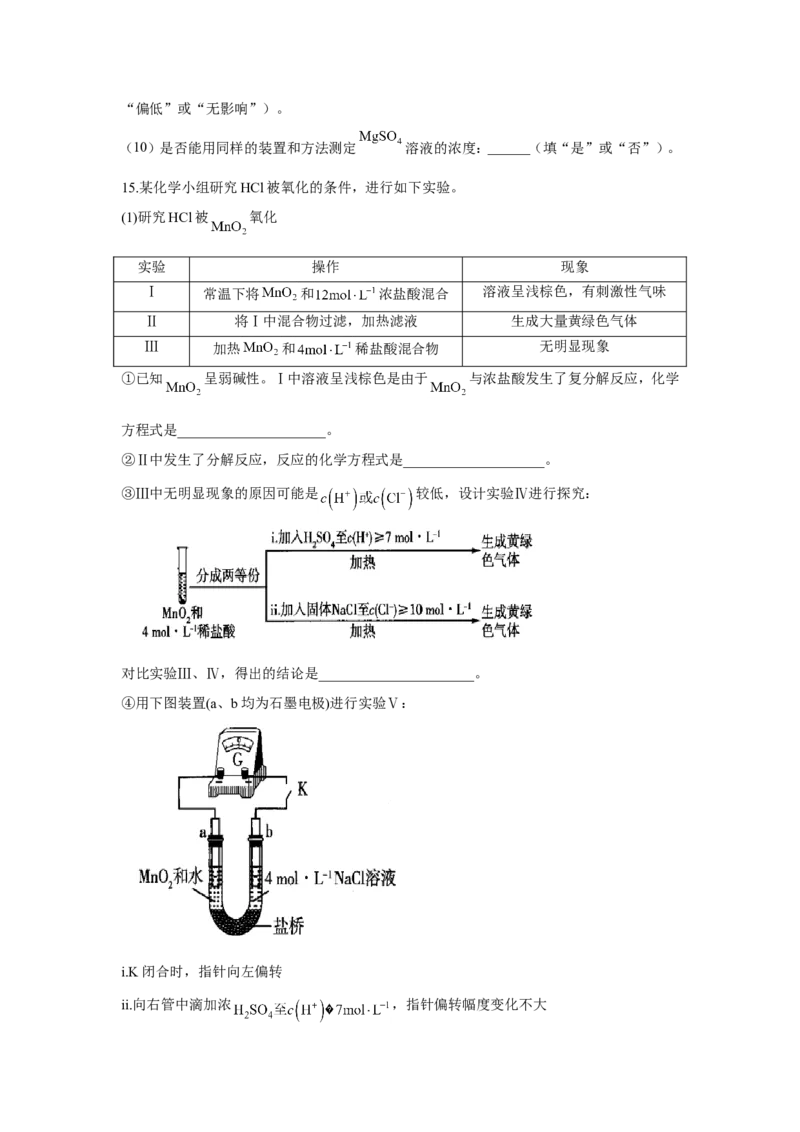
③Ⅲ中无明显现象的原因可能是 较低,设计实验Ⅳ进行探究:
对比实验Ⅲ、Ⅳ,得出的结论是______________________。
④用下图装置(a、b均为石墨电极)进行实验Ⅴ:
i.K闭合时,指针向左偏转
ii.向右管中滴加浓 ,指针偏转幅度变化不大ⅲ.再向左管中滴加浓 ,指针向左偏转幅度增大
对比i、ⅱ、ⅲ,得出的结论是_____________________。
(2)研究HCl能否被氧化性酸氧化
①烧瓶中放入浓 ,通过分液漏斗向烧瓶中滴加浓盐酸,烧瓶上方立即产生白雾,用湿
润的淀粉KI试纸检验,无明显现象。由此得出浓硫酸______________(填“能”或“不能”)
氧化HCl。
②向试管中加入3 mL浓盐酸,再加入1 mL浓 ,试管内液体逐渐变为橙色,加热,产生
棕黄色气体,经检验气体中含有 。通过实验1、2、3证明混合气体中含有 ,实验3的
操作是____________________。
实验 操作 现象
1 将湿润的淀粉KI试纸伸入棕黄色气体中 试纸先变蓝,后褪色
2 将湿润的淀粉KI试纸伸入纯净的 中 试纸先变蓝,后褪色
3
(3)由上述实验得出:HC1能否被氧化与氧化剂的种类、________________有关。
16.三硫代碳酸钠 在农业上用作杀菌剂和杀线虫剂。在工业上用于处理废水中的重
金属离子,某化学兴趣小组对 的一些性质进行了探究性实验。
实验Ⅰ:探究 的性质
步骤 操作及现象
① 取少量 固体溶于蒸馏水中,配制成溶液并分成两等份
② 向其中一份溶液中滴加几滴酚酞试液,溶液变红色
③ 向另一份溶液中滴加硫酸酸性 溶液,紫色褪去
(1) 是________酸(填“强”或“弱”)。
(2)已知步骤③的氧化产物是 ,则该反应的离子方程式为:________________________。
(3) 某同学取步骤③反应后所得溶液于试管中,滴加足量盐酸和氯化钡溶液,他认为通过测
定产生的白色沉淀的质量即可求出实验中所用的 的质量。你是否同意他的观点,并
说明理由:_________________________。
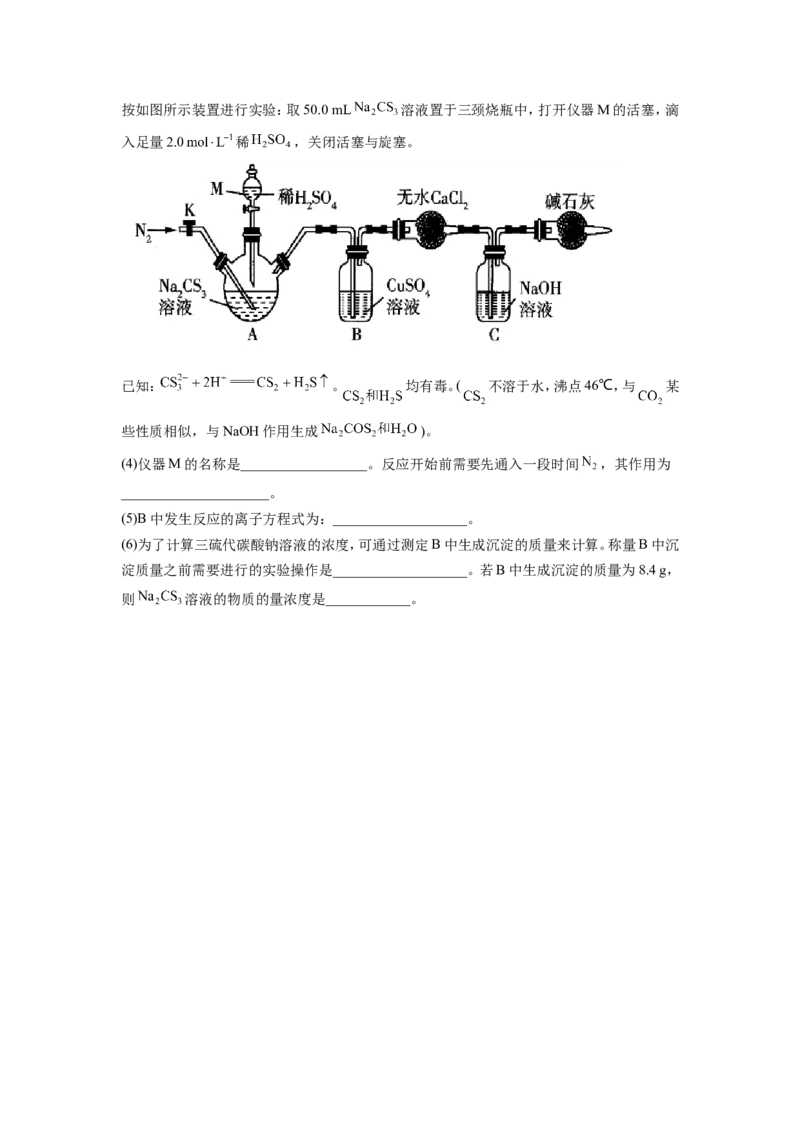
实验Ⅱ:测定 溶液的浓度按如图所示装置进行实验:取50.0 mL 溶液置于三颈烧瓶中,打开仪器M的活塞,滴
入足量2.0 稀 ,关闭活塞与旋塞。
已知: 。 均有毒。( 不溶于水,沸点46℃,与 某
些性质相似,与NaOH作用生成 )。
(4)仪器M的名称是__________________。反应开始前需要先通入一段时间 ,其作用为
_____________________。
(5)B中发生反应的离子方程式为:___________________。
(6)为了计算三硫代碳酸钠溶液的浓度,可通过测定B中生成沉淀的质量来计算。称量B中沉
淀质量之前需要进行的实验操作是___________________。若B中生成沉淀的质量为8.4 g,
则 溶液的物质的量浓度是____________。答案
1.答案:D
解析:将 通入溴水中,发生反应 ,溴水褪色, 表
现出还原性,A项错误;将铁屑放入稀 中反应生成的是NO而不是 ,不能证明Fe比
活泼,B项错误;将澄清石灰水滴入某溶液,产生浑浊,溶液中可能含有 或 或
或 等,不能证明溶液中存在 ,C项错误;将乙烯通入 酸性溶液,溶液
紫色褪去,可以证明乙烯具有还原性,D项正确。
2.答案:D
解析:本题考查氨气的制备、氢氧化亚铁的制备、酸性比较、乙烯制取实验的设计。氨气的密
度小于空气,应用向下排空气法收集氨气,图甲中是向上排空气法,A错误;装置乙中铁作阴
极,不能生成亚铁离子,进而不能生成 ,B错误;醋酸具有挥发性,醋酸、二氧化碳都
能与苯酚钠反应生成苯酚,不能用装置丙验证碳酸和苯酚的酸性强弱,C错误;乙醇在浓硫
酸作用下加热到170℃发生消去反应生成乙烯和水,实验室中可用装置丁制取少量乙烯,D
正确。
3.答案:B
解析:淀粉水解液加NaOH溶液至中性,再加入少量碘水,溶液变蓝,说明溶液中含有淀粉,
淀粉溶液在稀硫酸加热时肯定发生水解反应,根据实验现象可确定淀粉部分水解,A项错误;
稀盐酸和镁粉反应后溶液温度升高,可判断镁与盐酸的反应为放热反应,B项正确;向浓度
均为 的 和 混合溶液中加入 溶液,没有给出溶度积数据和
溶液的用量,无法确定白色沉淀的成分,若 溶液足量,会得到 和
两种沉淀,C项错误; 溶液具有强氧化性,与 反应时 表现出还原性,D项错误。
4.答案:C
解析:本题考查化学实验方案的设计与评价。因为乙醇与水互溶,不能分层,则不能用乙醇萃
取碘水中的碘,A错误;乙酸乙酯在氢氧化钠溶液中易发生水解,所以不能用氢氧化钠溶液
除去乙酸乙酯中的乙酸,可用饱和碳酸钠溶液,B错误;乙酸中的羧基易电离,水溶液呈酸性,
而乙醇中的羟基不活泼,分别向乙醇和乙酸中加入钠,钠与乙醇反应比较缓慢,而钠与乙酸
反应比较剧烈,可以此比较其官能团的活泼性,C正确;银镜反应须在碱性环境下进行,则应
先加入氢氧化钠溶液中和稀硫酸,使溶液呈碱性,再加入少量银氨溶液,水浴加热,若出现银
镜,可说明生成了葡萄糖,D错误。
5.答案:B
解析:本题考查催化效果比较、溶度积比较、二氧化氮收集、制取胆矾晶体的实验设计。将等
体积、等物质的量浓度的 和 溶液加入等体积、等浓度的 溶液中,前者
产生气泡更快,但由于两溶液中硫酸根离子浓度不同,因此不能说明 的催化效果好于
,A错误;在一定量硫酸锌溶液中加入少量硫化钠溶液,生成ZnS白色沉淀,过滤、洗涤
后,向沉淀中加入适量硫酸铜溶液,沉淀变成黑色,说明 ZnS 转化为 CuS 沉淀,则
,B正确; 密度比空气大,应用向上排空气法收集,用图中装置收集
会使空气留存在集气瓶的上方,导致气体不纯,且 会从长导管中逸出,被NaOH溶
液吸收,C错误;胆矾晶体受热容易失去结晶水,且铜离子易水解,应该用冷却热饱和硫酸铜
溶液的方法得到胆矾晶体,D错误。
6.答案:C
解析:向 溶液中加入足量铁粉后, 完全转化为 ,滴入KSCN溶液,溶液不变色,
可证明还原性 ,A项不符合题意;燃着的金属钠能在装有 的集气瓶中反应生成
和C,说明 具有氧化性,B项不符合题意; 受热分解生成的 能使湿润的红色石蕊试纸变蓝,只能说明 为碱性气体,不能确定 的酸碱性,C项符
合题意;根据题中描述可知黄色沉淀为AgI,另一支试管中无明显现象,说明没有AgCl析出,
可证明 ,D项不符合题意。
7.答案:A
解析:盐酸易挥发,且HCl与CuO能反应,装置①中盛装无水 时不能吸收挥发出的
HCl,A项错误;装置②中发生反应 ,装置③吸收反应生成的水,实验
前后装置②的质量差为生成的水中氧元素的质量,实验前后装置③的质量差为生成的水的
质量,根据水和氧元素的质量即可计算出生成的水中氢元素的质量,B项正确;为防止生成
的Cu再被氧化,实验结束需先移走酒精灯,再停止通氢气,C项正确;由B项分析知,装置②
中CuO是否被完全还原对实验结果无影响,D项正确。
8.答案:A
解析:A项,乙烯通入酸性高锰酸钾溶液,溶液紫色褪去,但溶液不分层,错误;B项,镁条和
发生反应: 2MgO+C,集气瓶中产生浓烟并有黑色颗粒产生,正确;C项,
硫代硫酸钠和稀盐酸发生反应: ,有刺激性气味
气体产生,溶液变浑浊,正确;D项, 溶液中加入过量铁粉,发生反应:
,黄色逐渐消失, 遇 不显色,加入KSCN后溶液颜色不变,正
确。
9.答案:D
解析: 固体受热后分别变为碘蒸气、氨气和碘化氢气体,在烧瓶底遇冷,又转化为
固体,装置①不能用于分离 固体, A项错误;比较 的催化活性,要求两份溶液中 的含量相同,B项错误;装置③中缺少环形玻璃搅拌棒,不能用
于测定中和热,C项错误;方案④中,两份酸的浓度和体积相同,所用碳酸钠溶液的浓度和体
积也相同,能用于比较醋酸和硼酸的酸性强弱,D项正确。
10.答案:BC
解析:本题考查基本实验操作、物质的性质检验和简单实验方案的设计。苯酚和氢氧化钠反
应生成苯酚钠和水,苯酚钠溶于水而苯不溶于水,可以用分液的方法分离,A项正确;盐酸具
有挥发性,盐酸和碳酸氢钠混合产生的气体中既有 ,又有HCl,二者均能使苯酚钠溶液
变浑浊,无法证明碳酸的酸性强于苯酚,B项错误;除去碱式滴定管内气泡的方法是把橡胶
管向上弯曲,出口上斜,挤捏玻璃球,使溶液从尖嘴快速喷出,气泡即可随之排出,C项错误;
可以用新制的氢氧化铜悬浊液检验醛基,并且碱要过量,D项正确。
11. 答 案 : ( 1 ) 平 衡 气 压 , 使 浓 盐 酸 顺 利 滴 下 ; NaOH 溶 液 ;
(2)在装置A、B之间加装盛有饱和食盐水的洗气瓶
(3)酸式;C
(4) ;BD
解析:(1)本题考查 的制备实验以及利用 滴定法测定含 样品
的组成。a为恒压滴液漏斗,在装置A中起到平衡气压,使浓盐酸顺利滴下的作用。漂白粉和
浓盐酸反应制得氯气,氯气是一种有毒气体,直接排放会污染环境,故需要在装置C中加入
氢氧化钠溶液,目的是用来吸收多余的氯气。漂白粉的主要成分为 ,装置A中制备
氯气的化学方程式为 。
(2)由于制得的氯气中混有HCl,结合已知信息,溶液碱性减弱时, 发生副反应生成,导致 产率降低,故需要在装置A、B之间加装盛有饱和食盐水的洗气瓶,来吸
收挥发出来的氯化氢。
(3)高锰酸钾具有强氧化性,能够腐蚀碱式滴定管的橡皮管,故需要将其装入酸式滴定管中。
由于滴定管的特殊构造,其尖嘴部分没有刻度,且其“0”刻度在最上,故滴定管中实际盛有
溶液的体积大于(50.00-15.00)mL=35.00mL。
(4)设 的物质的量为 mol, 的物质的量为 mol,
的物质的量为 mol,步骤Ⅰ中 和 均被氧化,结合得失电子守恒
有: , ,所以 ,步骤Ⅱ中加入
还原剂后Fe元素全部以 形式存在,由 可知, ,联立
两 个 方 程 解 得 : , 所 以 的 质 量 分 数 为
。 时, 的质量
分数为 ,样品中不含 ,中可能含 杂质,A
错误; 越大,由 的质量分数表达式可知,其含量一定越高,B正确;Fe元素
的质量为 ,若步骤Ⅰ中 溶液不足,则步骤Ⅰ中
可能有一部分 没有被氧化,但不影响 的大小,则对于测得Fe元素的含量无影响,C错
误:结合C项可知,若 溶液浓度偏低,则消耗 溶液的体积偏大,V2偏大,Fe
元素的质量偏大,则测得样品中Fe元素含量偏高,D正确。12.答案:(1)① ;②排除通入的 与水反应引起硝酸浓度增大的影响;通入 可以
带走溶液中的部分 因此三份溶液中 的浓度:B>C>A,反应速率随 浓度降低而
减慢,说明 对该反应有催化作用;③ ; 固体(或 等)
(2)
(3)
解析:(1)①向A中加入少量硝酸铜溶液,溶液呈浅蓝色,放入铜片没有明显变化,由于引入
了铜离子,但化学反应没有明显变化,故可证明 不能起催化作用,假设1不成立。②
可与水反应生成 ,会引起硝酸浓度的增大,为排除硝酸浓度增大对实验的影响,
需补充对比实验。通入 可以带走溶液中的部分 ,因此三份溶液中 的浓度:
B>C>A,反应速率随 浓度降低而减慢,说明 对该反应有催化作用,假设2成立。③
与水反应生成 ,N元素化合价降低,则必有元素化合价升高,N元素发生歧化反
应,另一种产物为 ;证明 有催化作用,则向溶液中引入 即可,可加入
固体(或 等)。
(2)由铜跟稀硝酸的反应,结合催化剂在反应前后质量和化学性质不变分析知,反应ⅱ应该
是Cu和 生成 的反应: 。
(3)硝酸盐受热易分解,铜活泼性较弱,硝酸铜晶体受热分解最终会生成铜的氧化物,假设该
晶体为1mol,质量为296g,当温度升高到 时,剩余固体的质量为296g×24.33%≈72g,其中Cu为64g,则氧元素为8g,剩余物质中铜元素与氧元素的物质的量之比为1:0.5=2:1,故其
化学式为 。
13.答案:(1)无
(2)溶液变为红色;④;产生蓝色沉淀;酸性环境下 具有强氧化性,可将Fe氧化为
(3) ; ; 和 可以发生氧化还原反应生成 和
(4) 与 生成沉淀的速率比发生氧化还原反应的速率大;生成沉淀的平衡常数较大,则
生成沉淀的复分解反应进行的程度大
解析:(1) 与 反应生成的AgI是黄色沉淀,可以直接观察到,如果二者发生氧化还原反
应,可生成 ,溶液颜色变为棕黄色。
(2)可以向少量待测液中加入KSCN溶液来检验 ,若有 ,则溶液变为红色;检验
可选择 溶液,若有 ,则产生蓝色沉淀。
(3)原溶液中的离子有 与 不能大量共存,则盐桥
中阴离子应选择 ,又 和 的电迁移率最相近,所以盐桥中应选择 作为电解
质。正极有银析出,说明电极反应式为 ,为还原反应,则负极的电极反应式为
。电流表指针发生偏转,说明该原电池成立,即发生了能自发进行的氧化还原
反应,所以结论为 与 可以发生氧化还原反应生成Ag和 。
(4) 与 生成沉淀的速率比发生氧化还原反应的速率大;生成沉淀的平衡常数较大,则生成沉淀的复分解反应进行的程度大。
14.答案:(1)向上层清液中继续滴加 溶液,无白色沉淀生成,则沉淀完全
(2) 溶液
(3)坩埚
(4)
(5)偏低
(6)检查装置气密性
(7)b
(8)
(9)偏高
(10)否
解析:(1)本题通过 溶液浓度的测定,考查实验方案的设计与评价、离子检验、有关方
程式的计算等。判断 沉淀完全,可通过检验上层清液中无 ,一般用 溶液检验
,具体操作为向上层清液中继续滴加 溶液,若无白色沉淀生成,则沉淀完全。
(2)过滤时沉淀上会附着有 等,则步骤②中判断沉淀是否洗净,可通过检验最后一次洗涤
液中是否含有 ,通常选用 溶液来检验 。
(3)灼烧固体物质用坩埚。
( 4 ) 根 据 , ,
。
(5)若步骤①转移沉淀时未洗涤烧杯, 会偏小,则测得 偏低。
(6)乙方案需准确测定生成 的体积,则步骤②为检查装置的气密性。(7)步骤⑥保证体系恢复到室温是为了准确测定生成气体的体积。气体的体积受温度影响较
大, ,则气体的密度受温度影响,答案选b。
( 8 ) 与 反 应 后 剩 余 Zn 粉 的 物 质 的 量 为
,与 反应的Zn的物质的量 ,根据关系式 ,
。
(9)若步骤⑥E管液面高于D管,未调液面即读数,测得的 体积偏小,则 偏高。
(10)因为Mg比Zn活泼,且Mg也能与稀疏酸反应置换出氢气,所以不能用同样的装置和方
法测定 溶液的浓度。
15.答案:(1)① ②
③Ⅲ中没有明显现象的原因是 较低,需要增大到一定浓度HCl才能被
氧化
④HCl的还原性与 无关; 的氧化性与 有关, 越大, 的氧化性
越强
(2)①不能 ②将湿润的淀粉KI试纸伸入纯净的 中
(3) 、
解析:(1)①由于 呈弱碱性,与浓盐酸发生复分解反应,则该反应的化学方程式为
。②将Ⅰ中混合物过滤后,所得滤液为 溶液,加热后产生的黄绿色气体为 ,由于该反应为分解反应,因此反应的化学方程式为:
。
③实验Ⅳ中增大 或 后,均能产生黄绿色气体,说明实验Ⅲ中无明显现象是由于
溶液中 较低,需要增大到一定浓度HCl才能被 氧化。④右管中滴加浓
,溶液中 增大,但指针偏转幅度变化不大,说明 不影响的还原性;左管中
滴加浓 ,溶液中 增大,指针偏转幅度增大,说明 对 的氧化性有影
响,且 越大, 的氧化性煺强。
(2)①烧瓶上方立即产生白雾,用湿润的淀粉KI试纸检验,无明显现象,说明产生的白雾中没
有 ,则HCl不能被浓硫酸氧化。②实验2中将湿润的淀粉KI试纸伸入纯净的 中,观
察到试纸先变蓝,后褪色,因此实验3需检验NO2对湿润的淀粉KI试纸颜色变化的影响,从
而证明混合气体中是否含有Cl2,因此实验3的操作是将湿润的淀粉KI试纸仲入纯净的
中。
(3)由题给实验分析可得,HCl能否被氧化与氧化剂的种类、 和 有关 。
16.答案:(1)弱
(2)
(3)不同意,因为步骤③中加入的酸性 溶液是用 酸化的,引入额外的
(4)分液漏斗;排尽装置中的空气,防止生成的 被氧化
(5)
(6)过滤、洗涤、干燥;
解析:(1) 的水溶液中加入酚酞变红色,说明 是强碱弱酸盐,则 为弱酸。
(2)步骤③的氧化产物是 ,还原产物是锰离子,同时还生成二氧化碳、水,离子方程式为
。
(3)因酸性高锰酸钾溶液用稀硫酸酸化,所以不能通过计算白色沉淀的质量来计算
的量。
(4)仪器M的名称为分液漏斗;因 为还原性气体,易被空气氧化,故反应开始前需要先通
入一段时间 ,排尽装置中的空气,防止生成的 被氧化。
(5)A中发生反应 ,生成的硫化氢可与B中的硫
酸铜反应生成CuS沉淀,反应的离子方程式为 。
(6)当A中反应完全后,打开K缓慢通入 一段时间,然后对B中混合物进行过滤、洗涤、干
燥、称重,得8.4 g沉淀, ,根据关系式
得 、
。