文档内容
单元检测七 物质结构 元素周期律
一、选择题(本题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.14C是一种放射性同位素,在高层大气中由宇宙射线产生的中子或核爆炸产生的中子轰
击14N可使它转变为14C。下列说法正确的是( )
A.14C和14N互为同位素
B.14C和C 互为同素异形体
60
C.14C核素中的中子数为8
D.14CO 的摩尔质量为46
2
2.R、X、Y、Z为原子序数依次增大的短周期元素,且Y的某种浓酸与铜反应后溶液呈绿
色,这四种元素组成的一种化合物的结构如图所示。下列说法正确的是( )
A.原子半径的大小顺序:X>Y>Z>R
B.最高价氧化物对应水化物的酸性:X>Y
C.R、X、Y能形成化合物R X—YR
3 3
D.由R、Y两种元素只能形成一种化合物
3.下列关于元素周期表的说法正确的是( )
A.第ⅠA族的元素称之为碱金属元素
B.原子序数为14的元素位于元素周期表的第三周期第ⅣA族
C.稀有气体元素原子的最外层电子数均为8
D.第二周期第ⅣA族元素的原子核电荷数和中子数一定为6
4.W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的
最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列
叙述正确的是( )
A.原子半径:Z>Y>X>W
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
5.我国嫦娥五号探测器带回1.731 kg的月球土壤,经分析发现其构成与地球土壤类似,土
壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15,X、
Y、Z为同周期相邻元素,且均不与W同族。下列结论正确的是( )
A.原子半径大小顺序为W>X>Y>ZB.化合物XW中的化学键为离子键
C.Y单质的导电性能弱于Z单质的
D.Z的氧化物的水化物的酸性强于碳酸
6.“铷(Rb)原子钟”被誉为卫星的“心脏”。下列说法正确的是( )
A.铷的熔点高于钾
B.Rb的中子数为48
C.Rb和Rb化学性质不同
D.铷元素属于第ⅠB族
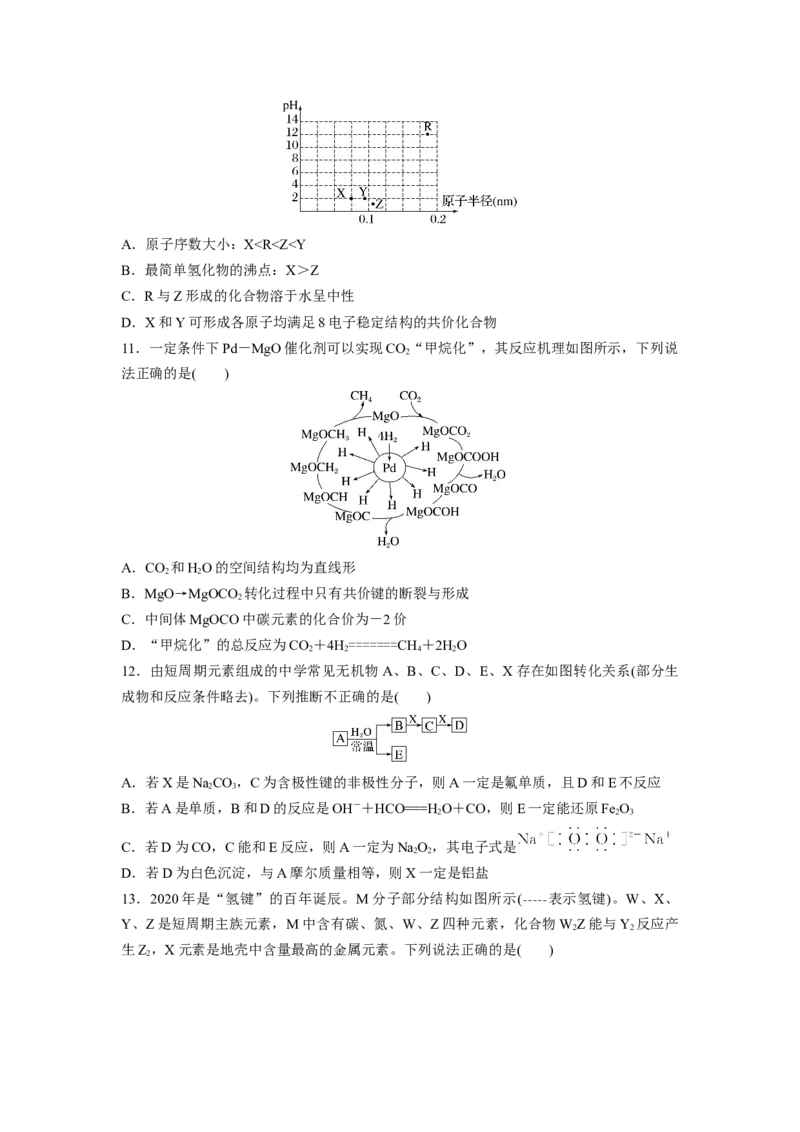
7.一种由短周期元素组成的有机化合物(如图所示),常用作分析试剂。元素 X、Y、Z、
V、W的原子序数依次增大,V的单质为黄色固体,该分子中的Y、Z、W原子均为8电子
稳定结构。下列有关叙述一定正确的是( )
A.原子半径:r(Z)>r(Y)
B.Y元素形成的单质只有两种
C.非金属性:W>V
D.W的氧化物的水化物为强酸
8.X、Y、Z、W为四种短周期元素,已知X、Z同主族,Y、W同周期;X的气态氢化物
比Z的稳定;Y的阳离子比W的阳离子氧化性强;Y的阳离子比Z的阴离子少一个电子层。
下列表示正确的是( )
A.原子序数:X>Y>Z>W
B.简单离子半径:Z>X>W>Y
C.原子半径:Y>W>Z>X
D.原子的得电子能力:Z>X
9.下列说法正确的是( )
A.核外电子的排布应优先排布在能量最低的电子层
B.对于主族元素而言,若最外层电子数为m,电子层数为n,则值越大,金属性越强
C.同一周期中,随着核电荷数的增加,阴离子半径逐渐增大
D.第三、四周期中,同族元素原子的核电荷数相差一定为8
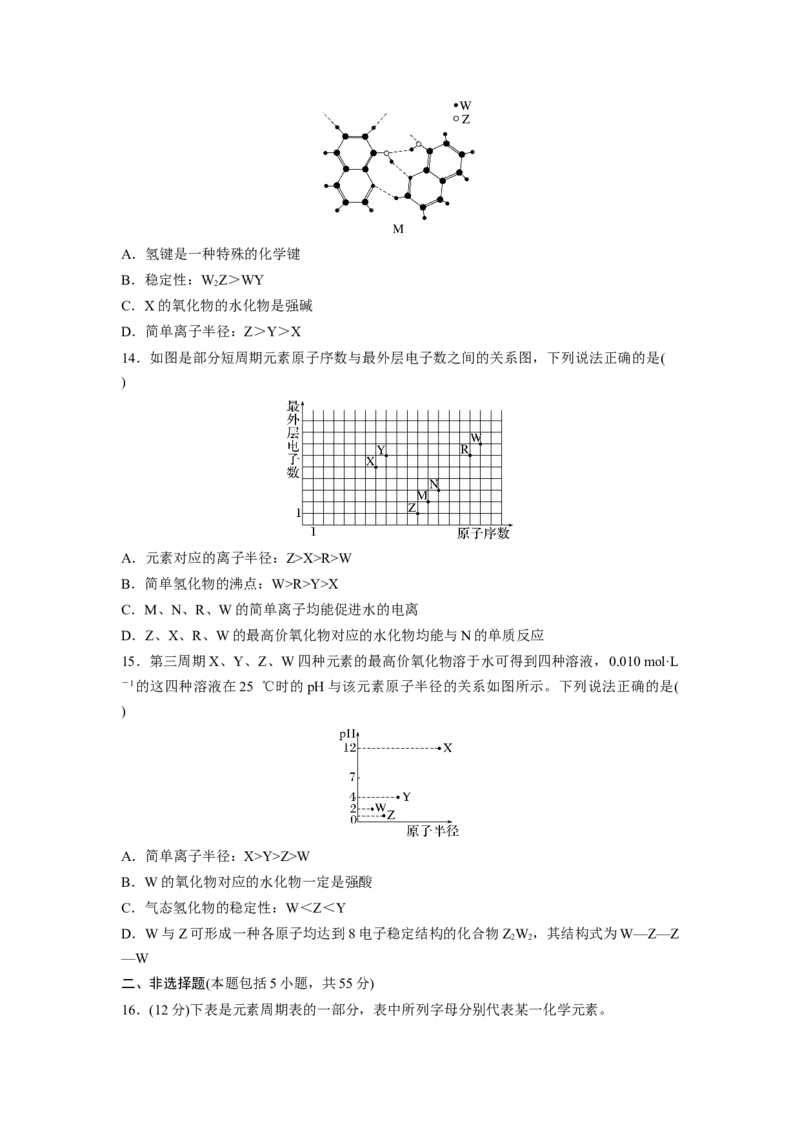
10.R、X、Y、Z为短周期元素,室温下,浓度均为0.01 mol·L-1的各元素最高价氧化物
对应水化物的pH与原子半径的关系如图所示。下列叙述错误的是( )A.原子序数大小:XX>R>W
B.简单氢化物的沸点:W>R>Y>X
C.M、N、R、W的简单离子均能促进水的电离
D.Z、X、R、W的最高价氧化物对应的水化物均能与N的单质反应
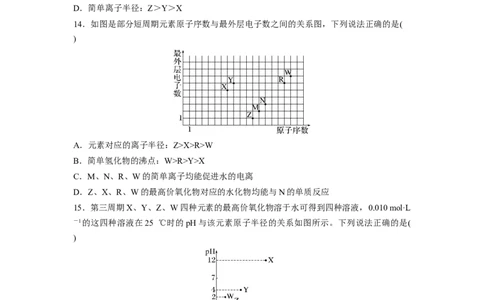
15.第三周期X、Y、Z、W四种元素的最高价氧化物溶于水可得到四种溶液,0.010 mol·L
-1的这四种溶液在25 ℃时的pH与该元素原子半径的关系如图所示。下列说法正确的是(
)
A.简单离子半径:X>Y>Z>W
B.W的氧化物对应的水化物一定是强酸
C.气态氢化物的稳定性:W<Z<Y
D.W与Z可形成一种各原子均达到8电子稳定结构的化合物ZW,其结构式为W—Z—Z
2 2
—W
二、非选择题(本题包括5小题,共55分)
16.(12分)下表是元素周期表的一部分,表中所列字母分别代表某一化学元素。(1) 表 中 字 母 h 代 表 的 元 素 在 周 期 表 中 的 位 置 :
_______________________________________。
(2) 写 出 b 元 素 的 最 高 价 氧 化 物 对 应 的 水 化 物 所 含 化 学 键 类 型 :
_________________________。
(3)下列事实能说明a元素的非金属性比c元素的非金属性强的有______(填字母)。
A.a单质与c的氢化物溶液反应,溶液变浑浊
B.在氧化还原反应中,1 mol a单质比1 mol c单质得电子数目多
C.a和c两元素的简单氢化物受热分解,前者的分解温度高
(4)g与h两元素的单质反应生成1 mol g的最高价化合物。恢复至室温,放热687 kJ。已知
该化合物的熔、沸点分别为-69 ℃和 58 ℃。写出该反应的热化学方程式:
___________________
________________________________________________________________________。
(5)常温下d遇浓硫酸形成致密氧化膜,若薄膜为具有磁性的该元素氧化物,写出该反应的
化学方程式:______________________________________________________________。
(6)e与f形成的1 mol化合物Q与水反应,生成2 mol氢氧化物和1 mol烃,该烃分子中碳
氢质量比为9∶1,写出烃分子的电子式:______________________________________。
17.(10分)a、b、c、d、e五种短周期元素的原子序数逐渐增大。a为非金属元素,且a、e
同主族,c、d为同周期的相邻元素。e原子的质子数等于c、d原子最外层电子数之和。b
原子最外层电子数是内层电子数的2倍。c的气态氢化物分子中有3个共价键。
(1)写出b元素在周期表中的位置:__________________________________________。
(2)写出一种由a、c、d所形成的离子化合物:____________(填化学式),它与e的最高价氧
化物对应水化物的溶液加热时反应的离子方程式是___________________________________。
(3)c的单质的电子式为__________。
(4)b和d相比,非金属性较强的是__________________________________(用元素符号表示),
下列事实能证明这一结论的是__________(填字母)。
A.常温下,b的单质呈固态,d的单质呈气态
B.d的最简单氢化物的稳定性强于b的最简单氢化物
C.b与d形成的化合物中,b呈正价
D.d的氢化物的沸点高于b的氢化物
18.(11分)A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元素周期
表中的相对位置如图,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D
是地壳中含量最多的金属元素。(1)C在元素周期表中的位置为________。
(2)AE 的电子式为__________。
2
(3)C、E、F的单质沸点最低的是________(填化学式)。
(4)C、D、E、F的离子半径由大到小的顺序是______________________________(填离子符
号)。
(5)实验室制取F 气体的离子方程式为______________________________________________。
2
(6)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂HO 的清除剂,所发生反
2 2
应的产物不污染环境,其化学方程式为_____________________________________________。
19.(10分)为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家
并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、
S、Hg”元素的代言人。回答下列问题:
(1)汞的原子结构示意图为 ,汞在元素周期表中位于第________周期。
(2)NH 、HO、HS中最稳定的是______。
3 2 2
(3)下列有关性质的比较能用元素周期律解释的是____________(填字母,下同)。
a.酸性:HCl>H SO
2 3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)
2
d.热稳定性:NaCO>NaHCO
2 3 3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是____________。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO )具有还原性
2
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外
最外层电子数是Y核外电子数的一半。
①Y的元素符号为________。
②X的氢化物的电子式为__________。
20.(12分)A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电
子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子
最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)W在元素周期表中的位置是________。A与E组成的化合物是常用的溶剂,写出其电子式:____________。
(2)下列事实能用元素周期表相应规律解释的是______(填字母)。
a.D的最高价氧化物对应水化物的碱性弱于Mg(OH)
2
b.E的气态氢化物的稳定性小于HF
c.A的单质能与二氧化硅高温下制得粗品硅单质
(3)WE 的 溶 液 可 用 于 刻 蚀 铜 制 的 印 刷 电 路 板 , 反 应 的 离 子 方 程 式 为
3
_____________________。
(4)① 工 业 上 用 电 解 法 制 备 D 的 单 质 , 反 应 的 化 学 方 程 式 为
_____________________________。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反
应 的 化 学 方 程 式 为
_________________________________________________________________。
(5)W的单质可用于处理酸性废水中的NO,使其转换为NH,同时生成有磁性的W的氧化
物X,再进行后续处理,上述反应的离子方程式为___________________________________。
上 述 W 的 氧 化 物 X 能 与 D 的 单 质 反 应 , 写 出 该 反 应 的 化 学 方 程 式 为
_____________________。
单元检测七 物质结构 元素周期律答案解析
1.答案 C
解析 14C和14N的质子数分别为6、7,中子数分别为8、7,不互为同位素,故A错误;
同素异形体为同种元素的不同单质,其中C 为一种单质,而14C仅为一种元素的原子,故
60
B错误;14C核素中的中子数为14-6=8,故C正确;摩尔质量的单位为g·mol-1,故D错
误。
2.答案 C
解析 由上图知,左边阳离子类似铵根离子,Y的某种浓酸与铜反应后溶液呈绿色,该浓
酸应为硝酸,Y元素应为N元素,R原子序数最小,应为H元素,Z与X形成的是单键,
应满足8电子稳定结构,Z最外层应有7个电子,X元素应结合一个Z-,Z元素应为F或
者Cl,X原子序数小于N元素,应为B元素。由以上分析知,R为H元素,X为B元素,
Y为
N元素,Z为F元素或者Cl元素,若Z为Cl元素,原子半径的大小顺序是Z>Y>X>R,A
错误;硼酸为弱酸,硝酸为强酸,所以最高价氧化物对应水化物的酸性:Y>X,B错误;
因为硼原子和氮原子之间可以形成配位键,则可以形成HB—NH ,C正确;由H和N元
3 3
素形成的化合物,常见的有NH 和NH,D错误。
3 2 4
3.答案 B解析 H位于第ⅠA族,为非金属元素,除H外第ⅠA族均为碱金属元素,A错误;原子
序数为14的元素为Si,位于元素周期表的第三周期第ⅣA族,B正确;He原子的最外层
电子数为2,除He外稀有气体元素原子的最外层电子数均为8,C错误;第二周期第ⅣA
族元素为C,存在同位素,质子数一定为6,中子数可能为6、7、8等,D错误。
4.答案 D
解析 W为H元素,X为N元素,Y为Al元素,Z为S元素。电子层数越多元素的原子半
径越大,同周期元素从左到右原子半径依次减小,则原子半径:Y(Al)>Z(S)>X(N)>
W(H),A错误;W(H)和X(N)可形成NH 和NH ,B错误;Y为Al元素,其氧化物为两性
3 2 4
氧化物,可与强酸、强碱反应,C错误;W、X和Z可形成(NH )S、NH HS,两者既含有
4 2 4
离子键又含有共价键,D正确。
5.答案 B
解析 由短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15, X、
Y、Z为同周期相邻元素,可知W所在主族可能为第ⅢA族或第ⅥA族,又因X、Y、Z
均不与W同族,故W一定不是第ⅢA族元素,即W一定是第ⅥA族元素,进一步结合已
知可推知W、X、Y、Z依次为O、Mg、Al、Si。O原子有两个电子层,Mg、Al、Si均有
三个电子层且原子序数依次增大,故原子半径大小顺序为 Mg>Al>Si>O,即X>Y>Z>
W,A错误;化合物XW即MgO为离子化合物,其中的化学键为离子键,B正确;Y单质
为铝单质,属于导体,导电性很强,Z单质为硅,为半导体,半导体导电性介于导体和绝
缘体之间,故Y单质的导电性能强于Z单质的,C错误;Z的氧化物的水化物为硅酸,硅
酸酸性弱于碳酸,D错误。
6.答案 B
解析 A项,铷和钾属于金属晶体,铷原子半径大于钾原子半径,则铷中金属键比钾中弱,
故铷的熔点低于钾,错误;B项,Rb的中子数为85-37=48,正确;C项,Rb和Rb互为
同位素,化学性质几乎完全相同,错误;D项,铷属于碱金属元素,位于第ⅠA族,错误。
7.答案 C
解析 几种元素均为短周期元素,V的单质为黄色固体,则V为S元素,W的原子序数大
于S,则W为Cl元素,分子中的Y、Z、W原子均为8电子稳定结构,Z可以和S形成双
键,应为O元素,X可以形成1个共价键,原子序数小于O,则X为H元素,Y可以形成
4个共价键,原子序数小于O,则Y为C元素。同周期主族元素从左至右原子半径依次减
小,所以C原子半径较大,即r(Z)S,即W>V,故C正确;W为Cl元素,其氧化物的水化物有多种,如HClO为弱酸,
故D错误。
8.答案 B解析 X、Y、Z、W为短周期元素,X、Z同主族,X的气态氢化物比Z的稳定,X、Z为
非金属,非金属性:X>Z,原子序数:Z>X,X处于第二周期,Z处于第三周期,Y、W
同周期,Y的阳离子的氧化性强于W的阳离子的氧化性,二者为金属元素,金属性:W>
Y,原子序数:W<Y,Y的阳离子比Z的阴离子少一个电子层,则Y、Z同周期,即Y、
Z、W处于第三周期,且原子序数:W<Y<Z。
9.答案 A
解析 一般来说,对于主族元素而言,若最外层电子数为m,电子层数为n,值越大,则
该元素越远离“左下角”,金属性越弱,B错误;同一周期中,阴离子核外电子排布相同,
核电荷数越大,阴离子半径越小,即同一周期中,随着核电荷数的增加,阴离子半径逐渐
减小,C错误;第三、四周期中,同族元素原子的核电荷数相差8或18,D错误。
10.答案 C
解析 由已知信息和图可知:R半径最大,对应pH为12,所以R为Na元素,X、Y对应
的pH都是2,根据半径大小关系,X为N元素,Y为Cl元素,Z对应的pH小于2,所以
Z为S元素。原子序数大小为NH S,B正确;R与Z形成的化合物NaS溶于水呈碱性,C错误;X和Y
3 2 2
可形成共价化合物NCl ,各原子均满足8电子稳定结构,D正确。
3
11.答案 D
解析 二氧化碳分子中C原子形成2个σ键,没有孤电子对,价层电子对数为 2,采取sp
杂化,二氧化碳为直线形,水分子中O原子形成2个O—H键,含有2对孤电子对,价层
电子对数为4,水分子为V形,故A错误;MgO只含有离子键,MgOCO 中含有离子键和
2
共价键,则MgO→MgOCO 时,没有共价键的断裂,故B错误。
2
12.答案 A
解析 若X是NaCO ,C为含极性键的非极性分子,则C为CO ,B为强酸;与水反应生
2 3 2
成强酸,可能是氯气与水反应生成的HCl,也可能是二氧化氮与水反应生成的HNO,A错
3
误;根据B、D反应为OH-+HCO===HO+CO可知,A为活泼金属Na,B为NaOH,E
2
为 H ,X 为 CO ,C 为 NaCO ,D 为 NaHCO ,B 正确;若 D 为 CO,可以判断
2 2 2 3 3
O――→CO――→CO,X为C,B为O,C为CO,A与水反应生成氧气,A为过氧化钠
2 2 2 2
或氟气,结合二氧化碳能与E反应判断A为NaO ,C正确;若D为白色沉淀,与A摩尔
2 2
质量相等,可以判断为OH-――→AlO――→Al(OH) ,X为铝盐,C为偏铝酸盐,铝盐和
3
偏铝酸盐在溶液中发生双水解反应生成Al(OH) ,则A为NaO,D正确。
3 2 2
13.答案 D
解析 W、X、Y、Z是短周期主族元素,M中含有碳、氮、W、Z四种元素,且能形成氢
键,根据原子结构可知,W是H,Z是O;化合物WZ能与Y 反应产生Z ,则Y的非金
2 2 2
属性强于Z,Y是F;X元素是地壳中含量最高的金属元素,则X是Al。氢键是一种特殊的分子间作用力,影响物质的物理性质,A错误;非金属性越强,对应氢化物的热稳定性
越强,故稳定性:HF>HO,B错误;氢氧化铝是两性氢氧化物,C错误;离子电子排布
2
相同,原子序数越大,半径越小,故简单离子半径:O>F>Al,D正确。
14.答案 D
解析 由部分短周期元素原子序数与最外层电子数之间的关系图,可知X为N,Y为O,Z
为Na,M为Mg,N为Al,R为S,W为Cl。常温下水为液态,NH 、HCl、HS均为气体,
3 2
所以水的沸点最高,NH 分子之间存在氢键,沸点高于HS、HCl,而HCl相对分子质量较
3 2
大,分子间作用力较强,沸点高于HS,所以简单氢化物的沸点:HO>NH >HCl>HS,
2 2 3 2
B错误;Mg2+、Al3+、S2-在溶液中均发生水解,促进水的电离,而Cl-不发生水解,不能
促进水的电离,C错误;Al能够与强酸、强碱溶液发生反应,Z、X、R、W的最高价氧化
物对应的水化物分别为NaOH、HNO 、HSO 、HClO ,因此它们均能与Al发生反应,D
3 2 4 4
正确。
15.答案 D
解析 第三周期元素中,X最高价氧化物对应水化物的溶液 pH为12,氢氧根离子浓度为
0.010 mol·
L-1,故为一元强碱,则X为Na元素;Y、W、Z对应的最高价氧化物对应水化物的溶液
pH均小于7,均为酸,W最高价含氧酸溶液中氢离子浓度为0.010 mol·L-1,故为一元强酸,
则W为Cl元素;最高价含氧酸中,Z对应的酸性比W的强、Y对应的酸性比W的弱,而
原子半径:Y>Z>W,故Z为S元素,Y为P元素。W的氧化物对应的水化物如果是次氯酸
则是弱酸,故B错误;W与Z可形成一种各原子均达到8电子稳定结构的化合物SCl,其
2 2
结构式为Cl—S—S—Cl,故D正确。
16.答案 (1)第三周期第ⅦA族 (2)离子键、(极性)共价键
(3)AC
(4)Si(s)+2Cl(g)===SiCl (l) ΔH=-687 kJ·mol-1
2 4
(5)3Fe+4HSO (浓)===Fe O+4SO ↑+4HO
2 4 3 4 2 2
(6)
解析 由元素周期表可知:a为氧元素、b为钠元素、c为硫元素、d为铁元素、e为镁元素、
f为碳元素、g为硅元素、h为氯元素。
(3)a为氧元素,O 与HS溶液反应,溶液变浑浊,说明有S生成,即O 的氧化性比S强,
2 2 2
即氧元素的非金属性比硫元素的非金属性强,故A正确;元素的非金属性强弱体现得电子
能力,与得电子数目无关,故B错误;O和S两元素的简单氢化物受热分解,前者的分解
温度高,说明HO比HS稳定,即氧元素的非金属性比硫元素的非金属性强,故C正确。
2 2
(5)常温下Fe遇浓硫酸形成致密氧化膜,该薄膜具有磁性说明是 Fe O ,则反应的化学方程
3 4式为3Fe+4HSO (浓)===Fe O +4SO ↑+4HO。(6)C与Mg形成的1 mol化合物Q与水反
2 4 3 4 2 2
应,生成2 mol氢氧化物和1 mol烃,此氢氧化物应为Mg(OH) ,设化合物Q分子中含有x
2
个C原子,则由原子守恒可知化合物Q的化学式为MgC ;已知烃分子中碳氢质量比为
2 x
9∶1,其分子中C、H原子数之比为∶=3∶4,结合化合物Q的化学式MgC,可知该烃
2 x
分子式为C H,C H 为共价化合物,其电子式为 。
3 4 3 4
17.答案 (1)第二周期第ⅣA族
(2)NH NO NH+OH-=====NH ↑+HO
4 3 3 2
(3) (4)O BC
解析 a、b、c、d、e五种短周期元素的原子序数逐渐增大,b原子最外层电子数是内层电
子数的2倍,原子只能有2个电子层,最外层电子数为4,则b为C元素;c的氢化物分子
中有3个共价键,则c处于第ⅤA族,c、d为同周期的相邻元素,d处于第ⅥA族,e原子
的质子数等于c、d原子最外层电子数之和,则e的质子数为5+6=11,则e为Na元素;a
为非金属元素,且a、e同主族,则a为H元素,结合原子序数可知,c、d只能处于第二周
期,故c为N元素、d为O元素。
(4)b为碳元素、d为氧元素,C、O同周期,随原子序数增大元素非金属性增强,故非金属
性:O>C,物质的状态属于物理性质,不能比较非金属性,故 A错误;d的最简单氢化物
的稳定性强于b的最简单氢化物,说明非金属性d强,故B正确;b与d形成的化合物中,
b呈正价,说明d对键合电子的吸引力更强,故d的非金属性更强,故C正确;沸点属于
物理性质,不能比较非金属性强弱,故D错误。
18.答案 (1)第二周期第ⅥA族
(2)
(3)O
2
(4)S2->Cl->O2->Al3+
(5)MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(6)2NH ·H O+3HO===N↑+8HO
3 2 2 2 2 2
解析 A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A与氧元素能形成两
种无色气体,为CO、CO ,则A为C元素;结合A、E在元素周期表中的相对位置可知E
2
为S元素;C是地壳中含量最多的元素,C为O元素,则B只能为N元素;D是地壳中含
量最多的金属元素,D为Al元素,F的原子序数最大,F只能为Cl元素,据此分析解答。
19.答案 (1)六 (2)H O (3)bc (4)ab (5)①Si ②
2
解析 (1)原子的电子层数=周期序数,由于 Hg原子的核外有6个电子层,故其位于第六
周期。(2)元素的非金属性越强,对应氢化物的稳定性越强,由 N、O、S的非金属性为O>N>S,故氢化物最稳定的是HO。(3)非金属性的强弱和氢化物酸性没有关系,则酸性:
2
HCl>H SO 不能用元素周期律解释,a错误;同主族元素从上到下非金属性逐渐减弱,则
2 3
非金属性:O>S能用元素周期律解释,b正确;金属性越强,其最高价氧化物对应水化物
的碱性越强,则碱性:NaOH>Mg(OH) 能用元素周期律解释,c 正确;热稳定性:
2
NaCO>NaHCO 不能用元素周期律解释,d错误。(5)R、X、Y、Z为同一短周期元素,根
2 3 3
据图知,Y能形成4个共价键,Z能形成1个共价键,则Y位于第ⅣA族,Z位于第ⅦA
族,且Z核外最外层电子数是Y核外电子数的一半,Z最外层有7个电子,则Y原子核外
有14个电子,Y为Si元素,Z为Cl元素,该阴离子中Cl元素为-1价、Y元素为+4价,
根据化合价的代数和为-1可知,X为-3价,所以X为P元素,根据阳离子所带电荷知,
R为Na元素,所以①Y的元素符号为Si。②X的氢化物为PH ,其电子式为 。
3
20.答案 (1)第四周期第Ⅷ族
(2)ab (3)2Fe3++Cu===2Fe2++Cu2+
(4)①2Al O(熔融)=====4Al+3O↑
2 3 2
②2Al+2NaOH+2HO===2NaAlO +3H↑
2 2 2
(5)3Fe+NO+2H++HO===Fe O+NH 8Al+3Fe O=====4Al O+9Fe
2 3 4 3 4 2 3
解析 A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数
是次外层的2倍,A为C元素;D的氧化物属于两性氧化物,D为Al元素;D、E位于同
周期,A、D、E的原子最外层电子数之和为14,则E的最外层电子数为14-4-3=7,E
为Cl元素;W是人体必需的微量元素,缺乏W会导致贫血症状,W为Fe元素,据此分析
解答。
(2)同周期元素从左到右,金属性依次减弱,铝的金属性弱于镁,所以氢氧化铝的碱性弱于
Mg(OH) ,故a选;同主族元素从上到下,非金属性依次减弱,所以 F的非金属性强于
2
Cl,则氢化物稳定性HCl小于HF,故b选;高温下,碳能与二氧化硅制得粗品硅单质,是
因为生成的CO是气体,沸点远低于二氧化硅,不能用元素周期律解释,故c不选。