文档内容
单元检测九 化学反应速率与化学平衡
一、选择题(本题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.下列对化学反应2NO+2CO N+2CO 的叙述正确的是( )
2 2
A.使用催化剂不影响反应的活化能
B.使用光催化剂能增大反应物的转化率
C.升高温度能增加反应物分子中活化分子的百分数,从而加快反应速率
D.改变压强对反应速率无影响
2.工业上,合成氨反应:N +3H 2NH 的微观历程如图所示,用 、 、
2 2 3
分别表示N、H、NH ,下列说法不正确的是( )
2 2 3
A.①→②催化剂在吸附N、H 时,未形成新的化学键
2 2
B.②→③形成N原子和H原子是放热过程
C.③→④形成了新的化学键
D.使用合适的催化剂,能提高合成氨反应的速率
3.已知298.15 K时,可逆反应Pb2+(aq)+Sn(s) Pb(s)+Sn2+(aq)的平衡常数K=2.2,
若溶液中Pb2+和Sn2+的浓度均为0.10 mol·L-1时,则此时反应进行的方向是( )
A.向正反应方向进行
B.向逆反应方向进行
C.处于平衡状态
D.无法判断
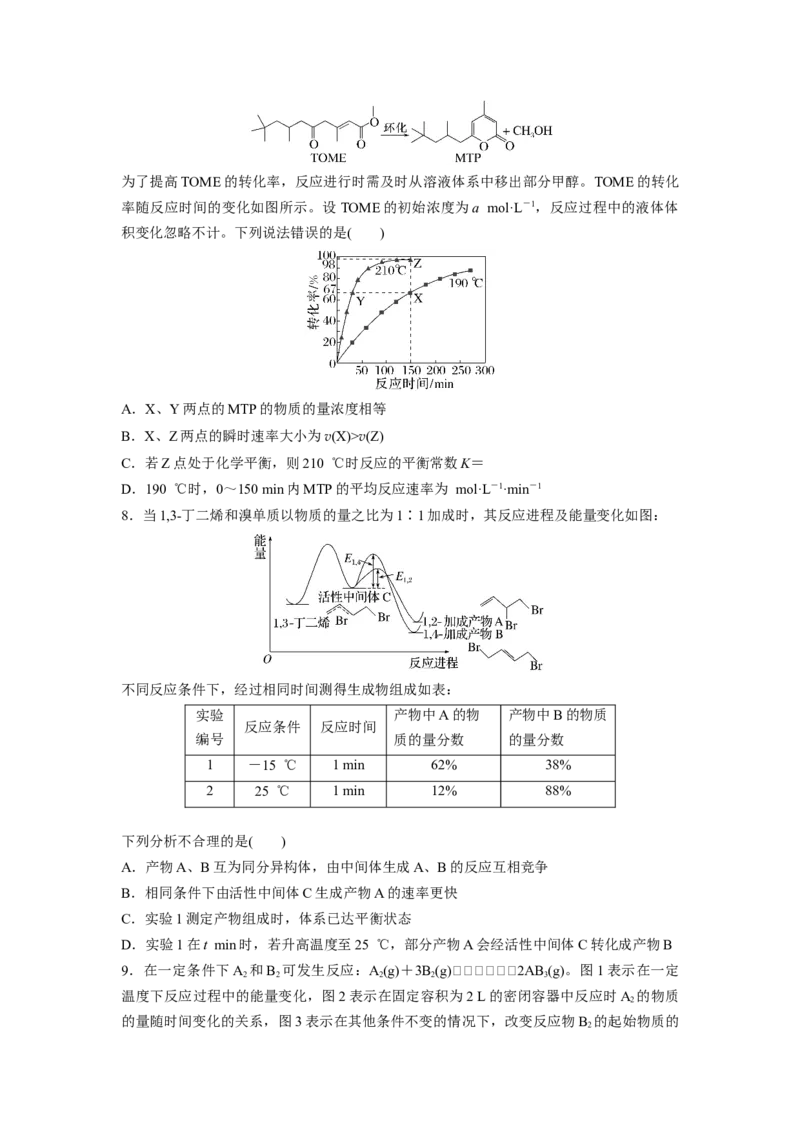
4.两个容积均为 2 L的密闭容器Ⅰ和Ⅱ中充入NO及CO气体,发生反应:2NO(g)+
2CO(g) N(g)+2CO(g) ΔH,各物质的起始物质的量见下表。实验测得两容器不同
2 2
温度下达到平衡时CO 的物质的量如图所示,下列说法正确的是( )
2
起始物质的量
容器
NO CO
Ⅰ 1 mol 3 mol
Ⅱ 6 mol 2 molA.ΔH>0
B.N点的平衡常数为0.04
C.若将容器Ⅰ的容积改为1 L,T 温度下达到平衡时NO的转化率为25%
1
D.图中M点所示条件下,再通入CO、N
2
各2 mol,此时v正 <v逆
5.不同温度下,将1 mol CO 和3 mol H 充入体积为1 L的恒容密闭容器中发生反应:
2 2
CO(g)+3H(g) CHOH(g)+HO(g) ΔH。平衡时CHOH的物质的量分数随温度变化
2 2 3 2 3
如图所示。
下列说法不正确的是( )
A.该反应的ΔH<0
B.240 ℃时,该反应的化学平衡常数K=
C.240 ℃时,若充入2 mol CO 和6 mol H ,平衡时CHOH的物质的量分数大于25%
2 2 3
D.240 ℃时,若起始时充入0.5 mol CO 、2 mol H 、1 mol CH OH、1 mol H O,反应向正
2 2 3 2
反应方向进行
6.已知:3CH(g)+2N(g) 3C(s)+4NH (g) ΔH>0,在700 ℃,CH 与N 在不同物质
4 2 3 4 2
的量之比[]时CH 的平衡转化率如图所示。下列说法正确的是( )
4
A.越大,N 的平衡转化率越高
2
B.不变时 若升温,NH 的体积分数会减小
3
C.b点对应的平衡常数比a点的大
D.a点对应的 NH 的体积分数约为26%
3
7.MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式为为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化
率随反应时间的变化如图所示。设TOME的初始浓度为a mol·L-1,反应过程中的液体体
积变化忽略不计。下列说法错误的是( )
A.X、Y两点的MTP的物质的量浓度相等
B.X、Z两点的瞬时速率大小为v(X)>v(Z)
C.若Z点处于化学平衡,则210 ℃时反应的平衡常数K=
D.190 ℃时,0~150 min内MTP的平均反应速率为 mol·L-1·min-1
8.当1,3-丁二烯和溴单质以物质的量之比为1∶1加成时,其反应进程及能量变化如图:
不同反应条件下,经过相同时间测得生成物组成如表:
实验 产物中A的物 产物中B的物质
反应条件 反应时间
编号 质的量分数 的量分数
1 -15 ℃ 1 min 62% 38%
2 25 ℃ 1 min 12% 88%
下列分析不合理的是( )
A.产物A、B互为同分异构体,由中间体生成A、B的反应互相竞争
B.相同条件下由活性中间体C生成产物A的速率更快
C.实验1测定产物组成时,体系已达平衡状态
D.实验1在t min时,若升高温度至25 ℃,部分产物A会经活性中间体C转化成产物B
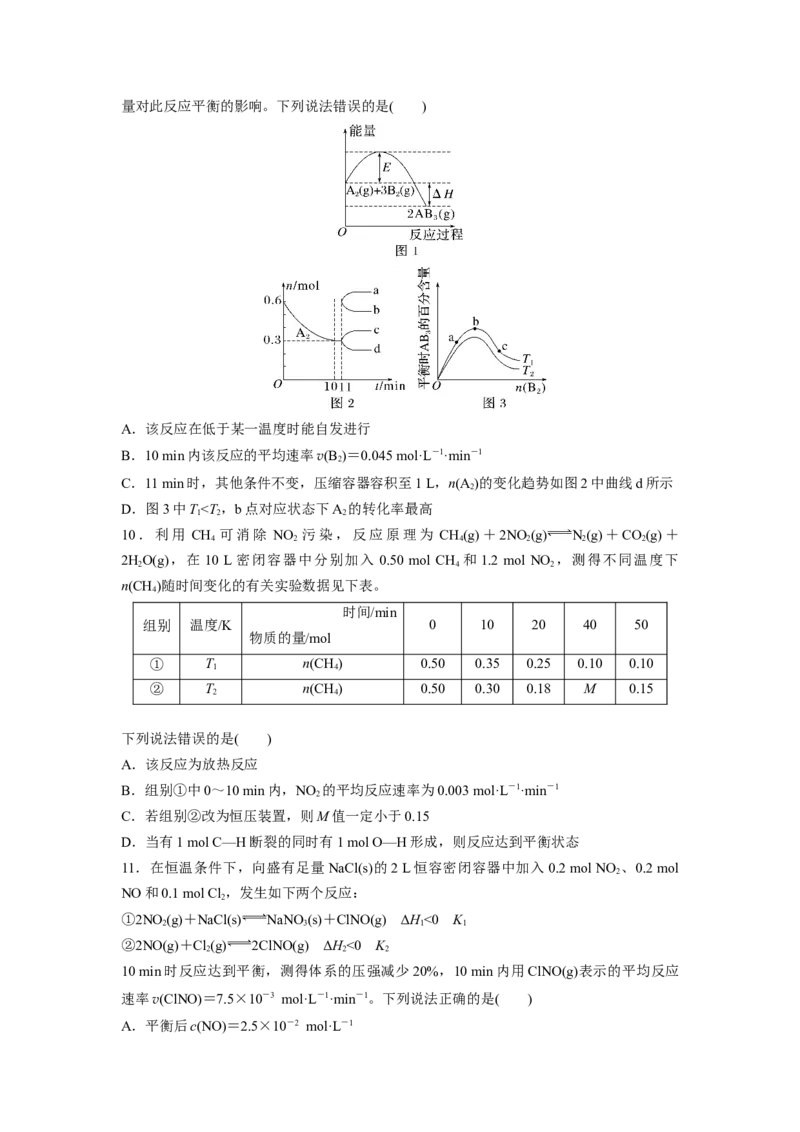
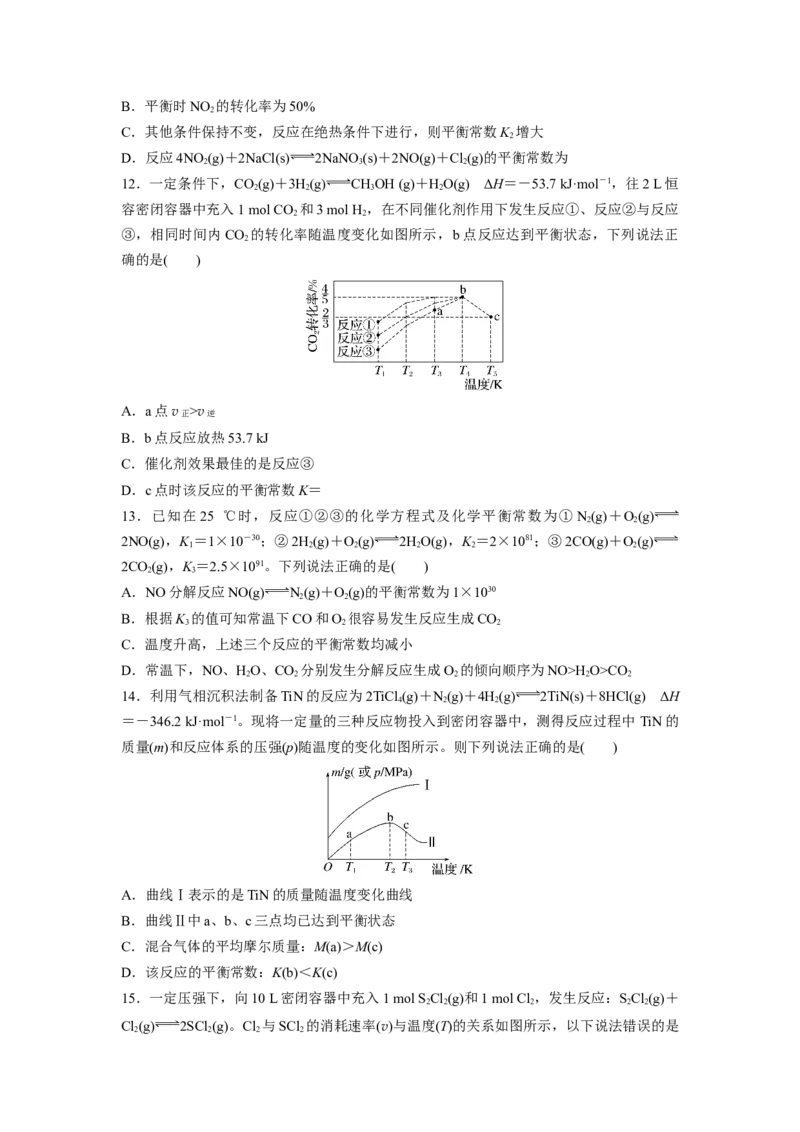
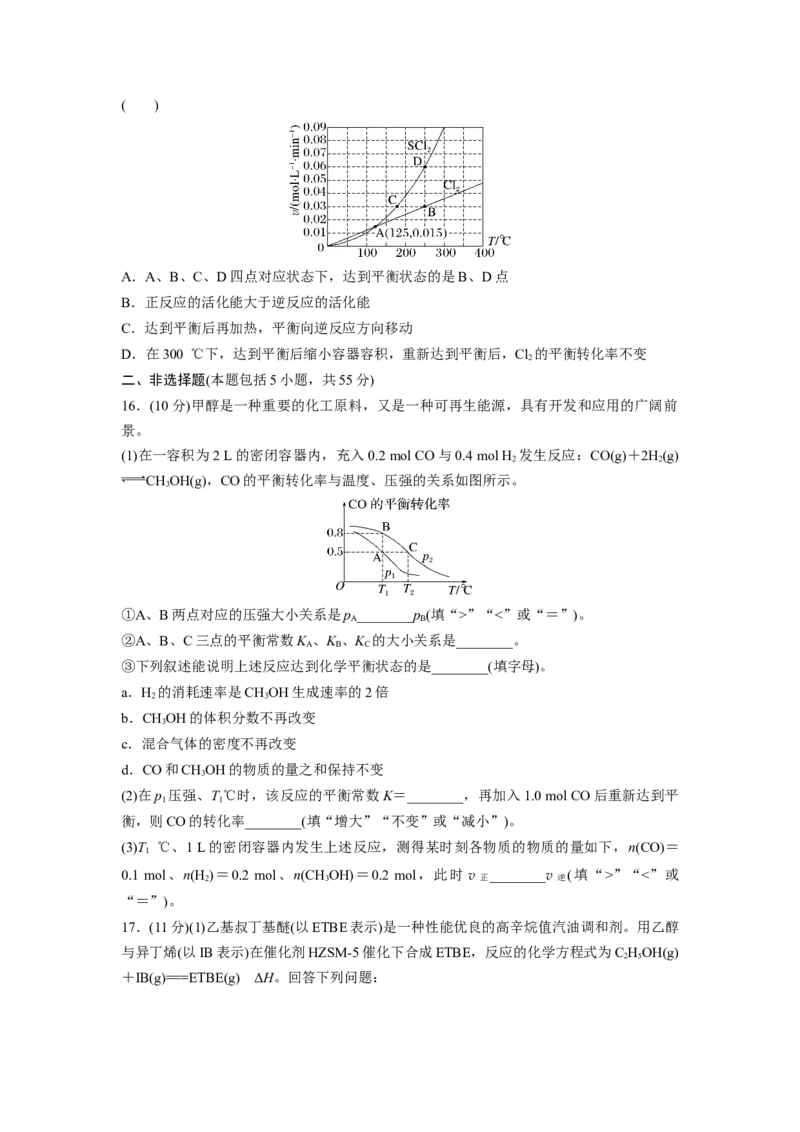
9.在一定条件下A 和B 可发生反应:A(g)+3B (g)2AB (g)。图1表示在一定
2 2 2 2 3
温度下反应过程中的能量变化,图2表示在固定容积为2 L的密闭容器中反应时A 的物质
2
的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物B 的起始物质的
2量对此反应平衡的影响。下列说法错误的是( )
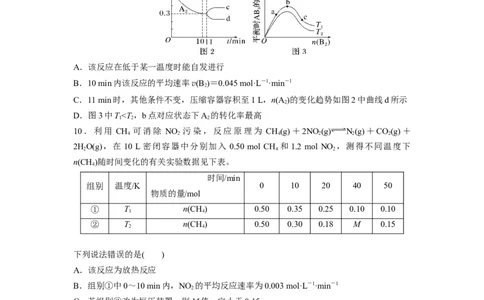
A.该反应在低于某一温度时能自发进行
B.10 min内该反应的平均速率v(B )=0.045 mol·L-1·min-1
2
C.11 min时,其他条件不变,压缩容器容积至1 L,n(A )的变化趋势如图2中曲线d所示
2
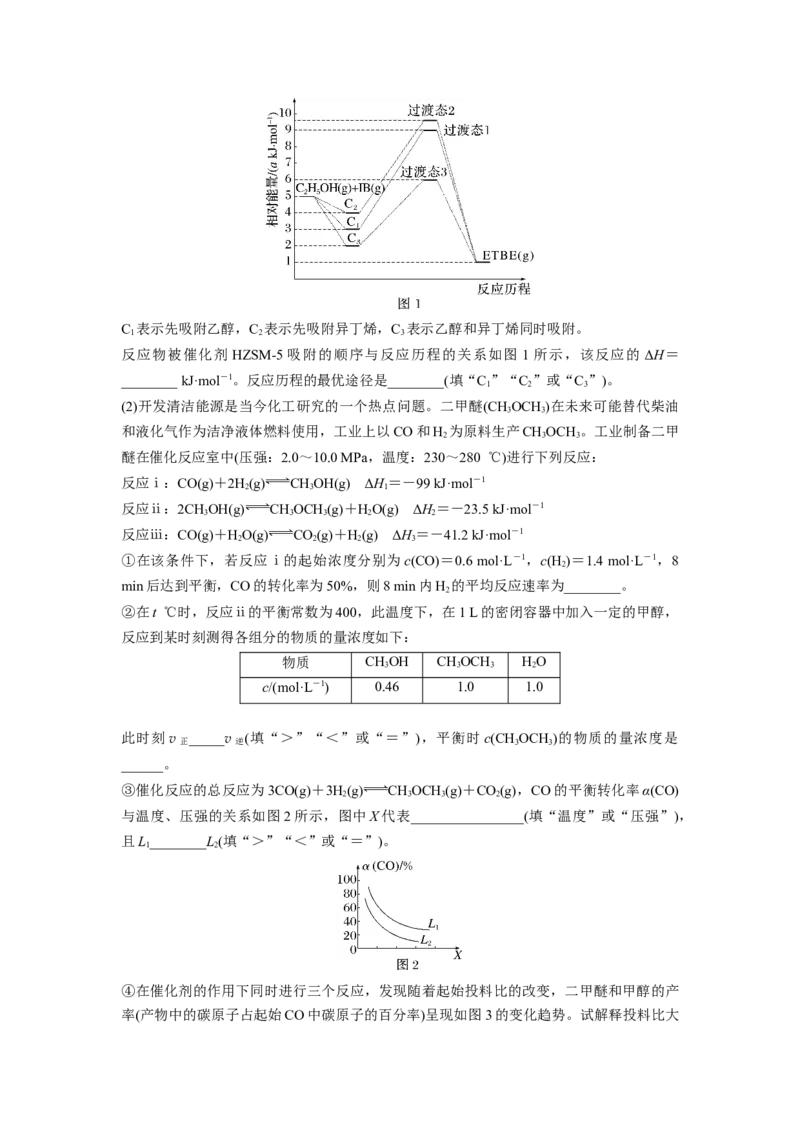
D.图3中Tv逆
B.b点反应放热53.7 kJ
C.催化剂效果最佳的是反应③
D.c点时该反应的平衡常数K=
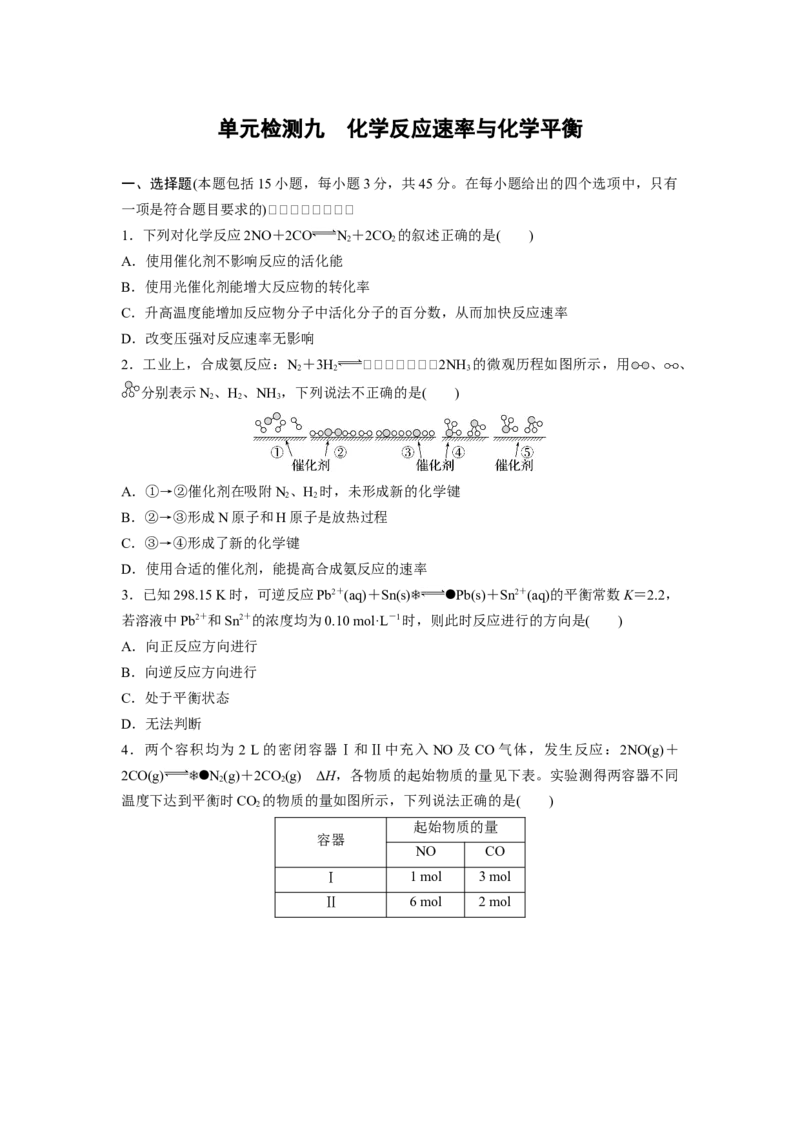
13.已知在 25 ℃时,反应①②③的化学方程式及化学平衡常数为①N(g)+O(g)
2 2
2NO(g),K =1×10-30;②2H(g)+O(g) 2HO(g),K =2×1081;③2CO(g)+O(g)
1 2 2 2 2 2
2CO(g),K =2.5×1091。下列说法正确的是( )
2 3
A.NO分解反应NO(g) N(g)+O(g)的平衡常数为1×1030
2 2
B.根据K 的值可知常温下CO和O 很容易发生反应生成CO
3 2 2
C.温度升高,上述三个反应的平衡常数均减小
D.常温下,NO、HO、CO 分别发生分解反应生成O 的倾向顺序为NO>H O>CO
2 2 2 2 2
14.利用气相沉积法制备TiN的反应为2TiCl (g)+N(g)+4H(g) 2TiN(s)+8HCl(g) ΔH
4 2 2
=-346.2 kJ·mol-1。现将一定量的三种反应物投入到密闭容器中,测得反应过程中 TiN的
质量(m)和反应体系的压强(p)随温度的变化如图所示。则下列说法正确的是( )
A.曲线Ⅰ表示的是TiN的质量随温度变化曲线
B.曲线Ⅱ中a、b、c三点均已达到平衡状态
C.混合气体的平均摩尔质量:M(a)>M(c)
D.该反应的平衡常数:K(b)<K(c)
15.一定压强下,向10 L密闭容器中充入1 mol S Cl(g)和1 mol Cl ,发生反应:SCl(g)+
2 2 2 2 2
Cl(g) 2SCl (g)。Cl 与SCl 的消耗速率(v)与温度(T)的关系如图所示,以下说法错误的是
2 2 2 2( )
A.A、B、C、D四点对应状态下,达到平衡状态的是B、D点
B.正反应的活化能大于逆反应的活化能
C.达到平衡后再加热,平衡向逆反应方向移动
D.在300 ℃下,达到平衡后缩小容器容积,重新达到平衡后,Cl 的平衡转化率不变
2
二、非选择题(本题包括5小题,共55分)
16.(10分)甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前
景。
(1)在一容积为2 L的密闭容器内,充入0.2 mol CO与0.4 mol H 发生反应:CO(g)+2H(g)
2 2
CHOH(g),CO的平衡转化率与温度、压强的关系如图所示。
3
①A、B两点对应的压强大小关系是p ________p (填“>”“<”或“=”)。
A B
②A、B、C三点的平衡常数K 、K 、K 的大小关系是________。
A B C
③下列叙述能说明上述反应达到化学平衡状态的是________(填字母)。
a.H 的消耗速率是CHOH生成速率的2倍
2 3
b.CHOH的体积分数不再改变
3
c.混合气体的密度不再改变
d.CO和CHOH的物质的量之和保持不变
3
(2)在p 压强、T℃时,该反应的平衡常数K=________,再加入1.0 mol CO后重新达到平
1 1
衡,则CO的转化率________(填“增大”“不变”或“减小”)。
(3)T ℃、1 L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,n(CO)=
1
0.1 mol、n(H 2 )=0.2 mol、n(CH 3 OH)=0.2 mol,此时 v 正 ________v 逆 (填“>”“<”或
“=”)。
17.(11分)(1)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇
与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为C HOH(g)
2 5
+IB(g)===ETBE(g) ΔH。回答下列问题:C 表示先吸附乙醇,C 表示先吸附异丁烯,C 表示乙醇和异丁烯同时吸附。
1 2 3
反应物被催化剂 HZSM-5 吸附的顺序与反应历程的关系如图 1 所示,该反应的 ΔH=
________ kJ·mol-1。反应历程的最优途径是________(填“C ”“C ”或“C ”)。
1 2 3
(2)开发清洁能源是当今化工研究的一个热点问题。二甲醚(CHOCH )在未来可能替代柴油
3 3
和液化气作为洁净液体燃料使用,工业上以CO和H 为原料生产CHOCH 。工业制备二甲
2 3 3
醚在催化反应室中(压强:2.0~10.0 MPa,温度:230~280 ℃)进行下列反应:
反应ⅰ:CO(g)+2H(g) CHOH(g) ΔH=-99 kJ·mol-1
2 3 1
反应ⅱ:2CHOH(g) CHOCH (g)+HO(g) ΔH=-23.5 kJ·mol-1
3 3 3 2 2
反应ⅲ:CO(g)+HO(g) CO(g)+H(g) ΔH=-41.2 kJ·mol-1
2 2 2 3
①在该条件下,若反应ⅰ的起始浓度分别为c(CO)=0.6 mol·L-1,c(H )=1.4 mol·L-1,8
2
min后达到平衡,CO的转化率为50%,则8 min内H 的平均反应速率为________。
2
②在t ℃时,反应ⅱ的平衡常数为400,此温度下,在1 L的密闭容器中加入一定的甲醇,
反应到某时刻测得各组分的物质的量浓度如下:
物质 CHOH CHOCH HO
3 3 3 2
c/(mol·L-1) 0.46 1.0 1.0
此时刻v正 _____v逆 (填“>”“<”或“=”),平衡时c(CH
3
OCH
3
)的物质的量浓度是
______。
③催化反应的总反应为3CO(g)+3H(g) CHOCH (g)+CO(g),CO的平衡转化率α(CO)
2 3 3 2
与温度、压强的关系如图2所示,图中X代表________________(填“温度”或“压强”),
且L________L(填“>”“<”或“=”)。
1 2
④在催化剂的作用下同时进行三个反应,发现随着起始投料比的改变,二甲醚和甲醇的产
率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图3的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:____________________________________
________________________________________________________________________。
18.(11分)(2022·北京房山模拟)乙醇是一种优良燃料,在推动能源变革方面具有重要的作
用。某地煤制乙醇的过程表示如下。
煤→…→乙酸甲酯――→乙醇
(1)Cu(NO ) 是制备“催化剂X”的重要试剂。
3 2
①气体A的名称是______________。
②实验室用Cu(NO ) 固体配制溶液,常加入少量稀HNO 。运用化学平衡原理简述HNO
3 2 3 3
的作用:____________________。
(2)过程a包括以下3个主要反应:
Ⅰ.CH COOCH (g)+2H(g) C HOH(g)+CHOH(g) ΔH
3 3 2 2 5 3 1
Ⅱ.CH COOCH (g)+C HOH(g) CHCOOC H(g)+CHOH(g) ΔH
3 3 2 5 3 2 5 3 2
Ⅲ.CH COOCH (g)+H(g)CHCHO(g)+CHOH(g) ΔH
3 3 2 3 3 3
相同时间内,测得CHCOOCH 转化率、乙醇和乙酸乙酯的选择性[如乙醇选择性=]如图所
3 3
示。
① 已知:ΔH<0。随温度降低,反应Ⅰ化学平衡常数的变化趋势是__________。
1
②下列说法不合理的是______(填字母)。a.温度可影响反应的选择性
b.225~235 ℃,反应Ⅰ处于平衡状态
c.增大H 的浓度,可以提高CHCOOCH 的转化率
2 3 3
③为防止“反应Ⅲ”发生,反应温度应控制的范围是__________。
④ 在185 ℃下,CHCOOCH 起始物质的量为5 mol,生成乙醇的物质的量是__________。
3 3
19.(11分)(2022·北京模拟)以CO 为原料合成甲醇可以减少CO 的排放,实现碳的循环利
2 2
用。一种Cu/ZnO催化剂对该反应有良好的催化效果。
Ⅰ.催化剂的合成
(1)氨水与Cu(NO ) 的反应________(填“属于”或“不属于”)氧化还原反应。
3 2
(2)补全上述过程中生成CuO的离子方程式:
____[Cu(NH )]2++____HO=====____CuO↓+________+________。
3 4 2
Ⅱ.催化剂的性能测试
一定条件下使CO 、H 混合气体通过反应器,检测反应器出口气体的成分及其含量,计算
2 2
CO 的转化率和CHOH的选择性以评价催化剂的性能。
2 3
已知:ⅰ.反应器内发生的反应:
a.CO(g)+3H(g) CHOH(g)+HO(g) ΔH=-49.5 kJ·mol-1
2 2 3 2
b.CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2 kJ·mol-1
2 2 2
ⅱ.CH OH选择性=×100%
3
(3)220 ℃ 时 , 测 得 反 应 器 出 口 气 体 中 全 部 含 碳 物 质 的 物 质 的 量 之 比
n(CHOH)∶n(CO)∶n(CO)=1∶7.20∶0.11,则该温度下CO 转化率=________×100%(列
3 2 2
出计算式)。
(4)其他条件相同时,反应温度对CO 的转化率和CHOH的选择性的影响如图所示:
2 3
①由图1可知实验中反应均未达到化学平衡状态的依据是______________。
② 温 度 高 于 260 ℃ 时 , CO 平 衡 转 化 率 变 化 的 原 因 是
2
___________________________________
________________________________________________________________________。
③温度相同时,CHOH选择性的实验值略高于平衡值(见图2),从化学反应速率的角度解
3
释原因:______________________。20.(12分)异丁烯为重要的化工原料,工业上可采用叔丁醇(TBA)气相脱水法制备高纯异丁
烯产品,主要涉及以下反应:
反应1(主反应):(CH)C—OH(g)―→(CH)C==CH(g)+HO(g)
3 3 3 2 2 2
反应2(副反应):2(CH)C==CH(g)―→(CH)C==CH—C(CH )(g)
3 2 2 3 2 3 3
(1)标准摩尔生成焓是指由稳态单质生成 1 mol该化合物的焓变,几种物质的标准生成焓如
表,求反应1的ΔH=________ kJ·mol-1。
组分 HO (CH)C—OH (CH)C==CH
2 3 3 3 2 2
焓变/
-241.83 -339.21 -17.1
(kJ·mol-1)
(2)该脱水反应的标准平衡常数K随温度的变化关系如图1所示,则反应2的ΔH___0(填
“<”或“>”),向体积可变的容器中充入1 mol叔丁醇,容器体积为1 L,保持300 ℃、
100 kPa的条件,反应一段时间后达到平衡(忽略副反应),则K=________(已知K为以标
c
准分压表示的平衡常数,各组分的标准分压p=,pθ=105Pa)
(3)理论计算反应条件对叔丁醇转化率的影响如图2、3所示,脱水反应温度T<200 ℃时,
N/叔丁醇摩尔比对叔丁醇转化率有影响,试从平衡移动的角度分析充入 N 的原因:
2 2
________
________________________________________________________________________。
根据图示该脱水反应适宜采用条件为T= 200 ℃,P=________ MPa,N/叔丁醇摩尔比=
2
3/1。(4)已知工业原料叔丁醇中存在不同含量的水分,相同温度下不同初始原料中HO/TBA比
2
例对叔丁醇平衡转化率的影响如图4所示,实际生产最佳工艺条件为T=204~426 ℃,请
从 HO/TBA 比 例 角 度 分 析 该 条 件 下 的 优 点 :
2
___________________________________________。
单元检测九 化学反应速率与化学平衡答案解析
1.
答案 C
解析 使用催化剂影响反应的活化能,改变反应速率,但不能改变反应物的平衡转化率,
A、B项错误;当反应中有气体参与时,改变压强可以影响化学反应速率,D项错误。
2.
答案 B
解析 由图知,①→②催化剂在吸附N 、H 时,没有化学键的形成与断裂,故A正确;
2 2
②→③断键形成N原子和H原子是吸热过程,故B错误;③→④形成了新的化学键——氮
氢键,故C正确;使用合适的催化剂,能提高合成氨反应的速率,故D正确。
3.
答案 A
解析 已知在298.15 K时,可逆反应Pb2+(aq)+Sn(s) Pb(s)+Sn2+(aq)的平衡常数K=2.2,若溶液中Pb2+和Sn2+的浓度均为0.10 mol·L-1时,Q==1v(Z),正
确;C项,若Z点为平衡点,此时c(TOME)=0.02a mol·L-1,c(MTP)= 0.98a mol·L-1,
但因移出甲醇,甲醇浓度不为0.98a mol·L-1,错误;D项,0~150 min时间内,Δc(MTP)=
0.67a mol·L-1,正确。
8.
答案 C
解析 A项,产物A、B分子式相同、结构不同,互为同分异构体,反应过程中放热不同,
活性中间体C根据温度不同可以转化成产物B或A,正确;B项,由图像中反应活化能分
析可知,相同条件下由活性中间体C生成产物A的活化能小,速率更快,正确;C项,实
验1测定产物组成时,不能说明物质含量保持不变,体系不一定达平衡状态,错误;D项,
反应为放热反应,实验1在t min时,若升高温度至25 ℃,产物中B的物质的量分数增大,
说明升温部分产物A会经活性中间体C转化成产物B,正确。
9.
答案 D
解析 体系的自由能ΔG=ΔH-TΔS,根据图示可知,该反应为放热反应,ΔH<0,由于该
反应的正反应是气体体积减小的反应,所以ΔS<0。当温度较低时,ΔG=ΔH-TΔS<0,反应能够自发进行,A正确;10 min内该反应的平均速率v(A )===0.015 mol·L-1·
2
min-1,根据化学方程式可知v(B )=3v(A )=0.045 mol·L-1·min-1,B正确;11 min时,其
2 2
他条件不变,压缩容器容积至1 L,由于压强增大,化学平衡正向移动,不断消耗A ,所
2
以n(A )的物质的量会进一步减少,n(A )变化趋势如图2中曲线d所示,C正确;在温度不
2 2
变时,增大某种反应物的浓度,化学平衡正向移动,可以使其他反应物的转化率提高,故
当Tv ,故A正确;b
2 正 逆
点反应达到平衡状态,参加反应的CO 小于1 mol,反应放热小于53.7 kJ,故B错误;相
2
同温度下,反应①反应速率最快,所以催化剂效果最佳的是反应①,故C错误;c点CO
2
的转化率是,则:
CO(g)+3H(g) HO(g)+CHOH(g)
2 2 2 3
开始/mol·L-1 0.5 1.5 0 0
转化/mol·L-1 ×0.5 ×0.5×3 ×0.5 ×0.5
平衡/mol·L-1 0.5
K=,故D错误。
13.
答案 D
解析 A项,NO(g) N(g)+O(g)的平衡常数为 =1015,错误;B项,CO和O 之
2 2 2
间的反应需要点燃才能进行,错误;C项,反应①为吸热反应,升高温度平衡正向移动,
平衡常数增大,错误;D项,常温下,NO、HO、CO 三种物质分解放出O 的平衡常数依
2 2 2
次为1×1030、5×10-82、4×10-92,平衡常数越大,则反应进行的程度越大,正确。
14.
答案 C
解析 依据起点的纵坐标及曲线的变化趋势可知,曲线Ⅰ呈上升趋势,曲线Ⅱ先升后降,
因为该反应为放热反应,故升高温度,平衡逆移,TiN的质量减小,所以曲线Ⅰ表示的是
压强随温度的变化,曲线Ⅱ表示的是TiN的质量随温度的变化,故A错误;温度越高反应
速率越快,达到平衡的时间越短,b点为恰好达到平衡的点,a点还未达到平衡,c点是在
b点基础上升高温度,平衡逆向移动,故B错误;由图可知a、b、c三点体系内固体质量大
小关系是m(b)>m(c)>m(a),依据质量守恒,则气体质量大小关系为m(b)<m(c)<m(a),结
合化学方程式可知,当气体质量越大时,气体的物质的量就越小,根据M=可知M(a)>
M(c)>M(b),故C正确;平衡常数只与温度有关,a、b、c三点的温度依次升高,反应是
放热反应,温度越高平衡常数越小,所以K(b)>K(c),故D错误。
15.答案 B
解析 反应达到平衡时正逆反应速率相等,所以Cl 与SCl 的消耗速率之比为1∶2,据图
2 2
可知B、D点满足条件,为平衡状态,故 A正确;据图可知B、D点之后继续升高温度
SCl 的消耗速率变大的更多,即逆反应速率大于正反应速率,平衡逆向移动,所以正反应
2
为放热反应,ΔH<0,所以正反应的活化能小于逆反应的活化能,故B错误,C正确;该
反应前后气体系数之和相等,压强不影响平衡,所以缩小容器容积,重新达到平衡后与原
平衡为等效平衡,氯气的转化率不变,故D正确。
16.
答案 (1)①< ②K =K >K ③b (2)100 减小 (3)>
A B C
解析 (1)①反应CO(g)+2H(g) CHOH(g)是气体体积减小的反应,加压平衡正向移动,
2 3
反应物转化率增大,所以p <p 。
A B
②据图分析,随温度升高CO转化率降低,说明正反应放热,升温平衡逆向移动,平衡常
数减小,所以K =K >K 。
A B C
③H 的消耗速率是CHOH生成速率的2倍,都是正反应速率,不能说明反应达到平衡状态,
2 3
故a错误;CHOH的体积分数不再改变说明正、逆反应速率相等,反应达到平衡状态,故
3
b正确;容器体积和气体质量始终不变,所以混合气体的密度始终不变,因此密度不变不
能说明反应达到平衡状态,故c错误;CO和甲醇的化学计量数都为1,所以CO和CHOH
3
的物质的量之和始终保持不变,不能说明反应达到平衡状态,故d错误。
(2)p 压强、T ℃时CO的转化率为0.5,则
1 1
CO(g)+2H(g) CHOH(g)
2 3
起始浓度/mol·L-1 0.1 0.2 0
转化浓度/mol·L-1 0.05 0.1 0.05
平衡浓度/mol·L-1 0.05 0.1 0.05
化学平衡常数K==100。若温度不变,再加入1.0 mol CO,平衡向正反应方向移动,重新
达到平衡,氢气的转化率增大,CO的转化率减小。
(3)T℃、1 L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:n(CO)=0.1
1
mol、n(H )=0.2 mol、n(CHOH)=0.2 mol,此时反应的浓度商Q==50<K=100,此时v
2 3 正
>v 。
逆
17.
答案 (1)-4a C (2)①0.075 mol·L-1·min-1 ②> 1.2 mol·L-1 ③温度 > ④当投
3
料比大于1时,随着c(H )增大,反应ⅰ被促进,而反应ⅲ被抑制,c(H O)增大,最终抑制
2 2
反应ⅱ,因此甲醇的产率继续增大而二甲醚的产率减小
解析 (1)由图可知,反应物的总能量为5a kJ·mol-1,生成物的总能量为a kJ·mol-1,所以
反应的ΔH=-4a kJ·mol-1。反应历程的最优途径是C ,其所需要的活化能最小。
3(2)①在该条件下,若反应ⅰ的起始浓度分别为c(CO)=0.6 mol·L-1,c(H )=1.4 mol·L-1,8
2
min后达到平衡,CO的转化率为50%,则8 min内H 的平均反应速率为 v===0.075
2
mol·L-1·min-1。③催化反应的总反应为3CO(g)+3H(g)CHOCH (g)+CO(g)是由反应式
2 3 3 2
ⅰ×2+ⅱ+ⅲ而得,故总反应的ΔH=ΔH×2+ΔH +ΔH =-262.7 kJ·mol-1<0,该反应
1 2 3
是放热反应,若升温,则CO的平衡转化率会减小,总反应是气体体积减小的反应,若增
压,则CO的平衡转化率会增大,则图2中,横坐标X代表的是温度,L代表的是压强,根
据压强增大CO的平衡转化率也增大可判断:L>L。
1 2
18.
答案 (1)①一氧化氮 ②Cu2++2HO Cu(OH) +2H+,增大溶液中H+的浓度,抑制
2 2
Cu2+的水解 (2)①增大 ②b ③小于205 ℃ ④0.2 mol
解析 (1)②在Cu(NO ) 溶液中,Cu2+会发生水解:Cu2++2HO Cu(OH) +2H+,加入
3 2 2 2
稀HNO 可以增大溶液中H+的浓度,抑制Cu2+的水解。(2)①ΔH <0,反应为放热反应,
3 1
降低温度,反应Ⅰ的化学平衡常数增大。②如图2所示,温度不同,乙醇和乙酸乙酯的选
择性不同,即温度可影响反应的选择性,a正确;225~235 ℃之间,乙醇的选择性几乎不
变,但是乙酸乙酯的选择性降低;若反应Ⅰ处于平衡状态,则反应Ⅰ产生的C HOH的量
2 5
保持不变,而反应Ⅱ是消耗C HOH、生成乙酸乙酯的反应,乙酸乙酯的选择性降低,说
2 5
明反应Ⅱ向左移动,C HOH的量增加,使得反应Ⅰ向左移动,则反应Ⅰ不能处于平衡状
2 5
态,b错误;增大H 浓度,可以使得反应Ⅰ、反应Ⅲ向右移动,增大CHCOOCH 的转化
2 3 3
率,同时还增大了C HOH的浓度,引起反应Ⅱ向右移动,因此也间接地增大了反应Ⅱ中
2 5
CHCOOCH 的转化率,c正确。③根据图2,温度超过205 ℃时,乙醇的选择性变化不大,
3 3
但乙酸乙酯的选择性变化较大,如果温度升高,乙酸乙酯的选择性大幅度减小,不利于反
应生成乙醇,为防止“反应Ⅲ”发生,应控制温度低于205 ℃。④在185 ℃下,乙醇选择
性为20%,CHCOOCH 的转化率为20%,则5 mol CH COOCH 反应生成乙醇的物质的量为
3 3 3 3
5 mol×20%×20%=0.2 mol。
19.
答案 (1)不属于 (2)1 1 1 2NH ↑
3
2NH (3) (4)①CO 的实验转化率未达到平衡转化率 ②温度升高,反应a逆向移动,反
2
应b正向移动,温度高于260 ℃时,反应b正向移动的程度大于反应a逆向移动的程度
③在该条件下反应a的速率大于反应b,单位时间内生成甲醇的量比生成CO的量多
解析 (1)氨水与Cu(NO ) 反应生成[Cu(NH )]2+,元素化合价没发生变化,不属于氧化还
3 2 3 4
原反应。(2)[Cu(NH )]2+和HO反应生成产物之一为CuO,元素化合价没发生变化,不属
3 4 2
于氧化还原反应,根据电荷守恒和原子守恒可判断还生成了 NH和NH ,配平后得到上述
3
过程中生成CuO的离子方程式为[Cu(NH )]2++HO=====CuO↓+2NH ↑+2NH。(3)220
3 4 2 3
℃时,测得反应器出口气体中全部含碳物质的物质的量之比n(CHOH)∶n(CO)∶n(CO)=
3 21∶7.20∶0.11,假设生成的CHOH的物质的量为1 mol,则生成的CO的物质的量为0.11
3
mol,剩余的CO 的物质的量为7.20 mol,根据碳原子守恒,起始的CO 的物质的量为(1+
2 2
7.20+0.11) mol,则该温度下CO 转化率的计算式为×100%。
2
20.
答案 (1)+80.28 (2)< 100 (3)叔丁醇脱水反应是分子数增加的反应,而副反应是分子
数减小的反应,N 为稀释剂,降低反应原料的分压,有利于主反应正向进行,抑制副反应
2
正向进行 0.1 (4)该条件下叔丁醇平衡转化率受HO/TBA比例的影响很小,故工业上可
2
忽略水对叔丁醇转化率的影响,无需对原料进行烘干处理
解析 (1)根据标准摩尔生成焓的定义,结合盖斯定律可知 ΔH=生成物的标准摩尔生成焓
-反应物的标准摩尔生成焓=-241.83 kJ·mol-1+(-17.1 kJ·mol-1)-(-339.21 kJ·mol-1)=
+80.28 kJ·mol-1。(2)由图像分析,反应2的K随温度的升高逐渐降低,说明该反应为放热
反应,ΔH<0;由图像信息知K==100,由题干信息各组分的标准分压p=,pθ=105Pa,
可得K =K×pθ=107Pa,列三段式
p
(CH)C—OH―→(CH)C==CH+HO
3 3 3 2 2 2
起始n/mol 1 0 0
0
转化n/mol x x x
1
平衡n/mol 1-x x x
平衡时总物质的量为(1+x) mol,反应前气体总物质的量为1 mol,体系的体积为1 L,根据
PV=nRT,平衡时体系的体积为(1+x) L,各组分的浓度及物质的量分数分别为 c(H O)=
2
mol·L-1,x(H O)=,c[(CH )C==CH]= mol·L-1,x[(CH )C==CH]=,c[(CH )C—OH]
2 3 2 2 3 2 2 3 3
= mol·L-1,x[(CH )C—OH]=,则K===100。
3 3 c
(4)由图像4可知在T<200 ℃,叔丁醇平衡转化率随着HO/TBA比例的增加有一定程度的
2
降低,即反应时需要除去原料中包含的水,T>200 ℃时,HO对叔丁醇平衡转化率的影响
2
可以忽略不计,故工业上可忽略水对叔丁醇转化率的影响,无需对原料进行烘干处理。