文档内容
单元检测五 金属及其化合物
一、选择题(本题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.下列关于金属在自然界中存在形态的说法正确的是( )
A.大多数金属在自然界中以单质的形式存在
B.金属在自然界中只能以化合态的形式存在
C.金属在自然界中都能以化合态和游离态两种形式存在
D.金属在自然界中的存在形态与其化学活动性有关
2.下列有关物质性质及应用的说法正确的是( )
A.过量的铜与浓硝酸反应可生成NO
B.Fe在O 中的燃烧产物可用于制红色涂料
2
C.Na、Al、Cu分别可以用电解冶炼法、热还原法和热分解法得到
D.Fe2+、SO 都能使酸性高锰酸钾溶液褪色,前者表现出还原性,后者表现出漂白性
2
3.某黑色粉末可能是Fe O 或Fe O 与FeO的混合物,为进一步确认该黑色粉末的成分,
3 4 3 4
下列实验方案不可行的是( )
A.准确称量一定质量的黑色粉末,用H 充分还原,并用干燥剂收集所得的水,获得水的
2
准确质量,进行计算
B.准确称量一定质量的黑色粉末,溶于足量盐酸,加热蒸干溶液并在空气中灼烧至质量
不变,称量所得粉末质量,进行计算
C.准确称量一定质量的黑色粉末,用CO充分还原,在CO气流中冷却后准确称量剩余固
体的质量,进行计算
D.准确称量一定质量的黑色粉末,与一定量铝粉混合后点燃,充分反应后冷却,准确称
量剩余固体质量,进行计算
4.某工厂用 FeCl 溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的
3
废液的组成,进行如下实验:(1)取10 mL废液加入足量的AgNO 溶液,生成沉淀 8.61 g;
3
(2)另取10 mL废液放入铜片充分反应,铜片质量减少了0.256 g。下列关于废液组成的判断
错误的是( )
A.一定含有Fe2+、 Fe3+、 Cu2+、 Cl-
B.c(Fe2+)∶c(Cu2+)=2∶1
C.c(Cl-)=6 mol·L-1,c(Fe2+)=1.2 mol·L-1
D.c(Fe2+)∶c(Fe3+)=3∶1
5.下列说法不正确的是( )
A.硅酸钠是一种难溶于水的硅酸盐
B.镁在空气中燃烧可生成氧化镁和氮化镁
C.钠与水反应生成氢氧化钠和氢气D.常温下,铝遇浓硝酸或浓硫酸时会发生钝化
6.在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关Fe O
2 3
及其硫酸盐的信息,用以证明火星上存在或曾经存在过水。以下叙述正确的是( )
A.Fe O 与Fe O 互为同素异形体
2 3 3 4
B.制备Al用电解法,制备Fe、Cu可用还原法
C.将SO 通入BaCl 溶液中至饱和,有沉淀产生
2 2
D.检验从火星上带回来的红色物质是否是Fe O 的操作步骤:样品→粉碎→加水溶解→过
2 3
滤→向滤液中滴加KSCN溶液
7.下列说法正确的是( )
A.Na露置在空气中最终变为NaOH
B.可以用H 还原MgO来冶炼金属Mg
2
C.擦去氧化膜的Al条在酒精灯上加热,铝会熔化但不滴落
D.向Fe (SO ) 溶液中加入过量Zn粉生成FeSO 溶液
2 4 3 4
8.下列说法正确的是( )
A.NaO在空气中加热可得固体NaO
2 2 2
B.Mg加入到过量FeCl 溶液中可得Fe
3
C.FeS 在沸腾炉中与O 反应主要生成SO
2 2 3
D.HO 溶液中加入少量MnO 粉末生成H 和O
2 2 2 2 2
9.下列“推理”合理的是( )
A.因为MgCl 溶液低温蒸干得到Mg(OH) ,所以NaCl溶液低温蒸干也可得到NaOH
2 2
B.氯气能使湿润的pH试纸褪色,可推出氯气具有漂白性
C.因为氧化性:浓硝酸强于稀硝酸,所以相同条件下铁在浓硝酸中反应一定更剧烈
D.因为电离出H+的能力:苯酚强于HCO,所以在苯酚浊液中加入碳酸钠溶液能变澄清
10.由氧化铜、氧化铁、氧化锌组成的混合物a g,加入50 mL 2 mol·L-1硫酸时固体恰好
完全溶解,若将a g该混合物在足量的一氧化碳中加热充分反应,冷却后剩余固体的质量
为( )
A.1.6 g B.(a-1.6)g
C.(a-3.2)g D.无法确定
11.将O 、CH 、NaO 放入密闭容器中,在150 ℃条件下用电火花引燃反应,恰好完全
2 4 2 2
反应,此时容器中的压强为零,由此得出原混合物中O 、CH 、NaO 的物质的量之比为(
2 4 2 2
)
A.1∶1∶1 B.2∶2∶6
C.1∶2∶6 D.无法确定
12.下列关于铝的叙述正确的是( )
A.由于铝在空气中不会锈蚀,所以铝制品的使用寿命都很长
B.由于铝具有强还原性,所以常用铝来冶炼某些高熔点金属C.常温下,铝被浓硫酸钝化,所以可用浓硫酸除去铝表面的铜镀层
D.由于铝的导电性能比铜强,所以常用铝制造电线、电缆
13.为测定含镁3%~5%的铝镁合金中镁的质量分数,设计了两种实验方案:
方案一:镁铝合金加入足量的氢氧化钠溶液中充分反应后过滤,测定剩余固体质量;
方案二:称量m g铝镁合金粉末,放在图中惰性电热板上,通电使其充分灼烧。测得固体
质量增重。下列说法不正确的是( )
A.方案一中若称取5.4 g合金粉末样品,投入V mL 2.0 mol·L-1 NaOH溶液中反应,则
V≥100
B.方案一中测定剩余固体质量时,过滤后未洗涤固体就干燥、称量,则镁的质量分数偏
高
C.方案二中欲计算镁的质量分数,实验中还需测定灼烧后固体的质量
D.方案二中若用空气代替O 进行实验,则测定结果偏高
2
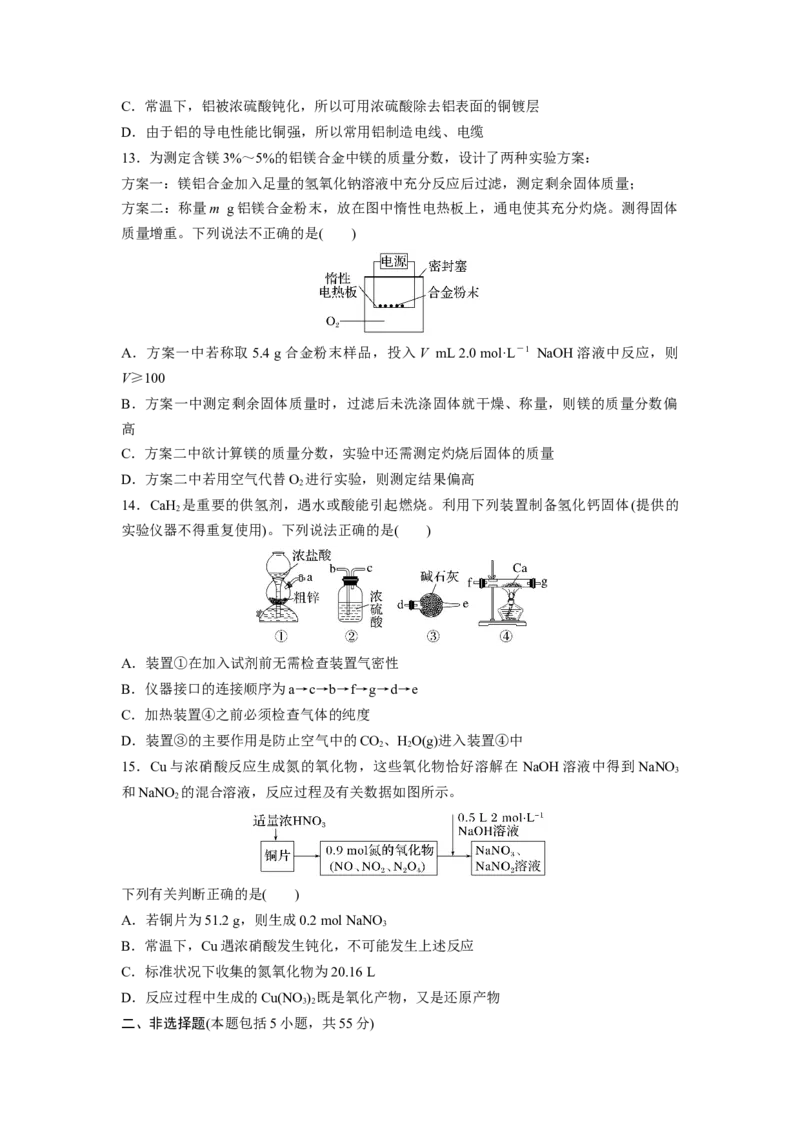
14.CaH 是重要的供氢剂,遇水或酸能引起燃烧。利用下列装置制备氢化钙固体(提供的
2
实验仪器不得重复使用)。下列说法正确的是( )
A.装置①在加入试剂前无需检查装置气密性
B.仪器接口的连接顺序为a→c→b→f→g→d→e
C.加热装置④之前必须检查气体的纯度
D.装置③的主要作用是防止空气中的CO、HO(g)进入装置④中
2 2
15.Cu与浓硝酸反应生成氮的氧化物,这些氧化物恰好溶解在 NaOH溶液中得到NaNO
3
和NaNO 的混合溶液,反应过程及有关数据如图所示。
2
下列有关判断正确的是( )
A.若铜片为51.2 g,则生成0.2 mol NaNO
3
B.常温下,Cu遇浓硝酸发生钝化,不可能发生上述反应
C.标准状况下收集的氮氧化物为20.16 L
D.反应过程中生成的Cu(NO ) 既是氧化产物,又是还原产物
3 2
二、非选择题(本题包括5小题,共55分)16.(10分)铁是人类较早使用的金属之一。运用所学知识回答下列问题。
(1) 用 丁 达 尔 效 应 鉴 别 Fe(OH) 胶 体 和 FeCl 溶 液 的 操 作 是
3 3
_______________________________
_______________________________________________________________________________
。
(2)电子工业用FeCl 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 FeCl 溶液与铜
3 3
反应的离子方程式:_____________________________________________________________。
(3)某研究性学习小组为检验FeCl 腐蚀铜后所得溶液中是否含有Fe2+,正确的实验方法是
3
_______________________________________________________________________________
_
(写出具体的实验操作、现象、结论)。
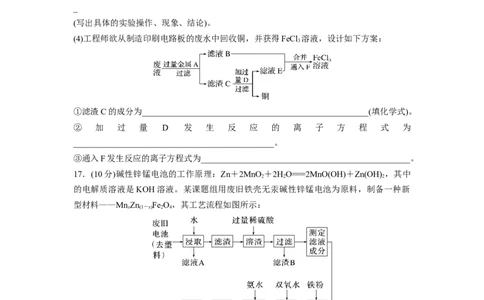
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl 溶液,设计如下方案:
3
①滤渣C的成分为_____________________________________________________(填化学式)。
② 加 过 量 D 发 生 反 应 的 离 子 方 程 式 为
_______________________________________________。
③通入F发生反应的离子方程式为_________________________________________________。
17.(10分)碱性锌锰电池的工作原理:Zn+2MnO +2HO===2MnO(OH)+Zn(OH) ,其中
2 2 2
的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新
型材料——MnZn Fe O,其工艺流程如图所示:
x (1-x) 2 4
(1)已知MnZn Fe O 中锰元素的化合价与实验室中用二氧化锰制取氯气时还原产物中的
x (1-x) 2 4
锰元素的化合价相同,则铁元素的化合价为______。
(2)“浸取”工序得到的滤液 A 经蒸发结晶,可以获得化工产品 M,M 的电子式为
____________。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2
+ , 写 出 该 反 应 的 离 子 方 程 式 :________________________________________________________。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与
产品的化学式 MnZn Fe O 相符合。写出“调铁”工序中发生反应的离子方程式:
x (1-x) 2 4
________________、________________。
(5)在“氧化”工序中,加入双氧水的目的是__________________;生产过程中发现实际消
耗 双 氧 水 的 量 大 于 理 论 值 , 其 可 能 原 因 除 温 度 外 , 主 要 是
_________________________________。
(6)用氨水“调pH”后,经“结晶”“过滤”可得到产品和滤液C,从滤液C中还可分离出
一 种 氮 肥 。 该 氮 肥 的 溶 液 中 离 子 浓 度 由 大 到 小 的 顺 序 为
________________________________。
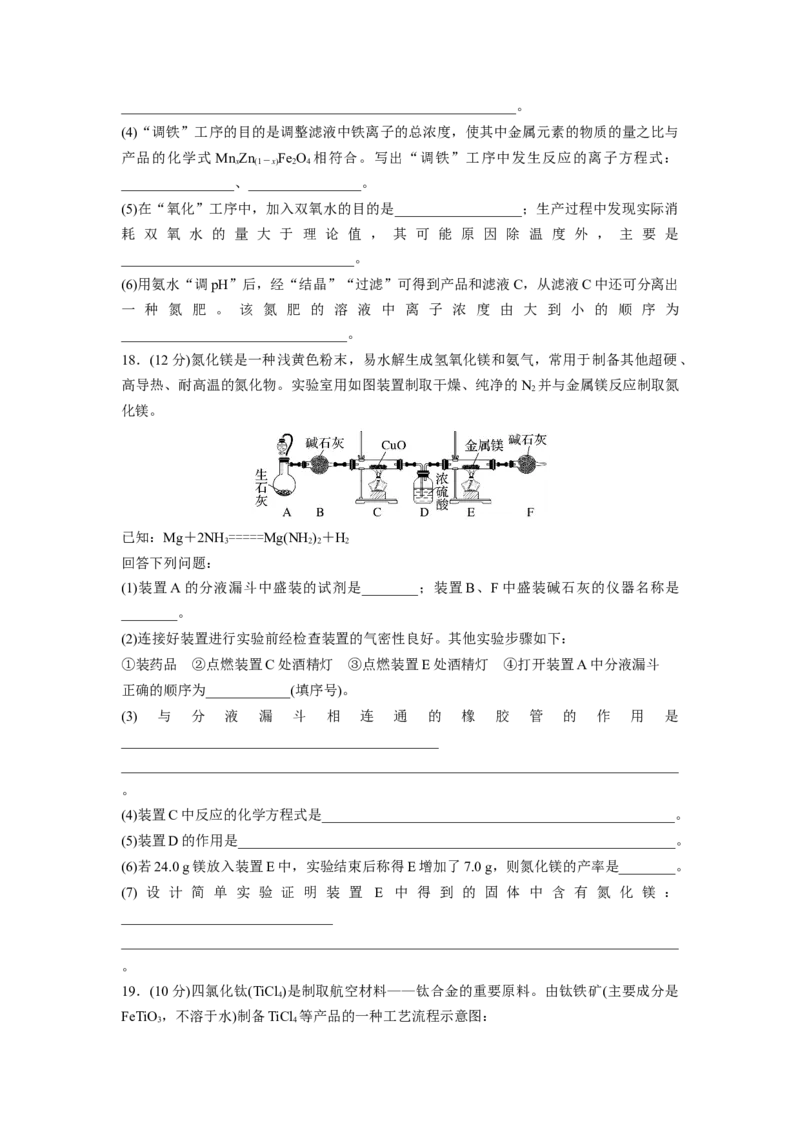
18.(12分)氮化镁是一种浅黄色粉末,易水解生成氢氧化镁和氨气,常用于制备其他超硬、
高导热、耐高温的氮化物。实验室用如图装置制取干燥、纯净的N 并与金属镁反应制取氮
2
化镁。
已知:Mg+2NH =====Mg(NH)+H
3 2 2 2
回答下列问题:
(1)装置A的分液漏斗中盛装的试剂是________;装置B、F中盛装碱石灰的仪器名称是
________。
(2)连接好装置进行实验前经检查装置的气密性良好。其他实验步骤如下:
①装药品 ②点燃装置C处酒精灯 ③点燃装置E处酒精灯 ④打开装置A中分液漏斗
正确的顺序为____________(填序号)。
(3) 与 分 液 漏 斗 相 连 通 的 橡 胶 管 的 作 用 是
_____________________________________________
_______________________________________________________________________________
。
(4)装置C中反应的化学方程式是__________________________________________________。
(5)装置D的作用是______________________________________________________________。
(6)若24.0 g镁放入装置E中,实验结束后称得E增加了7.0 g,则氮化镁的产率是________。
(7) 设 计 简 单 实 验 证 明 装 置 E 中 得 到 的 固 体 中 含 有 氮 化 镁 :
______________________________
_______________________________________________________________________________
。
19.(10分)四氯化钛(TiCl )是制取航空材料——钛合金的重要原料。由钛铁矿(主要成分是
4
FeTiO,不溶于水)制备TiCl 等产品的一种工艺流程示意图:
3 4回答下列问题:
(1)“ 酸 浸 ” 时 需 要 将 钛 铁 矿 粉 碎 , 其 目 的 是
_________________________________________。
(2)浸出液呈强酸性,含有TiO2+、Fe2+及少量Fe3+、Al3+等离子,则生成TiO2+的离子方程
式是______________________________________________________________________。
(3)“反应”时需加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发
生:
2Fe3++Fe===3Fe2+
2TiO2+(无色)+Fe+4H+===2Ti3+(紫色)+Fe2++2HO
2
Ti3+(紫色)+Fe3++HO===TiO2+(无色)+Fe2++2H+
2
加入铁屑的作用是______________。
(4)通过控制条件,可以使过程①中生成的TiO·nHO形成一种液态分散系,用一束光照射
2 2
该分散系能够产生丁达尔效应,则分散质颗粒直径的范围是________________________。
(5)过程①制得的固体TiO·nHO需用过量酸清洗以除去其中的Fe(OH) 杂质,检验Fe(OH)
2 2 3 3
杂质除净的实验方法是___________________________________________________________。
(6)过程③生成的废气中含有CO,则TiO 和焦炭、氯气在高温下发生反应的化学方程式是
2
________________________________________________________________________。
(7)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程
中存在的不足之处是__________________________(只要求写出一项)。
(8)依据下表中信息,可采用________的方法精制含少量SiCl 杂质的TiCl 。
4 4
TiCl SiCl
4 4
熔点/℃ -25.0 -68.8
沸点/℃ 136.4 57.6
20.(13分)磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、CaO以及少量
2 2 2 3
的Fe O。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
回答下列问题:
(1)“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、 MgO、CaO、 Fe O 转化为相应的
2 2 2 3 2 3
硫 酸 盐 。 写 出 Al O 转 化 为 NH Al(SO ) 的 化 学 方 程 式 :
2 3 4 4 2
__________________________________。
(2)“水浸”后“滤液”的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,依
次析出的金属离子是__________________________。
(3)“母液①”中Mg2+浓度为______________mol·L-1。
(4)“水浸渣”在 160 ℃“酸溶”,最适合的酸是________,“酸溶渣” 的成分是
_________。
(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO·xHO沉淀,该反应的离子方
2 2
程式是______________________________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得____________, 循环利用。
单元检测五 金属及其化合物答案解析
1.答案 D
解析 自然界中的金属绝大多数以化合物的形式存在,只有极少数化学性质非常稳定的金
属以单质形式存在,自然界中金属的存在形态取决于金属的化学活动性,故D正确。
2.答案 A
解析 铜与浓硝酸反应生成NO ,过量的铜可与变稀的硝酸反应生成NO,故A正确;制
2
红色涂料的物质的主要成分是氧化铁,Fe在O 中的燃烧产物是四氧化三铁,故B错误;
2
Al是活动性较强的金属,用电解冶炼法得到,铜用热还原法得到,故 C错误;Fe2+、SO
2
都能使酸性高锰酸钾溶液褪色,都表现出还原性,故D错误。
3.答案 D
解析 A项,根据水的质量可以计算得到氧元素的质量,再根据黑色粉末的质量得到铁元素的质量,进而确定黑色粉末的成分;B项,灼烧至质量不变所得粉末是氧化铁,依据氧
化铁的质量可以计算得到铁元素的质量,再根据黑色粉末的质量得到氧元素的质量,进而
确定黑色粉末的成分;C项,剩余固体是铁,根据黑色粉末的质量得到氧元素的质量,进
而确定黑色粉末的成分;D项,反应前后都是固体,而且固体质量不变,不能确定该黑色
粉末的成分。
4.答案 D
解析 铜片放入废液中充分反应,铜片质量减少了0.256 g,说明废液中含有Fe3+,结合反
应2FeCl +Cu===2FeCl +CuCl 可知,废液中一定含有Fe2+、Fe3+、Cu2+、Cl-,故A正确;
3 2 2
由 2FeCl +Cu===2FeCl +CuCl 可知,废液中 c(Fe2+)=2c(Cu2+),c(Fe2+)∶c(Cu2+)=
3 2 2
2∶1,故B正确;废液中加入足量的AgNO 溶液,生成沉淀8.61 g,沉淀为AgCl,其物质
3
的量为0.06 mol,废液中c(Cl-)==6 mol·L-1,废液放入铜片充分反应,铜片质量减少了
0.256 g,物质的量为=0.004 mol,设10 mL废液中Fe3+为n mol,则
2FeCl +Cu===2FeCl +CuCl
3 2 2
2 1
n mol 0.004 mol
故n=0.008 mol,所以废液中c(Fe3+)==0.8 mol·L-1,又c(Fe2+)=2c(Cu2+),根据电荷守恒,
废液中:3c(Fe3+)+2c(Fe2+)+2c(Cu2+)=c(Cl-),故3×0.8 mol·L-1+2c(Fe2+)+c(Fe2+)=6
mol·L-1,解得c(Fe2+)=1.2 mol·L-1,故废液中c(Fe2+)∶c(Fe3+)=1.2 mol·L-1∶0.8 mol·
L-1=3∶2,故C正确、D错误。
5.答案 A
解析 硅酸钠是能溶于水的硅酸盐,故A错误;镁在空气中燃烧时,与氧气和二氧化碳反
应生成氧化镁,与氮气反应生成氮化镁,故B正确;钠具有强还原性,能与冷水反应生成
氢氧化钠和氢气,故C正确;浓硫酸和浓硝酸具有强氧化性,常温下铝在浓硝酸和浓硫酸
中会发生钝化,阻碍反应的继续进行,故D正确。
6.答案 B
解析 A项,同素异形体是指同种元素组成的不同单质,Fe O 与Fe O 是铁的不同氧化物,
2 3 3 4
不互为同素异形体,错误;B项,电解熔融氧化铝冶炼Al,还原剂还原Fe、Cu的化合物
冶炼金属Fe、Cu,正确;C项,盐酸的酸性大于亚硫酸,SO 与BaCl 溶液不反应,错误;
2 2
D项,氧化铁不溶于水,无法证明溶液中是否含有铁离子,错误。
7.答案 C
解析 Na露置在空气中被空气中的 O 氧化产生NaO,NaO与HO反应产生NaOH,
2 2 2 2
NaOH溶液吸收CO 生成NaCO,因此Na露置在空气中最终变为NaCO,A错误;Mg是
2 2 3 2 3
活泼金属,要用电解熔融MgCl 的方法冶炼,不能采用H 还原MgO的方法,B错误;擦
2 2
去氧化膜的Al条在酒精灯上加热,Al与空气中的O 反应产生Al O ,由于Al O 的熔点高
2 2 3 2 3达2 050 ℃,因此铝熔化后被表面熔点高的氧化膜包裹,故铝熔化但不滴落,C正确;向
Fe (SO ) 溶液中加入过量Zn粉,首先发生反应:Fe (SO ) +Zn===2FeSO +ZnSO ,然后
2 4 3 2 4 3 4 4
发生反应:Zn+FeSO ===ZnSO +Fe,故Fe (SO ) 溶液最终被过量Zn粉还原,产生Fe单
4 4 2 4 3
质,D错误。
8.答案 A
解析 无水状态下NaO 比NaO更稳定,NaO在空气中加热可以生成更稳定的NaO ,A
2 2 2 2 2 2
正确;Mg加入到FeCl 溶液中,Mg具有较强的还原性,先与Fe3+反应,生成Mg2+和Fe2
3
+,若Mg过量,Mg与Fe2+继续反应生成Mg2+和Fe,但由于反应中FeCl 过量,Mg已消
3
耗完,所以无Mg和Fe2+反应,所以不会生成Fe,B错误;FeS 在沸腾炉中与O 发生的反
2 2
应为4FeS+11O=====2Fe O+8SO ,产物主要是SO 而不是SO ,C错误;HO 溶液中加
2 2 2 3 2 2 3 2 2
入少量MnO 粉末生成HO和O,化学方程式为2HO=====2HO+O↑,D错误。
2 2 2 2 2 2 2
9.答案 D
解析 氯化钠为强碱强酸盐,所以蒸干得到的还是 NaCl,A错误;常温下铁在浓硝酸中会
发生钝化,无法持续反应,C错误;因为电离出H+的能力苯酚强于HCO,则在苯酚浊液
中加入碳酸钠生成可溶于水的苯酚钠和碳酸氢钠,溶液变澄清,D正确。
10.答案 B
解析 铁、铜和锌的氧化物在足量的CO中加热,最终得到的固体是相应元素的单质,所
以要求固体的质量,若能求出氧化物中氧元素的总质量,在氧化物总质量的基础上扣除即
可。上述氧化物与硫酸反应过程不涉及变价,实质是复分解反应,可以简单表示为 MO+
x
2xH+===M2x++xHO,其中x不一定为整数。因此,消耗的H+的物质的量是金属氧化物中
2
O元素的两倍,所以该金属氧化物的混合物中:n(O)==0.1 mol,所以金属元素总质量为
(a-1.6)g,B项正确。
11.答案 C
解析 由题意知,三种物质完全反应后压强为零,说明最终剩余固体为 NaCO 和NaOH。
2 3
根据元素守恒和质量守恒可得出总反应的化学方程式:2CH +O +6NaO=====2NaCO
4 2 2 2 2 3
+8NaOH,即C项正确。
12.答案 B
解析 铝在空气中与O 反应,生成致密的氧化物薄膜,Al本身易于锈蚀,A错误;由于铝
2
具有强还原性,可利用铝热反应来冶炼难熔金属,B正确;铜与浓硫酸常温下不反应,C
错误;铝的导电性能比铜差,但价格相对低廉且密度较小,故常用铝制造电线、电缆,D
错误。
13.答案 A
解析 A项,含镁为5%时,金属铝的含量最低,5.4 g合金中铝的质量为5.4×(1-5%) g,
则根据反应:2Al+2NaOH+2HO===2NaAlO +3H↑可知,Al~NaOH,∶
2 2 2(V×10-3×2.0)=1∶1,解得V=95,因此V≥95,错误;B项,方案一中金属铝与氢氧化
钠溶液反应,剩余固体为镁;测定剩余固体质量时,过滤后未洗涤固体就干燥、称量,相
当于镁的质量偏大,则镁的质量分数偏高,正确;C项,Mg、Al均与氧气反应生成金属氧
化物,则还需测定生成物的质量,根据质量守恒,列方程可以求出金属镁的质量,进而求
出镁的质量分数,正确;D项,金属镁能够与氮气反应生成氮化镁,金属镁的质量偏大,
测定结果偏高,正确。
14.答案 C
解析 装置①为启普发生器,加入试剂之前必须检查装置气密性,A项错误;装置①中产
生的H 会混有氯化氢、水蒸气,通过装置③可以除去这两种杂质,所以仪器接口的连接顺
2
序为a→d→e→f→g(g→f)→b→c,B项错误;为了防止金属钙与空气中的物质发生反应,
需要在加热前通入氢气排尽装置④中的空气,通过检查氢气纯度判断空气是否排尽,C项
正确;装置③的作用是除去氢气中混有的氯化氢、水蒸气,D项错误。
15.答案 A
解析 分析整个反应过程可知仅有两种元素的化合价发生变化,即 Cu→Cu2+,NO→NO,
51.2 g Cu的物质的量为0.8 mol,共失去电子0.8 mol×2=1.6 mol,由得失电子守恒可知
NO→NO得到1.6 mol电子,故产物中NaNO 的物质的量为0.8 mol,由Na原子守恒可得
2
另一种产物NaNO 的物质的量为0.2 mol,A正确;常温下,Cu能与浓硝酸反应,B错误;
3
部分NO 会转化为NO ,且NO 、NO 在标准状况下不是气体,C错误;反应过程中生成
2 2 4 2 2 4
的Cu(NO ) 是氧化产物,不是还原产物,D错误。
3 2
16.答案 (1)用平行光照射两种分散系,Fe(OH) 胶体会产生一条光亮的通路,而FeCl 溶
3 3
液不能
(2)Cu+2Fe3+===Cu2++2Fe2+
(3)取适量溶液于试管中,滴入铁氰化钾溶液,若生成蓝色沉淀,则含有Fe2+
(4)①Fe、Cu
②Fe+2H+===Fe2++H↑
2
③2Fe2++Cl===2Fe3++2Cl-
2
17.答案 (1)+3 (2)
(3)MnO(OH)+Fe2++3H+===Mn2++Fe3++2HO (4)Fe+2Fe3+===3Fe2+ Fe+2H+===Fe2
2
++H ↑ (5)把Fe2+氧化为Fe3+ 生成的 Fe3+催化了双氧水的分解
2
(6)c(NH)>c(SO)>c(H+ )>c(OH- )
解析 (1)实验室用二氧化锰制取氯气时还原产物为氯化锰,其中锰元素的化合价为+2。
则MnZn Fe O 中锰元素的化合价为+2价、Zn为+2价、O为-2价,根据化合物中化
x (1-x) 2 4
合价的代数和为0,铁元素的化合价为+3。(2) 碱性锌锰电池用水浸取,过滤后的滤液A
中的溶质是KOH,电子式为 。(4)“调铁”工序之前的滤液中含有Fe3+、过量的硫酸,因此发生反应的离子方程式有 Fe+2Fe3+===3Fe2+、Fe+2H+===Fe2++H↑。
2
(6)用氨水“调pH”后,经“结晶”“过滤”可得到产品和滤液C,从滤液C中分离出一种
氮肥为硫酸铵[(NH )SO ],铵根离子水解,导致溶液显酸性,溶液中离子浓度由大到小的
4 2 4
顺序为c(NH)>c(SO)>c(H+ )>c(OH- )。
18.答案 (1)浓氨水 (球形)干燥管 (2)①④②③ (3)平衡分液漏斗内外压强,便于液体
顺利流下 (4)3CuO+2NH =====3Cu+N +3HO (5)吸收氨气并干燥氮气 (6)75.0% (7)
3 2 2
取所得固体放入试管中,滴入少量蒸馏水,用镊子夹取一块湿润的红色石蕊试纸接近试管
口,试纸变蓝色,证明含有氮化镁
解析 (1)装置A是用生石灰和浓氨水制备NH 的装置。
3
(2)装置内含有空气,对装置E反应会有影响,所以要先点燃C处酒精灯,利用产生的N
2
排尽装置中的空气后,再点燃E处酒精灯。
(5)装置E中镁和氮气反应,NH 和水蒸气会干扰实验,用装置D除去。
3
(7)根据氮化镁水解生成氢氧化镁沉淀与氨气,氨气可使湿润的红色石蕊试纸变蓝,据此设
计实验证明有氮化镁生成。
19.答案 (1)增大接触面积,加快反应速率
(2)FeTiO+4H+===TiO2++Fe2++2HO
3 2
(3)将Fe3+还原为Fe2+
(4)10-9~10-7m
(5)用试管取少量最后一次洗涤液,加入KSCN溶液,若溶液未变为红色,则说明Fe(OH)
3
杂质已除净
(6)TiO+2C+2Cl=====TiCl +2CO
2 2 4
(7)过程③中产生的CO和残留的Cl 有毒,污染空气
2
(8)蒸馏
20.答案 (1) Al O +4(NH )SO =====2NH Al(SO ) +6NH ↑+3HO↑ (2)Fe3+、Al3+、
2 3 4 2 4 4 4 2 3 2
Mg2+ (3)1.0×10-6 (4)硫酸 SiO 、CaSO (5)TiO2++(x+1)H O=====TiO·xHO↓+2H
2 4 2 2 2
+ (6)(NH )SO
4 2 4
解析 (1)氧化铝转化为硫酸铝铵发生的反应为氧化铝、硫酸铵在高温条件下反应生成硫酸
铝铵、氨气和水,反应的化学方程式为Al O +4(NH )SO =====2NH Al(SO ) +6NH ↑+
2 3 4 2 4 4 4 2 3
3HO↑。
2
(2)由题给开始沉淀和完全沉淀的pH可知,将pH约为2.0的滤液加入氨水调节溶液pH为
11.6时,铁离子首先沉淀,然后是铝离子、镁离子,钙离子没有沉淀。
(3)由镁离子完全沉淀时,溶液pH为11.1可知,氢氧化镁的溶度积为1×10-5×(1×10-2.9)2
=1×10-10.8,当溶液pH为11.6时,溶液中镁离子的浓度为mol·L-1=1×10-6 mol·L-1。
(4)增大溶液中硫酸根离子的浓度,有利于使微溶的硫酸钙转化为沉淀,为了使微溶的硫酸钙完全沉淀,减少TiOSO 溶液中含有的硫酸钙的量,应加入浓硫酸加热到 160 ℃酸溶;
4
由分析可知,二氧化硅和硫酸钙与硫酸不反应,则酸溶渣的主要成分为二氧化硅和硫酸钙。
(5)酸溶后将TiOSO 溶液适当稀释并加热,能使TiOSO 完全水解生成TiO·xHO沉淀和硫
4 4 2 2
酸,反应的离子方程式为TiO2++(x+1)H O=====TiO·xHO↓+2H+。
2 2 2
(6)由分析可知,尾气为氨气,母液①为硫酸铵、母液②为硫酸,将母液①和母液②混合后
吸收氨气得到硫酸铵溶液,可以循环使用。