文档内容
专项特训 9 分子结构与性质简答
类型一 和共价键有关的问题
1.Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或
三键。从原子结构角度分析,原因是______________________________________________。
答案 Ge原子半径大,原子间形成的σ键较长,p-p轨道肩并肩重叠程度很小或几乎不能重
叠,难以形成π键,不易形成双键或三键
2.碳及其化合物广泛存在于自然界中,碳在形成化合物时,其键型以共价键为主,原因是
_____________________________________________________________________________。
答案 C原子有4个价电子且半径较小,难以通过得失电子达到稳定结构
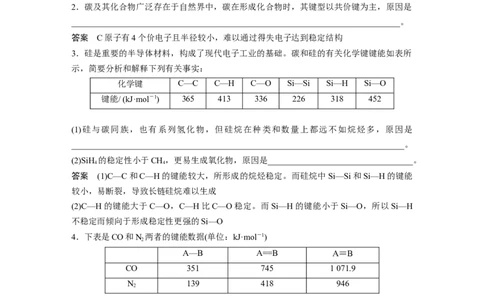
3.硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所
示,简要分析和解释下列有关事实:
化学键 C—C C—H C—O Si—Si Si—H Si—O
键能/ (kJ·mol-1) 365 413 336 226 318 452
(1)硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是
______________________________________________________________________________。
(2)SiH 的稳定性小于CH,更易生成氧化物,原因是__________________________________。
4 4
答案 (1)C—C和C—H的键能较大,所形成的烷烃稳定。而硅烷中Si—Si和Si—H的键能
较小,易断裂,导致长链硅烷难以生成
(2)C—H的键能大于C—O,C—H比C—O稳定。而Si—H的键能小于Si—O,所以Si—H
不稳定而倾向于形成稳定性更强的Si—O
4.下表是CO和N 两者的键能数据(单位:kJ·mol-1)
2
A—B A==B A≡B
CO 351 745 1 071.9
N 139 418 946
2
结合数据说明CO比N 活泼的原因:_________________________________________
2
________________________________________________________________________。
答案 CO中第一个π键的键能是326.9 kJ·mol-1,N 中第一个π键的键能是528 kJ·mol-1,
2
则CO的第一个π键比N 的第一个π键更容易断裂
2
5.CH 的键角大于NH 的原因为__________________________________________________
4 3
_______________________________________________________________________________
。
答案 CH、NH 的中心原子均为sp3杂化,NH 分子中有未成键的孤电子对,对成键电子对
4 3 3斥力较大,键角较小
6.高温陶瓷材料Si N 晶体中键角N—Si—N______Si—N—Si(填“>”“<”或“=”),原
3 4
因是________________________________________________________________________
____________________________________________________________________________。
答案 > N原子上有孤电子对,由于孤电子对与成键电子对的排斥力更大,使得 Si—N—
Si键角较小
7.两种三角锥形气态氢化物膦(PH )和氨(NH )的键角分别为93.6°和107°,试分析PH 的键
3 3 3
角小于NH 的原因:____________________________________________________________。
3
答案 N原子的电负性强于P原子,对成键电子对吸引能力更强,成键电子对离中心原子更
近,成键电子对之间距离更小,排斥力更大致使键角更大,因而PH 的键角小于NH
3 3
8.NF 的键角______NH 的键角(填“>”“<”或“=”),理由是_____________________。
3 3
答案 < F的电负性比H大,NF 中N周围电子云密度减小,成键电子对之间的排斥力较
3
小
9.比较NH 和[Cu(NH )]2+中H—N—H键角的大小:NH ______[Cu(NH )]2+(填“>”或
3 3 4 3 3 4
“<”),并说明理由:__________________________________________________________。
答案 < NH 提供孤电子对与Cu2+形成配位键后,N—H成键电子对受到的排斥力减小
3
类型二 和氢键有关的问题
10.乙二胺分子(H N—CH —CH—NH )中氮原子杂化类型为sp3,乙二胺和三甲胺[N(CH )]
2 2 2 2 3 3
均属于胺,但乙二胺比三甲胺的沸点高得多,原因是__________________________________。
答案 乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键
11.丙酸钠(CHCHCOONa)和氨基乙酸钠均能水解,水解产物有丙酸(CHCHCOOH)和氨
3 2 3 2
基乙酸(H NCH COOH),常温下丙酸为液体,而氨基乙酸为固体,主要原因是
2 2
________________________________________________________________________。
答案 羧基的存在使丙酸形成分子间氢键,而氨基乙酸分子中,羧基和氨基均能形成分子间
氢键
12.硝酸和尿素( )的相对分子质量接近,但常温下硝酸为挥发性液体,尿素
为固体,请解释原因:___________________________________________________________。
答案 尿素分子间存在氢键,使其熔、沸点升高,而硝酸分子内存在氢键,使其熔、沸点降
低
13.氨(NH )的熔、沸点比联氨(H N—NH)低的主要原因:___________________________。
3 2 2
答案 联氨分子间形成的氢键数目多于氨分子间形成的氢键数目
14.苯胺( )与甲苯( )的相对分子质量相近,但苯胺的熔点(-5.9
℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-95.0 ℃)、沸点(110.6 ℃),原因是___________。
答案 苯胺分子之间存在氢键