文档内容
第 19 讲 卤素的性质及提取
复习目标 1.掌握卤素的性质及X-的检验。2.掌握溴、碘单质的提取。
考点一 卤素的性质及 X-的检验
1.溴、碘单质物理性质比较
性质 Br I
2 2
颜色 深红棕色 紫黑色
状态 液体 固体
①在水中溶解度不大
溶解性
②易溶于有机溶剂
①易升华
特性 易挥发、有毒
②使淀粉溶液变蓝
2.氯、溴、碘单质化学性质比较X+HO HX + HXO
2 2
与水反应
氯、溴、碘与水反应由易到难
与碱(NaOH) 2NaOH+X=== NaX + NaXO + H O
2 2
①Cl>Br >I,还原性:Cl-<Br-<I-;
2 2 2
氧化性 ②氯、溴、碘与氢气化合由易到难;
③I 与Fe只生成FeI,其他卤素单质可将Fe氧化为+3价
2 2
3.氟的特殊性
(1)氟无正化合价。
(2)F 能与水反应放出O,故F 不能从其他卤化物的水溶液中将卤素单质置换出来。
2 2 2
(3)在HX中,HF的熔、沸点最高,氢氟酸是弱酸,能腐蚀玻璃。
4.卤素离子的检验方法
(1)AgNO 溶液——沉淀法
3
未知液――――――→生成
(2)置换——萃取法
未知液――――――――→
―――――――――――――→
有机层呈
(3)氧化——淀粉法检验I-
未知液―――――――――――――――→ ―――→蓝色溶液,表明有I-
1.卤素气态氢化物的水溶液都是强酸溶液( )
2.类比Fe与Cl 的反应判断Fe与I 反应时生成FeI( )
2 2 3
3.浓HSO 能干燥HCl,所以浓硫酸也能干燥HBr( )
2 4
4.加碘盐能使淀粉变蓝( )
5.清洗碘升华实验所用试管的操作是先用酒精清洗,再用水清洗( )
6.液溴易挥发,在存放液溴的试剂瓶中应加水封( )
7.碘易溶于酒精,所以可用酒精将碘萃取出来( )
8.用加热的方法可将NaHCO 中混有的少量碘除去( )
3
9.氟气跟氯化钠溶液反应,一定有氟化氢和氧气生成( )
答案 1.× 2.× 3.× 4.× 5.√ 6.√ 7.× 8.× 9.√
一、卤素离子的检验
1.下列叙述正确的是( )A.氯水久置过程中,氯水的氧化性增强,酸性减弱
B.用硝酸酸化的AgNO 溶液能一次鉴别NaCl、NaBr、KI三种失去标签的溶液
3
C.向某溶液中加入CCl ,振荡、静置后,CCl 层显紫红色,证明原溶液中存在I-
4 4
D.某浅黄色的溴水,加CCl 振荡、静置后,上层显橙红色
4
答案 B
2.鉴别NaCl溶液、NaBr溶液、NaI溶液可以选用的试剂是( )
①碘水、淀粉溶液 ②氯水、CCl ③溴水、苯 ④硝酸、AgNO 溶液 ⑤氯水、苯
4 3
⑥CCl 、淀粉溶液
4
A.①②④ B.②③⑥
C.②④⑤ D.④⑤⑥
答案 C
二、拟卤素和卤素互化物
3.氰[(CN) ]的结构简式为N≡C—C≡N,其化学性质与卤素(X )很相似,化学上称之为拟
2 2
卤素,其氧化性介于Br 和I 之间。
2 2
(1)写出(CN) 的电子式:_________________________________________________。
2
(2)写出(CN) 在常温下与烧碱溶液反应的化学方程式:_______________________。
2
(3)在KBr、KI、KCN的混合溶液中通入少量氯气,发生反应的离子方程式为___
______________________________________________________________________。
答案 (1)
(2)(CN) +2NaOH===NaCN+NaCNO+HO
2 2
(3)2I-+Cl===I+2Cl-
2 2
4.一氯化碘(ICl)、三氯化碘(ICl )是卤素互化物,它们的性质与卤素单质相似。
3
(1)ICl 与水反应的产物可能为___________________________(填化学式)。
3
(2)ICl在常温下与烧碱溶液反应的离子方程式为
________________________________________________________________________,
该反应是否是氧化还原反应?__________(填“是”或“否”)。
答案 (1)HCl、HIO
2
(2)ICl+2OH-===Cl-+IO-+HO 否
2
三、卤素单质氧化性的实验探究
5.为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,
气密性已检查)。实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是________。
(2)验证氯气的氧化性强于碘的实验现象是___________________________________
________________________________________________________________________。
(3)B中溶液发生反应的离子方程式是_______________________________________
________________________________________________________________________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是_________________________。
(5)过程Ⅲ实验的目的是___________________________________________________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,__________,得电子
能力逐渐减弱。
答案 (1) (2)湿润的淀粉-KI试纸变蓝 (3)Cl +2Br-===Br +2Cl- (4)打开活
2 2
塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡,静置后CCl 层变为紫红色
4
(5)确认C的黄色溶液中无Cl,排除Cl 对溴置换碘实验的干扰 (6)原子半径逐渐增大
2 2
解析 A中滴加浓盐酸后,发生反应:2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+
4 2 2
8HO,生成黄绿色气体Cl ,在A、B、C中分别发生反应:Cl +2KI===2KCl+I 、Cl +
2 2 2 2 2
2NaBr===2NaCl+Br 、Cl+2NaBr===2NaCl+Br ,由于B、C中生成了Br 而使溶液变为黄
2 2 2 2
色,打开活塞b,C中生成的Br 在D中发生反应:Br +2KI===2KBr+I 。实验过程Ⅲ,当
2 2 2
B中黄色溶液继续通入过量Cl 时,溶液变为红棕色,以此为对照,说明 C中黄色溶液无
2
Cl,从而排除Cl 对溴置换碘实验的干扰。
2 2
考点二 卤素的提取
1.氯的提取——氯碱工业
电解饱和食盐水的化学方程式为2NaCl+2HO=====2NaOH+H↑+Cl↑。
2 2 2
2.海水提取溴
(1)工艺流程(2)发生反应的化学方程式
①2NaBr+Cl===Br +2NaCl;
2 2
②Br +SO +2HO===2HBr+HSO ;
2 2 2 2 4
③2HBr+Cl===2HCl+Br 。
2 2
3.海带中提取碘
(1)工艺流程
(2)发生反应的离子方程式:Cl+2I-===I+2Cl-。
2 2
1.为了从海带浸取液中提取碘,某同学设计了如图实验方案,下列说法正确的是( )
A.①中反应的离子方程式:2I-+HO===I+2OH-
2 2 2
B.②中分液时含I 的CCl 溶液从分液漏斗上口倒出
2 4
C.③中得到的上层溶液中含有I-
D.操作Z的名称是加热
答案 C
解析 该反应为酸性环境,①中反应的离子方程式:2I-+2H++HO===I +2HO,故A错
2 2 2 2
误;四氯化碳的密度比水的大,在下层,②中分液时含I 的CCl 溶液从分液漏斗下口放出,
2 4
故B错误;操作Z的名称是过滤,故D错误。
2.从淡化海水中提取溴的流程如下:下列有关说法不正确的是( )
A.X试剂可用NaSO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:2Br-+Cl===2Cl-+Br
2 2
C.工业上每获得1 mol Br ,需要消耗Cl 44.8 L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏
答案 C
解析 NaSO +Br +HO===NaSO +2HBr,A正确;步骤Ⅲ根据氯的非金属性比溴的强,
2 3 2 2 2 4
利用置换反应制取Br ,B正确;步骤Ⅰ和步骤Ⅲ均使用到Cl ,故制取1 mol Br 消耗2 mol
2 2 2
氯气,但未标明氯气所处的温度和压强,C错误;从浓溴水中提取溴,可利用有机溶剂(如
苯)萃取溴,然后分液得到溴的有机溶液,再经蒸馏可得纯净的溴,D正确。
3.某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br 的沸
2
点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:
请你参与分析讨论:
(1)图中仪器B的名称是__________。
(2)整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是____________。
(3)实验装置气密性良好,要达到提纯溴的目的,操作中控制温度计b为____________℃。
(4)C中溶液颜色为 __________,为除去该产物中残留的Cl ,可向其中加入NaBr溶液,反
2
应的离子方程式为_______________________________________________________。
答案 (1)(直形)冷凝管 (2)Br 能腐蚀橡胶 (3)59 (4)深红棕色 2Br-+ Cl=== Br +2Cl-
2 2 2
4.用离子交换法从海带中提取碘是一种较为先进的制碘工艺应用技术。
已知:I+I-I;交换吸附原理:R—Cl+IR—I +Cl-。试回答下列问题:
2 3
(1)操作Ⅰ的正确图示为______________(填字母)。(2)在清液中加入HSO 和NaClO溶液后,溶液最终变为棕红色,该步骤中NaClO的量要适
2 4
中,请说明原因:____________________________________________________________。
(3)其中交换吸附装置如下图所示,交换柱内装有氯型阴离子交换树脂(用R—Cl表示),溶液
转化原理为:R—Cl+IR—I +Cl-,全部通过后,树脂颜色变为黑红色,再通过洗脱,
3
离心分离后得到粗碘。已知洗脱分两步进行:
第一步:取40 mL 8%~10%的NaOH溶液注入交换柱中。碱性洗脱原理为3R—I +6OH-
3
===3R—I+5I-+IO+3HO。往碱性洗脱液中滴加HSO 溶液,烧杯底部析出一层泥状粗碘。
2 2 4
第二步:取40 mL 10%的NaCl溶液注入上述交换柱中。氯化钠洗脱原理为 R—I+Cl-===R
—Cl+I-。再往氯化钠洗脱液中滴加HSO 溶液使之酸化,再滴加NaNO 溶液,溶液由无色
2 4 2
转变棕黑色浑浊。
①根据交换吸附及洗脱过程可知强碱性阴离子交换树脂也可以对 I-进行交换吸附,那实验
中将I-转化成I的原因可能是________________。
②往氯化钠洗脱液中滴加HSO 溶液使之酸化,再滴加NaNO 溶液反应的离子方程式:
2 4 2
____________________。
答案 (1)D
(2)因为交换吸附原理:R—Cl+IR—I +Cl-,最佳效果是都转化为I,因此NaClO量过
3
少,I-氧化不充分,过多会使溶液中I-含量太低,不利于生成I,不利于后续的交换吸附,
结果都会使产率下降
(3)①强碱性阴离子交换树脂对I的吸附能力远大于对I-的吸附能力 ②2NO+2I-+4H+===2NO↑+I+2HO
2 2
解析 (1)操作Ⅰ是将清液分离的操作,有机杂质不溶于水在清液的下方,所以使用倾倒的
方法就可以了。(2)根据吸附原理R—Cl+IR—I +Cl-,可知是I被吸附,在清液中加入
3
HSO 和NaClO溶液目的是将一部分碘离子氧化为碘单质,还要剩余一部分碘离子,所以
2 4
NaClO过多或者过少都会影响I的生成。
(3)①实验的目的是尽可能多的吸附碘元素,实验中将I-转化成I再进行吸附是为了提高吸
附的效率,应该是强碱性阴离子交换树脂对I的吸附能力远大于对I-的吸附能力。
②在酸性条件下 NO 具有氧化性,将 I-氧化成 I ,同时本身被还原为一氧化氮。
2
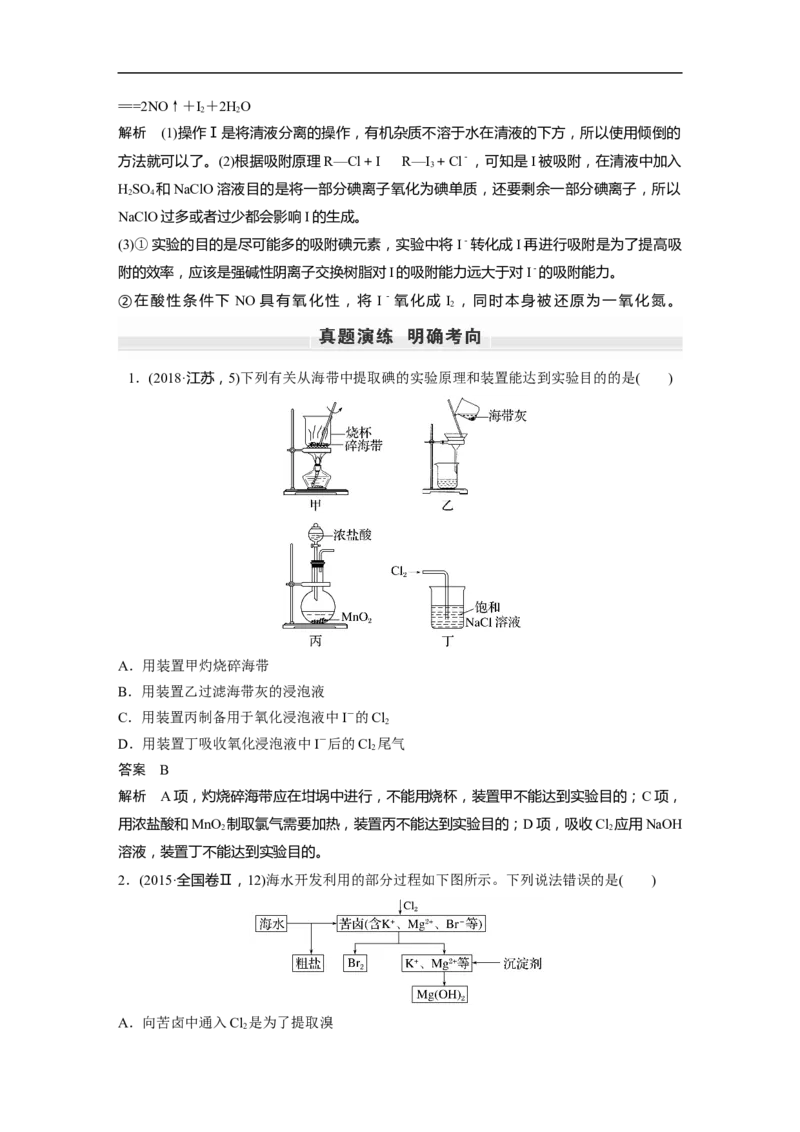
1.(2018·江苏,5)下列有关从海带中提取碘的实验原理和装置能达到实验目的的是( )
A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中I-的Cl
2
D.用装置丁吸收氧化浸泡液中I-后的Cl 尾气
2
答案 B
解析 A项,灼烧碎海带应在坩埚中进行,不能用烧杯,装置甲不能达到实验目的;C项,
用浓盐酸和MnO 制取氯气需要加热,装置丙不能达到实验目的;D项,吸收Cl 应用NaOH
2 2
溶液,装置丁不能达到实验目的。
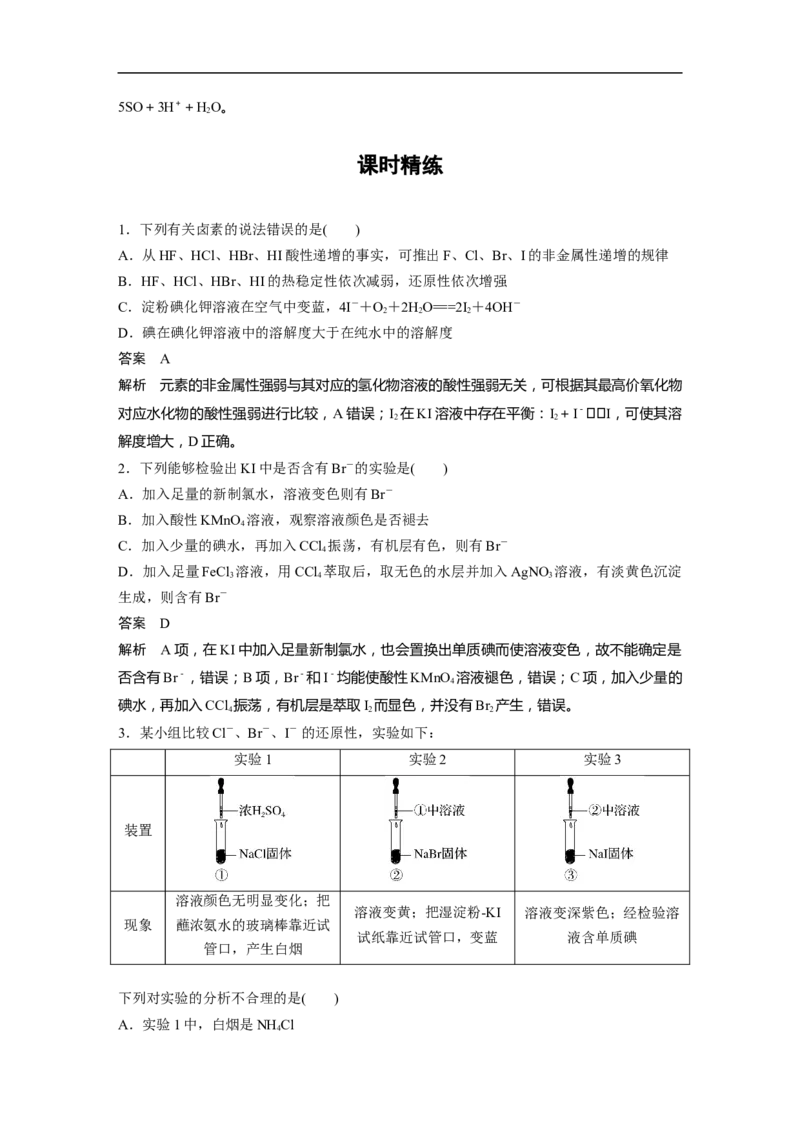
2.(2015·全国卷Ⅱ,12)海水开发利用的部分过程如下图所示。下列说法错误的是( )
A.向苦卤中通入Cl 是为了提取溴
2B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO 将其还原吸收
2
答案 C
解析 A项,向苦卤中通入Cl 时发生反应Cl +2Br-===2Cl-+Br ,故其是为了提取溴,
2 2 2
正确;B项,可将粗盐溶解、过滤除去难溶性杂质,然后向滤液中加入沉淀剂,过滤除去可
溶性杂质,最后重结晶可得精盐,正确;C项,工业生产常选用廉价的Ca(OH) 作为沉淀剂,
2
错误;D项,由于通入Cl 后所得溶液中Br 的浓度很小,因此利用Br 的挥发性,可先用热
2 2 2
空气和水蒸气吹出Br ,再用SO 将其还原为HBr进行富集,正确。
2 2
3.[2021·全国甲卷,26(1)(2)]碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等
方面。回答下列问题:
(1)I 的一种制备方法如图所示:
2
①加入Fe粉进行转化反应的离子方程式为______________________________________,生
成的沉淀与硝酸反应,生成____________后可循环使用。
②通入Cl 的过程中,若氧化产物只有一种,反应的化学方程式为__________________;
2
若反应物用量比=1.5时,氧化产物为______________;当>1.5后,单质碘的收率会降低,
原因是__________________________。
(2)以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO ,生成碘化物;
3 2 3 3
再向混合溶液中加入 NaIO 溶液,反应得到 I 。上述制备 I 的总反应的离子方程式为
3 2 2
________________________________________________________________________。
答案 (1)①2AgI+Fe===2Ag+Fe2++2I- AgNO ②FeI +Cl===I +FeCl I 、FeCl I
3 2 2 2 2 2 3 2
被过量的Cl 进一步氧化 (2)2IO+5HSO===I+5SO+3H++HO
2 2 2
解析 (1) ①由流程图可知悬浊液中含AgI,AgI可与Fe反应生成FeI 和Ag,FeI 易溶于水,
2 2
在离子方程式中能拆,故加入Fe粉进行转化反应的离子方程式为2AgI+Fe===2Ag+Fe2++
2I-,生成的银能与硝酸反应生成硝酸银参与循环中。
②通入Cl 的过程中,因I-还原性强于Fe2+,Cl 先氧化还原性强的I-,若氧化产物只有一
2 2
种,则该氧化产物只能是I ,故反应的化学方程式为FeI +Cl===I +FeCl ;若反应物用量
2 2 2 2 2
比=1.5时即Cl 过量,先氧化完全部I-再氧化Fe2+,恰好将全部I-和Fe2+氧化,故氧化产
2
物为I 、FeCl ;当>1.5即Cl 过量,多余的氯气会与生成的单质碘以及水继续发生氧化还原
2 3 2
反应,单质碘的收率会降低。
(2)制备I 的两个反应中I-为中间产物,总反应为IO与HSO发生氧化还原反应,生成SO和
2
I ,根据得失电子守恒、电荷守恒及元素守恒配平离子方程式即可得:2IO+5HSO===I +
2 25SO+3H++HO。
2
课时精练
1.下列有关卤素的说法错误的是( )
A.从HF、HCl、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规律
B.HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强
C.淀粉碘化钾溶液在空气中变蓝,4I-+O+2HO===2I+4OH-
2 2 2
D.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
答案 A
解析 元素的非金属性强弱与其对应的氢化物溶液的酸性强弱无关,可根据其最高价氧化物
对应水化物的酸性强弱进行比较,A错误;I 在KI溶液中存在平衡:I +I-I,可使其溶
2 2
解度增大,D正确。
2.下列能够检验出KI中是否含有Br-的实验是( )
A.加入足量的新制氯水,溶液变色则有Br-
B.加入酸性KMnO 溶液,观察溶液颜色是否褪去
4
C.加入少量的碘水,再加入CCl 振荡,有机层有色,则有Br-
4
D.加入足量FeCl 溶液,用CCl 萃取后,取无色的水层并加入AgNO 溶液,有淡黄色沉淀
3 4 3
生成,则含有Br-
答案 D
解析 A项,在KI中加入足量新制氯水,也会置换出单质碘而使溶液变色,故不能确定是
否含有Br-,错误;B项,Br-和I-均能使酸性KMnO 溶液褪色,错误;C项,加入少量的
4
碘水,再加入CCl 振荡,有机层是萃取I 而显色,并没有Br 产生,错误。
4 2 2
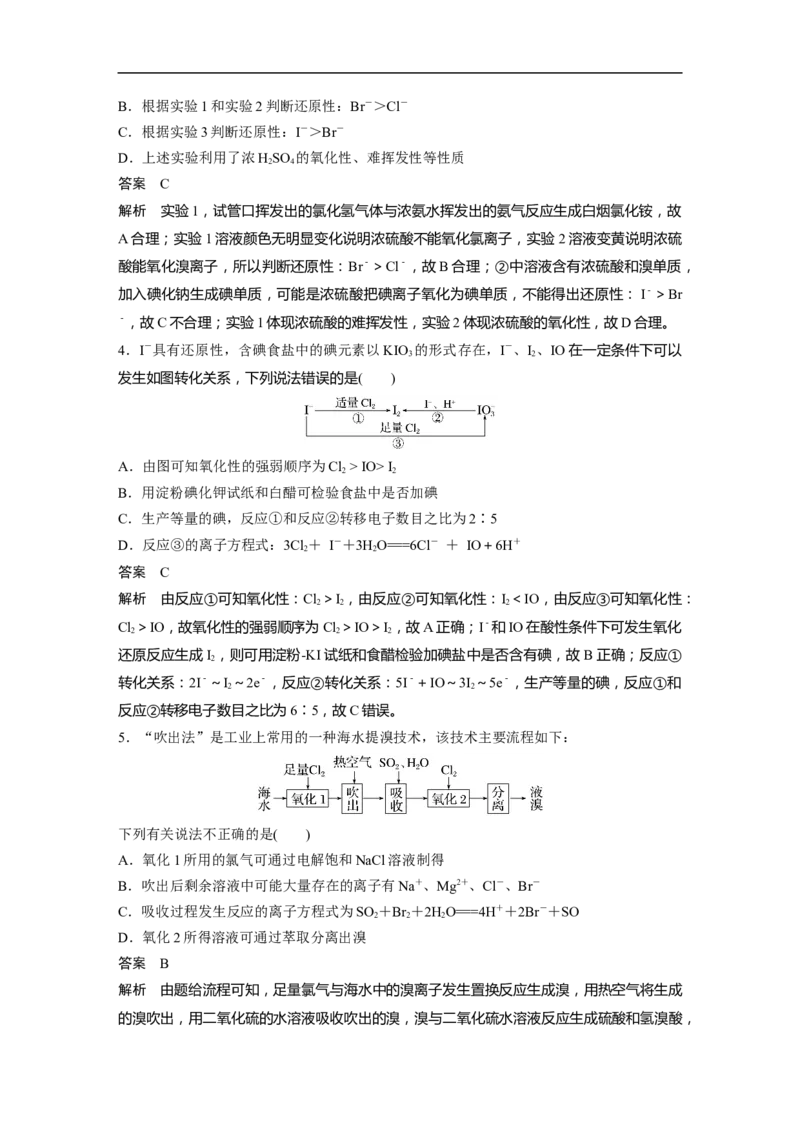
3.某小组比较Cl-、Br-、I- 的还原性,实验如下:
实验1 实验2 实验3
装置
溶液颜色无明显变化;把
溶液变黄;把湿淀粉-KI 溶液变深紫色;经检验溶
现象 蘸浓氨水的玻璃棒靠近试
试纸靠近试管口,变蓝 液含单质碘
管口,产生白烟
下列对实验的分析不合理的是( )
A.实验1中,白烟是NH Cl
4B.根据实验1和实验2判断还原性:Br->Cl-
C.根据实验3判断还原性:I->Br-
D.上述实验利用了浓HSO 的氧化性、难挥发性等性质
2 4
答案 C
解析 实验1,试管口挥发出的氯化氢气体与浓氨水挥发出的氨气反应生成白烟氯化铵,故
A合理;实验1溶液颜色无明显变化说明浓硫酸不能氧化氯离子,实验2溶液变黄说明浓硫
酸能氧化溴离子,所以判断还原性:Br->Cl-,故B合理;②中溶液含有浓硫酸和溴单质,
加入碘化钠生成碘单质,可能是浓硫酸把碘离子氧化为碘单质,不能得出还原性:I->Br
-,故C不合理;实验1体现浓硫酸的难挥发性,实验2体现浓硫酸的氧化性,故D合理。
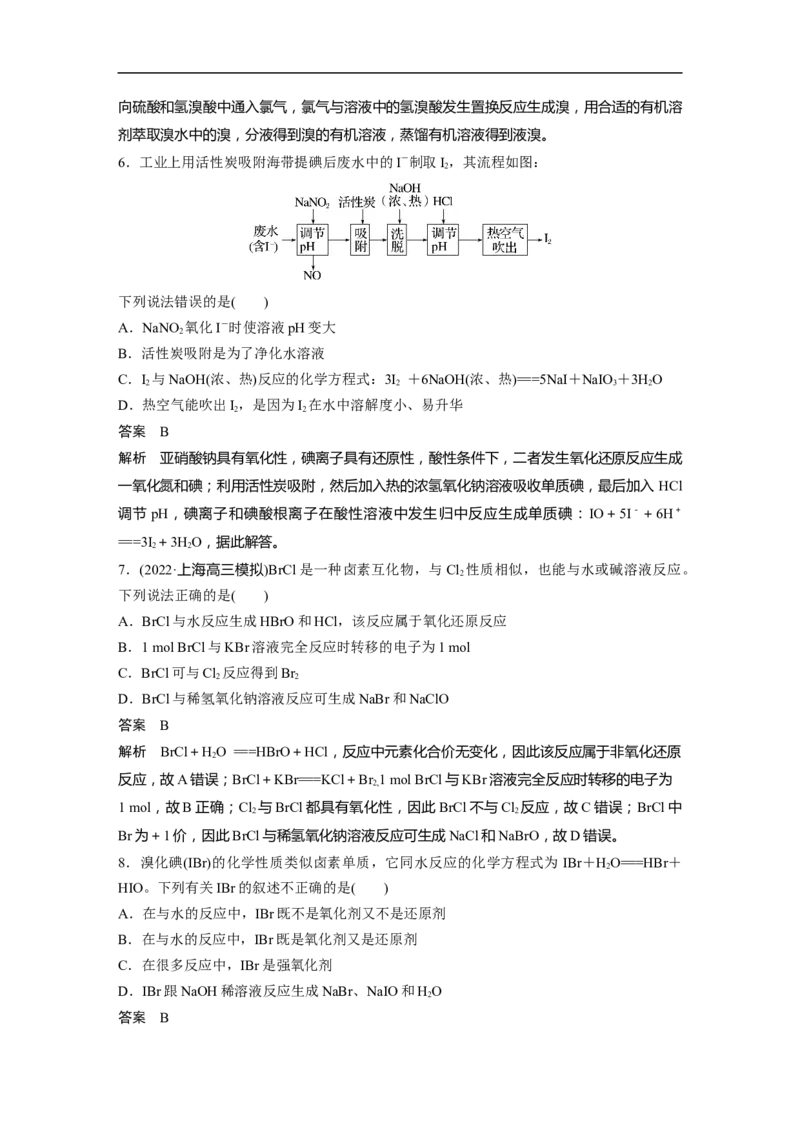
4.I-具有还原性,含碘食盐中的碘元素以KIO 的形式存在,I-、I 、IO在一定条件下可以
3 2
发生如图转化关系,下列说法错误的是( )
A.由图可知氧化性的强弱顺序为Cl > IO> I
2 2
B.用淀粉碘化钾试纸和白醋可检验食盐中是否加碘
C.生产等量的碘,反应①和反应②转移电子数目之比为2∶5
D.反应③的离子方程式:3Cl+ I-+3HO===6Cl- + IO+6H+
2 2
答案 C
解析 由反应①可知氧化性:Cl >I ,由反应②可知氧化性:I <IO,由反应③可知氧化性:
2 2 2
Cl>IO,故氧化性的强弱顺序为Cl>IO>I,故A正确;I-和IO在酸性条件下可发生氧化
2 2 2
还原反应生成I ,则可用淀粉-KI试纸和食醋检验加碘盐中是否含有碘,故 B正确;反应①
2
转化关系:2I-~I ~2e-,反应②转化关系:5I-+IO~3I ~5e-,生产等量的碘,反应①和
2 2
反应②转移电子数目之比为6∶5,故C错误。
5.“吹出法”是工业上常用的一种海水提溴技术,该技术主要流程如下:
下列有关说法不正确的是( )
A.氧化1所用的氯气可通过电解饱和NaCl溶液制得
B.吹出后剩余溶液中可能大量存在的离子有Na+、Mg2+、Cl-、Br-
C.吸收过程发生反应的离子方程式为SO +Br +2HO===4H++2Br-+SO
2 2 2
D.氧化2所得溶液可通过萃取分离出溴
答案 B
解析 由题给流程可知,足量氯气与海水中的溴离子发生置换反应生成溴,用热空气将生成
的溴吹出,用二氧化硫的水溶液吸收吹出的溴,溴与二氧化硫水溶液反应生成硫酸和氢溴酸,向硫酸和氢溴酸中通入氯气,氯气与溶液中的氢溴酸发生置换反应生成溴,用合适的有机溶
剂萃取溴水中的溴,分液得到溴的有机溶液,蒸馏有机溶液得到液溴。
6.工业上用活性炭吸附海带提碘后废水中的I-制取I,其流程如图:
2
下列说法错误的是( )
A.NaNO 氧化I-时使溶液pH变大
2
B.活性炭吸附是为了净化水溶液
C.I 与NaOH(浓、热)反应的化学方程式:3I +6NaOH(浓、热)===5NaI+NaIO +3HO
2 2 3 2
D.热空气能吹出I,是因为I 在水中溶解度小、易升华
2 2
答案 B
解析 亚硝酸钠具有氧化性,碘离子具有还原性,酸性条件下,二者发生氧化还原反应生成
一氧化氮和碘;利用活性炭吸附,然后加入热的浓氢氧化钠溶液吸收单质碘,最后加入 HCl
调节pH,碘离子和碘酸根离子在酸性溶液中发生归中反应生成单质碘:IO+5I-+6H+
===3I+3HO,据此解答。
2 2
7.(2022·上海高三模拟)BrCl是一种卤素互化物,与Cl 性质相似,也能与水或碱溶液反应。
2
下列说法正确的是( )
A.BrCl与水反应生成HBrO和HCl,该反应属于氧化还原反应
B.1 mol BrCl与KBr溶液完全反应时转移的电子为1 mol
C.BrCl可与Cl 反应得到Br
2 2
D.BrCl与稀氢氧化钠溶液反应可生成NaBr和NaClO
答案 B
解析 BrCl+HO ===HBrO+HCl,反应中元素化合价无变化,因此该反应属于非氧化还原
2
反应,故A错误;BrCl+KBr===KCl+Br 1 mol BrCl与KBr溶液完全反应时转移的电子为
2,
1 mol,故B正确;Cl 与BrCl都具有氧化性,因此BrCl不与Cl 反应,故C错误;BrCl中
2 2
Br为+1价,因此BrCl与稀氢氧化钠溶液反应可生成NaCl和NaBrO,故D错误。
8.溴化碘(IBr)的化学性质类似卤素单质,它同水反应的化学方程式为 IBr+HO===HBr+
2
HIO。下列有关IBr的叙述不正确的是( )
A.在与水的反应中,IBr既不是氧化剂又不是还原剂
B.在与水的反应中,IBr既是氧化剂又是还原剂
C.在很多反应中,IBr是强氧化剂
D.IBr跟NaOH稀溶液反应生成NaBr、NaIO和HO
2
答案 B解析 IBr+HO ===HBr+HIO中,没有元素的化合价变化,IBr既不是氧化剂又不是还原
2
剂,故A正确、B错误;溴化碘(IBr)的化学性质类似卤素单质,在与金属反应时,IBr是氧
化剂,故C正确;由氯气与NaOH的反应可知,IBr和NaOH稀溶液反应生成NaBr、NaIO
和HO,故D正确。
2
9.“XY ”表示不同卤素之间靠共用电子对形成的卤素互化物(非金属性:XBr >I 。
2 2 2 2