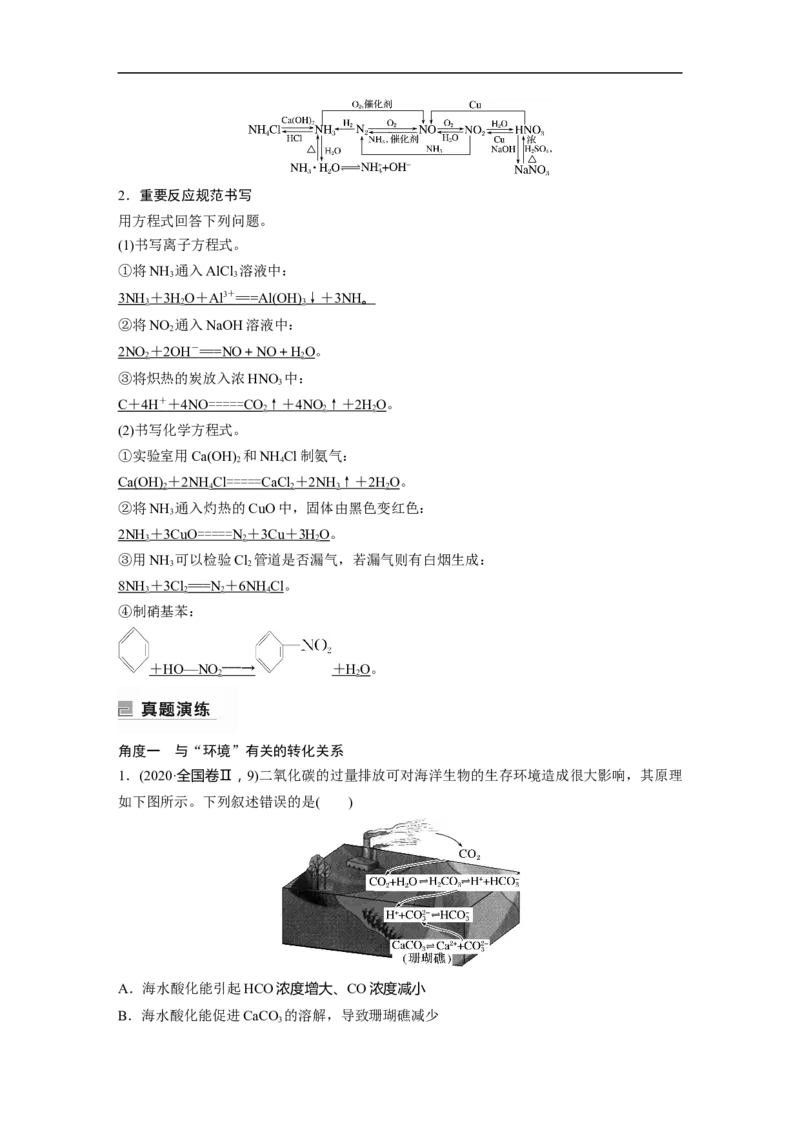
文档内容
[复习目标] 1.掌握常见无机物性质的转化关系。2.掌握无机物性质的转化在环境保护、化
工流程、微型实验中的应用。
(一)钠及其化合物
钠是“极其活泼”金属的代表,学习钠的性质可类比知道第 Ⅰ A族、第 Ⅱ A族活泼金属
的一般性质,复习时应从以下几个方面掌握:
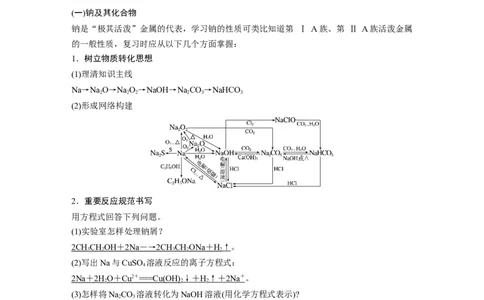
1.树立物质转化思想
(1)理清知识主线
Na→NaO→NaO→NaOH→NaCO→NaHCO
2 2 2 2 3 3
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)实验室怎样处理钠屑?
2CHCH OH + 2Na ― → 2CH CH ONa + H ↑。
3 2 3 2 2
(2)写出Na与CuSO 溶液反应的离子方程式:
4
2Na + 2H O + Cu 2 + == = Cu(OH) ↓ + H ↑ + 2N a + 。
2 2 2
(3)怎样将NaCO 溶液转化为NaOH溶液(用化学方程式表示)?
2 3
NaCO + Ca(OH ) == = CaCO ↓ + 2NaOH 。
2 3 2 3
(4)向NaOH、NaCO、NaHCO 溶液中逐滴滴入少量盐酸,写出发生反应的离子方程式:
2 3 3
OH - + H + == = H O; CO + H + == = HCO ;
2
HCO + H + == = H O + CO ↑。
2 2
(5)怎样除去CO 中的SO 气体(用离子方程式表示)?
2 2
SO + 2HCO == = 2CO + SO + H O。
2 2 2
(6)怎样除去NaCO 溶液中的NaHCO (用离子方程式表示)?
2 3 3
HCO + OH - == = CO + H O。
2(7)怎样除去NaHCO 溶液中的NaCO(用离子方程式表示)?
3 2 3
CO + H O + CO == = 2HCO 。
2 2
(8)用化学方程式表示呼吸面具中产生O 的原理:
2
2NaO + 2H O == = 4NaOH + O ↑;
2 2 2 2
2NaO + 2CO == = 2Na CO + O 。
2 2 2 2 3 2
(二)铝及其化合物
铝是“氢前”且其氧化物、氢氧化物均具有两性的金属代表,它是典型的轻金属。学习铝的
性质可类比知道铍、锌等元素的一般性质,复习时应从以下几个方面掌握:
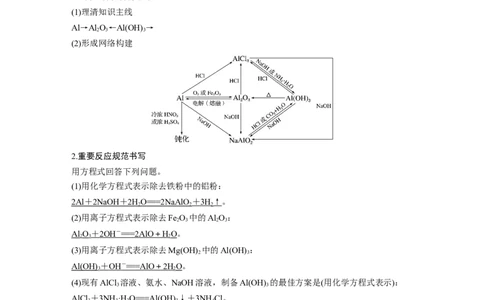
1.树立物质转化思想
(1)理清知识主线
Al→Al O←Al(OH) →
2 3 3
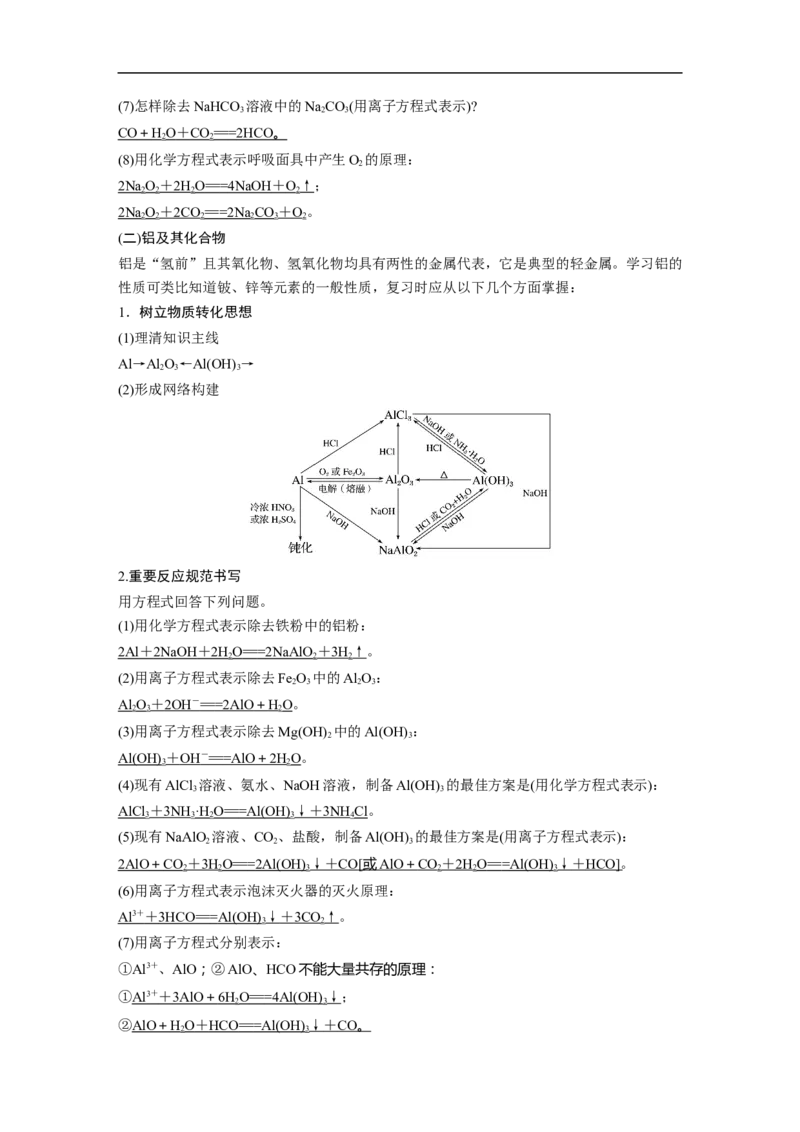
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)用化学方程式表示除去铁粉中的铝粉:
2Al + 2NaOH + 2H O == = 2NaAlO + 3H ↑。
2 2 2
(2)用离子方程式表示除去Fe O 中的Al O:
2 3 2 3
Al O + 2OH - == = 2AlO + H O。
2 3 2
(3)用离子方程式表示除去Mg(OH) 中的Al(OH) :
2 3
Al(OH) + OH - == = AlO + 2H O。
3 2
(4)现有AlCl 溶液、氨水、NaOH溶液,制备Al(OH) 的最佳方案是(用化学方程式表示):
3 3
AlCl + 3NH ·H O == = Al(OH) ↓ + 3NH Cl。
3 3 2 3 4
(5)现有NaAlO 溶液、CO、盐酸,制备Al(OH) 的最佳方案是(用离子方程式表示):
2 2 3
2AlO + CO + 3H O == = 2Al(OH) ↓ + CO [ 或 AlO + CO + 2H O == = Al(OH) ↓ + HCO ]。
2 2 3 2 2 3
(6)用离子方程式表示泡沫灭火器的灭火原理:
Al 3 + + 3HCO == = Al(OH) ↓ + 3CO ↑。
3 2
(7)用离子方程式分别表示:
①Al3+、AlO;②AlO、HCO不能大量共存的原理:
① Al 3 + + 3AlO + 6H O == = 4Al(OH) ↓;
2 3
② AlO + H O + HCO == = Al(OH) ↓ + CO 。
2 3(8)铵明矾[NH Al(SO )·12H O]是常见的食品添加剂,用于焙烤食品,向铵明矾溶液中逐滴
4 4 2 2
滴入NaOH溶液,试写出反应的离子方程式:
Al 3 + + 3OH - == = Al(OH) ↓;
3
NH + OH - == = NH ·H O;
3 2
Al(OH) + OH - == = AlO + 2H O。
3 2
(三)铁及其重要化合物
铁是“氢前”且是“变价”金属的代表,它是典型的黑色金属,也是工农业生产中用途最广
的金属。复习时应从以下几个方面掌握:
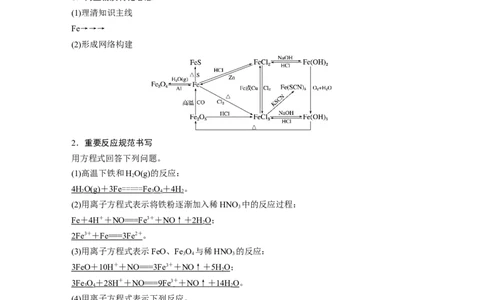
1.树立物质转化思想
(1)理清知识主线
Fe→→→
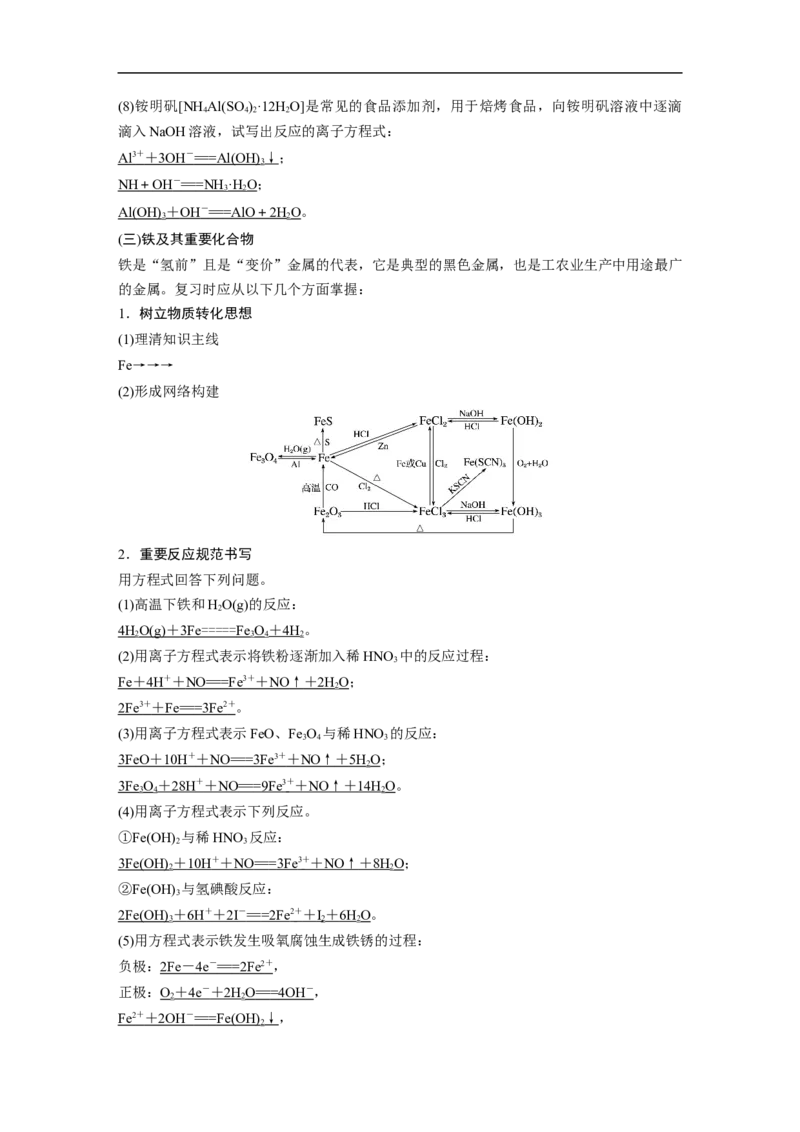
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)高温下铁和HO(g)的反应:
2
4H O(g) + 3Fe ===== Fe O + 4H 。
2 3 4 2
(2)用离子方程式表示将铁粉逐渐加入稀HNO 中的反应过程:
3
Fe + 4H + + NO == = Fe 3 + + NO ↑ + 2H O;
2
2Fe 3 + + Fe == = 3Fe 2 + 。
(3)用离子方程式表示FeO、Fe O 与稀HNO 的反应:
3 4 3
3FeO + 10H + + NO == = 3Fe 3 + + NO ↑ + 5H O;
2
3Fe O + 28H + + NO == = 9F e 3 + + NO ↑ + 14H O。
3 4 2
(4)用离子方程式表示下列反应。
①Fe(OH) 与稀HNO 反应:
2 3
3Fe(OH) + 10H + + NO == = 3F e 3 + + NO ↑ + 8H O;
2 2
②Fe(OH) 与氢碘酸反应:
3
2Fe(OH) + 6H + + 2 I - == = 2F e 2 + + I + 6H O。
3 2 2
(5)用方程式表示铁发生吸氧腐蚀生成铁锈的过程:
负极: 2Fe - 4e - == = 2Fe 2 + ,
正极:O + 4 e - + 2H O == = 4OH - ,
2 2
Fe 2 + + 2OH - == = Fe(OH) ↓,
24Fe(OH) + O + 2H O == = 4Fe(OH) ,
2 2 2 3
Fe(OH) 脱去一部分水生成Fe O·xHO。
3 2 3 2
(6)怎样除去Fe (SO ) 中的FeSO (用适当的文字和离子方程式说明)?
2 4 3 4
答案 加入HSO 酸化的HO,2H++2Fe2++HO===2Fe3++2HO。
2 4 2 2 2 2 2
(7)怎样检验Fe O 中的FeO(用适当的文字和离子方程式说明)?
2 3
答案 ①取少量样品于试管中,加稀HSO 使其溶解,离子方程式为Fe O +6H+===2Fe3+
2 4 2 3
+3HO,FeO+2H+===Fe2++HO。
2 2
②再加入少量酸性 KMnO 溶液,若紫红色褪去,证明溶液中含有 Fe2+,原样品中含有
4
FeO,离子方程式为5Fe2++MnO+8H+===5Fe3++Mn2++4HO。
2
(四)铜及其重要化合物
铜是“氢后”且是“变价”金属的代表,它是典型的有色金属,也是典型的重金属。复习时
应从以下几个方面掌握:
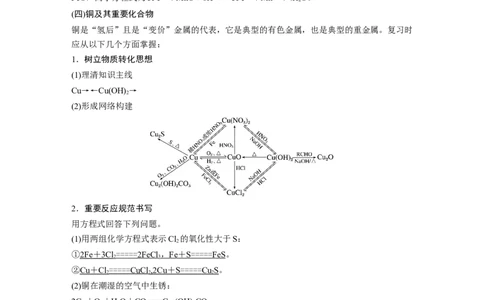
1.树立物质转化思想
(1)理清知识主线
Cu→←Cu(OH) →
2
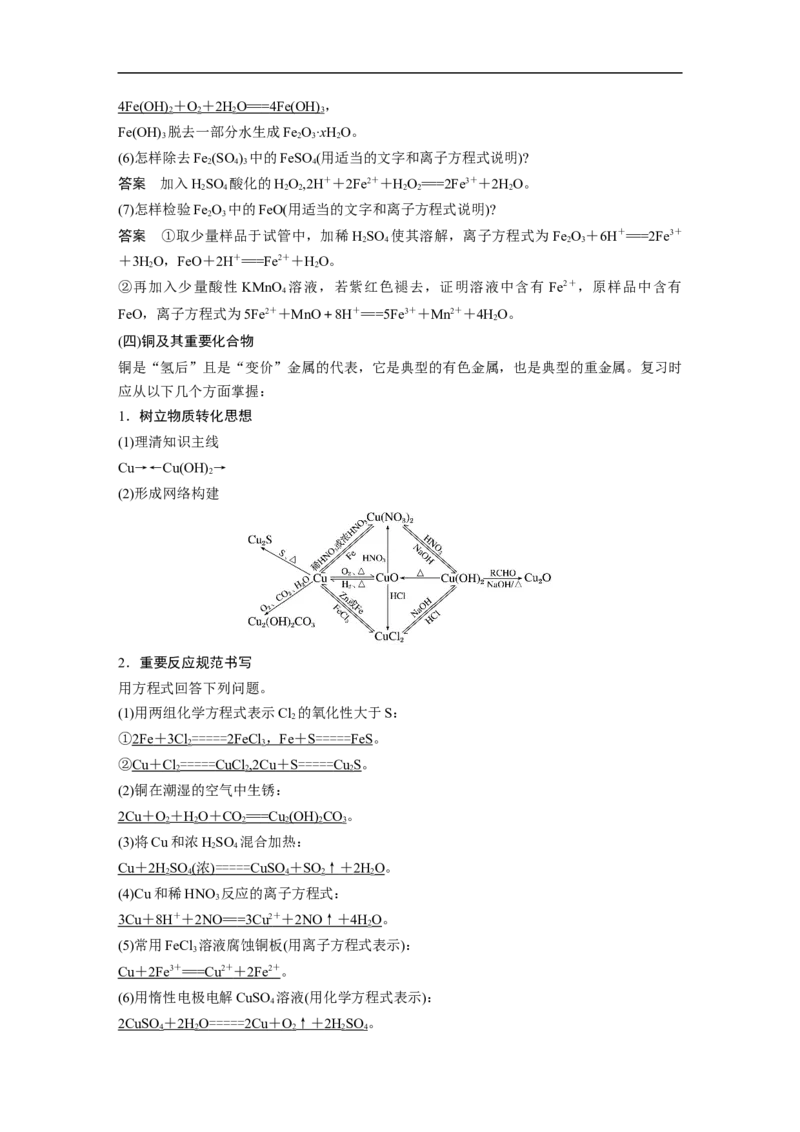
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)用两组化学方程式表示Cl 的氧化性大于S:
2
① 2Fe + 3Cl ==== = 2FeC l , F e + S ==== = FeS 。
2 3
② Cu + Cl ==== = CuC l ,2Cu + S ===== Cu S。
2 2 2
(2)铜在潮湿的空气中生锈:
2Cu + O + H O + CO == = Cu (OH) CO。
2 2 2 2 2 3
(3)将Cu和浓HSO 混合加热:
2 4
Cu + 2H SO ( 浓 ) ===== CuSO + SO ↑ + 2H O。
2 4 4 2 2
(4)Cu和稀HNO 反应的离子方程式:
3
3Cu + 8H + + 2NO == = 3Cu 2 + + 2NO ↑ + 4H O。
2
(5)常用FeCl 溶液腐蚀铜板(用离子方程式表示):
3
Cu + 2Fe 3 + == = Cu 2 + + 2Fe 2 + 。
(6)用惰性电极电解CuSO 溶液(用化学方程式表示):
4
2CuSO + 2H O ===== 2Cu + O ↑ + 2H SO 。
4 2 2 2 4(五)碳、硅及其重要化合物
硅元素的非金属性不强,但其具有“亲氧”特性,使硅元素在自然界中没有游离态,只有化
合态,其主要以二氧化硅和硅酸盐的形式存在。对于碳、硅两元素,复习时应从以下几个方
面掌握:
1.树立物质转化思想
(1)理清知识主线
CH←―C ―→CO―→CO
4 2
SiH←―Si ―→SiO(H SiO)
4 2 2 3
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)Mg在CO 中燃烧:
2
2Mg + CO ==== = 2MgO + C 。
2
(2)“水滴石穿”的反应原理(用离子方程式表示):
CaCO + CO + H O == = Ca 2 + + 2HCO 。
3 2 2
(3)“钟乳石”的形成过程(用化学方程式表示):
CaCO + CO + H O == = Ca(HCO ),
3 2 2 3 2
Ca(HCO ) ==== = CaCO ↓ + CO ↑ + H O。
3 2 3 2 2
(4)向饱和NaCO 溶液中通入过量CO 的离子方程式:
2 3 2
2Na + + CO + CO + H O == = 2NaHCO ↓。
2 2 3
(5)氢氟酸不能用玻璃瓶盛放,其原因是(用化学方程式表示):
SiO + 4HF == = SiF ↑ + 2H O。
2 4 2
(6)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):
SiO + 2OH - == = SiO + H O。
2 2
(7)侯氏制碱法的原理(用化学方程式表示):
CO + NH + NaC l + H O == = NaHCO ↓ + NH Cl。
2 3 2 3 4
(六)卤素及其重要化合物(以氯为例)
氯是典型的活泼非金属元素,在自然界中以化合态存在,复习时应从以下几个方面掌握:1.树立物质转化思想
(1)理清知识主线
HCl―→Cl―→HClO ―→HClO―→HClO―→HClO
2 2 3 4
(2)形成网络构建
2.重要反应规范书写
用方程式回答下列问题。
(1)实验室用MnO 和浓盐酸反应制取Cl 的化学方程式:
2 2
MnO + 4HCl ( 浓 ) ==== = MnC l + C l ↑ + 2H O。
2 2 2 2
(2)将浓盐酸滴到KMnO 固体上(用离子方程式表示):
4
2MnO + 16H + + 10Cl - == = 2Mn 2 + + 5Cl ↑ + 8H O。
2 2
(3)将Cl 通入石灰乳中(用化学方程式表示):
2
2Cl + 2Ca(OH ) == = CaCl + Ca(ClO ) + 2H O。
2 2 2 2 2
(4)在空气中漂白粉漂白的原理(用化学方程式表示):
Ca(ClO) + CO + H O == = CaCO ↓ + 2HClO 。
2 2 2 3
(5)向FeBr 溶液中通入少量Cl 的离子方程式:
2 2
2Fe 2 + + Cl == = 2Fe 3 + + 2Cl - 。
2
(6)向FeBr 溶液中通入等物质的量Cl 的离子方程式:
2 2
2Fe 2 + + 2Br - + 2Cl == = 2Fe 3 + + Br + 4C l - 。
2 2
(7)向FeBr 溶液中通入过量Cl 的离子方程式:
2 2
2Fe 2 + + 4Br - + 3Cl == = 2Fe 3 + + 2Br + 6C l - 。
2 2
(8)将SO 和Cl 混合,漂白性减弱的原因(用离子方程式表示):
2 2
SO + C l + 2H O == = 4H + + SO + 2Cl - 。
2 2 2
(七)硫及其重要化合物
硫是与化工生产、生活和生态环境密切相关的元素,在自然界中既可以以化合态存在,又可
以以游离态存在。复习时应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
HS―→S―→SO―→SO(H SO)
2 2 3 2 4
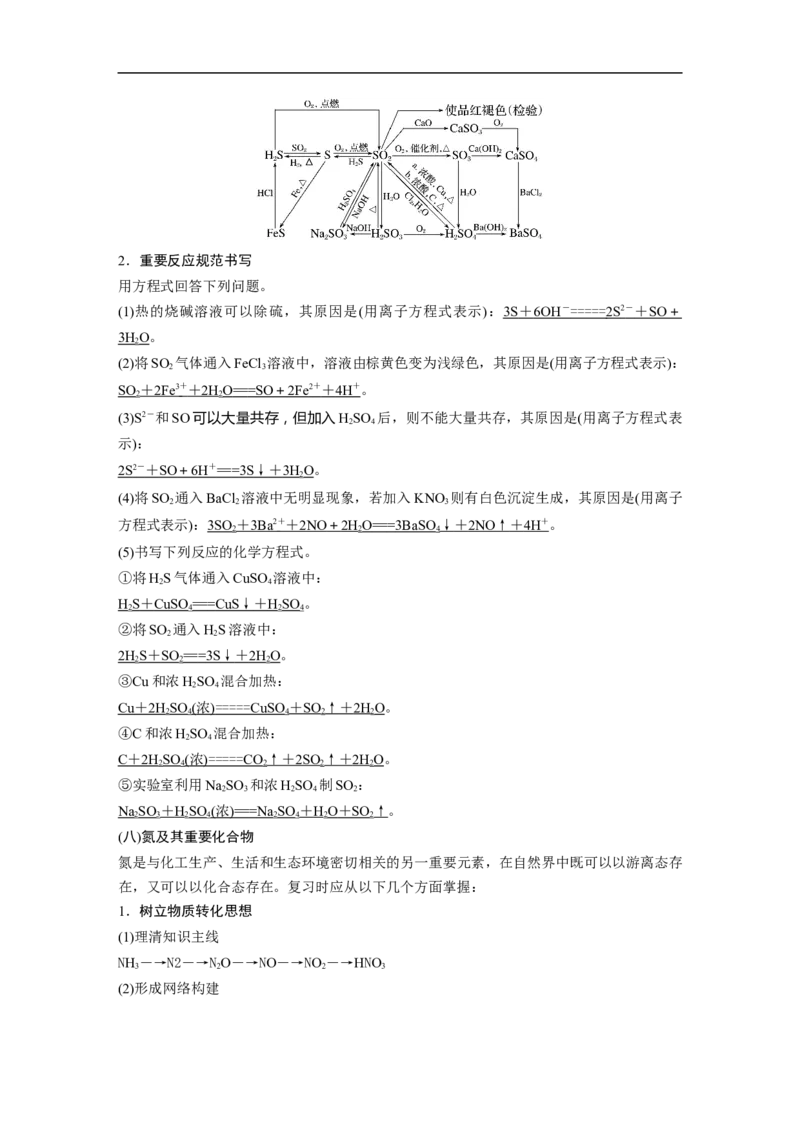
(2)形成网络构建2.重要反应规范书写
用方程式回答下列问题。
(1)热的烧碱溶液可以除硫,其原因是(用离子方程式表示): 3S + 6OH - ===== 2S 2 - + SO +
3HO。
2
(2)将SO 气体通入FeCl 溶液中,溶液由棕黄色变为浅绿色,其原因是(用离子方程式表示):
2 3
SO + 2F e 3 + + 2H O == = SO + 2Fe 2 + + 4H + 。
2 2
(3)S2-和SO可以大量共存,但加入HSO 后,则不能大量共存,其原因是(用离子方程式表
2 4
示):
2S 2 - + SO + 6H + == = 3S ↓ + 3H O。
2
(4)将SO 通入BaCl 溶液中无明显现象,若加入KNO 则有白色沉淀生成,其原因是(用离子
2 2 3
方程式表示):3SO + 3B a 2 + + 2NO + 2H O == = 3BaSO ↓ + 2NO ↑ + 4H + 。
2 2 4
(5)书写下列反应的化学方程式。
①将HS气体通入CuSO 溶液中:
2 4
H S + CuSO == = CuS ↓ + H SO 。
2 4 2 4
②将SO 通入HS溶液中:
2 2
2H S + SO == = 3S ↓ + 2H O。
2 2 2
③Cu和浓HSO 混合加热:
2 4
Cu + 2H SO ( 浓 ) ===== CuSO + SO ↑ + 2H O。
2 4 4 2 2
④C和浓HSO 混合加热:
2 4
C + 2H SO ( 浓 ) ===== CO ↑ + 2SO ↑ + 2H O。
2 4 2 2 2
⑤实验室利用NaSO 和浓HSO 制SO :
2 3 2 4 2
NaSO + H SO ( 浓 ) == = Na SO + H O + SO ↑。
2 3 2 4 2 4 2 2
(八)氮及其重要化合物
氮是与化工生产、生活和生态环境密切相关的另一重要元素,在自然界中既可以以游离态存
在,又可以以化合态存在。复习时应从以下几个方面掌握:
1.树立物质转化思想
(1)理清知识主线
NH―→N2―→NO―→NO―→NO―→HNO
3 2 2 3
(2)形成网络构建2.重要反应规范书写
用方程式回答下列问题。
(1)书写离子方程式。
①将NH 通入AlCl 溶液中:
3 3
3NH + 3H O + Al 3 + == = Al(OH) ↓ + 3NH 。
3 2 3
②将NO 通入NaOH溶液中:
2
2NO + 2OH - == = NO + NO + H O。
2 2
③将炽热的炭放入浓HNO 中:
3
C + 4H + + 4NO ===== CO ↑ + 4NO ↑ + 2H O。
2 2 2
(2)书写化学方程式。
①实验室用Ca(OH) 和NH Cl制氨气:
2 4
Ca(OH) + 2NH Cl ===== CaCl + 2NH ↑ + 2H O。
2 4 2 3 2
②将NH 通入灼热的CuO中,固体由黑色变红色:
3
2NH + 3CuO ==== = N + 3C u + 3H O。
3 2 2
③用NH 可以检验Cl 管道是否漏气,若漏气则有白烟生成:
3 2
8NH + 3C l == = N + 6NH Cl。
3 2 2 4
④制硝基苯:
+ HO—NO ―――→ + H O。
2 2
角度一 与“环境”有关的转化关系
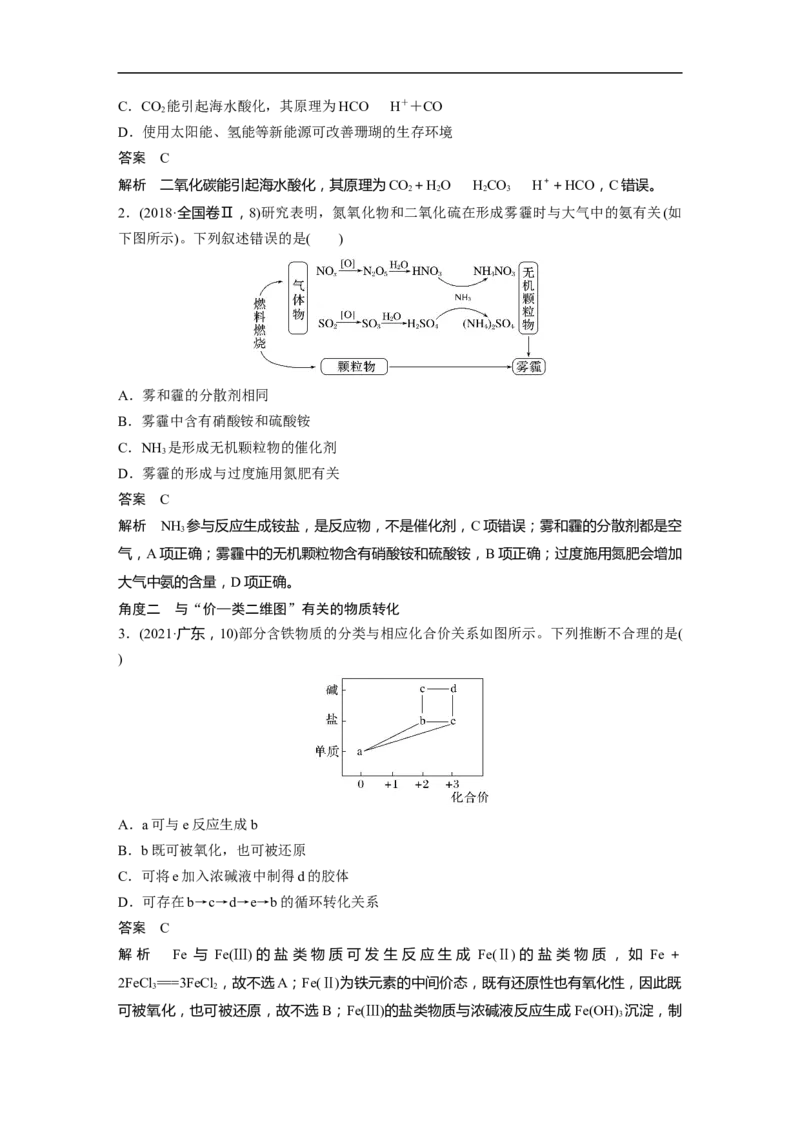
1.(2020·全国卷Ⅱ,9)二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理
如下图所示。下列叙述错误的是( )
A.海水酸化能引起HCO浓度增大、CO浓度减小
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3C.CO 能引起海水酸化,其原理为HCOH++CO
2
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
答案 C
解析 二氧化碳能引起海水酸化,其原理为CO+HOHCOH++HCO,C错误。
2 2 2 3
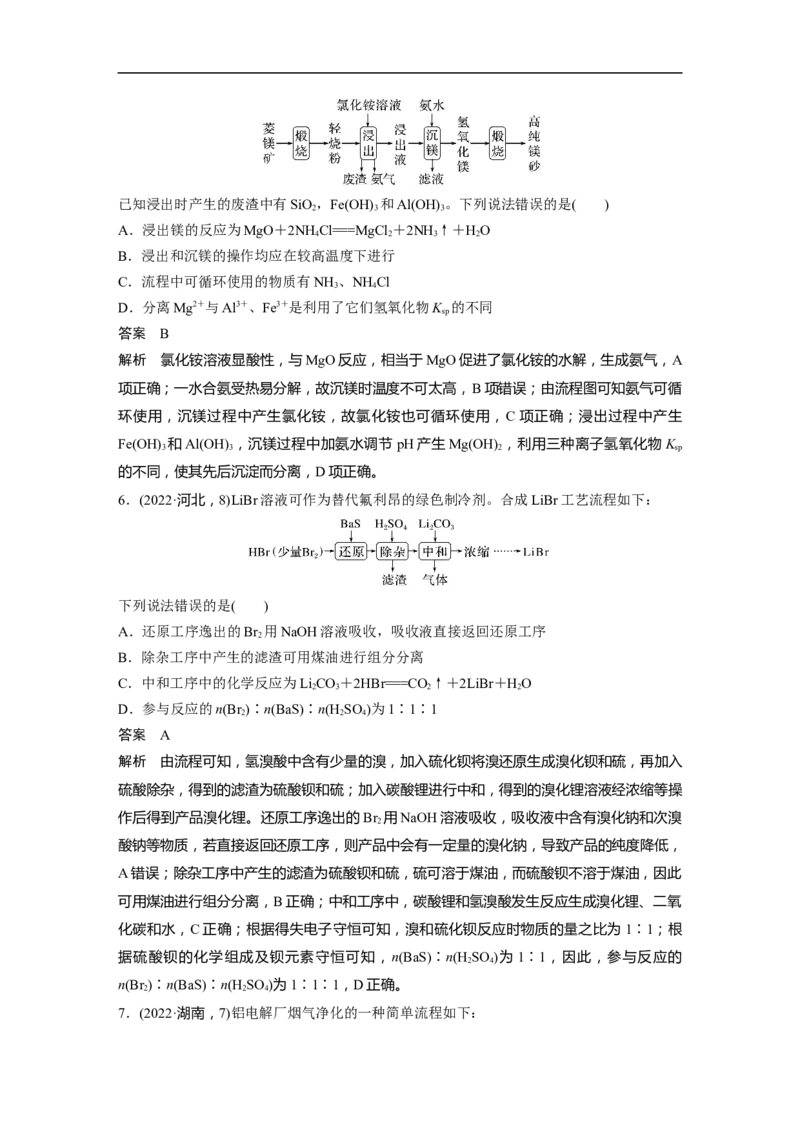
2.(2018·全国卷Ⅱ,8)研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如
下图所示)。下列叙述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH 是形成无机颗粒物的催化剂
3
D.雾霾的形成与过度施用氮肥有关
答案 C
解析 NH 参与反应生成铵盐,是反应物,不是催化剂,C项错误;雾和霾的分散剂都是空
3
气,A项正确;雾霾中的无机颗粒物含有硝酸铵和硫酸铵,B项正确;过度施用氮肥会增加
大气中氨的含量,D项正确。
角度二 与“价—类二维图”有关的物质转化
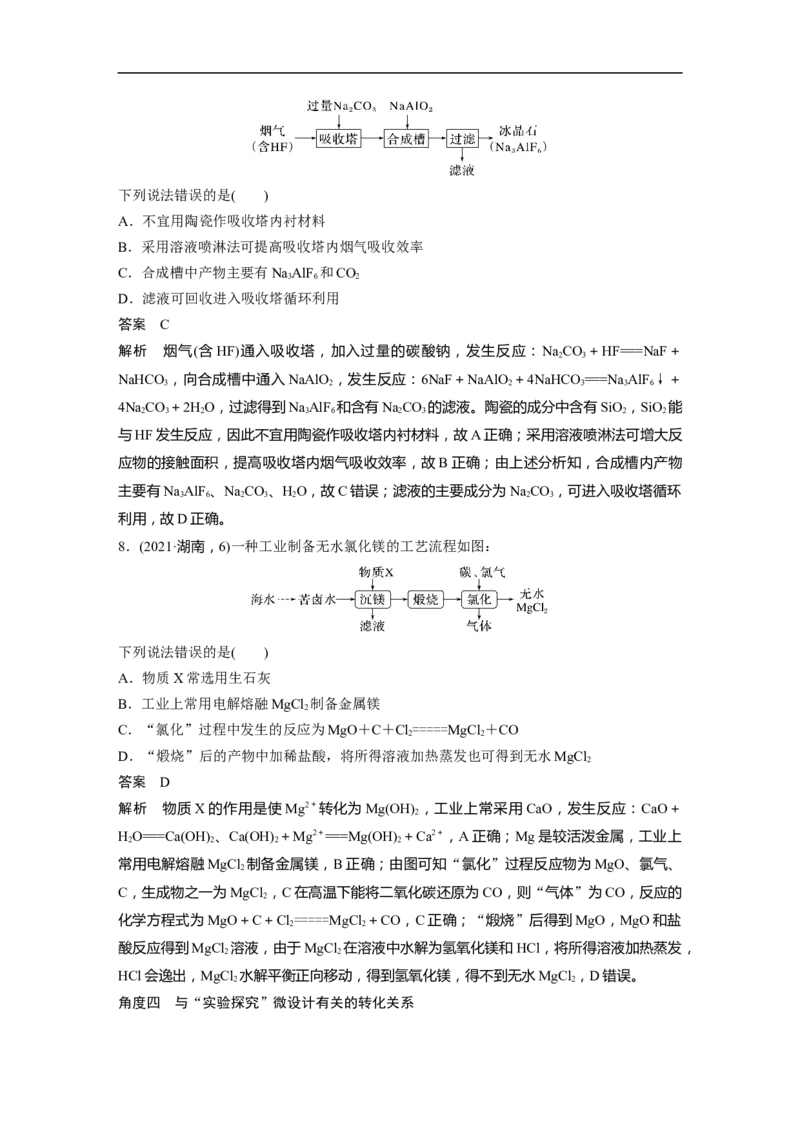
3.(2021·广东,10)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是(
)
A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
答案 C
解 析 Fe 与 Fe(Ⅲ) 的 盐 类 物 质 可 发 生 反 应 生 成 Fe(Ⅱ) 的 盐 类 物 质 , 如 Fe +
2FeCl ===3FeCl ,故不选A;Fe(Ⅱ)为铁元素的中间价态,既有还原性也有氧化性,因此既
3 2
可被氧化,也可被还原,故不选B;Fe(Ⅲ)的盐类物质与浓碱液反应生成Fe(OH) 沉淀,制
3备Fe(OH) 胶体的操作为向沸水中逐滴加入饱和FeCl 溶液,继续煮沸至溶液呈红褐色,停
3 3
止 加 热 , 故 选 C ; b→c→d→e→b 的 转 化 如
FeCl ――→Fe(OH) ―――→Fe(OH) ――→FeCl ――→FeCl ,故不选D。
2 2 3 3 2
角度三 与“化工流程”微设计有关的转化关系
4.(2022·山东,12)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元
素的杂质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
Fe(OH) Cu(OH) Zn(OH)
3 2 2
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是( )
A.固体X主要成分是Fe(OH) 和S;金属M为Zn
3
B.浸取时,增大O 压强可促进金属离子浸出
2
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
答案 D
解析 CuS精矿(含有杂质Zn、Fe元素)在高压O 作用下,用硫酸溶液浸取,与CuS反应生
2
成CuSO 、S、HO,Fe2+被氧化为Fe3+,然后加入NH 调节溶液pH,使Fe3+形成Fe(OH)
4 2 3 3
沉淀,而Cu2+、Zn2+仍以离子形式存在于溶液中,过滤得到的滤渣中含有 S、Fe(OH) ;滤
3
液中含有Cu2+、Zn2+;然后向滤液中通入高压H ,根据元素活动性:Zn>H>Cu,Cu2+被
2
还原为Cu单质,通过过滤分离出来;而Zn2+仍然以离子形式存在于溶液中,再经一系列处
理可得到Zn单质。经过上述分析可知,固体X主要成分是S、Fe(OH) ,金属M为Zn,A
3
正确;CuS难溶于硫酸,在溶液中存在沉淀溶解平衡:CuS(s)Cu2+(aq)+S2-(aq),增大
O 的浓度,可以反应消耗S2-,使之转化为S,从而使沉淀溶解平衡正向移动,从而可促进
2
金属离子的浸出,B正确;根据流程图可知,用NH 调节溶液pH时,要使Fe3+转化为沉淀,
3
而Cu2+、Zn2+仍以离子形式存在于溶液中,结合离子沉淀的pH范围,可知中和时应该调节
溶液pH范围为3.2~4.2,C正确;在用H 还原Cu2+变为Cu单质时,H 失去电子被氧化为H
2 2
+,与溶液中OH-结合形成HO,若还原时增大溶液的酸度,c(H+)增大,不利于H 失去电
2 2
子还原Cu单质,因此不利于Cu的生成,D错误。
5.(2020·山东,9)以菱镁矿(主要成分为MgCO ,含少量SiO 、Fe O 和Al O)为原料制备高
3 2 2 3 2 3
纯镁砂的工艺流程如下:已知浸出时产生的废渣中有SiO,Fe(OH) 和Al(OH) 。下列说法错误的是( )
2 3 3
A.浸出镁的反应为MgO+2NH Cl===MgCl +2NH ↑+HO
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
答案 B
解析 氯化铵溶液显酸性,与MgO反应,相当于MgO促进了氯化铵的水解,生成氨气,A
项正确;一水合氨受热易分解,故沉镁时温度不可太高,B项错误;由流程图可知氨气可循
环使用,沉镁过程中产生氯化铵,故氯化铵也可循环使用,C项正确;浸出过程中产生
Fe(OH) 和Al(OH) ,沉镁过程中加氨水调节pH产生Mg(OH) ,利用三种离子氢氧化物K
3 3 2 sp
的不同,使其先后沉淀而分离,D项正确。
6.(2022·河北,8)LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
下列说法错误的是( )
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为LiCO+2HBr===CO↑+2LiBr+HO
2 3 2 2
D.参与反应的n(Br)∶n(BaS)∶n(H SO )为1∶1∶1
2 2 4
答案 A
解析 由流程可知,氢溴酸中含有少量的溴,加入硫化钡将溴还原生成溴化钡和硫,再加入
硫酸除杂,得到的滤渣为硫酸钡和硫;加入碳酸锂进行中和,得到的溴化锂溶液经浓缩等操
作后得到产品溴化锂。还原工序逸出的Br 用NaOH溶液吸收,吸收液中含有溴化钠和次溴
2
酸钠等物质,若直接返回还原工序,则产品中会有一定量的溴化钠,导致产品的纯度降低,
A错误;除杂工序中产生的滤渣为硫酸钡和硫,硫可溶于煤油,而硫酸钡不溶于煤油,因此
可用煤油进行组分分离,B正确;中和工序中,碳酸锂和氢溴酸发生反应生成溴化锂、二氧
化碳和水,C正确;根据得失电子守恒可知,溴和硫化钡反应时物质的量之比为1∶1;根
据硫酸钡的化学组成及钡元素守恒可知,n(BaS)∶n(H SO )为1∶1,因此,参与反应的
2 4
n(Br)∶n(BaS)∶n(H SO )为1∶1∶1,D正确。
2 2 4
7.(2022·湖南,7)铝电解厂烟气净化的一种简单流程如下:下列说法错误的是( )
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有NaAlF 和CO
3 6 2
D.滤液可回收进入吸收塔循环利用
答案 C
解析 烟气(含HF)通入吸收塔,加入过量的碳酸钠,发生反应:NaCO +HF===NaF+
2 3
NaHCO ,向合成槽中通入NaAlO ,发生反应:6NaF+NaAlO +4NaHCO ===NaAlF↓+
3 2 2 3 3 6
4NaCO +2HO,过滤得到NaAlF 和含有NaCO 的滤液。陶瓷的成分中含有SiO ,SiO 能
2 3 2 3 6 2 3 2 2
与HF发生反应,因此不宜用陶瓷作吸收塔内衬材料,故A正确;采用溶液喷淋法可增大反
应物的接触面积,提高吸收塔内烟气吸收效率,故B正确;由上述分析知,合成槽内产物
主要有NaAlF 、NaCO 、HO,故C错误;滤液的主要成分为NaCO ,可进入吸收塔循环
3 6 2 3 2 2 3
利用,故D正确。
8.(2021·湖南,6)一种工业制备无水氯化镁的工艺流程如图:
下列说法错误的是( )
A.物质X常选用生石灰
B.工业上常用电解熔融MgCl 制备金属镁
2
C.“氯化”过程中发生的反应为MgO+C+Cl=====MgCl +CO
2 2
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
答案 D
解析 物质X的作用是使Mg2+转化为Mg(OH) ,工业上常采用CaO,发生反应:CaO+
2
HO===Ca(OH) 、Ca(OH) +Mg2+===Mg(OH) +Ca2+,A正确;Mg是较活泼金属,工业上
2 2 2 2
常用电解熔融MgCl 制备金属镁,B正确;由图可知“氯化”过程反应物为MgO、氯气、
2
C,生成物之一为MgCl ,C在高温下能将二氧化碳还原为CO,则“气体”为CO,反应的
2
化学方程式为MgO+C+Cl=====MgCl +CO,C正确;“煅烧”后得到MgO,MgO和盐
2 2
酸反应得到MgCl 溶液,由于MgCl 在溶液中水解为氢氧化镁和HCl,将所得溶液加热蒸发,
2 2
HCl会逸出,MgCl 水解平衡正向移动,得到氢氧化镁,得不到无水MgCl ,D错误。
2 2
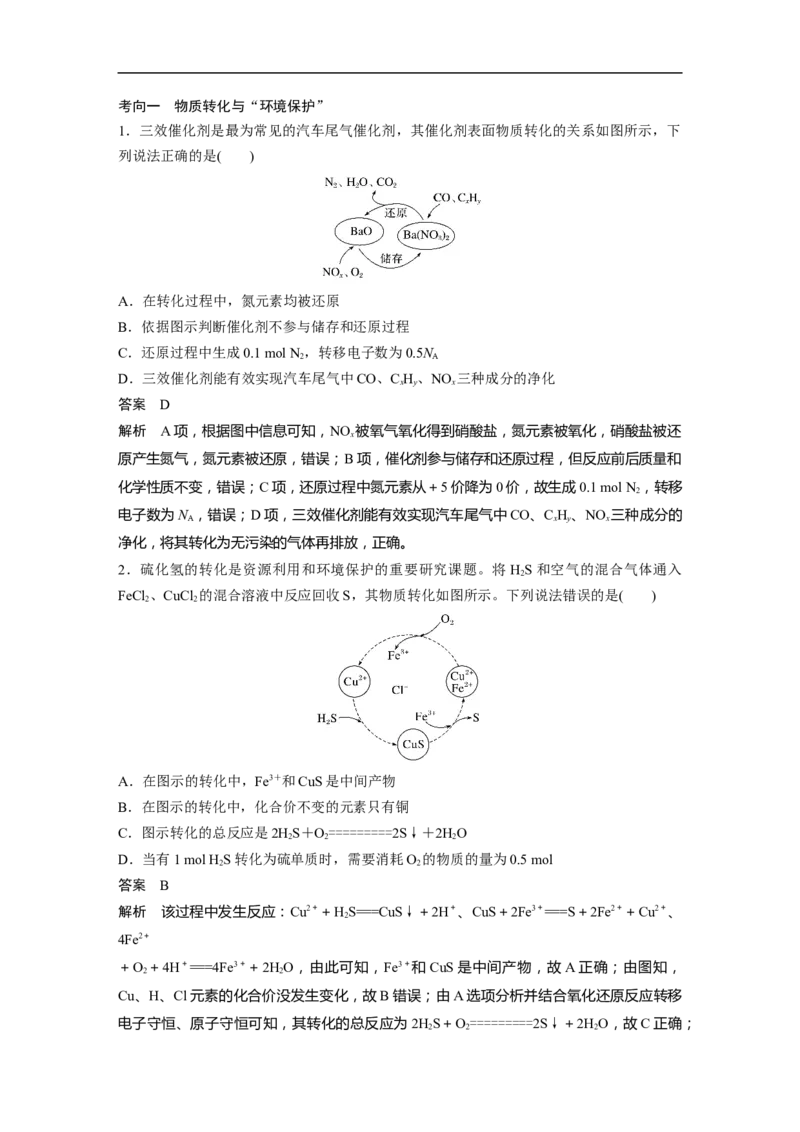
角度四 与“实验探究”微设计有关的转化关系9.(2022·广东,5)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的
探究实验,下列分析正确的是( )
A.Cu与浓硫酸反应,只体现HSO 的酸性
2 4
B.a处变红,说明SO 是酸性氧化物
2
C.b或c处褪色,均说明SO 具有漂白性
2
D.试管底部出现白色固体,说明反应中无HO生成
2
答案 B
解析 铜和浓硫酸反应生成CuSO ,体现浓硫酸的酸性,生成SO ,体现浓硫酸的强氧化性,
4 2
故A错误;a处的紫色石蕊变红,其原因是SO 溶于水生成了酸,可说明SO 是酸性氧化物,
2 2
故B正确;b处品红褪色,其原因是SO 具有漂白性,而c处酸性高锰酸钾褪色,其原因是
2
SO 和酸性KMnO 发生氧化还原反应,SO 体现还原性,故C错误;实验过程中试管底部出
2 4 2
现白色固体,其原因是浓硫酸具有吸水性,将反应生成的HO吸收,故D错误。
2
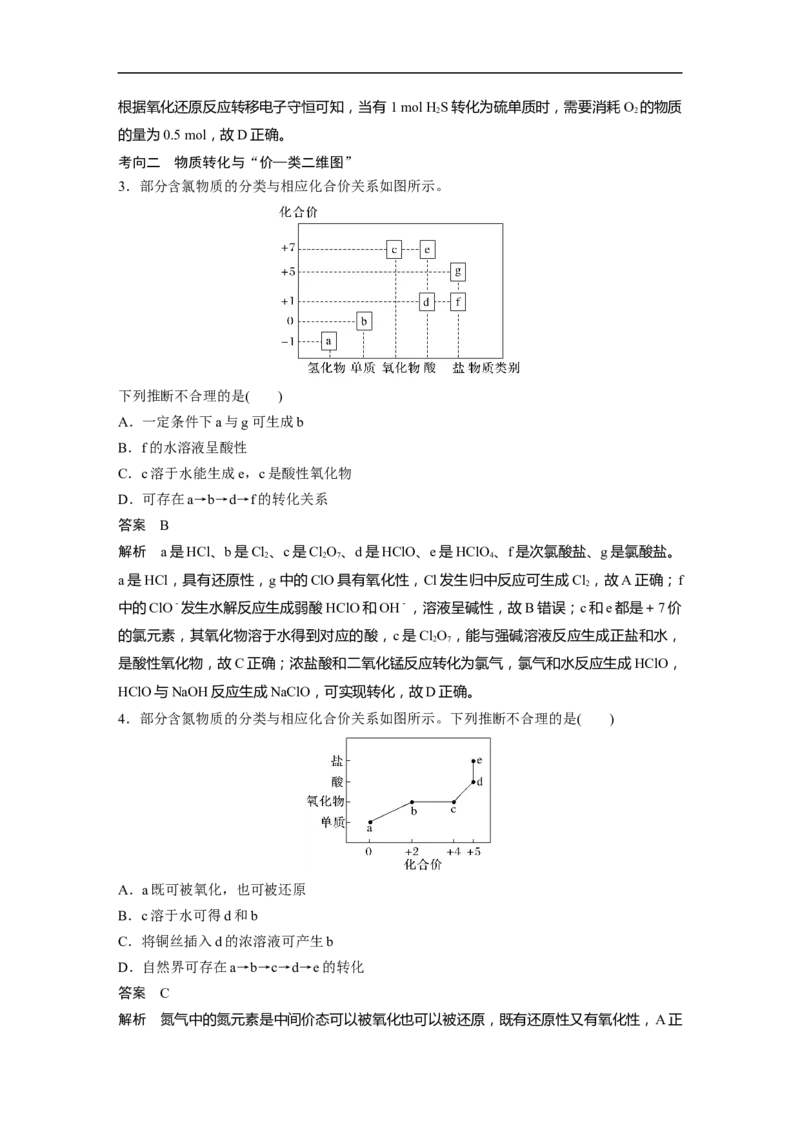
10.(2022·江苏,4)实验室制取少量SO 水溶液并探究其酸性,下列实验装置和操作不能达
2
到实验目的的是 ( )
A.用装置甲制取SO 气体
2
B.用装置乙制取SO 水溶液
2
C.用装置丙吸收尾气中的SO
2
D.用干燥pH试纸检验SO 水溶液的酸性
2
答案 C
解析 60%硫酸和NaHSO(s)可发生反应:HSO +2NaHSO===NaSO +2SO ↑+2HO,因
3 2 4 3 2 4 2 2
此装置甲可以制取SO 气体,A正确;气体通入液体时“长进短出”,装置乙可以制取SO
2 2
水溶液,B正确;SO 不会与饱和NaHSO 溶液发生反应,因此装置丙不能吸收尾气中的
2 3
SO ,C错误;SO 水溶液显酸性,可用干燥的pH试纸检验其酸性,D正确。
2 2考向一 物质转化与“环境保护”
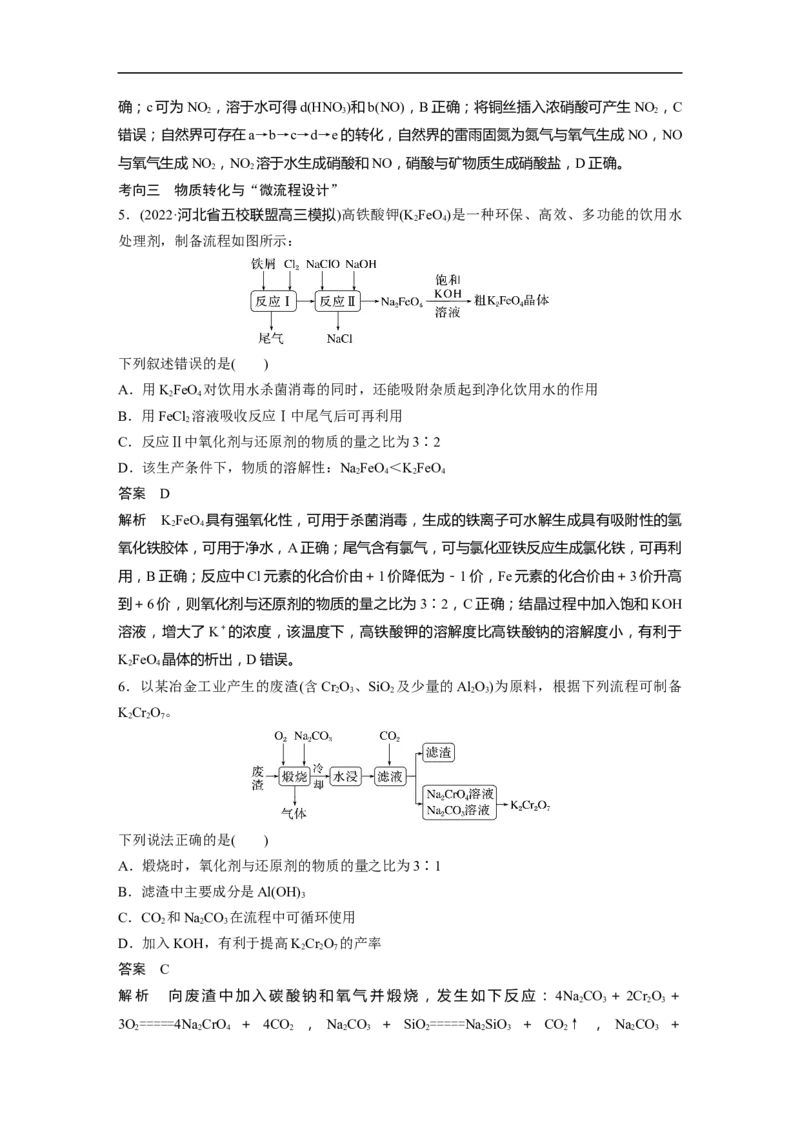
1.三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下
列说法正确的是( )
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1 mol N,转移电子数为0.5N
2 A
D.三效催化剂能有效实现汽车尾气中CO、CH、NO 三种成分的净化
x y x
答案 D
解析 A项,根据图中信息可知,NO 被氧气氧化得到硝酸盐,氮元素被氧化,硝酸盐被还
x
原产生氮气,氮元素被还原,错误;B项,催化剂参与储存和还原过程,但反应前后质量和
化学性质不变,错误;C项,还原过程中氮元素从+5价降为0价,故生成0.1 mol N,转移
2
电子数为N ,错误;D项,三效催化剂能有效实现汽车尾气中CO、CH、NO 三种成分的
A x y x
净化,将其转化为无污染的气体再排放,正确。
2.硫化氢的转化是资源利用和环境保护的重要研究课题。将 HS和空气的混合气体通入
2
FeCl 、CuCl 的混合溶液中反应回收S,其物质转化如图所示。下列说法错误的是( )
2 2
A.在图示的转化中,Fe3+和CuS是中间产物
B.在图示的转化中,化合价不变的元素只有铜
C.图示转化的总反应是2HS+O=========2S↓+2HO
2 2 2
D.当有1 mol H S转化为硫单质时,需要消耗O 的物质的量为0.5 mol
2 2
答案 B
解析 该过程中发生反应:Cu2++HS===CuS↓+2H+、CuS+2Fe3+===S+2Fe2++Cu2+、
2
4Fe2+
+O +4H+===4Fe3++2HO,由此可知,Fe3+和CuS是中间产物,故A正确;由图知,
2 2
Cu、H、Cl元素的化合价没发生变化,故B错误;由A选项分析并结合氧化还原反应转移
电子守恒、原子守恒可知,其转化的总反应为2HS+O=========2S↓+2HO,故C正确;
2 2 2根据氧化还原反应转移电子守恒可知,当有1 mol H S转化为硫单质时,需要消耗O 的物质
2 2
的量为0.5 mol,故D正确。
考向二 物质转化与“价—类二维图”
3.部分含氯物质的分类与相应化合价关系如图所示。
下列推断不合理的是( )
A.一定条件下a与g可生成b
B.f的水溶液呈酸性
C.c溶于水能生成e,c是酸性氧化物
D.可存在a→b→d→f的转化关系
答案 B
解析 a是HCl、b是Cl 、c是ClO 、d是HClO、e是HClO 、f是次氯酸盐、g是氯酸盐。
2 2 7 4
a是HCl,具有还原性,g中的ClO具有氧化性,Cl发生归中反应可生成Cl ,故A正确;f
2
中的ClO-发生水解反应生成弱酸HClO和OH-,溶液呈碱性,故B错误;c和e都是+7价
的氯元素,其氧化物溶于水得到对应的酸,c是ClO ,能与强碱溶液反应生成正盐和水,
2 7
是酸性氧化物,故C正确;浓盐酸和二氧化锰反应转化为氯气,氯气和水反应生成HClO,
HClO与NaOH反应生成NaClO,可实现转化,故D正确。
4.部分含氮物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a既可被氧化,也可被还原
B.c溶于水可得d和b
C.将铜丝插入d的浓溶液可产生b
D.自然界可存在a→b→c→d→e的转化
答案 C
解析 氮气中的氮元素是中间价态可以被氧化也可以被还原,既有还原性又有氧化性,A正确;c可为NO ,溶于水可得d(HNO)和b(NO),B正确;将铜丝插入浓硝酸可产生NO ,C
2 3 2
错误;自然界可存在a→b→c→d→e的转化,自然界的雷雨固氮为氮气与氧气生成NO,NO
与氧气生成NO ,NO 溶于水生成硝酸和NO,硝酸与矿物质生成硝酸盐,D正确。
2 2
考向三 物质转化与“微流程设计”
5.(2022·河北省五校联盟高三模拟)高铁酸钾(K FeO)是一种环保、高效、多功能的饮用水
2 4
处理剂,制备流程如图所示:
下列叙述错误的是( )
A.用KFeO 对饮用水杀菌消毒的同时,还能吸附杂质起到净化饮用水的作用
2 4
B.用FeCl 溶液吸收反应Ⅰ中尾气后可再利用
2
C.反应Ⅱ中氧化剂与还原剂的物质的量之比为3∶2
D.该生产条件下,物质的溶解性:NaFeO<KFeO
2 4 2 4
答案 D
解析 KFeO 具有强氧化性,可用于杀菌消毒,生成的铁离子可水解生成具有吸附性的氢
2 4
氧化铁胶体,可用于净水,A正确;尾气含有氯气,可与氯化亚铁反应生成氯化铁,可再利
用,B正确;反应中Cl元素的化合价由+1价降低为-1价,Fe元素的化合价由+3价升高
到+6价,则氧化剂与还原剂的物质的量之比为3∶2,C正确;结晶过程中加入饱和KOH
溶液,增大了K+的浓度,该温度下,高铁酸钾的溶解度比高铁酸钠的溶解度小,有利于
KFeO 晶体的析出,D错误。
2 4
6.以某冶金工业产生的废渣(含Cr O 、SiO 及少量的Al O)为原料,根据下列流程可制备
2 3 2 2 3
KCr O。
2 2 7
下列说法正确的是( )
A.煅烧时,氧化剂与还原剂的物质的量之比为3∶1
B.滤渣中主要成分是Al(OH)
3
C.CO 和NaCO 在流程中可循环使用
2 2 3
D.加入KOH,有利于提高KCr O 的产率
2 2 7
答案 C
解析 向废渣中加入碳酸钠和氧气并煅烧,发生如下反应:4NaCO +2Cr O +
2 3 2 3
3O=====4NaCrO + 4CO , NaCO + SiO=====NaSiO + CO↑ , NaCO +
2 2 4 2 2 3 2 2 3 2 2 3Al O=====2NaAlO +CO↑,用水浸之后,溶液中含有 NaCrO 、NaSiO 、NaAlO 、
2 3 2 2 2 4 2 3 2
NaCO ,向溶液中通入二氧化碳,生成氢氧化铝沉淀和硅酸沉淀,过滤,滤液中含有
2 3
NaCrO 、NaCO ,再向溶液中加硫酸,2NaCrO +HSO ===NaCr O +NaSO +HO,再
2 4 2 3 2 4 2 4 2 2 7 2 4 2
向溶液中加入KCl固体,就会析出溶解度更小的KCr O 晶体,以此分析解答。由反应:
2 2 7
4NaCO +2Cr O +3O=====4NaCrO +4CO ,O元素化合价降低,O 做氧化剂,Cr元素化
2 3 2 3 2 2 4 2 2
合价升高,Cr O 做还原剂,则氧化剂与还原剂的物质的量之比为3∶2,故A错误;从流程
2 3
图可知,CO 和NaCO 均可循环使用,故C正确。
2 2 3
考向四 物质转化与“微实验设计”
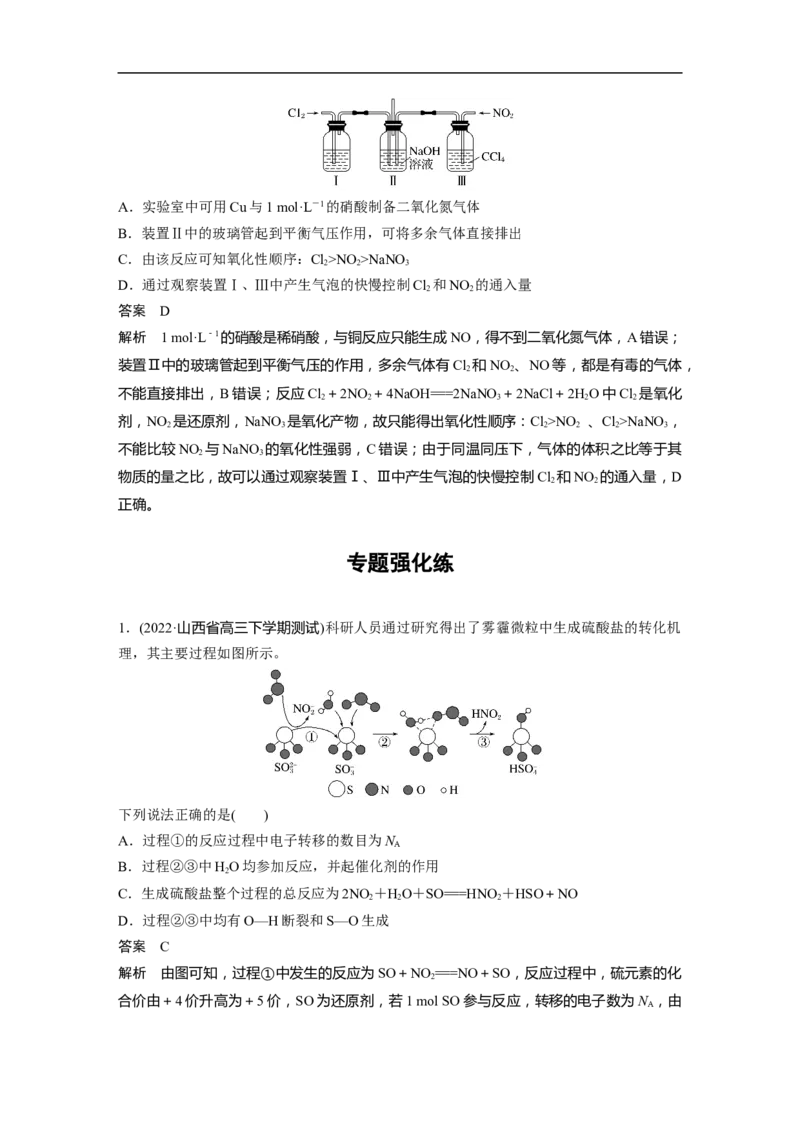
7.(2022·安徽省六安市示范高中高三质量检测)金属锡是一种具有银白色金属光泽且质地较
软的低熔点金属,常温下SnCl 为无色液体,沸点为114 ℃,在空气中易水解生成锡酸与
4
HCl。可用Cl 与熔融的金属锡反应制备SnCl ,装置如下(夹持装置略)。下列说法错误的是(
2 4
)
A.用恒压滴液漏斗代替针筒能更好的控制产生氯气的速率
B.戊装置的作用是冷凝、收集SnCl
4
C.实验过程中应该先点燃酒精灯融化金属锡,再向甲中注入浓盐酸
D.用装有碱石灰的干燥管代替己中NaOH溶液更合理
答案 C
解析 由于高锰酸钾与浓盐酸反应剧烈,故用恒压滴液漏斗能控制浓盐酸的滴速,进而控制
反应的速率,故A正确;常温下SnCl 为无色液体,沸点为114 ℃,故该物质的收集需要进
4
行冷凝液化,故B正确;由于金属锡的活动性仅次于铁,先点燃酒精灯融化金属锡会与空
气中的氧气反应,因此应该先制备氯气,将装置中空气排尽后再加热金属锡,故C错误;
己装置中水蒸气会进入到戊装置中,导致SnCl 水解,换用碱石灰既能吸收多余的氯气,又
4
能防止水蒸气扩散至戊装置中,故D正确。
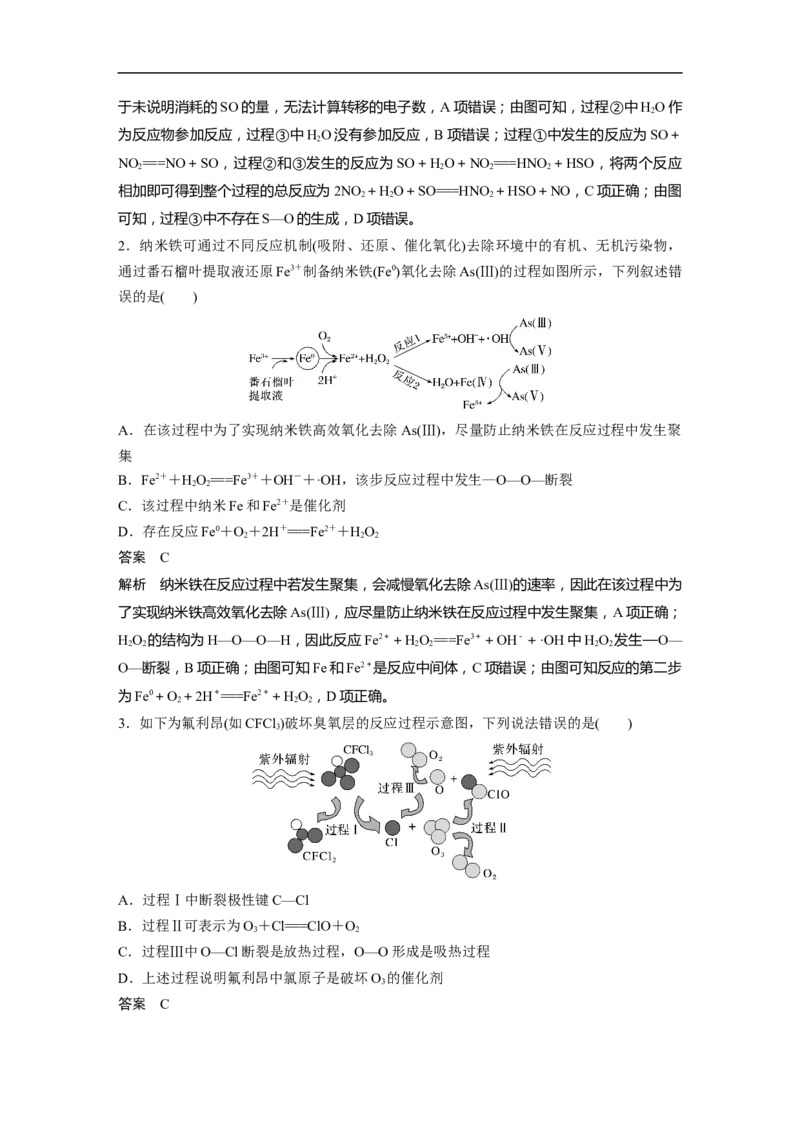
8.(2022·湖南省常德市临澧县第一中学高三阶段性考试)用如图装置探究Cl 和NO 在NaOH
2 2
溶液中的反应。通入适当比例的 Cl 和 NO ,发生的化学反应为 Cl +2NO +
2 2 2 2
4NaOH===2NaNO +2NaCl+2HO。下列叙述正确的是( )
3 2A.实验室中可用Cu与1 mol·L-1的硝酸制备二氧化氮气体
B.装置Ⅱ中的玻璃管起到平衡气压作用,可将多余气体直接排出
C.由该反应可知氧化性顺序:Cl>NO>NaNO
2 2 3
D.通过观察装置Ⅰ、Ⅲ中产生气泡的快慢控制Cl 和NO 的通入量
2 2
答案 D
解析 1 mol·L-1的硝酸是稀硝酸,与铜反应只能生成NO,得不到二氧化氮气体,A错误;
装置Ⅱ中的玻璃管起到平衡气压的作用,多余气体有Cl 和NO 、NO等,都是有毒的气体,
2 2
不能直接排出,B错误;反应Cl +2NO +4NaOH===2NaNO +2NaCl+2HO中Cl 是氧化
2 2 3 2 2
剂,NO 是还原剂,NaNO 是氧化产物,故只能得出氧化性顺序:Cl>NO 、Cl>NaNO ,
2 3 2 2 2 3
不能比较NO 与NaNO 的氧化性强弱,C错误;由于同温同压下,气体的体积之比等于其
2 3
物质的量之比,故可以通过观察装置Ⅰ、Ⅲ中产生气泡的快慢控制Cl 和NO 的通入量,D
2 2
正确。
专题强化练
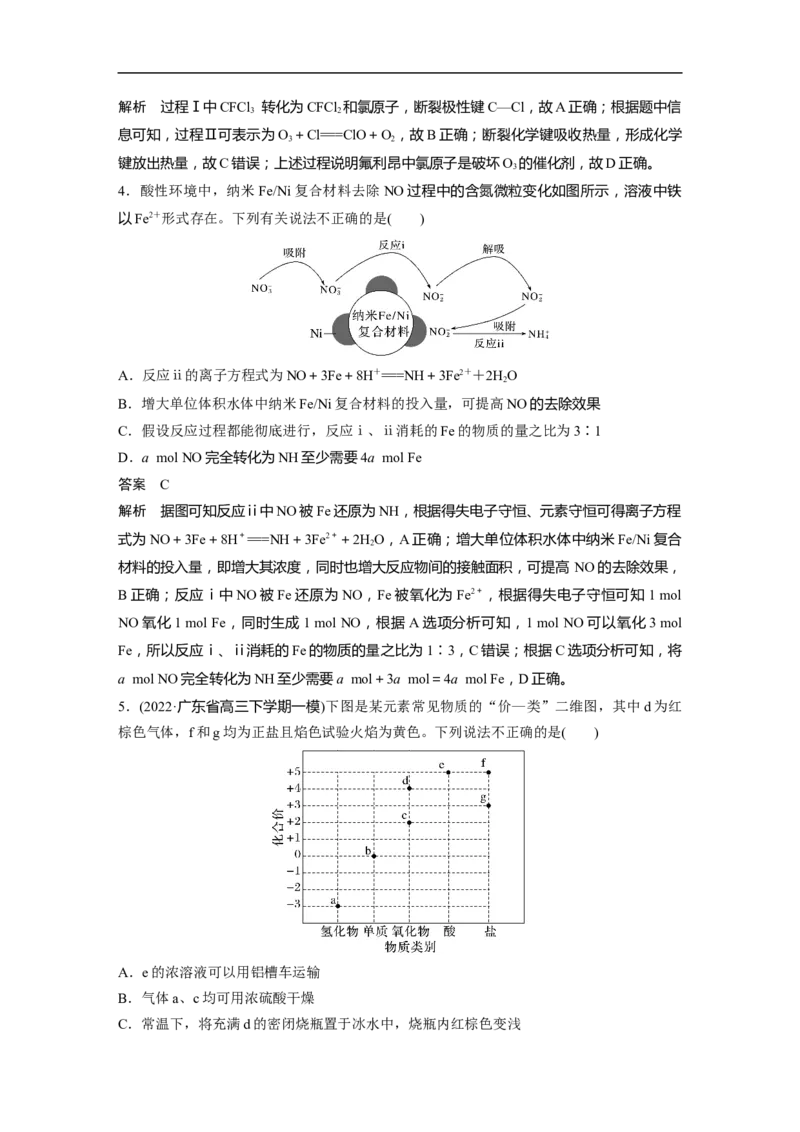
1.(2022·山西省高三下学期测试)科研人员通过研究得出了雾霾微粒中生成硫酸盐的转化机
理,其主要过程如图所示。
下列说法正确的是( )
A.过程①的反应过程中电子转移的数目为N
A
B.过程②③中HO均参加反应,并起催化剂的作用
2
C.生成硫酸盐整个过程的总反应为2NO +HO+SO===HNO+HSO+NO
2 2 2
D.过程②③中均有O—H断裂和S—O生成
答案 C
解析 由图可知,过程①中发生的反应为SO+NO ===NO+SO,反应过程中,硫元素的化
2
合价由+4价升高为+5价,SO为还原剂,若1 mol SO参与反应,转移的电子数为N ,由
A于未说明消耗的SO的量,无法计算转移的电子数,A项错误;由图可知,过程②中HO作
2
为反应物参加反应,过程③中HO没有参加反应,B项错误;过程①中发生的反应为SO+
2
NO ===NO+SO,过程②和③发生的反应为SO+HO+NO ===HNO +HSO,将两个反应
2 2 2 2
相加即可得到整个过程的总反应为2NO +HO+SO===HNO +HSO+NO,C项正确;由图
2 2 2
可知,过程③中不存在S—O的生成,D项错误。
2.纳米铁可通过不同反应机制(吸附、还原、催化氧化)去除环境中的有机、无机污染物,
通过番石榴叶提取液还原Fe3+制备纳米铁(Fe0)氧化去除As(Ⅲ)的过程如图所示,下列叙述错
误的是( )
A.在该过程中为了实现纳米铁高效氧化去除As(Ⅲ),尽量防止纳米铁在反应过程中发生聚
集
B.Fe2++HO===Fe3++OH-+·OH,该步反应过程中发生—O—O—断裂
2 2
C.该过程中纳米Fe和Fe2+是催化剂
D.存在反应Fe0+O+2H+===Fe2++HO
2 2 2
答案 C
解析 纳米铁在反应过程中若发生聚集,会减慢氧化去除As(Ⅲ)的速率,因此在该过程中为
了实现纳米铁高效氧化去除As(Ⅲ),应尽量防止纳米铁在反应过程中发生聚集,A项正确;
HO 的结构为H—O—O—H,因此反应Fe2++HO===Fe3++OH-+·OH中HO 发生—O—
2 2 2 2 2 2
O—断裂,B项正确;由图可知Fe和Fe2+是反应中间体,C项错误;由图可知反应的第二步
为Fe0+O+2H+===Fe2++HO,D项正确。
2 2 2
3.如下为氟利昂(如CFCl )破坏臭氧层的反应过程示意图,下列说法错误的是( )
3
A.过程Ⅰ中断裂极性键C—Cl
B.过程Ⅱ可表示为O+Cl===ClO+O
3 2
C.过程Ⅲ中O—Cl断裂是放热过程,O—O形成是吸热过程
D.上述过程说明氟利昂中氯原子是破坏O 的催化剂
3
答案 C解析 过程Ⅰ中CFCl 转化为CFCl 和氯原子,断裂极性键C—Cl,故A正确;根据题中信
3 2
息可知,过程Ⅱ可表示为O +Cl===ClO+O ,故B正确;断裂化学键吸收热量,形成化学
3 2
键放出热量,故C错误;上述过程说明氟利昂中氯原子是破坏O 的催化剂,故D正确。
3
4.酸性环境中,纳米Fe/Ni复合材料去除NO过程中的含氮微粒变化如图所示,溶液中铁
以Fe2+形式存在。下列有关说法不正确的是( )
A.反应ⅱ的离子方程式为NO+3Fe+8H+===NH+3Fe2++2HO
2
B.增大单位体积水体中纳米Fe/Ni复合材料的投入量,可提高NO的去除效果
C.假设反应过程都能彻底进行,反应ⅰ、ⅱ消耗的Fe的物质的量之比为3∶1
D.a mol NO完全转化为NH至少需要4a mol Fe
答案 C
解析 据图可知反应ⅱ中NO被Fe还原为NH,根据得失电子守恒、元素守恒可得离子方程
式为NO+3Fe+8H+===NH+3Fe2++2HO,A正确;增大单位体积水体中纳米Fe/Ni复合
2
材料的投入量,即增大其浓度,同时也增大反应物间的接触面积,可提高 NO的去除效果,
B正确;反应ⅰ中NO被Fe还原为NO,Fe被氧化为Fe2+,根据得失电子守恒可知 1 mol
NO氧化1 mol Fe,同时生成1 mol NO,根据A选项分析可知,1 mol NO可以氧化3 mol
Fe,所以反应ⅰ、ⅱ消耗的Fe的物质的量之比为1∶3,C错误;根据C选项分析可知,将
a mol NO完全转化为NH至少需要a mol+3a mol=4a mol Fe,D正确。
5.(2022·广东省高三下学期一模)下图是某元素常见物质的“价—类”二维图,其中d为红
棕色气体,f和g均为正盐且焰色试验火焰为黄色。下列说法不正确的是( )
A.e的浓溶液可以用铝槽车运输
B.气体a、c均可用浓硫酸干燥
C.常温下,将充满d的密闭烧瓶置于冰水中,烧瓶内红棕色变浅D.d可与NaOH溶液反应生成f和g
答案 B
解析 由题干信息d为红棕色气体,则d为NO ,说明该图为N元素的“价—类”二维图,
2
则可知:a为NH 、b为N 、c为NO、d为NO 、e为HNO ,f和g均为正盐且焰色试验火
3 2 2 3
焰为黄色,说明g、f含有Na+,则f为NaNO 、g为NaNO ,据此分析解题。e的浓溶液即
3 2
浓HNO ,由于常温下铝在浓硝酸中发生钝化,故可以用铝槽车运输浓 HNO ,A正确;气
3 3
体a为NH ,不能用浓硫酸干燥,c为NO,可用浓硫酸干燥,B错误;d为NO ,常温下,
3 2
将充满d的密闭烧瓶置于冰水中,由于反应2NO (g)NO(g) ΔH<0, 平衡正向移动,故
2 2 4
烧瓶内红棕色变浅,C正确;d为NO ,2NO +2NaOH===NaNO +NaNO +HO,即NO 可
2 2 3 2 2 2
与NaOH溶液反应生成f(NaNO )和g(NaNO ),D正确。
3 2
6.(2022·长沙市雅礼中学模拟)硫及其化合物的“价—类”二维图体现了化学变化之美。下
列有关说法正确的是( )
A.硫在氧气中燃烧直接生成Y
B.X能使酸性KMnO 溶液褪色,体现其漂白性
4
C.硫化氢与X反应的氧化产物和还原产物的物质的量之比为2∶1
D.N可由其相应单质直接化合生成
答案 C
解析 硫在氧气中燃烧直接生成SO ,不是SO ,A错误;X为SO ,能使酸性KMnO 溶液
2 3 2 4
褪色,体现其还原性,B错误;HS与SO 反应的化学方程式为2HS+SO ===2HO+3S,
2 2 2 2 2
氧化产物和还原产物的物质的量之比为2∶1,C正确;N是CuS,S的氧化性很弱,与变价
金属反应生成的是低价硫化物,所以不能由硫和铜直接反应生成CuS,D错误。
7.砷碱渣中含有大量的Na+、AsO、OH-、SO等,采用无废气、废水、废渣产生的工艺流
程如图:
下列说法错误的是( )
A.开始通入CO 时发生反应的离子方程式为CO+2OH-===CO+HO
2 2 2B.通入CO 进行脱碳酸盐,脱出的碳酸盐为NaHCO
2 3
C.脱砷的离子方程式为2AsO+5S2-+16H+===As S↓+8HO
2 5 2
D.脱硫酸根离子时的离子方程式为Ba2++SO===BaSO↓
4
答案 C
解析 根据流程图可知,开始通入CO 时,少量的CO 与碱反应的离子方程式为CO +2OH-
2 2 2
===CO+HO,A正确;在相同温度下,NaHCO 的溶解度小于NaCO 的溶解度,为了使
2 3 2 3
Na+更充分的沉淀,要通入足量的CO 使Na+形成NaHCO 析出,B正确;溶液显碱性,脱
2 3
砷时的离子方程式应为2AsO+5S2-+8HO===As S↓+16OH-,C错误;脱SO时,溶液
2 2 5
中的SO与加入的Ba2+反应生成BaSO 沉淀,D正确。
4
8.水合肼(N H·H O)是一种重要的化工原料,其沸点约为118 ℃,具有强还原性,实验室
2 4 2
将NaClO稀溶液缓慢滴加到CO(NH) 和NaOH的混合溶液中制备水合肼,其流程如图所示,
2 2
下列说法正确的是( )
A.“制备NaClO”过程中每消耗标准状况下2.24 L Cl ,转移0.2 mol电子
2
B.“蒸馏”操作需要用到的冷凝仪器有球形冷凝管
C.“氧化”步骤中药品的滴加顺序不能颠倒
D.“氧化”步骤中发生反应的离子方程式为 ClO-+CO(NH) +HO===Cl-+CO↑+
2 2 2 2
NH·H O
2 4 2
答案 C
解析 “制备NaClO”发生反应:Cl +2NaOH===NaClO+NaCl+HO,氯元素由0价升至
2 2
+1价,也降至-1价,标况下2.24 L氯气的物质的量为0.1 mol,转移电子0.1 mol,A项错
误;蒸馏所需的冷凝仪器为直形冷凝管,B项错误;若将CO(NH) 和NaOH的混合溶液滴
2 2
入NaClO溶液中,生成的水合肼由于具有强还原性,会和具有强氧化性的NaClO发生反应,
故“氧化”步骤中药品的滴加顺序不能颠倒,C项正确;依题知溶液呈碱性,则反应的离子
方程式为ClO-+CO(NH)+2OH-===Cl-+CO+NH·H O,D项错误。
2 2 2 4 2
9.CuCl为白色固体,难溶于水和乙醇,潮湿时易被氧化,常用于媒染剂。以废铜渣(主要
成分为Cu,含少量Ni、Al O 等)为原料制备CuCl的工艺流程如下:
2 3
下列说法正确的是( )
A.“碱溶”时发生了Al和NaOH的反应B.“洗涤”时使用乙醇防止CuCl被氧化
C.“还原”反应所得的溶液中大量存在Cu2+、H+、SO、Cl-
D.工艺流程中不包含化合反应和分解反应
答案 B
解析 根据流程分析,废铜渣(主要成分为Cu,含少量Ni、Al O 等)中通入一氧化碳气体后,
2 3
生成Ni(CO) ,达到除去镍的目的;剩余物质进行碱溶,只有氧化铝与强碱反应生成偏铝酸
4
盐,过滤后滤渣为铜,加入过氧化氢,在酸性环境下,铜被氧化为铜离子,加入亚硫酸钠和
氯化钠的混合物,+2价铜被还原为+1价铜,反应生成CuCl,过滤洗涤可以得到CuCl。
CuCl难溶于乙醇且乙醇易挥发,可以带出氯化亚铜表面的水分,起干燥作用,而氯化亚铜
在潮湿时易被氧化,故乙醇可以干燥氯化亚铜,从而防止CuCl被氧化,故B正确;还原后
的溶液中的铜离子反应生成CuCl,而亚硫酸根离子被氧化为硫酸根离子,故“还原”反应
所得的溶液中不会大量存在Cu2+、SO,故C错误;除镍过程中:Ni+4CO===Ni(CO) ,为
4
化合反应,故D错误。
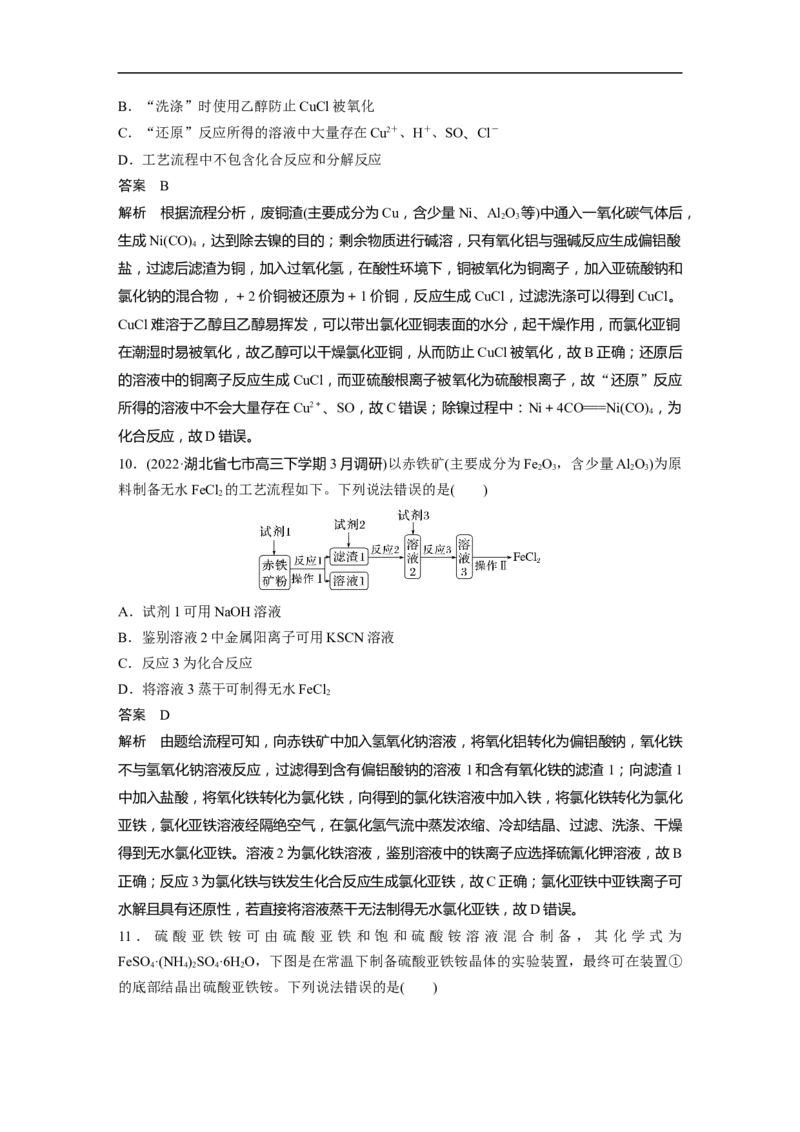
10.(2022·湖北省七市高三下学期3月调研)以赤铁矿(主要成分为Fe O ,含少量Al O)为原
2 3 2 3
料制备无水FeCl 的工艺流程如下。下列说法错误的是( )
2
A.试剂1可用NaOH溶液
B.鉴别溶液2中金属阳离子可用KSCN溶液
C.反应3为化合反应
D.将溶液3蒸干可制得无水FeCl
2
答案 D
解析 由题给流程可知,向赤铁矿中加入氢氧化钠溶液,将氧化铝转化为偏铝酸钠,氧化铁
不与氢氧化钠溶液反应,过滤得到含有偏铝酸钠的溶液 1和含有氧化铁的滤渣1;向滤渣1
中加入盐酸,将氧化铁转化为氯化铁,向得到的氯化铁溶液中加入铁,将氯化铁转化为氯化
亚铁,氯化亚铁溶液经隔绝空气,在氯化氢气流中蒸发浓缩、冷却结晶、过滤、洗涤、干燥
得到无水氯化亚铁。溶液2为氯化铁溶液,鉴别溶液中的铁离子应选择硫氰化钾溶液,故B
正确;反应3为氯化铁与铁发生化合反应生成氯化亚铁,故C正确;氯化亚铁中亚铁离子可
水解且具有还原性,若直接将溶液蒸干无法制得无水氯化亚铁,故D错误。
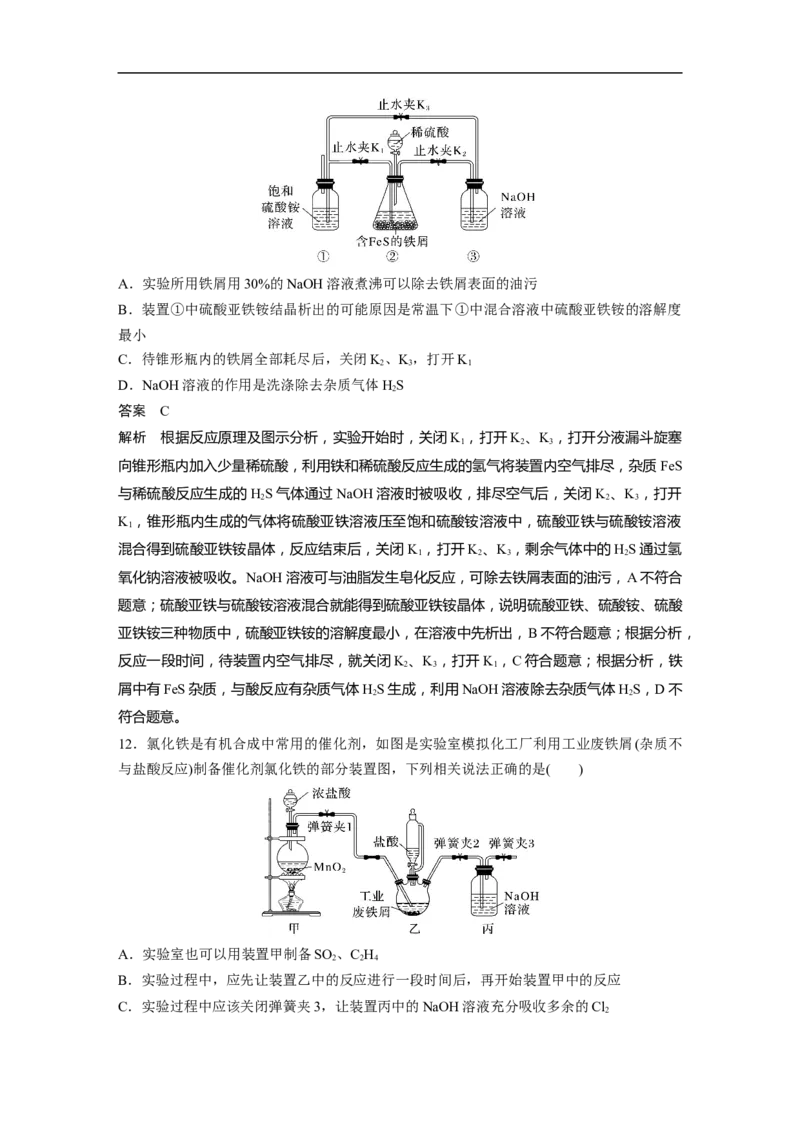
11 . 硫 酸 亚 铁 铵 可 由 硫 酸 亚 铁 和 饱 和 硫 酸 铵 溶 液 混 合 制 备 , 其 化 学 式 为
FeSO ·(NH )SO ·6H O,下图是在常温下制备硫酸亚铁铵晶体的实验装置,最终可在装置①
4 4 2 4 2
的底部结晶出硫酸亚铁铵。下列说法错误的是( )A.实验所用铁屑用30%的NaOH溶液煮沸可以除去铁屑表面的油污
B.装置①中硫酸亚铁铵结晶析出的可能原因是常温下①中混合溶液中硫酸亚铁铵的溶解度
最小
C.待锥形瓶内的铁屑全部耗尽后,关闭K、K,打开K
2 3 1
D.NaOH溶液的作用是洗涤除去杂质气体HS
2
答案 C
解析 根据反应原理及图示分析,实验开始时,关闭K ,打开K 、K ,打开分液漏斗旋塞
1 2 3
向锥形瓶内加入少量稀硫酸,利用铁和稀硫酸反应生成的氢气将装置内空气排尽,杂质FeS
与稀硫酸反应生成的HS气体通过NaOH溶液时被吸收,排尽空气后,关闭K 、K ,打开
2 2 3
K ,锥形瓶内生成的气体将硫酸亚铁溶液压至饱和硫酸铵溶液中,硫酸亚铁与硫酸铵溶液
1
混合得到硫酸亚铁铵晶体,反应结束后,关闭K ,打开K 、K ,剩余气体中的HS通过氢
1 2 3 2
氧化钠溶液被吸收。NaOH溶液可与油脂发生皂化反应,可除去铁屑表面的油污,A不符合
题意;硫酸亚铁与硫酸铵溶液混合就能得到硫酸亚铁铵晶体,说明硫酸亚铁、硫酸铵、硫酸
亚铁铵三种物质中,硫酸亚铁铵的溶解度最小,在溶液中先析出,B不符合题意;根据分析,
反应一段时间,待装置内空气排尽,就关闭K 、K ,打开K ,C符合题意;根据分析,铁
2 3 1
屑中有FeS杂质,与酸反应有杂质气体HS生成,利用NaOH溶液除去杂质气体HS,D不
2 2
符合题意。
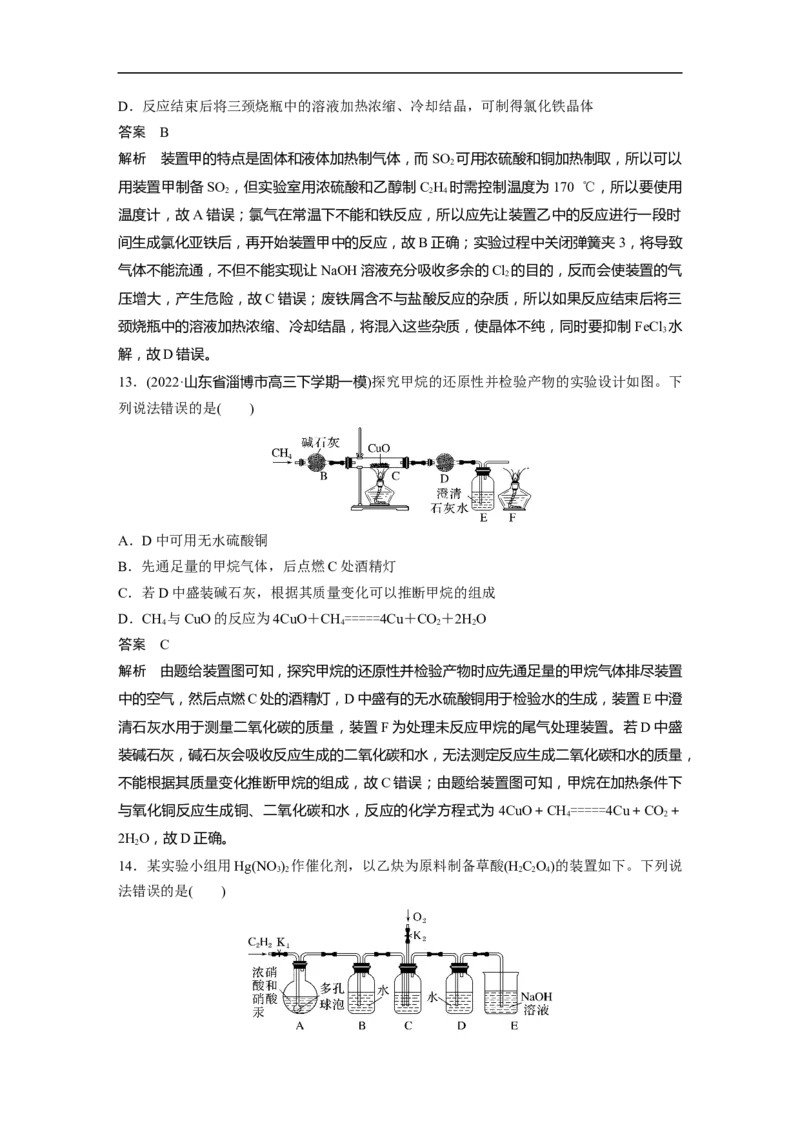
12.氯化铁是有机合成中常用的催化剂,如图是实验室模拟化工厂利用工业废铁屑(杂质不
与盐酸反应)制备催化剂氯化铁的部分装置图,下列相关说法正确的是( )
A.实验室也可以用装置甲制备SO 、C H
2 2 4
B.实验过程中,应先让装置乙中的反应进行一段时间后,再开始装置甲中的反应
C.实验过程中应该关闭弹簧夹3,让装置丙中的NaOH溶液充分吸收多余的Cl
2D.反应结束后将三颈烧瓶中的溶液加热浓缩、冷却结晶,可制得氯化铁晶体
答案 B
解析 装置甲的特点是固体和液体加热制气体,而SO 可用浓硫酸和铜加热制取,所以可以
2
用装置甲制备SO ,但实验室用浓硫酸和乙醇制C H 时需控制温度为170 ℃,所以要使用
2 2 4
温度计,故A错误;氯气在常温下不能和铁反应,所以应先让装置乙中的反应进行一段时
间生成氯化亚铁后,再开始装置甲中的反应,故B正确;实验过程中关闭弹簧夹3,将导致
气体不能流通,不但不能实现让NaOH溶液充分吸收多余的Cl 的目的,反而会使装置的气
2
压增大,产生危险,故C错误;废铁屑含不与盐酸反应的杂质,所以如果反应结束后将三
颈烧瓶中的溶液加热浓缩、冷却结晶,将混入这些杂质,使晶体不纯,同时要抑制 FeCl 水
3
解,故D错误。
13.(2022·山东省淄博市高三下学期一模)探究甲烷的还原性并检验产物的实验设计如图。下
列说法错误的是( )
A.D中可用无水硫酸铜
B.先通足量的甲烷气体,后点燃C处酒精灯
C.若D中盛装碱石灰,根据其质量变化可以推断甲烷的组成
D.CH 与CuO的反应为4CuO+CH=====4Cu+CO+2HO
4 4 2 2
答案 C
解析 由题给装置图可知,探究甲烷的还原性并检验产物时应先通足量的甲烷气体排尽装置
中的空气,然后点燃C处的酒精灯,D中盛有的无水硫酸铜用于检验水的生成,装置E中澄
清石灰水用于测量二氧化碳的质量,装置F为处理未反应甲烷的尾气处理装置。若D中盛
装碱石灰,碱石灰会吸收反应生成的二氧化碳和水,无法测定反应生成二氧化碳和水的质量,
不能根据其质量变化推断甲烷的组成,故C错误;由题给装置图可知,甲烷在加热条件下
与氧化铜反应生成铜、二氧化碳和水,反应的化学方程式为4CuO+CH=====4Cu+CO +
4 2
2HO,故D正确。
2
14.某实验小组用Hg(NO) 作催化剂,以乙炔为原料制备草酸(H C O)的装置如下。下列说
3 2 2 2 4
法错误的是( )A.装置A中使用多孔球泡可加快反应速率
B.装置B、D中得到的溶液可循环使用
C.装置E的作用是吸收氮氧化物和乙炔
D.生成草酸的反应为C H+8HNO=======HC O+8NO +4HO
2 2 3 2 2 4 2 2
答案 C
解析 装置A为反应装置,C H 在硝酸汞的作用下与浓硝酸反应生成HC O 和NO ,NO
2 2 2 2 4 2 2
气体进入B中发生反应:3NO +HO===2HNO +NO,NO进入C中与O 反应生成NO ,
2 2 3 2 2
NO 、O 与D中的水反应生成硝酸,为了能够除尽NO ,防止污染空气,再将装置D中剩
2 2 2
余气体通入装有NaOH溶液的烧杯中,据此分析。多孔球泡可增加C H 与溶液的接触面积,
2 2
加快反应速率,故A正确;根据上述分析,B、D中都有HNO 产生,HNO 可以在装置A
3 3
继续使用,故B正确;装置E吸收的是氮的氧化物,C H 不溶于水,且不能与NaOH溶液
2 2
反应,因此装置E不能吸收C H ,故C错误;C H 与HNO(浓)在硝酸汞作催化剂的条件下
2 2 2 2 3
反应生成草酸和NO ,其反应的化学方程式为C H+8HNO=======HC O+8NO +4HO,
2 2 2 3 2 2 4 2 2
故D正确。