文档内容
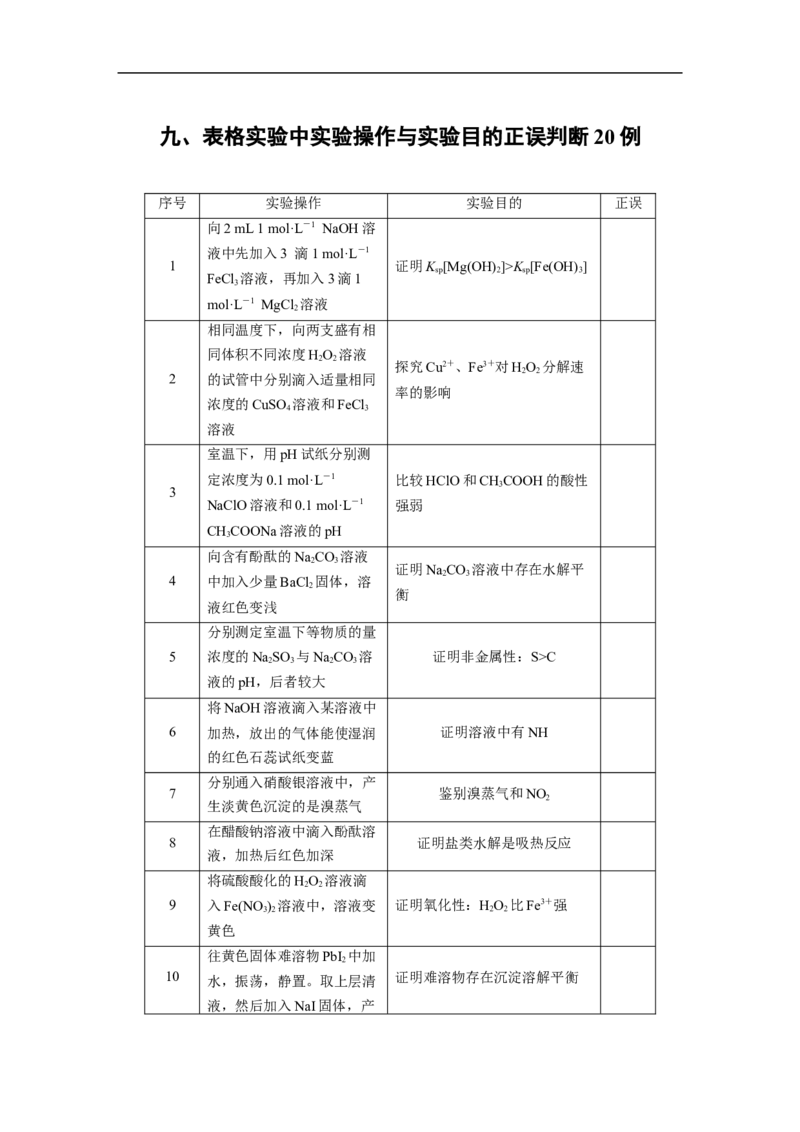
九、表格实验中实验操作与实验目的正误判断 20 例
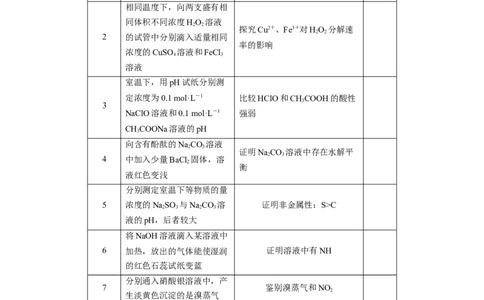
序号 实验操作 实验目的 正误
向2 mL 1 mol·L-1 NaOH溶
液中先加入3 滴1 mol·L-1
1 证明K [Mg(OH) ]>K [Fe(OH) ]
sp 2 sp 3
FeCl 溶液,再加入3滴1
3
mol·L-1 MgCl 溶液
2
相同温度下,向两支盛有相
同体积不同浓度HO 溶液
2 2
探究Cu2+、Fe3+对HO 分解速
2 2
2 的试管中分别滴入适量相同
率的影响
浓度的CuSO 溶液和FeCl
4 3
溶液
室温下,用pH试纸分别测
定浓度为0.1 mol·L-1 比较HClO和CHCOOH的酸性
3
3
NaClO溶液和0.1 mol·L-1 强弱
CHCOONa溶液的pH
3
向含有酚酞的NaCO 溶液
2 3
证明NaCO 溶液中存在水解平
2 3
4 中加入少量BaCl 固体,溶
2
衡
液红色变浅
分别测定室温下等物质的量
5 浓度的NaSO 与NaCO 溶 证明非金属性:S>C
2 3 2 3
液的pH,后者较大
将NaOH溶液滴入某溶液中
6 加热,放出的气体能使湿润 证明溶液中有NH
的红色石蕊试纸变蓝
分别通入硝酸银溶液中,产
7 鉴别溴蒸气和NO
2
生淡黄色沉淀的是溴蒸气
在醋酸钠溶液中滴入酚酞溶
8 证明盐类水解是吸热反应
液,加热后红色加深
将硫酸酸化的HO 溶液滴
2 2
9 入Fe(NO ) 溶液中,溶液变 证明氧化性:HO 比Fe3+强
3 2 2 2
黄色
往黄色固体难溶物PbI 中加
2
10 水,振荡,静置。取上层清 证明难溶物存在沉淀溶解平衡
液,然后加入NaI固体,产生黄色沉淀
向AgCl悬浊液中加入NaI
11 K (AgCl)