文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题04
1.下列指定反应的离子方程式正确的是
A. 向酸性氯化亚铁溶液中加入双氧水:2Fe2++2H++HO=2Fe3++2HO
2 2 2
B. 向Fe (SO ) 溶液中加入NaO:2NaO+2HO=4Na++4OH-+O↑
2 4 3 2 2 2 2 2 2
C. 向Ca(HCO ) 溶液中滴加少量澄清石灰水:Ca2++2HCO 2OH-=CaCO ↓+2HO+CO
3 2 + 3 2
D. 向Fe(NO ) 溶液中加入过量的HI溶液:2NO 8H++6I-=3I +2NO↑+4HO
3 3 + 2 2
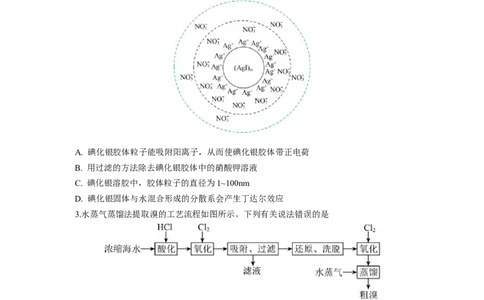
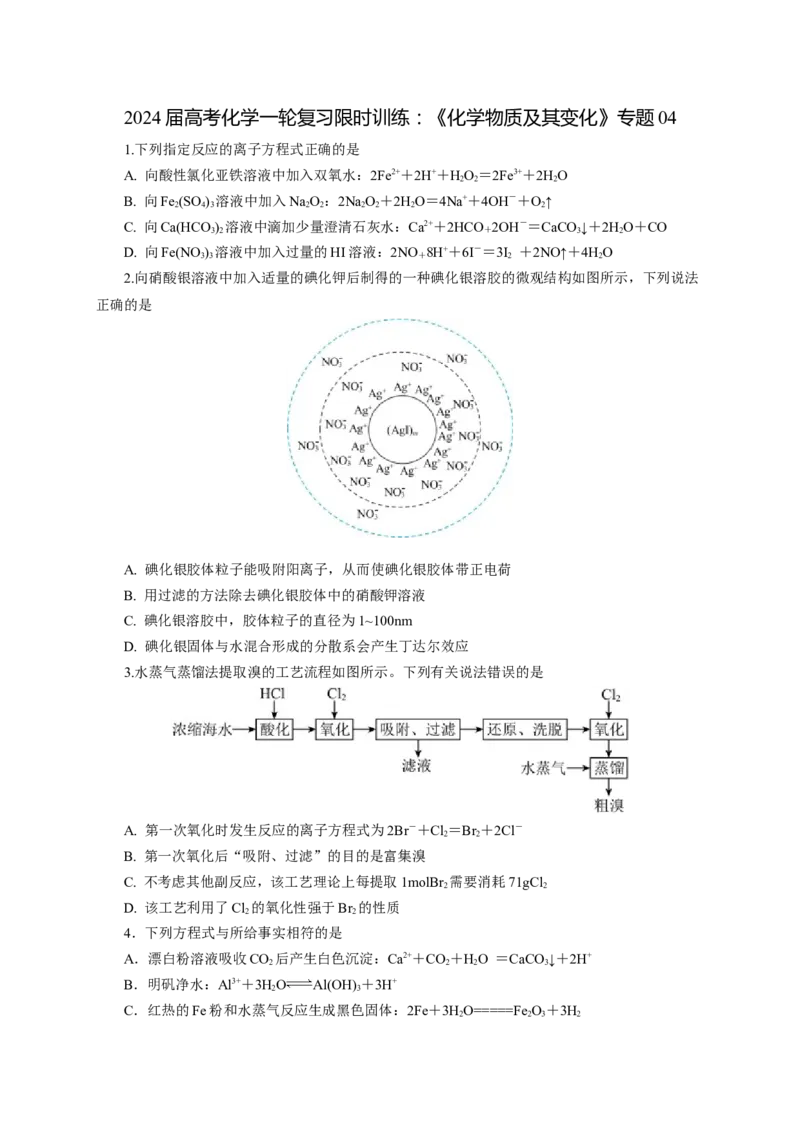
2.向硝酸银溶液中加入适量的碘化钾后制得的一种碘化银溶胶的微观结构如图所示,下列说法
正确的是
A. 碘化银胶体粒子能吸附阳离子,从而使碘化银胶体带正电荷
B. 用过滤的方法除去碘化银胶体中的硝酸钾溶液
C. 碘化银溶胶中,胶体粒子的直径为1~100nm
D. 碘化银固体与水混合形成的分散系会产生丁达尔效应
3.水蒸气蒸馏法提取溴的工艺流程如图所示。下列有关说法错误的是
A. 第一次氧化时发生反应的离子方程式为2Br-+Cl=Br +2Cl-
2 2
B. 第一次氧化后“吸附、过滤”的目的是富集溴
C. 不考虑其他副反应,该工艺理论上每提取1molBr 需要消耗71gCl
2 2
D. 该工艺利用了Cl 的氧化性强于Br 的性质
2 2
4.下列方程式与所给事实相符的是
A.漂白粉溶液吸收CO 后产生白色沉淀:Ca2++CO+HO =CaCO ↓+2H+
2 2 2 3
B.明矾净水:Al3++3HO Al(OH) +3H+
2 3
C.红热的Fe粉和水蒸气反应生成黑色固体:2Fe+3HO=====Fe O+3H
2 2 3 2D.苯酚钠溶液中通入CO 后变浑浊:2 +HO+CO——→2 +NaCO
2 2 2 2 3
5.下列物质的应用中,不涉及氧化还原反应的是
A.饮用水中加入KFeO 消毒 B.NaOH和铝粉的混合物疏通管道
2 4
C.雪天道路上撒盐融雪 D.硫粉除去温度计破碎时洒落的汞
6.下列反应的离子方程式正确的是
A.向FeSO 溶液中滴加HO 溶液:HO+2Fe2+=2Fe3++2H++O↑
4 2 2 2 2 2
B.向H18O中投入NaO 固体:2H18O+2NaO=4Na++4OH-+18O ↑
2 2 2 2 2 2 2
C.向CuSO 溶液通入HS:Cu2++S2-=CuS↓
4 2
D.用醋酸溶解石灰石:2CHCOOH+CaCO =Ca2++2CHCOO-+CO↑+HO
3 3 3 2 2
7.建筑承载着文明。下列建筑材料的主要成分属于合成高分子材料的是
塑料管道 不锈钢 砖瓦 砂石
A B C D
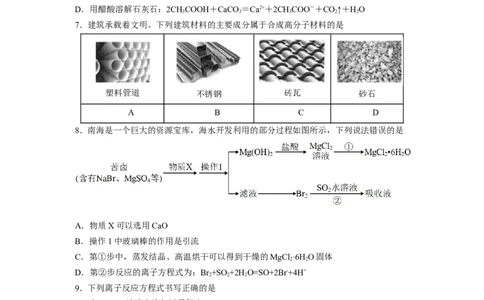
8.南海是一个巨大的资源宝库,海水开发利用的部分过程如图所示,下列说法错误的是
A.物质X可以选用CaO
B.操作1中玻璃棒的作用是引流
C.第①步中,蒸发结晶、高温烘干可以得到干燥的MgCl ·6H O固体
2 2
D.第②步反应的离子方程式为:Br +SO+2H O=SO+2Br-+4H+
2 2 2
9.下列离子反应方程式书写正确的是
A.向AgNO 溶液中滴加过量氨水:Ag++NH·H O=AgOH↓+NH
3 3 2
B.向Ca(ClO) 溶液中通入少量SO :SO +Ca2++2ClO-+H O=CaSO↓+2HClO
2 2 2 2 3
C.向NaHSO 溶液中滴加少量Ba(OH) 溶液:H++SO+Ba2++OH-=BaSO↓+H O
4 2 4 2
D.向甲苯中加入酸性高锰酸钾溶液:5 +6MnO +→5 +6Mn2++14H O
+18H 2
10.下列各组离子一定能大量共存的是
A.在酸性溶液中:K+、Fe2+、Cl-、NO
B.在含大量Fe3+的溶液中:NH、Na+、Cl-、SCN-
C.在pH=13的溶液中:NH、Al3+、NO SO
、D.与铝反应能产生大量氢气的溶液中:Na+、K+、ClO、SO
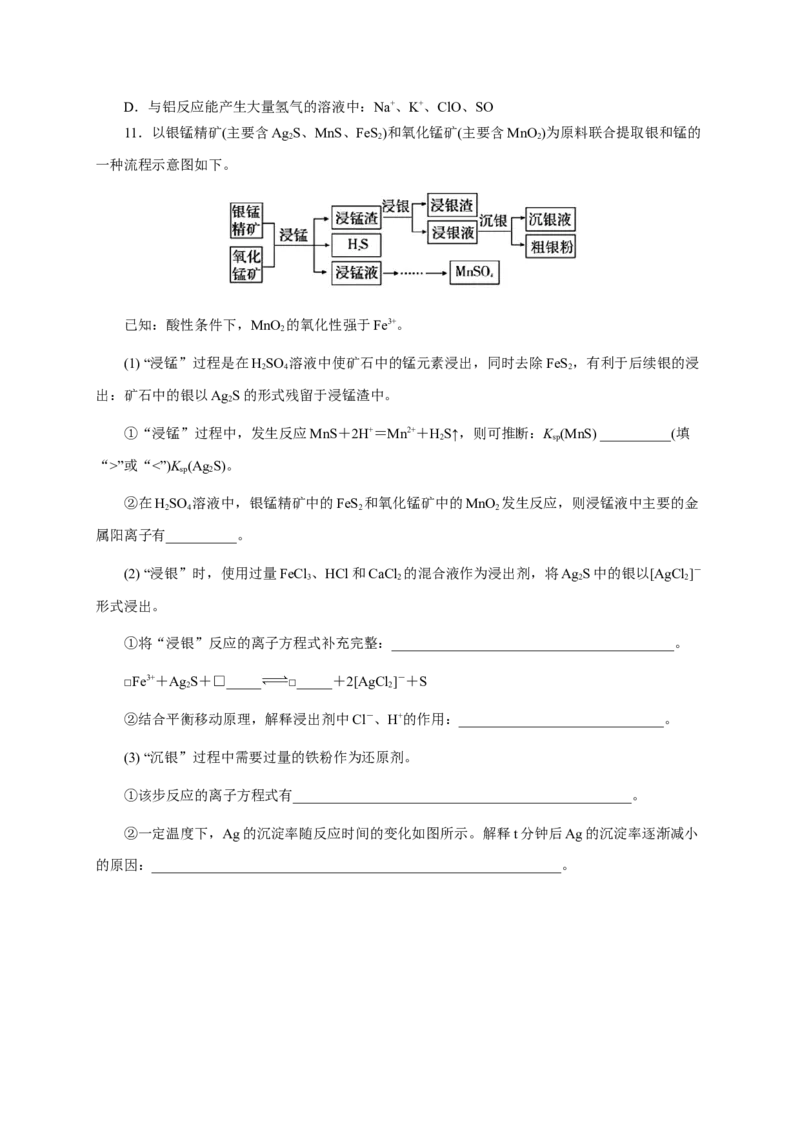
11.以银锰精矿(主要含Ag S、MnS、FeS)和氧化锰矿(主要含MnO )为原料联合提取银和锰的
2 2 2
一种流程示意图如下。
已知:酸性条件下,MnO 的氧化性强于Fe3+。
2
(1) “浸锰”过程是在HSO 溶液中使矿石中的锰元素浸出,同时去除FeS,有利于后续银的浸
2 4 2
出:矿石中的银以Ag S的形式残留于浸锰渣中。
2
①“浸锰”过程中,发生反应MnS+2H+=Mn2++HS↑,则可推断:K (MnS) __________(填
2 sp
“>”或“<”)K (Ag S)。
sp 2
②在HSO 溶液中,银锰精矿中的FeS 和氧化锰矿中的MnO 发生反应,则浸锰液中主要的金
2 4 2 2
属阳离子有__________。
(2) “浸银”时,使用过量FeCl 、HCl和CaCl 的混合液作为浸出剂,将Ag S中的银以[AgCl ]-
3 2 2 2
形式浸出。
①将“浸银”反应的离子方程式补充完整:________________________________________。
□Fe3++Ag S+□_____ □_____+2[AgCl ]-+S
2 2
②结合平衡移动原理,解释浸出剂中Cl-、H+的作用:_____________________________。
(3) “沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有________________________________________________。
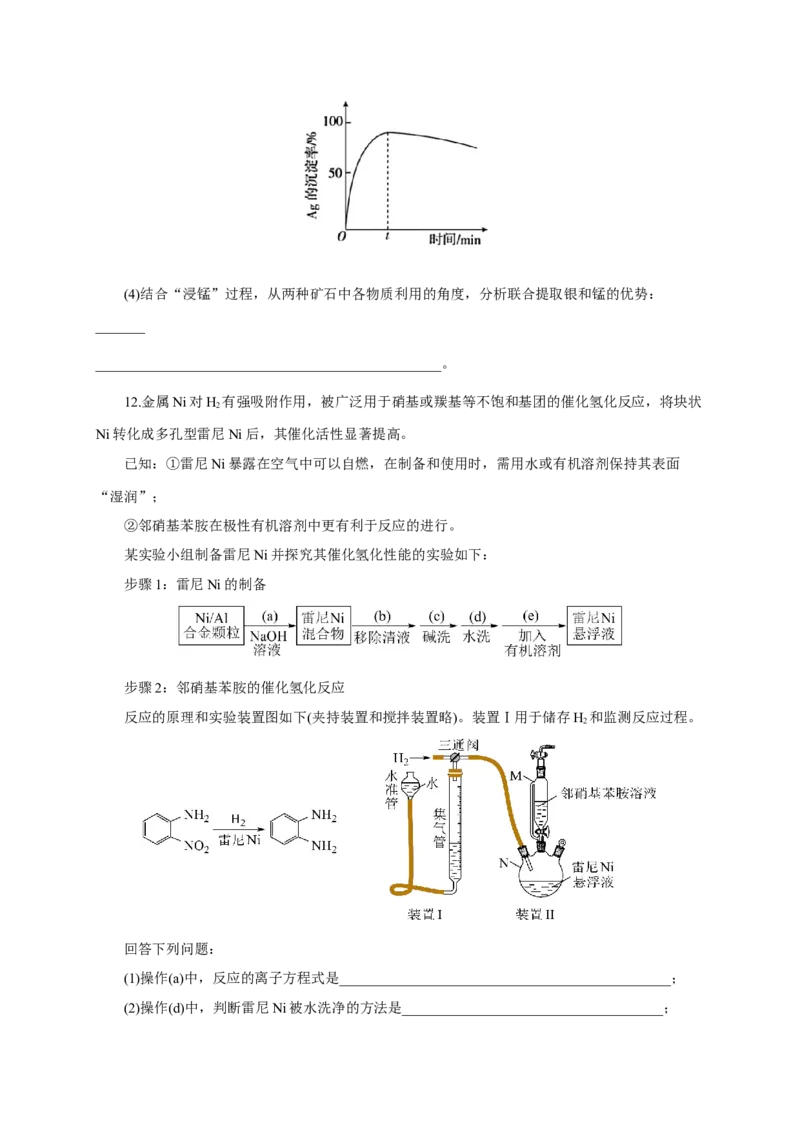
②一定温度下,Ag的沉淀率随反应时间的变化如图所示。解释t分钟后Ag的沉淀率逐渐减小
的原因:__________________________________________________________。(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:
_______
_________________________________________________。
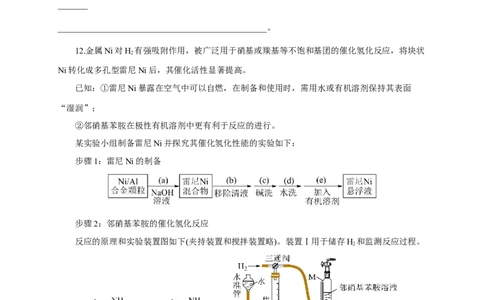
12.金属Ni对H 有强吸附作用,被广泛用于硝基或羰基等不饱和基团的催化氢化反应,将块状
2
Ni转化成多孔型雷尼Ni后,其催化活性显著提高。
已知:①雷尼Ni暴露在空气中可以自燃,在制备和使用时,需用水或有机溶剂保持其表面
“湿润”;
②邻硝基苯胺在极性有机溶剂中更有利于反应的进行。
某实验小组制备雷尼Ni并探究其催化氢化性能的实验如下:
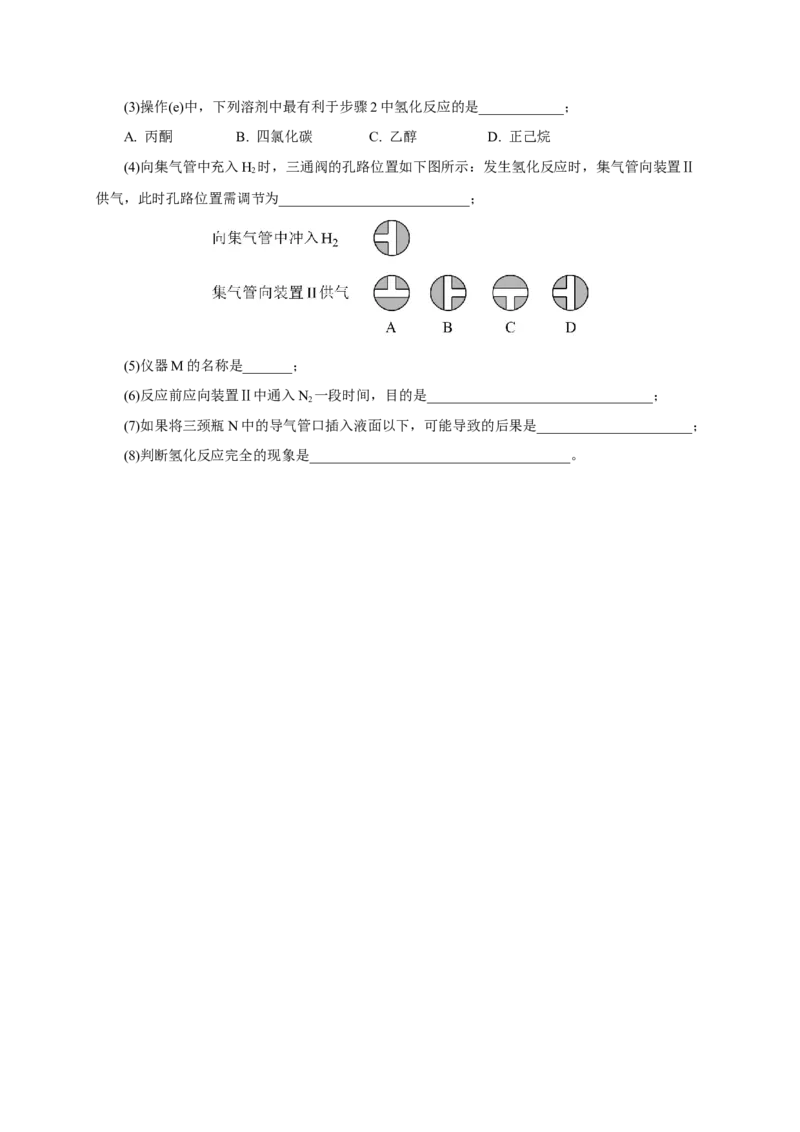
步骤1:雷尼Ni的制备
步骤2:邻硝基苯胺的催化氢化反应
反应的原理和实验装置图如下(夹持装置和搅拌装置略)。装置Ⅰ用于储存H 和监测反应过程。
2
回答下列问题:
(1)操作(a)中,反应的离子方程式是_______________________________________________;
(2)操作(d)中,判断雷尼Ni被水洗净的方法是_____________________________________;(3)操作(e)中,下列溶剂中最有利于步骤2中氢化反应的是____________;
A. 丙酮 B. 四氯化碳 C. 乙醇 D. 正己烷
(4)向集气管中充入H 时,三通阀的孔路位置如下图所示:发生氢化反应时,集气管向装置Ⅱ
2
供气,此时孔路位置需调节为___________________________;
(5)仪器M的名称是_______;
(6)反应前应向装置Ⅱ中通入N 一段时间,目的是________________________________;
2
(7)如果将三颈瓶N中的导气管口插入液面以下,可能导致的后果是______________________;
(8)判断氢化反应完全的现象是_____________________________________。