文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题07
1.下列物质在熔融状态下不导电且属于电解质是
A. Cu B. AlCl C. CaCl D. SiO
3 2 2
答案:B
解析:A.Cu是金属单质,在熔融状态下导电,但不属于电解质,故A不选;
B.AlCl 是共价化合物,在熔融状态下不导电,属于电解质,故B选;
3
C.CaCl 是电解质,在熔融状态下能导电,故C不选;
2
D.SiO 是非电解质,在熔融状态下不导电,故D不选;
2
2.下列方程式正确的是
A. 向硫化钠溶液中滴加过量HSO :2S2-+3HSO =3S↓+2SO 3HO
2 3 2 3 + 2
B. 用碳酸钠溶液处理水垢中的硫酸钙:CO CaSO=CaCO +SO
+ 4 3
C. 以铁为电极电解饱和食盐水:2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2
D.FeO在空气中受热:4FeO+O===2Fe O
2 2 3
答案:B
解析:A.向硫化钠溶液中滴加过量HSO ,其离子方程式为2S2-+HSO =3S↓+HO,故A错
2 3 2 3 2
误;
B.用碳酸钠溶液处理水垢中的硫酸钙,硫酸钙微溶、碳酸钙不溶,应写成化学式的形式,故
其离子方程式为CO CaSO=CaCO +SO,故B正确;
+ 4 3
C.铁为电极电解饱和食盐水,阳极为活泼电极,铁放电生成亚铁离子,而不是氯离子放电,
故C错误;
D.FeO在空气中受热被氧化为四氧化三铁,其方程式为6FeO+O===2Fe O,故D错误;
2 3 4
3.工业上以钛铁矿(FeTiO,其中Fe为+2价)为主要原料制备金属钛的工艺流程如图所示,下列
3
说法不正确的是
A. 为加快“氯化”速率,可将钛铁矿粉碎并与焦炭混合均匀
B.“氯化”过程中,每生成0.1molCO气体,转移电子0.2mol
C.由TiCl 制备Ti的过程中,Ar不可以换成N
4 2
D.理论上,每制得1molTi,需要2molMg
答案:B
解析:氯化发生的反应为:2FeTiO+7Cl+6C=====2FeCl +2TiCl +6CO,得到TiCl ,然后镁和
3 2 3 4 4
四氯化钛反应生成钛和氯化镁,化学方程式为TiCl + 2Mg======Ti+2MgCl 。
4 2A.将钛铁矿粉碎并与焦炭混合均匀,增大反应物的接触面积,可加快“氯化”速率,故A正
确;
B.反应2FeTiO+7Cl+6C=====2FeCl +2TiCl +6CO中,每生成6molCO,转移14mol电子,生
3 2 3 4
成0.1molCO气体,转移电子mol=mol,故B错误;
C.高温下Ti与N 反应,由TiCl 制备Ti的过程中,Ar气不可换成氮气,故C正确;
2 4
D.镁和四氯化钛反应生成钛和氯化镁,化学方程式为TiCl + 2Mg======Ti+2MgCl ,理论上,
4 2
每制得1molTi,需要2molMg,故D正确;
4.下列化合物中,不属于盐的是
A. KClO B. HClO C. (NH )SO D. NaCl
3 4 2 4
答案:B
解析:A.KClO 是由金属阳离子K+与酸根阳离子ClO构成,因此属于盐,A不符合题意;
3
B.HClO在水溶液中电离产生H+、ClO-,因此属于酸,而不属于盐,B符合题意;
C.(NH )SO 是由NH与酸根阴离子SO构成,因此属于盐,C不符合题意;
4 2 4
D.NaCl是由金属阳离子Na+与酸根阳离子Cl-构成,因此属于盐,D不符合题意;
5. 下列反应中,非金属单质只作氧化剂的是
A.Br +2NaOH=NaBr+NaBrO+HO B.2Al+2NaOH+2H O=2NaAlO +3H ↑
2 2 2 2 2
C.C+2CuO===2Cu+CO ↑ D.4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 2 3
答案:D
解析:A、Br 在反应中化合价由0价→+1价和-1价,即Br 既是氧化剂又是还原剂,故A错
2 2
误;B、反应物中没有非金属单质,故B错误;C、C的化合价由0价→+4价,化合价升高,C为
还原剂,故C错误;D、O 的化合价由0价→-2价,化合价降低,O 为氧化剂,故D正确。
2 2
6.下列分散系中,能产生“丁达尔效应”的是:
A. Na SO 溶液 B. NH Cl溶液 C. 石灰乳 D. Fe(OH) 胶体
2 4 4 3
答案:D
解析:胶体能产生“丁达尔效应”,溶液、悬浊液都不能产生“丁达尔效应”,石灰乳属于悬
浊液,故选D。
7.下列离子方程式不正确的是
A.Ba(OH) 溶液中滴加NaHSO 至完全沉淀:Ba2++OH-+H++SO=BaSO ↓+H O
2 4 4 2
B.漂白粉的生产原理:2OH-+Cl=Cl-+ClO-+H O
2 2
C.MnO 与浓盐酸加热:MnO +4H++2Cl-===Mn2++Cl↑+2H O
2 2 2 2
D.AlCl 溶液加入过量的氨水:Al3++3NH·H O=Al(OH) ↓+3NH
3 3 2 3
答案:B
解析:A.Ba(OH) 溶液中滴加NaHSO 至完全沉淀,假设Ba(OH) 物质的量为1mol,则沉淀完
2 4 2
全时,加入1molNaHSO ,此时氢离子和氢氧根离子参与反应物质的量均为1mol,离子方程式正确,
4
故A正确;
B. 氯气与石灰乳反应生成漂白粉,石灰乳不能拆,正确的离子方程式为:Cl+Ca(OH) =Ca2+
2 2+Cl-+ClO-+HO,故B错误;
2
C.MnO 与浓盐酸加热反应生成氯化锰、氯气和水,离子方程式为:MnO +4H++2Cl-
2 2
===Mn2++Cl↑+2HO,故C正确;
2 2
D.AlCl 溶液加入过量的氨水,发生复分解反应,生成氢氧化铝沉淀,氢氧化铝不能溶与弱碱,
3
离子方程式正确,故D正确;
8.关于反应2NaNH +N O=NaN +NaOH+NH ,下列说法正确的是
2 2 3 3
A.NaN 溶液通入CO 可以得到HN (酸性与醋酸相当)
3 2 3
B.氧化剂和还原剂的物质的量之比为2∶1
C.NaN 既是还原产物又是氧化产物
3
D.生成1molNaN ,共转移4mol电子
3
答案:C
解析:A.由HN 的酸性与醋酸相当可知,NaN 溶液通入二氧化碳不可能生成HN ,否则违背
3 3 3
强酸制弱酸的原理,故A错误;
B.由方程式可知,氨基钠中氮元素化合价升高被氧化,一氧化二氮中氮元素化合价降低被还
原,则氧化剂一氧化二氮和还原剂氨基钠的物质的量之比为1∶2,故B错误;
C.由方程式可知,氨基钠中氮元素化合价升高被氧化,一氧化二氮中氮元素化合价降低被还
原,则NaN 既是还原产物又是氧化产物,故C正确;
3
D.由方程式可知,氨基钠中氮元素化合价升高被氧化,一氧化二氮中氮元素化合价降低被还
原,则反应生成1molNaN ,共转移电子的物质的量为1mol××2=mol,故D错误;
3
9.下列离子方程式书写正确的是
A. 用FeS除去废水中的Hg2+:S2-+Hg2+=HgS↓
B. 向饱和食盐水中加浓盐酸析出固体:Na+(aq)+Cl-(aq) NaCl(s)
C. 在NaS溶液中滴加NaClO溶液:S2-+ClO-+2H+=S↓+Cl-+H O
2 2
D. 向血红色Fe(SCN) 溶液中加入过量铁粉至溶液褪色:2Fe3++Fe=3Fe2+
3
答案:B
解析:A.FeS为沉淀不能拆,用FeS除去废水中的Hg2+:FeS+Hg2+ HgS↓+Fe2+,A错误;
B.向饱和食盐水中加浓盐酸,氯离子浓度增大,促使氯离子和钠离子析出氯化钠固体:Na+
(aq)+Cl-(aq) NaCl(s),B正确;
C.在NaS溶液中滴加NaClO溶液发生氧化还原反应生成硫单质和氯离子、同时生成氢氧根
2
离子:S2-+ClO-+H O=S↓+Cl-+2OH-,C错误;
2
D.Fe(SCN) 为络合物不能拆,向血红色Fe(SCN) 溶液中加入过量铁粉至溶液褪色:
3 3
2Fe(SCN) +Fe=6SCN-+3Fe2+,D错误;
3
10. 2022年,在卡塔尔举办的世界杯备受全世界瞩目。下列说法错误的是
A. 开幕式的绚丽烟花利用的“焰色试验”是物理变化
B. 运动员需要补充的NaCl溶液是电解质
C. 制作奖杯的材料之一18K 金是合金D. 足球赛服材料聚酯纤维属于有机高分子材料
答案:B
解析:A.“焰色试验”过程中没有产生新物质,所以开幕式的绚丽烟花利用的“焰色试验”
是物理变化,A正确;
B.氯化钠是电解质,运动员需要补充的NaCl溶液属于混合物,不是电解质,也不是非电解质,
B错误;
C.18k金是黄金含量至少达到75%的合金,因此制作奖杯的材料之一18K金是合金,C正确;
D.聚酯纤维面料由有机二元酸和二元醇缩聚而成的聚酯经纺丝所得的合成纤维,因此足球赛
服材料聚酯纤维属于有机高分子材料,D正确;
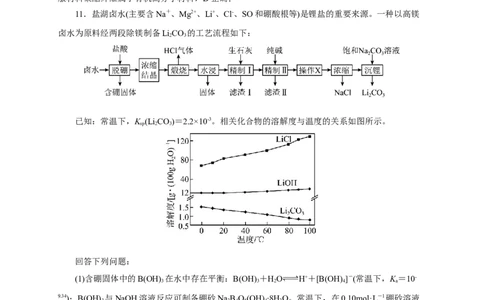
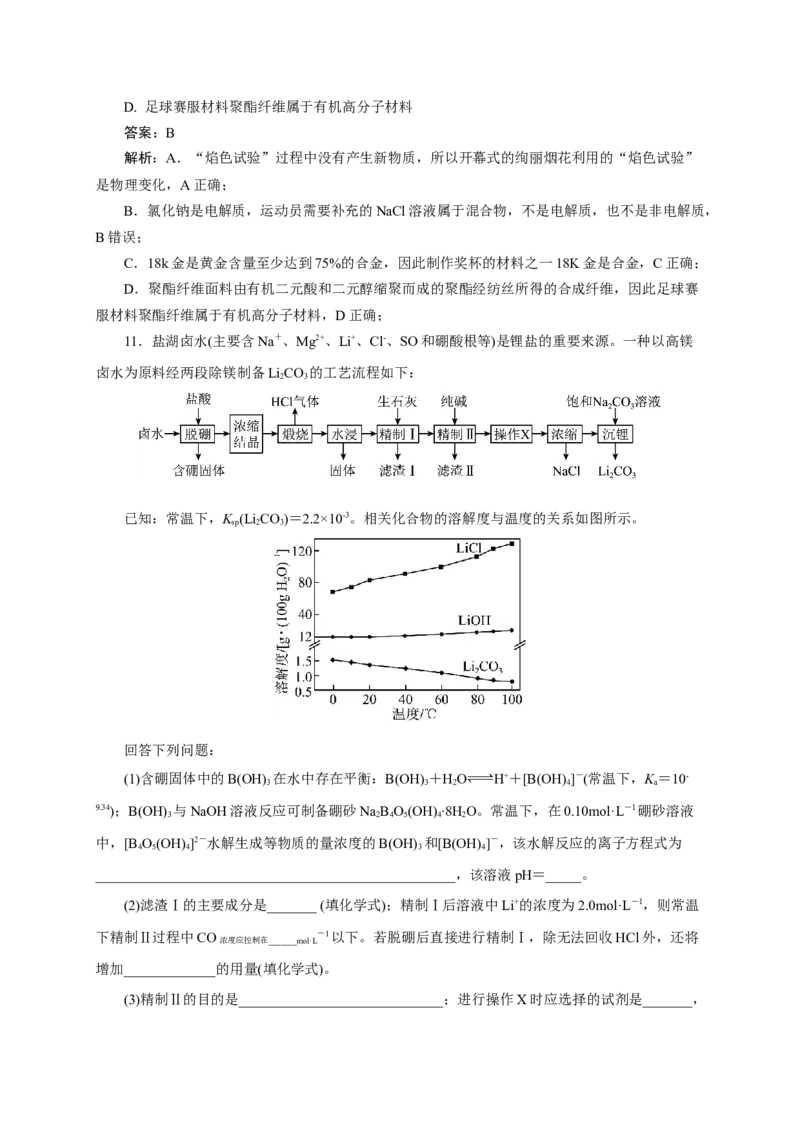
11.盐湖卤水(主要含Na+、Mg2+、Li+、Cl-、SO和硼酸根等)是锂盐的重要来源。一种以高镁
卤水为原料经两段除镁制备LiCO 的工艺流程如下:
2 3
已知:常温下,K (Li CO)=2.2×10-3。相关化合物的溶解度与温度的关系如图所示。
sp 2 3
回答下列问题:
(1)含硼固体中的B(OH) 在水中存在平衡:B(OH) +HO H++[B(OH) ]-(常温下,K=10-
3 3 2 4 a
9.34);B(OH) 与NaOH溶液反应可制备硼砂NaB O(OH) ∙8HO。常温下,在0.10mol·L-1硼砂溶液
3 2 4 5 4 2
中,[B O(OH) ]2-水解生成等物质的量浓度的B(OH) 和[B(OH) ]-,该水解反应的离子方程式为
4 5 4 3 4
___________________________________________________,该溶液pH=_____。
(2)滤渣Ⅰ的主要成分是_______ (填化学式);精制Ⅰ后溶液中Li+的浓度为2.0mol·L-1,则常温
下精制Ⅱ过程中CO -1以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将
浓度应控制在_______mol·L
增加_____________的用量(填化学式)。
(3)精制Ⅱ的目的是_____________________________;进行操作X时应选择的试剂是_______,若不进行该操作而直接浓缩,将导致_____________________________。
答案:(1) [B O(OH) ]2-+5HO=2B(OH) +2[B(OH) ]- 9.34
4 5 4 2 3 4
(2)CaSO 5.5×10-4 纯碱
4
(3)加入纯碱将精制Ⅰ所得滤液中的Ca2+转化为CaCO (或除去精制Ⅰ所得滤液中的Ca2+),提高
3
LiCO 纯度 盐酸 浓缩液中因CO +过早沉淀,即浓缩结晶得到的NaCl中会混有
2 3 浓度过大使得Li
LiCO,最终所得LiCO 的产率减小
2 3 2 3
解析:由流程可知,卤水中加入盐酸脱镁后过滤,所得滤液经浓缩结晶后得到晶体,该晶体中
含有Na+、Li+、Cl-、SO等,焙烧后生成HCl气体;烧渣水浸后过滤,滤液中加生石灰后产生沉淀,
在此条件下溶解度最小的是CaSO,则滤渣Ⅰ的主要成分为CaSO;由于CaSO 微溶于水,精制Ⅰ
4 4 4
所得滤液中再加纯碱又生成沉淀,则滤渣Ⅱ为CaCO ;精制Ⅱ所得滤液经操作X后,所得溶液经浓
3
缩结晶、过滤得到氯化钠,浓缩后的滤液中加入饱和碳酸钠溶液沉锂,得到LiCO。
2 3
(1)含硼固体中的B(OH) 在水中存在平衡:B(OH) +HO [B(OH) ]-+H+ (常温下,K=10-
3 3 2 4
9.34);B(OH) 与NaOH溶液反应可制备硼砂NaB O(OH) ∙8HO。常温下.在0.10mol·L-1硼砂溶液中,
3 2 4 5 4 2
[B O(OH) ]2-水解生成等物质的量浓度的B(OH) 和[B(OH) ]-,该水解反应的离子方程式为
4 5 4 3 4
[B O(OH) ]2-+5HO=2B(OH) +2[B(OH) ]-,由B元素守恒可知,B(OH) 和[B(OH) ]-的浓度均为
4 5 4 2 3 4 3 4
0.20mol·L-1,K==c(H+)=10-9.34,则该溶液pH=9.34。
(2)由分析可知,滤渣I的主要成分是CaSO;精制I后溶液中Li+的浓度为2.0mol·L-1,由
4
K (LiCO)=2.2×10-3可知,则常温下精制Ⅱ过程中CO mol·L-1=5.5×10-4mol·L-1以下。若
sp 2 3 浓度应控制在
脱硼后直接进行精制Ⅰ,除无法回收HCl外,后续在浓缩结晶时将生成更多的氯化钠晶体,因此,
还将增加纯碱(Na CO)的用量。
2 3
(3)精制Ⅰ中,烧渣水浸后的滤液中加生石灰后产生的滤渣Ⅰ的主要成分为CaSO;由于CaSO
4 4
微溶于水,精制Ⅰ所得滤液中还含有一定浓度的Ca2+,还需要除去Ca2+,因此,精制Ⅱ的目的是:
加入纯碱将精制Ⅰ所得滤液中的Ca2+转化为CaCO (或除去精制Ⅰ所得滤液中的Ca2+),提高LiCO
3 2 3
纯度。操作X是为了除去剩余的碳酸根离子,为了防止引入杂质离子,应选择的试剂是盐酸;加入
盐酸的目的是除去剩余的碳酸根离子,若不进行该操作而直接浓缩,将导致浓缩液中因CO
浓度过大使
+过早沉淀,即浓缩结晶得到的NaCl中会混有LiCO,最终所得LiCO 的产率减小。
得Li 2 3 2 3
12.实验室模拟“镁法工业烟气脱硫”并制备MgSO ∙HO,其实验过程可表示为
4 2
(1)在搅拌下向氧化镁浆料中匀速缓慢通入SO 气体,生成MgSO ,反应为Mg(OH) +HSO =
2 3 2 2 3MgSO +2HO,其平衡常数K与K [Mg(OH) ]、K (MgSO )、K (H SO )、K (H SO )的代数关系式
3 2 sp 2 sp 3 a1 2 3 a2 2 3
为K=___________;下列实验操作一定能提高氧化镁浆料吸收SO 效率的有___________(填序号)。
2
A.水浴加热氧化镁浆料 B.加快搅拌速率
C.降低通入SO 气体的速率 D.通过多孔球泡向氧化镁浆料中通SO
2 2
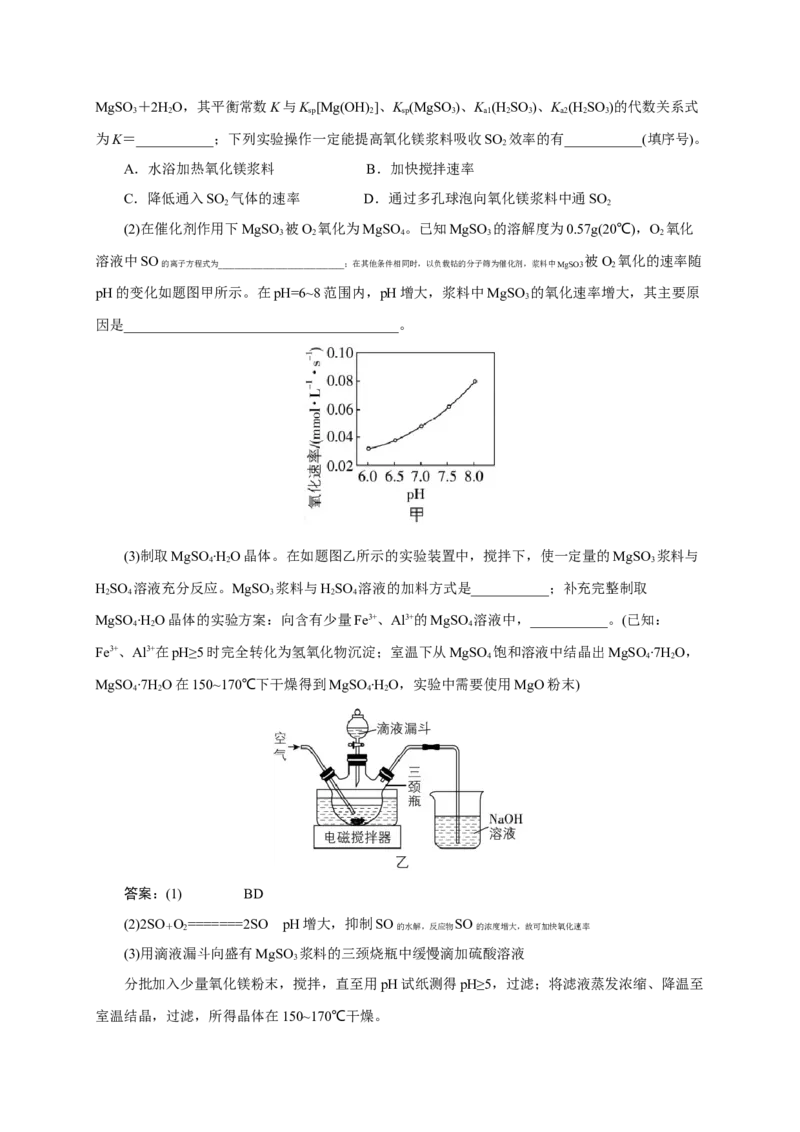
(2)在催化剂作用下MgSO 被O 氧化为MgSO 。已知MgSO 的溶解度为0.57g(20℃),O 氧化
3 2 4 3 2
溶液中SO 被O 氧化的速率随
的离子方程式为_______________________________;在其他条件相同时,以负载钴的分子筛为催化剂,浆料中MgSO3 2
pH的变化如题图甲所示。在pH=6~8范围内,pH增大,浆料中MgSO 的氧化速率增大,其主要原
3
因是_______________________________________。
(3)制取MgSO ∙HO晶体。在如题图乙所示的实验装置中,搅拌下,使一定量的MgSO 浆料与
4 2 3
HSO 溶液充分反应。MgSO 浆料与HSO 溶液的加料方式是___________;补充完整制取
2 4 3 2 4
MgSO ∙HO晶体的实验方案:向含有少量Fe3+、Al3+的MgSO 溶液中,___________。(已知:
4 2 4
Fe3+、Al3+在pH≥5时完全转化为氢氧化物沉淀;室温下从MgSO 饱和溶液中结晶出MgSO ∙7HO,
4 4 2
MgSO ∙7HO在150~170℃下干燥得到MgSO ∙HO,实验中需要使用MgO粉末)
4 2 4 2
答案:(1) BD
(2)2SO O=======2SO pH增大,抑制SO SO
+ 2 的水解,反应物 的浓度增大,故可加快氧化速率
(3)用滴液漏斗向盛有MgSO 浆料的三颈烧瓶中缓慢滴加硫酸溶液
3
分批加入少量氧化镁粉末,搅拌,直至用pH试纸测得pH≥5,过滤;将滤液蒸发浓缩、降温至
室温结晶,过滤,所得晶体在150~170℃干燥。解析:本实验的目的是为了制取MgSO ∙HO,首先在搅拌下向氧化镁浆料中匀速缓慢通入SO
4 2 2
气体,生成MgSO ,然后使一定量的MgSO 浆料与HSO 溶液充分反应生成硫酸镁,在硫酸镁的
3 3 2 4
溶液中加入氧化镁调节溶液的pH除去三价铁和三价铝,将滤液蒸发浓缩、降温至室温结晶,过滤,
所得晶体在150~170℃干燥即可得到MgSO ∙HO;
4 2
(1)已知下列反应:
①Mg(OH) +HSO =MgSO +2HO K
2 2 3 3 2
②Mg(OH) (s) Mg2+(aq)+2OH-(aq) K [Mg(OH) ]
2 sp 2
③MgSO (s) Mg2+(aq)+SO K (MgSO )
3 (aq) sp 3
④HSO H++HSO K (H SO )
2 3 ; a1 2 3
⑤HSO H++SO K (H SO )
; a2 2 3
⑥HO H++OH- ;K
2 w
根据盖斯定律,①=②-③+④+⑤-⑥×2,故K=
;
A.加热可加快反应速率,但温度升高,SO 在水中溶解度降低,且会导致HSO 受热分解,
2 2 3
不一定能提高吸收SO 效率,A错误;
2
B.加快搅拌速率,可以使反应物充分接触,提高吸收SO 效率,B正确;
2
C.降低通入SO 气体的速率,SO 可与MgO浆料充分接触,但会降低反应速率,不一定能提
2 2
高吸收SO 效率,C错误;
2
D.多孔球泡可以让SO 与MgO浆料充分接触,能提高吸收SO 效率,D正确;
2 2
(2)根据题意,O 氧化溶液中的SO SO SO,1molO 氧化2mol SO 氧化溶液中SO
2 , 被氧化为 2 ,故O2 的离
SO O=======2SO;
子方程式为:2 + 2
pH增大,抑制SO SO
的水解,反应物 的浓度增大,故可加快氧化速率;
(3)在进行含固体物质的反应物与液体反应的实验时,应将含固体物质的反应物放在三颈瓶中,
通过滴液漏斗滴加液体,HSO 溶液的滴加速率要慢,以免HSO 过量;
2 4 2 4
根据题意,首先需要调节pH≥5以除去Fe3+、Al3+杂质,需要用到的试剂为MgO粉末,操作细节为
分批加入少量MgO粉末,以免pH过高,不断搅拌进行反应直至检测到pH≥5,然后过滤除去氢氧
化铁、氢氧化铝沉淀;接着需要从溶液中得到MgSO ∙HO,根据题目信息,室温下结晶只能得到
4 2
MgSO ∙7HO,因此需要在150~170℃下干燥得到MgSO ∙HO,操作细节为将滤液蒸发浓缩、降温
4 2 4 2
至室温结晶,过滤,所得晶体在150~170℃干燥。