文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题08
1.下列离子方程式书写正确的是
A. 用饱和碳酸钠除去乙酸乙酯中的少量乙酸:2CHCOOH+CO COO-+CO ↑+H O
3 =2CH3 2 2
B. 硫氢化钠溶液与稀硫酸混合有气泡产生:HS-+SO+7H+=2SO↑+4H O
2 2
C. 将碳酸氢钙溶液与过量的澄清石灰水混合:Ca2++HCO -=CaCO ↓+H O
+OH 3 2
D. 向HO 溶液中滴加少量FeCl :2Fe3++H O=O ↑+2H++2Fe2+
2 2 3 2 2 2
2.汽车发生剧烈碰撞时,安全气囊中迅速发生反应:10NaN +2KNO=KO+5NaO+16N↑。
3 3 2 2 2
下列说法正确的是
A. 该反应中KNO 是还原剂
3
B. 氧化产物与还原产物的物质的量之比为15∶1
C. 若设计成原电池,KNO 在负极上反应
3
D. 每转移1mole-,可生成2.24LN
2
3.下列离子方程式书写正确的是
A.NaHCO 溶液的水解:HCO HO CO HO+
3 + 2 + 3
B. 向Al (SO ) 溶液中滴加NaCO 溶液:2Al3++3CO Al (CO)↓
2 4 3 2 3 = 2 3 3
C. 向Fe (SO ) 溶液中通入足量HS:2Fe3++S2-=2Fe2++S↓
2 4 3 2
D. 向Ca(ClO) 溶液中通入少量SO :Ca2++3ClO-+HO+SO =Cl-+CaSO↓+2HClO
2 2 2 2 4
4.下列物质中常作耐高温材料的碱性氧化物是
A. K O B. SiO C.Al O D. MgO
2 2 2 3
5.关于反应2Fe(CO) +7NO=2FeO+14NO+10CO,下列说法正确的是
5 2 4 2
A. N O 发生氧化反应 B. 生成1molCO ,转移2mol电子
2 4 2
C. 氧化产物与还原产物的物质的量之比为5∶7 D. FeO 可以和Fe反应生成Fe O
2 2 3
6. 下列反应的离子方程式正确的是
A. Na O 加入到足量的HO中:NaO+HO=2Na++2OH-+O↑
2 2 2 2 2 2 2
B. 少量澄清石灰水与足量Ca(HCO ):Ca2++OH-+HCO CaCO ↓+HO
3 2 = 3 2
C. 过量铁粉加入稀硝酸:Fe+4H++NO Fe3++NO↑+2HO
= 2
D. 水中通入氯气:Cl+HO 2H++Cl-+ClO-
2 2
7.下列叙述不涉及氧化还原反应的是
A. 海水提溴 B. 苏打用作食用碱
C. 谷物发酵酿酒 D. 漂白粉久置空气中失效
8.下列消毒剂的有效成分属于盐的是
A. 高锰酸钾溶液 B. 过氧乙酸溶液 C. 双氧水 D. 医用酒精
9.某工业废水中可能含有K+、Ag+、Mg2+、Cu2+、Al3+、NH、Cl-、CO NO SO、I-中的几种,
、 、
且各离子物质的量浓度均为0.2mol/L(忽略水的电离及离子的水解),欲探究废水的组成,进行了如
下实验:I.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加
II.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰
III.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇到空气变为红棕色
IV.向III中所得溶液中加入BaCl 溶液,有白色沉淀生成。
2
下列推断不正确的是
A. 溶液中一定不含的阳离子是K+、NH、Cu2+、Ag+
B. III中加入盐酸生成无色气体的离子方程式为:8H++6I-+2NO +2NO↑+4HO
=3I2 2
C. 原溶液除H+和OH-外只含有Mg2+、Al3+、NO SO、I-
、
D. 另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤、洗涤、灼烧沉淀至恒重,
得到固体质量0.8g
10. 能正确表示下列反应的离子方程式的是
A. 小苏打溶液与过量盐酸混合:CO +=CO↑+H O
+2H 2 2
B. 用铁电极电解饱和食盐水:2C1-+2H O=====Cl↑+H ↑+2OH-
2 2 2
C. Fe(NO ) 溶液中通入足量SO :Fe3++3NO +4H O=Fe2++3NO↑+5SO+8H+
3 3 2 +5SO2 2
D. 硫酸铜溶液中加入过量氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
3 2 2
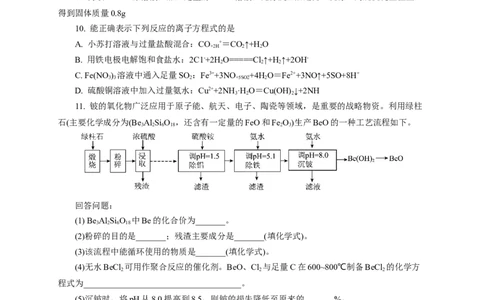
11. 铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用绿柱
石(主要化学成分为(Be Al Si O ,还含有一定量的FeO和Fe O)生产BeO的一种工艺流程如下。
3 2 6 18 2 3
回答问题:
(1) Be Al Si O 中Be的化合价为_______。
3 2 6 18
(2)粉碎的目的是_______;残渣主要成分是_______(填化学式)。
(3)该流程中能循环使用的物质是_______(填化学式)。
(4)无水BeCl 可用作聚合反应的催化剂。BeO、Cl 与足量C在600~800℃制备BeCl 的化学方
2 2 2
程式为_____________________________________。
(5)沉铍时,将pH从8.0提高到8.5,则铍的损失降低至原来的_______%。
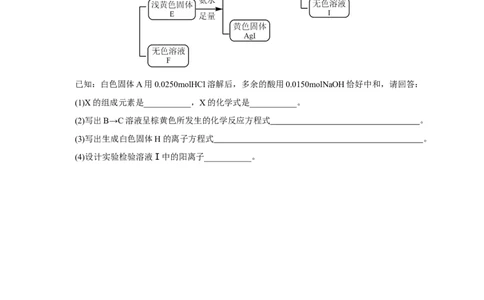
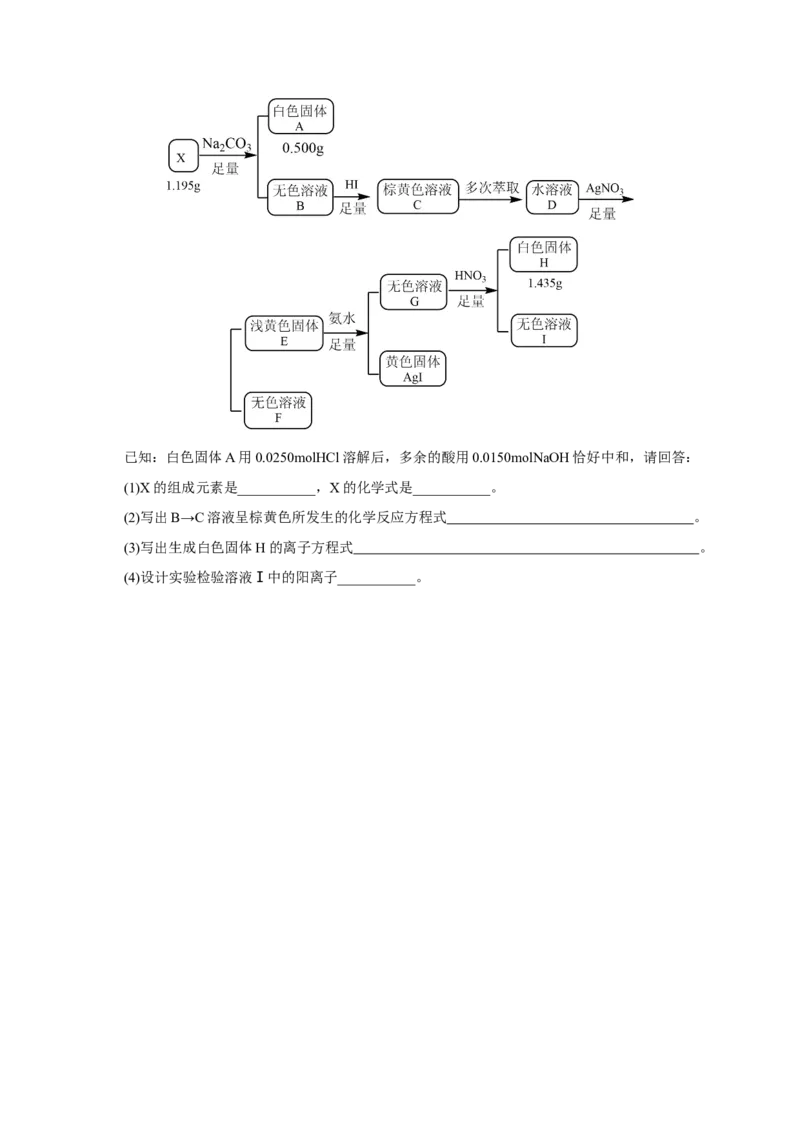
12.化合物X由三种元素组成,某学习小组按如下流程进行实验:已知:白色固体A用0.0250molHCl溶解后,多余的酸用0.0150molNaOH恰好中和,请回答:
(1)X的组成元素是___________,X的化学式是___________。
(2)写出B→C溶液呈棕黄色所发生的化学反应方程式 。
(3)写出生成白色固体H的离子方程式 。
(4)设计实验检验溶液Ⅰ中的阳离子___________。