文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题11
1.能正确表示下列反应的离子方程式是
A. 硫化亚铁和过量硝酸混合:FeS+2H+=Fe2++HS↑
2
B. 向FeBr 溶液中通入等物质的量的Cl:2Br-+Cl=Br +2Cl-
2 2 2 2
C. NaHCO 溶液中通入足量SO :CO 2SO +HO=2HSO CO
3 2 + 2 2 + 2
D. 等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO=
2 4 4
BaSO↓+2HO
4 2
答案:D
解析:A.硫化亚铁和过量硝酸混合会发生氧化还原反应,发生反应为:FeS+4H++NO
=
Fe3++NO↑+S↓+2HO,故A错误;
2
B.因为还原性是Fe2+ >Br-,向FeBr 溶液中通入等物质的量的Cl,Cl 会与Fe2+和Br-都反应,
2 2 2
离子反应为:2Fe2++2Br-+2Cl=2Fe3++Br +4Cl-,故B错误;
2 2
C.NaHCO 中HCO HCO SO =HSO CO,故C错误;
3 不能拆,离子反应为: + 2 + 2
D.等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合,则NH HSO 过量,
2 4 4 4 4
Ba(OH) 完全反应,离子方程式正确,故D正确;
2
2.含共价键的强电解质的是
A. MgCl B. NaHSO C. NH D. CH COOH
2 4 3 3
答案:B
解析:强电解质:在水溶液中或熔融状态下能完全电离的化合物;弱电解质:在水溶液中不能
完全电离的化合物。相邻原子之间通过共用电子对形成的化学键为共价键,据此判断。
A.氯化镁只含离子键,A错误;
B.硫酸氢钠是在水溶液中或熔融状态下能完全电离的化合物,属于强电解质,钠离子与硫酸
氢根离子之间存在离子键,硫酸氢根离子内氧原子与硫原子、氢原子和氧原子之间存在共价键,B
正确;
C.氨气为非电解质,C错误;
D.醋酸在水溶液中只能部分电离,属于弱电解质,D错误;
3.关于反应:FeS+7Fe (SO )+8HO=15FeSO +8HSO ,下列说法不正确的是
2 2 4 3 2 4 2 4
A.Fe (SO ) 中Fe在反应中得到电子 B.HO既不是氧化剂也不是还原剂
2 4 3 2
C.消耗0.2molFeS,转移2.8mol电子 D.氧化产物和还原产物物质的量之比8∶15
2
答案:D
解析:A.反应中,Fe元素的化合价由Fe (SO ) 中的+3价降至FeSO 中的+2价,Fe (SO )
2 4 3 4 2 4 3
中Fe元素化合价降低,在反应中得到电子,被还原,A项正确;
B.反应前后,HO中H、O元素的化合价都没有变化,HO既不是氧化剂也不是还原剂,B
2 2
项正确;
C.反应中,S元素的化合价由FeS 中的-1价升至SO中的+6价,1molFeS 参与反应转移
2 214mol电子,则消耗0.2molFeS 转移电子物质的量为0.2mol×14=2.8mol,C项正确;
2
D.反应中,Fe元素的化合价由Fe (SO ) 中的+3价降至FeSO 中的+2价,Fe (SO ) 是氧化剂,
2 4 3 4 2 4 3
FeSO 是还原产物,1molFe (SO ) 参与反应得到2mol电子生成2molFeSO ,S元素的化合价由FeS
4 2 4 3 4 2
中的-1价升至SO中的+6价,FeS 是还原剂,SO是氧化产物,1molFeS 参与反应失去14mol电子
2 2
生成2mol SO,根据得失电子守恒,氧化产物与还原产物物质的量之比为1∶7,D项错误;
4.下列反应的离子方程式书写正确的是
A.NaSO 溶液中滴加稀硝酸:SO 2H+=S↓+SO ↑+HO
2 2 3 2 + 2 2
B.NaAlO 溶液中加入足量Ca(HCO ) 溶液:AlO+HCO HO=Al(OH) ↓+CO
2 3 2 + 2 3
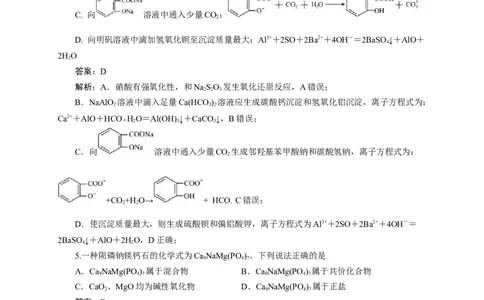
C. 向 溶液中通入少量CO:
2
D. 向明矾溶液中滴加氢氧化钡至沉淀质量最大:Al3++2SO+2Ba2++4OH-=2BaSO↓+AlO+
4
2HO
2
答案:D
解析:A.硝酸有强氧化性,和NaSO 发生氧化还原反应,A错误;
2 2 3
B.NaAlO 溶液中滴入足量Ca(HCO ) 溶液应生成碳酸钙沉淀和氢氧化铝沉淀,离子方程式为:
2 3 2
Ca2++AlO+HCO HO=Al(OH) ↓+CaCO↓,B错误;
+ 2 3 3
C.向 溶液中通入少量CO 生成邻羟基苯甲酸钠和碳酸氢钠,离子方程式为:
2
+CO +H O→ + HCO C错误;
2 2 ,
D.使沉淀质量最大,则生成硫酸钡和偏铝酸钾,离子方程式为Al3++2SO+2Ba2++4OH-=
2BaSO↓+AlO+2HO,D正确;
4 2
5.一种陨磷钠镁钙石的化学式为Ca NaMg(PO)。下列说法正确的是
9 4 7
A.Ca NaMg(PO) 属于混合物 B.Ca NaMg(PO) 属于共价化合物
9 4 7 9 4 7
C.CaO、MgO均为碱性氧化物 D.Ca NaMg(PO) 属于正盐
2 9 4 7
答案:D
解析:A.Ca NaMg(PO) 属于纯净物,故A错误;
9 4 7
B.Ca NaMg(PO) 属于离子化合物,故B错误;
9 4 7
C.CaO 属于过氧化物,MgO为碱性氧化物,故C错误;
2
D.Ca NaMg(PO) 属于正盐,故D正确;
9 4 7
6.关于反应2KMnO +2KF+10HF+3HO=2 K MnF +8HO+3O,下列说法正确的是
4 2 2 2 6 2 2
A. KF和HF均发生氧化反应 B. H O 是还原剂
2 2
C. 转移3mol电子,1mol KMnO 被氧化 D. K MnF 既是氧化产物又是还原产物
4 2 6
答案:B解析:A.该反应中KF和HF都没有化合价变化,没有发生氧化反应,A错误;
B.HO 中的氧元素化合价升高,是还原剂,B正确;
2 2
C.该反应中转移3mol电子,1mol KMnO 被还原,不是被氧化,C错误;
4
D.锰元素化合价降低,故KMnF 是还原产物,氧气为氧化产物,D错误;
2 6
7. 下列反应的离子方程式正确的是
A. 铜与浓硫酸(98.3%)加热下反应:Cu+2HSO (浓)===Cu2++SO+SO ↑+2HO
2 4 2 2
B. 用惰性电极电解饱和ZnCl 溶液:Zn2++2Cl-+2HO=====Zn(OH) ↓+Cl↑+H↑
2 2 2 2 2
C. 向含0.1mol[Co(NH )Cl]Cl 的溶液中加入含0.3mol AgNO 的溶液:[Co(NH )Cl]2++2Cl-+
3 2 3 3 5
3Ag+=[Co(NH )Cl]3++3AgCl↓
3 5
D. 向酸性重铬酸钾溶液中加少量乙醇溶液:2Cr O+3C HOH+16H+=4Cr3++3CHCOOH+
2 2 5 3
11HO
2
答案:BD
解析:A.98.3%的浓硫酸中含的水太少,则生成的CuSO 不能电离,选项A错误;
4
B.用惰性电极电解饱和氯化锌溶液,阳极反应式为2Cl - -2e- = Cl ↑,阴极反应为:2HO+ 2e-
2 2
=H↑+2OH-,总反应为Zn2++2Cl-+2HO=====Zn(OH) ↓+Cl↑+H↑,选项B正确;
2 2 2 2 2
C.配合物中内界不可以电离,外界可以电离,则只能生成0.2mol AgCl,离子方程式为C1- +
Ag+ = AgCl↓,选项C错误;
D.向酸性重铬酸钾溶液中加少量乙醇溶液,乙醇被氧化为乙酸,离子方程式为2Cr O+
2
3C HOH+16H+=4Cr3++3CHCOOH+11HO,选项D正确;
2 5 3 2
8. 古文献《余冬录》中对胡粉[主要成分为2PbCO ∙Pb(OH)]制法的相关描述:“铅块悬酒缸内,
3 2
封闭四十九日,开之则化为粉矣。化不白者(Pb),炒为黄丹(Pb O)。黄丹滓为密陀僧(PbO)”。下列
3 4
说法错误的是
A. Pb O 属于氧化物 B.黄丹与盐酸反应只生成PbCl 和水
3 4 2
C. 铅块制胡粉的过程中发生了氧化还原反应 D. 密陀僧与一氧化碳高温加热可以制得铅
答案:B
解析:A.Pb O 属于氧化物,A正确;
3 4
B.Pb O 中铅的化合价是+2和+4,+4价铅可以将盐酸氧化为氯气,所以与盐酸反应生成的不
3 4
只有PbCl 和水,B错误;
2
C.制胡粉过程中铅的化合价发生了改变,发生了氧化还原反应,C正确;
D.密陀僧(PbO)与一氧化碳高温加热,一氧化碳作还原剂可以制得铅,D正确;
9. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. pH=12的溶液中:K+、Na+、Br-、AlO
B. =10-12的溶液中:NH、Mg2+、CO SO
、
C. 滴加KSCN溶液显红色的溶液中:NH、Na+、F-、I-
D. 水电离的c(OH-)=1×10-13mol·L-1的溶液中:Na+、Cl-、CHCOO-、Cu2+
3
答案:A解析:A.pH=12的溶液显碱性,碱性条件下,该组离子均能共存,A正确;
B.=10-12的溶液呈酸性,酸性溶液中碳酸根离子不能大量共存,B错误;
C.滴加KSCN溶液显红色的溶液中,含有铁离子,铁离子具有氧化性,和碘离子不能共存,
C错误;
D.水电离的c(OH−)=1×10−13mol·L−1的溶液,可能为酸性,也可能为碱性,若为酸性,醋酸根
离子不能大量共存,若为碱性,铜离子不能大量共存,D错误;
10.下列离子反应方程式正确的是
A.漂白粉溶液中通入少量SO :Ca2++2ClO-+SO +HO=CaSO↓+2HClO
2 2 2 3
B.KClO碱性溶液与Fe(OH) 反应:3ClO-+2Fe(OH) =2FeO+3Cl-+4H++HO
3 3 2
C.向明矾溶液中加入Ba(OH) 溶液至生成沉淀的物质的量最多:Al3++2SO+2Ba2++4OH-=
2
AlO+2BaSO↓+2HO
4 2
D.用氢氧化钠溶液吸收工业废气中的NO :2NO +2OH-=NO NO O
2 2 + +H2
答案:D
解析:A项会发生氧化还原反应,产物应为CaSO,A项错误;B项碱性环境,产物不应有氢
4
离子,B项错误;C项要使沉淀的物质的量最大,铝离子也应生成沉淀,C项错误;D项发生歧化
反应,D项正确。
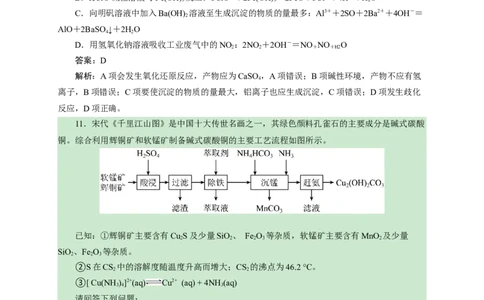
11.宋代《千里江山图》是中国十大传世名画之一,其绿色颜料孔雀石的主要成分是碱式碳酸
铜。综合利用辉铜矿和软锰矿制备碱式碳酸铜的主要工艺流程如图所示。
已知:①辉铜矿主要含有Cu S及少量SiO、 Fe O 等杂质,软锰矿主要含有MnO 及少量
2 2 2 3 2
SiO、Fe O 等杂质。
2 2 3
②S在CS 中的溶解度随温度升高而增大;CS 的沸点为46.2 °C。
2 2
③[ Cu(NH)]2+(aq) Cu2+ (aq) + 4NH(aq)
3 4 3
请回答下列问题:
(1)①“酸浸”时能提高浸取率的措施有________________(任填一条)。
②研究表明矿物中溶解生成的Fe3+可作催化剂,促进Cu S与MnO 的溶解,其过程有三个反应,
2 2
反应方程式分别为:(i) Fe O+ 3H SO =Fe (SO )+3H O;(ii) Cu S+ 2Fe (SO )=2CuSO+4FeSO+S;
2 3 2 4 2 4 3 2 2 2 4 3 4 4
写出(iii)的化学反应方程式__________。
(2)滤渣经CS 提取后可获得副产品硫单质。提取过程中必须控制适宜的温度,不宜过高或过低
2
的原因是_________。
(3)“除铁”时,Fe3+的萃取率与pH的关系如图所示。pH>1后,Fe3+萃取率下降的原因是
_______________。(4)“沉锰”过程中Mn2+沉淀离子方程式为__________。
(5)“赶氨”时,最适宜的操作方法是_______。
答案:(1) 粉碎矿石、充分搅拌、适当提高硫酸浓度等
MnO + 2H SO +2FeSO=Fe (SO )+ MnSO +2H O
2 2 4 4 2 4 3 4 2
(2)温度过低,硫的溶解度较小,温度过高,CS 沸点低大量气化
2
(3)pH>1.7之后,Fe3++3H O Fe(OH) +3H+的水解平衡正向移动,溶液中Fe3+浓度降低,所以
2 3
萃取率下降
(4)Mn2++HCO =MnCO↓+NH (5)加热
+NH3 3
解析:辉铜矿主要含有Cu S及少量SiO、Fe O 等杂质,软锰矿主要含有MnO 及少量SiO、
2 2 2 3 2 2
Fe O 等杂质,加入稀硫酸浸取,过滤得到滤渣为MnO 、SiO、单质S,滤液中含有Fe3+、Mn2+、
2 3 2 2
Cu2+,加入萃取剂除去Fe3+,分离后加入碳酸氢铵溶液沉淀锰,过滤得到滤液赶出氨气循环使用,
得到碱式碳酸铜,以此解答。
(1)①酸浸时,通过粉碎矿石、升高温度、进行搅拌、或适当提高硫酸浓度都可以加快浸取速
率;
②研究表明矿物中溶解生成的Fe3+可作催化剂,促进Cu S与MnO 的溶解,反应(iii)为FeSO
2 2 4
促进MnO 溶解为Mn2+的过程,该过程中Fe元素由+2价上升到+3价,Mn元素由+4价下降到+2价,
2
根据原子守恒和得失电子守恒配平离子方程式为:MnO + 2H SO + 2FeSO =Fe (SO )+ MnSO +
2 2 4 4 2 4 3 4
2HO。
2
(2)S在CS 中的溶解度随温度升高而增大,CS 的沸点为46.2 °C,温度过低,硫的溶解度较小,
2 2
温度过高,CS 沸点低大量气化,提取过程中必须控制适宜的温度。
2
(3)pH>1.7之后,Fe3++3H O Fe(OH) +3H+的水解平衡正向移动,溶液中Fe3+浓度降低,所以
2 3
萃取率下降。
(4)“沉锰”过程中Mn2+和HCO 反应得到MnCO 沉淀和铵盐,离子方程式为:Mn2+
、NH3 3
+HCO =MnCO↓+NH。
+NH3 3
(5)因氨气易挥发,加热可促进挥发,则可用加热的方法。
12.氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣[主要含铁酸镓Ga(Fe O)、铁酸锌
2 2 4 3
ZnFe O、SiO]制备GaN的工艺流程如下:
2 4 2已知:
①Ga与Al同主族,化学性质相似。
②常温下,K [Zn(OH) ]=10-16.6,K [Ga(OH)]=10-35.1,K [Fe(OH) ]=10-38.5。
sp 2 sp 3 sp 3
③Ga3+、Fe3+在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见
下表。
反萃取率/%
盐酸浓度/mol·L-1
Ga3+ Fe3+
2 86.9 9.4
4 69.1 52.1
6 17.5 71.3
回答下列问题:
(1)“酸浸”时Ga(Fe O) 发生反应的离子方程式为__________________________________。
2 2 4 3
“酸溶”所得滤渣的主要成分是________(填化学式)。
(2)“酸浸”所得浸出液中Ga3+、Zn2+浓度分别为0.21g∙L-1、65 g∙L-1。常温下,为尽可能多地提
取Ga3+并确保不混入Zn(OH) ,“调pH”时需用CaO调pH至_________(假设调pH时溶液体积不变)。
2
(3)“脱铁”和“反萃取”时,所用盐酸的浓度a=________,b=_______(选填上表中盐酸的浓
度)。
(4)“沉镓”时,若加入NaOH的量过多,会导致Ga3+的沉淀率降低,原因是_____________(用
离子方程式表示)。
(5)利用CVD(化学气相沉积)技术,将热分解得到的GaO 与NH 在高温下反应可制得GaN,同
2 3 3
时生成另一种产物,该反应化学方程式为__________________。
(6)①GaN的熔点为1700℃,GaCl 的熔点为77.9℃,它们的晶体类型依次为_________、
3
_________。
②GaN晶体的一种立方晶胞如图所示。该晶体中与Ga原子距离最近且相等的N原子个数为
________。该晶体密度为ρg∙cm-3,GaN的式量为Mr,则晶胞边长为________nm。(列出计算式,
N 为阿伏加德罗常数的值)
A答案:(1)Ga (Fe O)+24H+=2Ga3++6Fe3++12H O CaSO (2)略小于5.7
2 2 4 3 2 4
(3)6mol/L 2mol/L (4)Ga(OH) +OH-=GaO+2H O
3 2
(5)Ga O+2NH=====2GaN+3H O
2 3 3 2
(6)共价晶体 分子晶体 4 ×107
解析:矿渣中主要含铁酸镓、铁酸锌、SiO,矿渣中加入稀硫酸,SiO 不溶于稀硫酸,浸出渣
2 2
为SiO,加入CaO调节pH,从已知②可知,Zn(OH) K 相对Ga(OH) 和Fe(OH) 较大,因此控制
2 2 sp 3 3
pH可使Ga3+、Fe3+完全沉淀而Zn2+不沉淀,滤液中为硫酸锌,再加入稀硫酸酸溶,溶液中含有
Ga3+和Fe3+,加入萃取剂萃取,然后加入amol/L盐酸进行脱铁,再加入bmol/L的盐酸进行反萃取,
根据表中数据可知,脱铁时盐酸浓度较高,促使Fe3+更多地进入水相被除去,盐酸浓度为6mol/L,
反萃取中要保证Ga3+更可能多地进入水相,则此时盐酸浓度为2mol/L,随后加入NaOH沉镓生成
Ga(OH) ,Ga(OH) 经过热分解生成GaO,最后经过CVD得到GaN。
3 3 2 3
(1)Ga (Fe O) 与稀硫酸反应生成Ga3+、Fe3+和HO,反应的离子方程式为
2 2 4 3 2
Ga(Fe O)+24H+=2Ga3++6Fe3++12H O。酸溶前调节pH时加入了CaO,加入稀硫酸钙离子和硫酸根
2 2 4 3 2
离子反应生成硫酸钙,硫酸钙微溶于水,故酸溶滤渣中为CaSO。
4
(2)酸浸所得浸出液中Ga3+、Zn2+浓度分别为0.21g/L和65g/L即0.003mol/L和1mol/L,根据
K [Zn(OH) ]=10-16.6,Zn2+开始沉淀时c(OH-)=10-8.3mol/L,Zn2+开始沉淀的pH为5.7,根据
sp 2
K [Ga(OH)]=10-35.1,Ga3+开始沉淀时c(OH-)=1.49×10-11,则Ga3+开始沉淀的pH为3.17,则调节pH
sp 3
略小于5.7即可。
(3)根据分析可知脱铁时盐酸浓度较高,促使Fe3+更多地进入水相被除去,盐酸浓度为6mol/L,
反萃取中要保证Ga3+更可能多地进入水相,则此时盐酸浓度为2mol/L。
(4)Ga与Al同主族,化学性质相似,沉镓时加入NaOH过多,则生成的Ga(OH) 重新溶解生成
3
GaO,离子方程式为Ga(OH) +OH-=GaO+2H O。
3 2
(5)Ga O 与NH 高温下反应生成GaN和另一种物质,根据原子守恒,可得另一种物质为HO,
2 3 3 2
化学方程式为GaO+2NH=====2GaN+3H O。
2 3 3 2
(6)①GaN熔点较高为1700℃,GaCl 熔点较低为77.9℃,则GaN为共价晶体,GaCl 为分子晶
3 3
体。
②从图中可知,该晶体中与Ga原子距离最近且相等的N原子个数为4个,根据均摊法,该晶
胞中N原子个数为4,Ga原子个数为×8+×6=4,设晶胞边长为anm,则ρ=g∙cm-3,则a=×107nm。