文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题23
1. 能正确表示下列反应的离子方程式的是
A. 用NaSO 溶液吸收少量Cl:3SO Cl+HO=2HSO 2Cl-+SO
2 3 2 + 2 2 +
B. 向氯化铁溶液中滴加几滴KSCN溶液:Fe3++3SCN-=Fe(SCN) ↓
3
C. NO 通入水中制硝酸:2NO +HO=2H++NO
2 2 2 +NO
D. 电解MgCl 水溶液:2Cl-+2HO=====3OH-+Cl↑+H↑
2 2 2 2
答案:A
解析:A.用NaSO 溶液吸收少量Cl 反应生成亚硫酸钠和硫酸钠,离子方程式为:3SO Cl+
2 3 2 + 2
HO=2HSO 2Cl-+SO,故A正确;
2 +
B.氯化铁溶液中滴入几滴KSCN溶液,Fe3+和SCN-发生络合反应生成Fe(SCN) 而显红色,离
3
子方程式为:Fe3++3SCN-=Fe(SCN) ,故B错误;
3
C.NO 通入水中制硝酸,离子方程式为:3NO +HO=2H++2NO NO,故C错误;
2 2 2 +
D.用惰性电极电解MgCl 溶液的离子反应为:Mg2++2Cl- +2H O=====Mg(OH) ↓+Cl↑+H ↑,
2 2 2 2 2
故D错误;
2. “84消毒液”是一种常见的消毒剂,其主要成分是次氯酸钠。下列说法错误的是
A. 次氯酸钠溶液呈碱性:ClO-+H O HClO+OH-
2
B. 次氯酸钠溶液中能同时大量存在:K+、NH、S2-、SO
C. 次氯酸钠溶液与浓盐酸混合产生氯气:ClO-+Cl-+2H+=Cl↑+H O
2 2
D. 实验室制备次氯酸钠:Cl+2OH-=ClO-+Cl-+H O
2 2
答案:B
解析:A.次氯酸钠是强碱弱酸盐,次氯酸根离子水解,次氯酸钠溶液呈碱性:ClO-+H O
2
HClO+OH-,故A正确;
B.次氯酸钠具有强氧化性,S2-具有还原性,次氯酸钠溶液中不能同时大量存在S2-,故B错误;
C.次氯酸钠溶液与浓盐酸混合,次氯酸钠和浓盐酸反应生成氯化钠、氯气、水,反应的离子
方程式为ClO-+Cl-+2H+=Cl↑+H O,故C正确;
2 2
D.实验室氯气和氢氧化钠反应制备次氯酸钠,反应的离子方程式是Cl+2OH-=ClO-+Cl-
2
+H O,故D正确;
2
3.对于下列实验,其离子方程式描述错误的是
A. 稀硝酸中加入少量铁粉:3Fe+2NO 8H+=3Fe2++2NO↑+4HO
+ 2
B. 将足量FeCl 溶液滴入Mg(OH) 浊液中:3Mg(OH) +2Fe3+=2Fe(OH) +3Mg2+
3 2 2 3C. Cl 通入冷的KOH溶液中:Cl+2OH-=ClO-+Cl-+HO
2 2 2
D. NHHSO 溶液中加入少量Ba(OH) 溶液:Ba2++2OH-+2H++SO=2HO+BaSO↓
4 4 2 2 4
答案:A
解析:A.稀硝酸中加入少量铁粉生成硝酸铁和一氧化氮气体,Fe+NO 4H+=Fe3++2NO↑+
+
2HO,A错误;
2
B.足量FeCl 溶液滴入Mg(OH) 浊液中,氢氧化镁浊液转化为氢氧化铁浊液:3Mg(OH) +
3 2 2
2Fe3+=2Fe(OH) +3Mg2+,B正确;
3
C.Cl 通入冷的KOH溶液中生成氯化钾和次氯酸钾、水:Cl+2OH-=ClO-+Cl-+HO,C
2 2 2
正确;
D.NH HSO 溶液中加入少量Ba(OH) 溶液,钡离子和氢氧根离子完全反应生成硫酸钡沉淀和
4 4 2
水,Ba2++2OH-+2H++SO=2HO+BaSO↓,D正确;
2 4
4.下列反应的离子方程式正确的是
A. 用稀盐酸处理铜器表面的铜锈:CuO+2H+=Cu2++HO
2
B.少量SO 通入NaClO溶液中:SO +3ClO-+HO=SO+Cl-+2HClO
2 2 2
C. 邻羟基苯甲醛中加入足量浓溴水:
D. 用淀粉KI溶液检验NO:NO+2I-+2H+=NO↑+I+HO
2 2
答案:B
解析:A.铜锈为碱式碳酸铜,盐酸处理铜锈的离子方程式为:Cu (OH) CO+4H+=2Cu2++
2 2 3
2HO+CO↑,故A错误;
2 2
B.少量SO 通入NaClO中发生氧化还原反应,生成硫酸钠、氯化钠和次氯酸,离子方程式为:
2
SO +3ClO-+HO=SO+Cl-+2HClO,故B正确;
2 2
C.醛基能被溴单质氧化为羧基,反应错误,故C错误;
D.KI溶液检验NO:2NO+2I-+4H+=2NO↑+I+2HO,故D错误;
2 2
5.下列各组离子在指定环境中能大量共存的是
A. 0.1mol/L的NaOH溶液:Cl-、Ba2+、K+、NO
B. 0.1mol/L的AlCl 溶液:Mg2+、K+、AlO、Cl-
3
C. 0.1mol/L的FeCl 溶液:Na+、K+、SO、ClO-
2
D. 0.1mol/L的HI溶液:NO -、Na+、MnO
、Cl
答案:A
解析:A.0.1mol/L的NaOH溶液中Cl-、Ba2+、K+、NO
之间不反应,且与氢氧化钠也不反应,可以大量共存,A符合;
B.0.1mol/L的AlCl 溶液中AlO与铝离子发生双水解反应生成氢氧化铝沉淀,不能大量共存,
3
B不符合;
C.0.1mol/L的FeCl 溶液中亚铁离子被ClO-氧化,不能大量共存,C不符合;
2D.0.1mol/L的HI溶液中,NO MnO MnO
、 均能与氧化碘离子,且氯离子能被 氧化,不能大量共存,D不符合;
6.“宏观辨识与微观探析”是学科核心素养之一,下列离子方程式正确且符合题意的是
A. 在过量银氨溶液中滴加甲醛溶液并加热:2[Ag(NH)]++2OH-+HClO—→2Ag↓+HCOO-
3 2
+NH+HO+3NH
2 3
B. 用铜片作电极,电解饱和食盐水:2HO +2Cl-=====H↑+Cl↑+2OH-
2 2 2
C. 下水道堵塞用铝粉和烧碱溶液疏通:2Al+2OH-+2HO=2AlO+3H↑
2 2
D. 向过量的NaHSO 溶液中滴加少量“84”消毒液:HSO -=SO+H++Cl-
3 +ClO
答案:C
解析:A.甲酸铵含醛基,能与银氨溶液反应,A项错误;
B.铜为电极,阳极上Cu发生反应,B项错误;
C.铝与氢氧化钠溶液反应生成氢气,C项正确;
D.次氯酸钠与过量亚硫酸氢钠反应,离子方程式为2HSO -=SO+HO+SO ↑+Cl-,D项
+ClO 2 2
错误;
7.下列离子方程式书写正确的是
A. 将1molCl 通入含1molFeI 的溶液中:2Fe2++Cl=2Fe3++2Cl-
2 2 2
B. 海水提溴工艺中,用纯碱溶液富集Br :3Br +3CO 5Br-+BrO ↑
2 2 = +3CO2
C. 向NaClO溶液中通入少量SO :ClO-+SO+H O=SO+Cl-+2H+
2 2 2
D. 自来水长期煮沸时生成水垢:xCa2++yMg2++(2x+y)HCO xCaCO ↓+yMgCO ↓+
=== 3 3
(x+y)CO ↑+(x+y)HO
2 2
答案:B
解析:A.将1molCl 通入含1molFeI 的溶液中,I-还原性强于Fe2+,先与I-反应,故离子方程
2 2
式为:2I-+Cl=I+2Cl-,A错误;
2 2
B.纯碱与Br 反应,离子方程式 :3Br +3CO 5Br-+BrO ↑,B正确;
2 2 = +3CO2
C.向NaClO溶液中通入少量SO 的离子方程式为:3ClO-+SO+H O=SO+Cl-+2HClO,C错误;
2 2 2
D.自来水长期煮沸时生成水垢的离子方程式为:xCa2++yMg2++(2x+2y)HCO xCaCO ↓+
=== 3
yMg(OH) ↓+(x+2y)CO ↑+xHO,D错误;
2 2 2
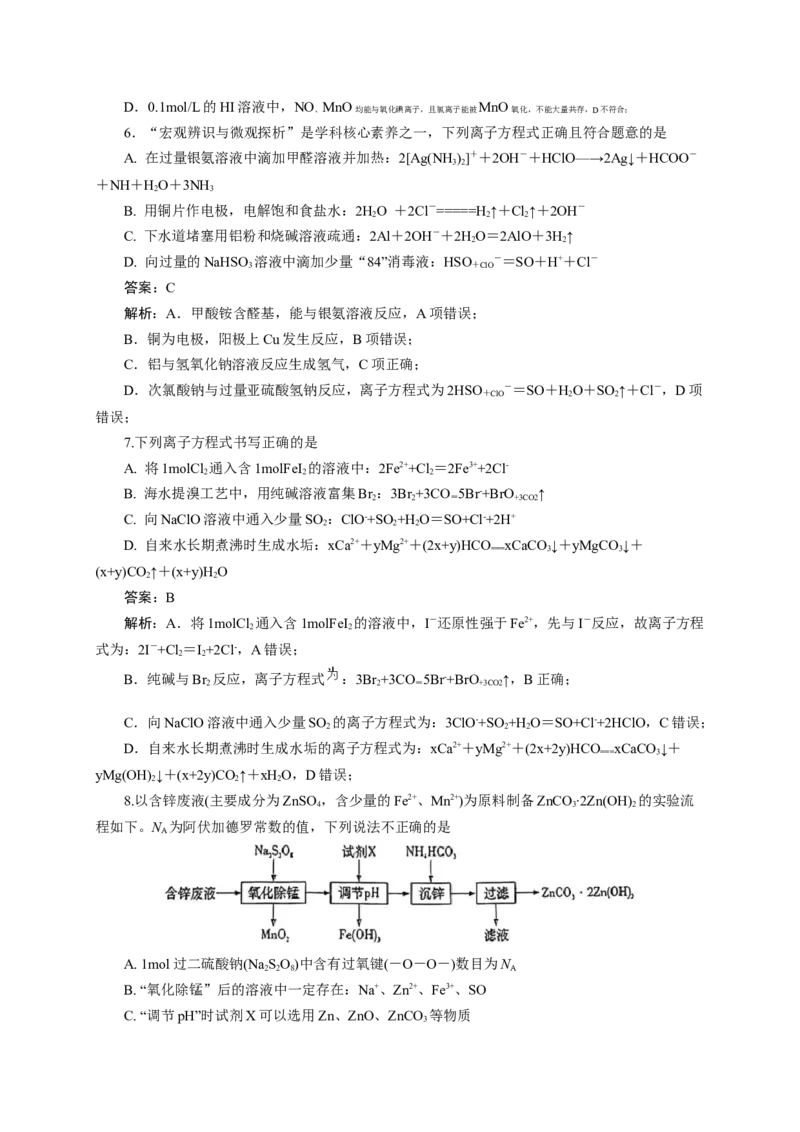
8.以含锌废液(主要成分为ZnSO,含少量的Fe2+、Mn2+)为原料制备ZnCO ∙2Zn(OH) 的实验流
4 3 2
程如下。N 为阿伏加德罗常数的值,下列说法不正确的是
A
A. 1mol过二硫酸钠(Na SO)中含有过氧键(-O-O-)数目为N
2 2 8 A
B. “氧化除锰”后的溶液中一定存在:Na+、Zn2+、Fe3+、SO
C. “调节pH”时试剂X可以选用Zn、ZnO、ZnCO 等物质
3D. “氧化除锰”过程中生成MnO 的离子方程式:Mn2++SO+2HO=MnO ↓+2SO+4H+
2 2 2 2
答案:C
解析:含锌废液中加入过二硫酸钠,可以将亚铁离子氧化生成铁离子,将锰离子氧化生成二氧
化锰而除去,再条件溶液的pH使铁离子转化为氢氧化铁沉淀,滤液中加入碳酸氢铵得到
ZnCO ∙2Zn(OH) ,然后过滤得到ZnCO ∙2Zn(OH) 。
3 2 3 2
A.SO中S为+6价,则有6个O为-2价,有2个-1价的氧,故含有1个过氧键(-O-O
2
-),因此1mol过二硫酸钠(Na SO)中含有过氧键数为N ,A正确;
2 2 8 A
B.分析可知,氧化除锰后的溶液中存在的离子为Na+、Zn2+、Fe3+、SO, B正确;
C.溶液中Fe3+能与锌反应生成Fe2+和Zn2+,所以调节溶液pH时试剂X不能选用Zn,C错误;
D.分析可知,“氧化除锰”工序用NaSO 把Fe2+、Mn2+氧化为Fe3+、MnO ,根据电子转移
2 2 8 2
守恒和质量守恒可知,除锰发生反应的离子反应方程式是Mn2++SO+2HO=MnO ↓+2SO+4H+,
2 2 2
D正确;
9.下列各组离子在指定溶液中能大量共存的是
A. 0.1 mol·L−1 NaHCO 溶液中:H+、Mg2+ 、Cl-、SO
3
B. 0. 1 mol·L−1 FeCl 溶液中:Fe2+、NH、I-、 NO
3
C. 0. 1 mol·L−1 HCl溶液中:Fe2+、NH、Br-、SO
D. 0.1 mol·L−1 NaOH溶液中:K+、Ba2+、SO、Br-
答案:C
解析:A.0.1 mol·L−1 NaHCO 溶液中不能大量存在H+,否则会反应产生二氧化碳和水,选项
3
A错误;
B.0.1 mol·L−1 FeCl 溶液中,Fe3+与I-因发生氧化还原反应而不能大量共存,选项B错误;
3
C.0.1 mol·L−1 HCl溶液中,H+、Cl-、Fe2+、NH、Br-、SO各离子之间相互不反应,能大量共
存,选项C正确;
D.Ba2+与SO因发生反应生成硫酸钡沉淀而不能大量共存,选项D错误;
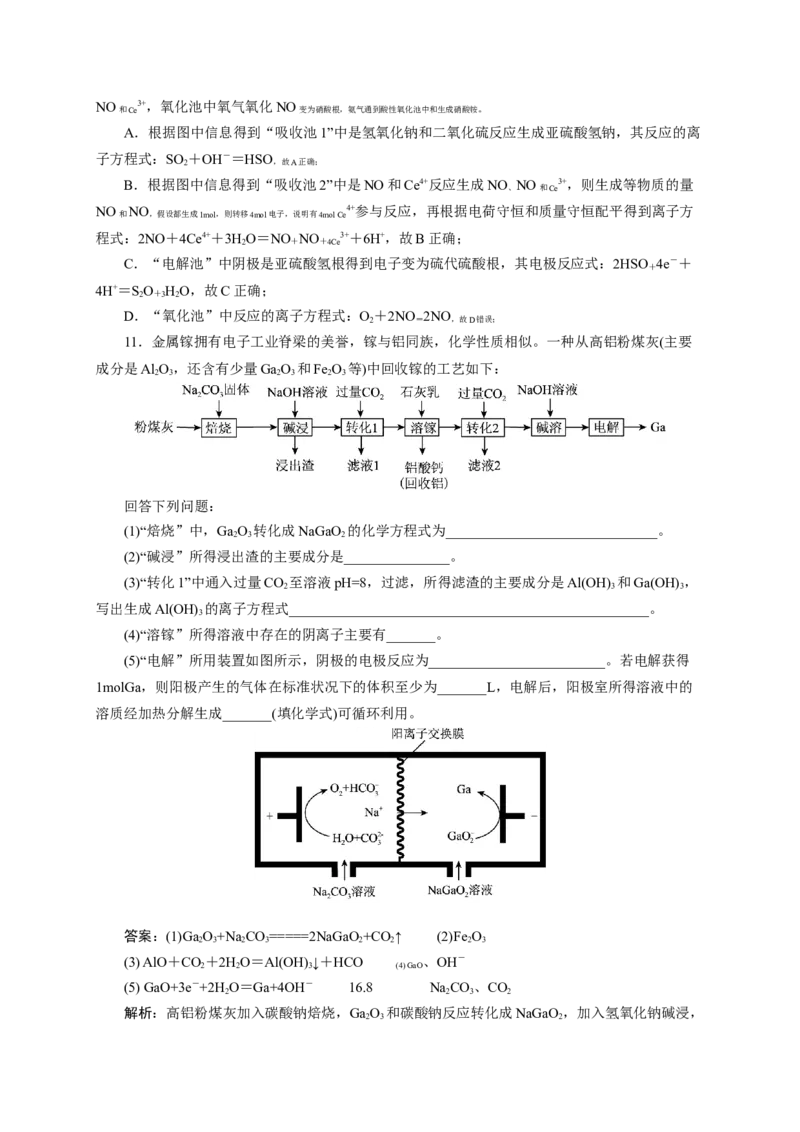
10.利用雾霾中的污染物NO、SO 获得产品NH NO 的流程图如下,下列方程式错误的是
2 4 3
A.“吸收池1”中反应的离子方程式:SO +OH-=HSO
2
B.“吸收池2”中生成等物质的量NO NO NO+4Ce4++3HO=NO NO 3++6H+
和 的离子方程式:2 2 + +4Ce
C.“电解池”中阴极的电极反应式:2HSO 4e-+4H+=SO HO
+ 2 +3 2
D.“氧化池”中反应的离子方程式:2NH +O+2NO 2NH+2NO
3 2 =
答案:D
解析:污染物NO、SO 通到氢氧化钠溶液中,NO不反应,二氧化硫和氢氧化钠溶液反应生成
2
亚硫酸氢钠,亚硫酸氢钠在电解池中电解得到硫代硫酸钠,NO和Ce4+在吸收池2中反应生成NO
、NO 3+,氧化池中氧气氧化NO
和Ce 变为硝酸根,氨气通到酸性氧化池中和生成硝酸铵。
A.根据图中信息得到“吸收池1”中是氢氧化钠和二氧化硫反应生成亚硫酸氢钠,其反应的离
子方程式:SO +OH-=HSO
2 ,故A正确;
B.根据图中信息得到“吸收池2”中是NO和Ce4+反应生成NO NO 3+,则生成等物质的量
、 和Ce
NO NO 4+参与反应,再根据电荷守恒和质量守恒配平得到离子方
和 ,假设都生成1mol,则转移4mol电子,说明有4mol Ce
程式:2NO+4Ce4++3HO=NO NO 3++6H+,故B正确;
2 + +4Ce
C.“电解池”中阴极是亚硫酸氢根得到电子变为硫代硫酸根,其电极反应式:2HSO 4e-+
+
4H+=SO HO,故C正确;
2 +3 2
D.“氧化池”中反应的离子方程式:O+2NO 2NO
2 = ,故D错误;
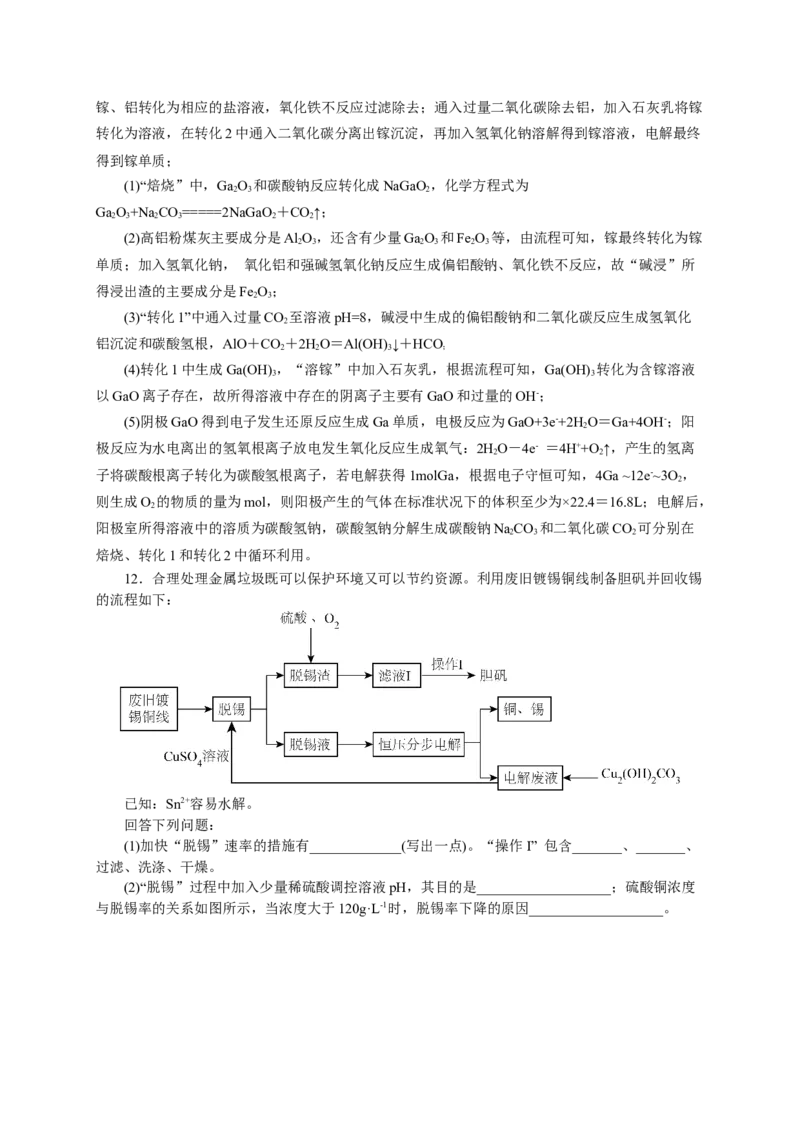
11.金属镓拥有电子工业脊梁的美誉,镓与铝同族,化学性质相似。一种从高铝粉煤灰(主要
成分是Al O,还含有少量GaO 和Fe O 等)中回收镓的工艺如下:
2 3 2 3 2 3
回答下列问题:
(1)“焙烧”中,GaO 转化成NaGaO 的化学方程式为______________________________。
2 3 2
(2)“碱浸”所得浸出渣的主要成分是_______________。
(3)“转化1”中通入过量CO 至溶液pH=8,过滤,所得滤渣的主要成分是Al(OH) 和Ga(OH) ,
2 3 3
写出生成Al(OH) 的离子方程式___________________________________________________。
3
(4)“溶镓”所得溶液中存在的阴离子主要有_______。
(5)“电解”所用装置如图所示,阴极的电极反应为_________________________。若电解获得
1molGa,则阳极产生的气体在标准状况下的体积至少为_______L,电解后,阳极室所得溶液中的
溶质经加热分解生成_______(填化学式)可循环利用。
答案:(1)Ga O+Na CO=====2NaGaO +CO ↑ (2)Fe O
2 3 2 3 2 2 2 3
(3) AlO+CO+2HO=Al(OH) ↓+HCO 、OH-
2 2 3 (4) GaO
(5) GaO+3e-+2H O=Ga+4OH- 16.8 Na CO、CO
2 2 3 2
解析:高铝粉煤灰加入碳酸钠焙烧,GaO 和碳酸钠反应转化成NaGaO ,加入氢氧化钠碱浸,
2 3 2镓、铝转化为相应的盐溶液,氧化铁不反应过滤除去;通入过量二氧化碳除去铝,加入石灰乳将镓
转化为溶液,在转化2中通入二氧化碳分离出镓沉淀,再加入氢氧化钠溶解得到镓溶液,电解最终
得到镓单质;
(1)“焙烧”中,GaO 和碳酸钠反应转化成NaGaO ,化学方程式为
2 3 2
GaO+Na CO=====2NaGaO +CO↑;
2 3 2 3 2 2
(2)高铝粉煤灰主要成分是Al O,还含有少量GaO 和Fe O 等,由流程可知,镓最终转化为镓
2 3 2 3 2 3
单质;加入氢氧化钠, 氧化铝和强碱氢氧化钠反应生成偏铝酸钠、氧化铁不反应,故“碱浸”所
得浸出渣的主要成分是Fe O;
2 3
(3)“转化1”中通入过量CO 至溶液pH=8,碱浸中生成的偏铝酸钠和二氧化碳反应生成氢氧化
2
铝沉淀和碳酸氢根,AlO+CO+2HO=Al(OH) ↓+HCO
2 2 3 ;
(4)转化1中生成Ga(OH) ,“溶镓”中加入石灰乳,根据流程可知,Ga(OH) 转化为含镓溶液
3 3
以GaO离子存在,故所得溶液中存在的阴离子主要有GaO和过量的OH-;
(5)阴极GaO得到电子发生还原反应生成Ga单质,电极反应为GaO+3e-+2H O=Ga+4OH-;阳
2
极反应为水电离出的氢氧根离子放电发生氧化反应生成氧气:2HO-4e- =4H++O ↑,产生的氢离
2 2
子将碳酸根离子转化为碳酸氢根离子,若电解获得1molGa,根据电子守恒可知,4Ga ~12e-~3O ,
2
则生成O 的物质的量为mol,则阳极产生的气体在标准状况下的体积至少为×22.4=16.8L;电解后,
2
阳极室所得溶液中的溶质为碳酸氢钠,碳酸氢钠分解生成碳酸钠NaCO 和二氧化碳CO 可分别在
2 3 2
焙烧、转化1和转化2中循环利用。
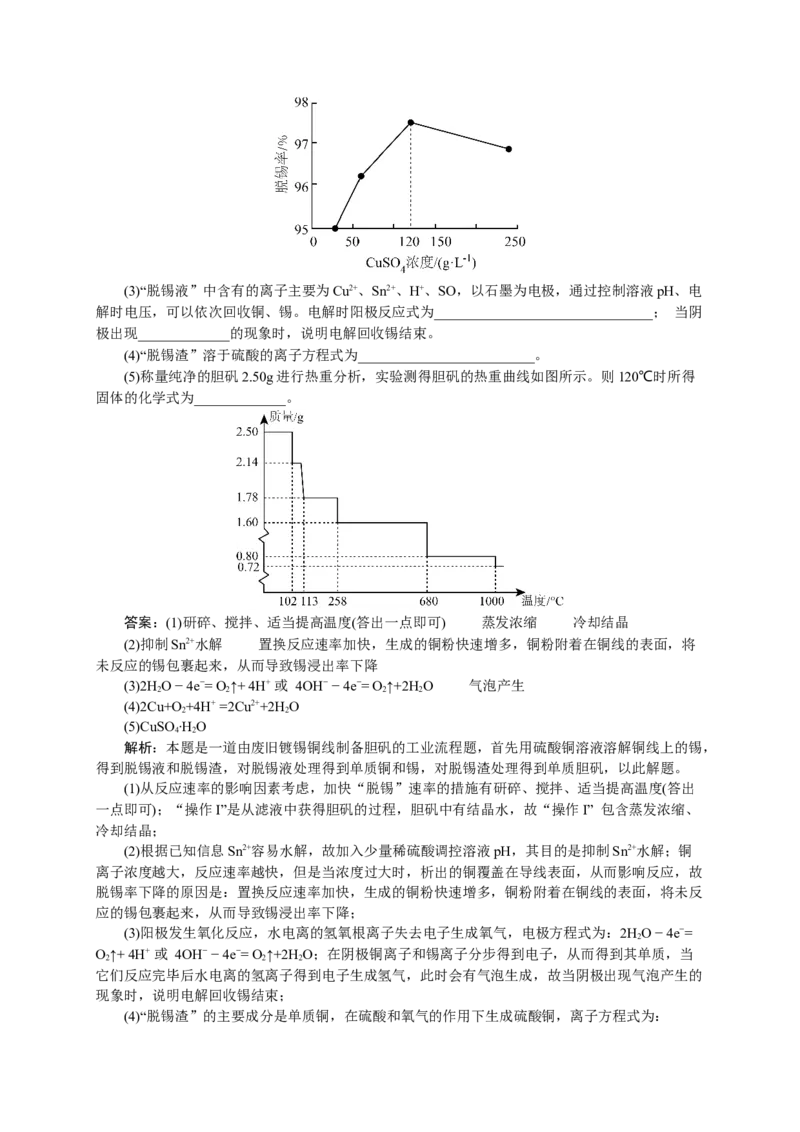
12.合理处理金属垃圾既可以保护环境又可以节约资源。利用废旧镀锡铜线制备胆矾并回收锡
的流程如下:
已知:Sn2+容易水解。
回答下列问题:
(1)加快“脱锡”速率的措施有_____________(写出一点)。“操作I” 包含_______、_______、
过滤、洗涤、干燥。
(2)“脱锡”过程中加入少量稀硫酸调控溶液pH,其目的是___________________;硫酸铜浓度
与脱锡率的关系如图所示,当浓度大于120g·L-1时,脱锡率下降的原因___________________。(3)“脱锡液”中含有的离子主要为Cu2+、Sn2+、H+、SO,以石墨为电极,通过控制溶液pH、电
解时电压,可以依次回收铜、锡。电解时阳极反应式为_______________________________; 当阴
极出现_____________的现象时,说明电解回收锡结束。
(4)“脱锡渣”溶于硫酸的离子方程式为_________________________。
(5)称量纯净的胆矾2.50g进行热重分析,实验测得胆矾的热重曲线如图所示。则120℃时所得
固体的化学式为_____________。
答案:(1)研碎、搅拌、适当提高温度(答出一点即可) 蒸发浓缩 冷却结晶
(2)抑制Sn2+水解 置换反应速率加快,生成的铜粉快速增多,铜粉附着在铜线的表面,将
未反应的锡包裹起来,从而导致锡浸出率下降
(3)2H O − 4e−= O ↑+ 4H+ 或 4OH− − 4e−= O ↑+2H O 气泡产生
2 2 2 2
(4)2Cu+O +4H+ =2Cu2++2H O
2 2
(5)CuSO ∙H O
4 2
解析:本题是一道由废旧镀锡铜线制备胆矾的工业流程题,首先用硫酸铜溶液溶解铜线上的锡,
得到脱锡液和脱锡渣,对脱锡液处理得到单质铜和锡,对脱锡渣处理得到单质胆矾,以此解题。
(1)从反应速率的影响因素考虑,加快“脱锡”速率的措施有研碎、搅拌、适当提高温度(答出
一点即可);“操作I”是从滤液中获得胆矾的过程,胆矾中有结晶水,故“操作I” 包含蒸发浓缩、
冷却结晶;
(2)根据已知信息Sn2+容易水解,故加入少量稀硫酸调控溶液pH,其目的是抑制Sn2+水解;铜
离子浓度越大,反应速率越快,但是当浓度过大时,析出的铜覆盖在导线表面,从而影响反应,故
脱锡率下降的原因是:置换反应速率加快,生成的铜粉快速增多,铜粉附着在铜线的表面,将未反
应的锡包裹起来,从而导致锡浸出率下降;
(3)阳极发生氧化反应,水电离的氢氧根离子失去电子生成氧气,电极方程式为:2HO − 4e−=
2
O↑+ 4H+ 或 4OH− − 4e−= O ↑+2H O;在阴极铜离子和锡离子分步得到电子,从而得到其单质,当
2 2 2
它们反应完毕后水电离的氢离子得到电子生成氢气,此时会有气泡生成,故当阴极出现气泡产生的
现象时,说明电解回收锡结束;
(4)“脱锡渣”的主要成分是单质铜,在硫酸和氧气的作用下生成硫酸铜,离子方程式为:2Cu+O +4H+ =2Cu2++2H O;
2 2
(5)设120℃时固体物质的相对分子质量为M,2.50∶250=1.78∶M,M=178,故120℃时固体物质
的成分为:CuSO ∙H O。
4 2