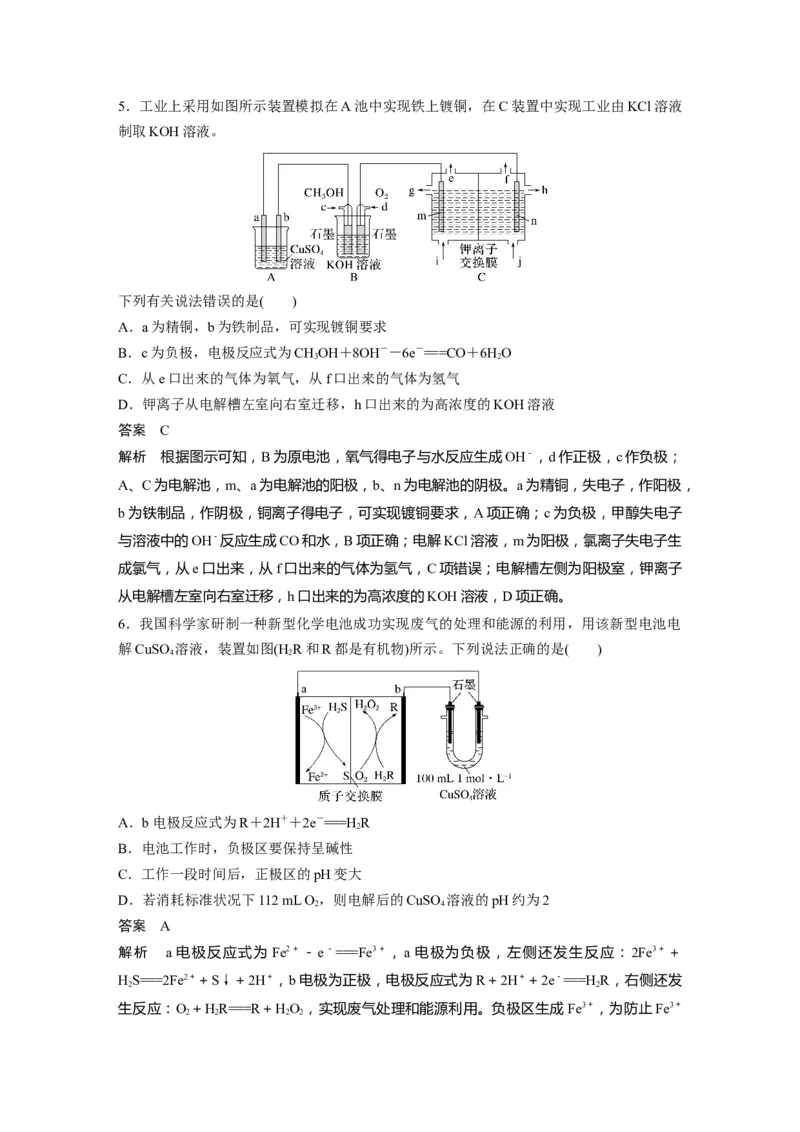
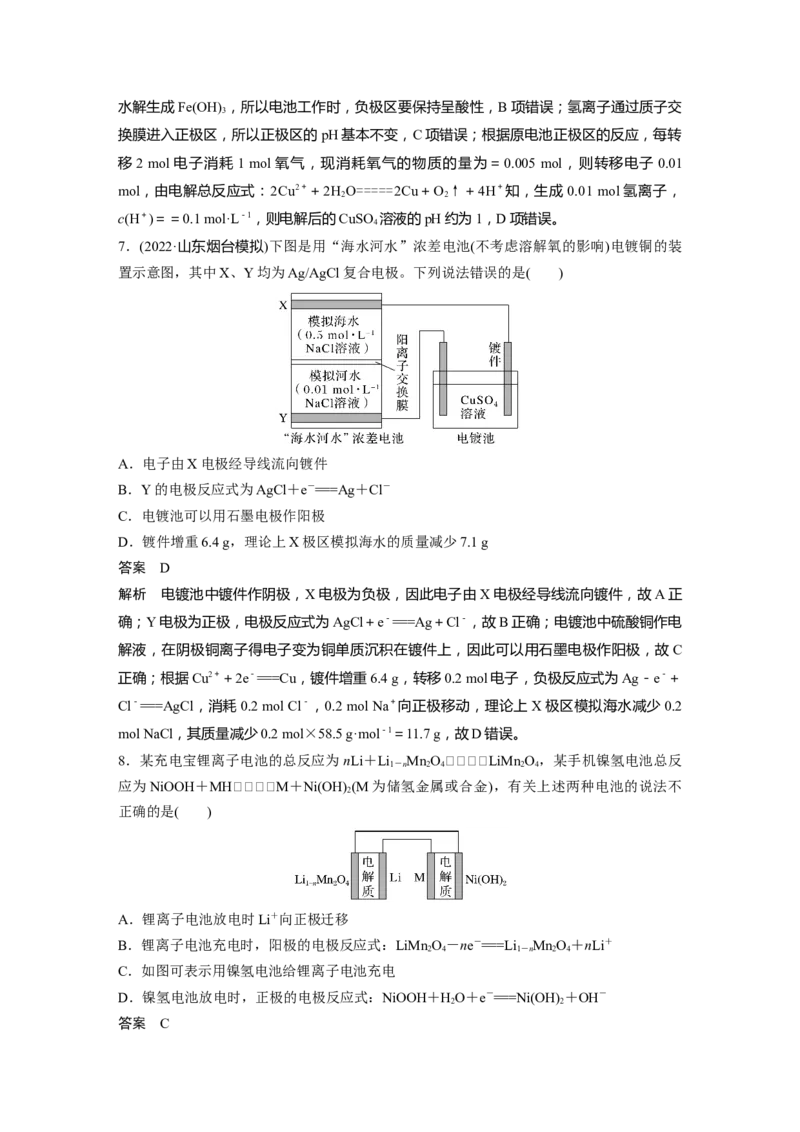
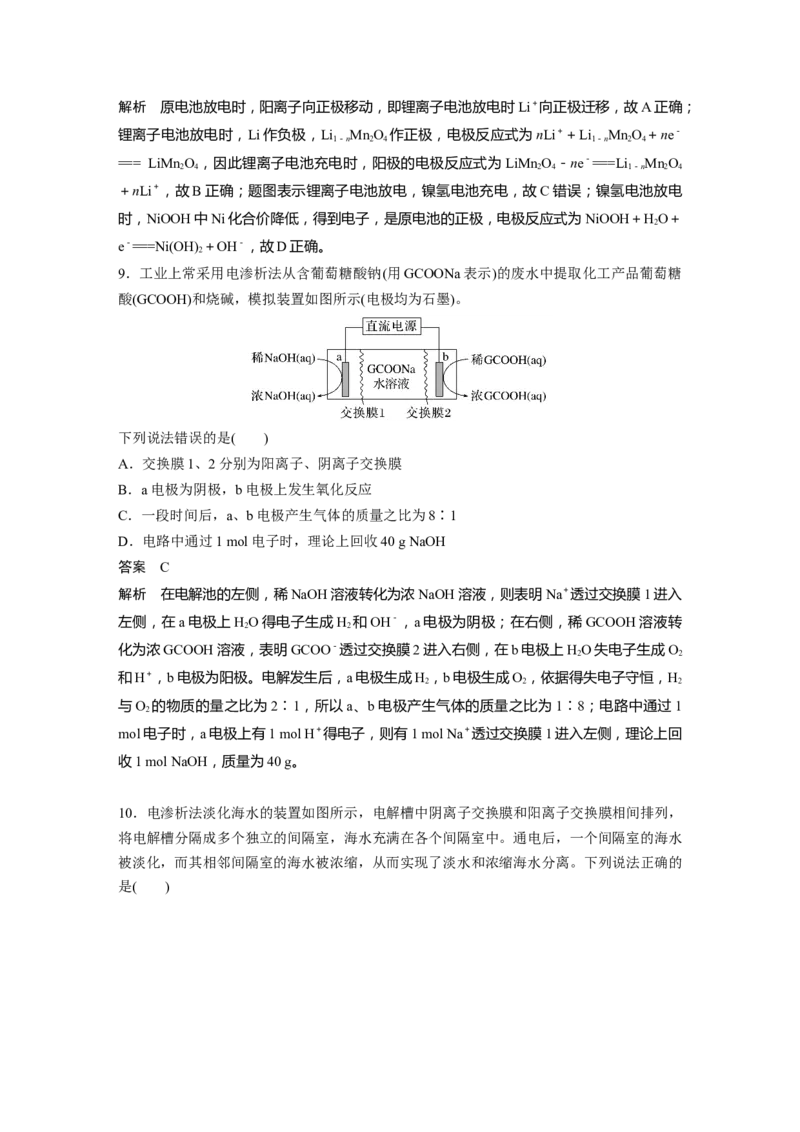
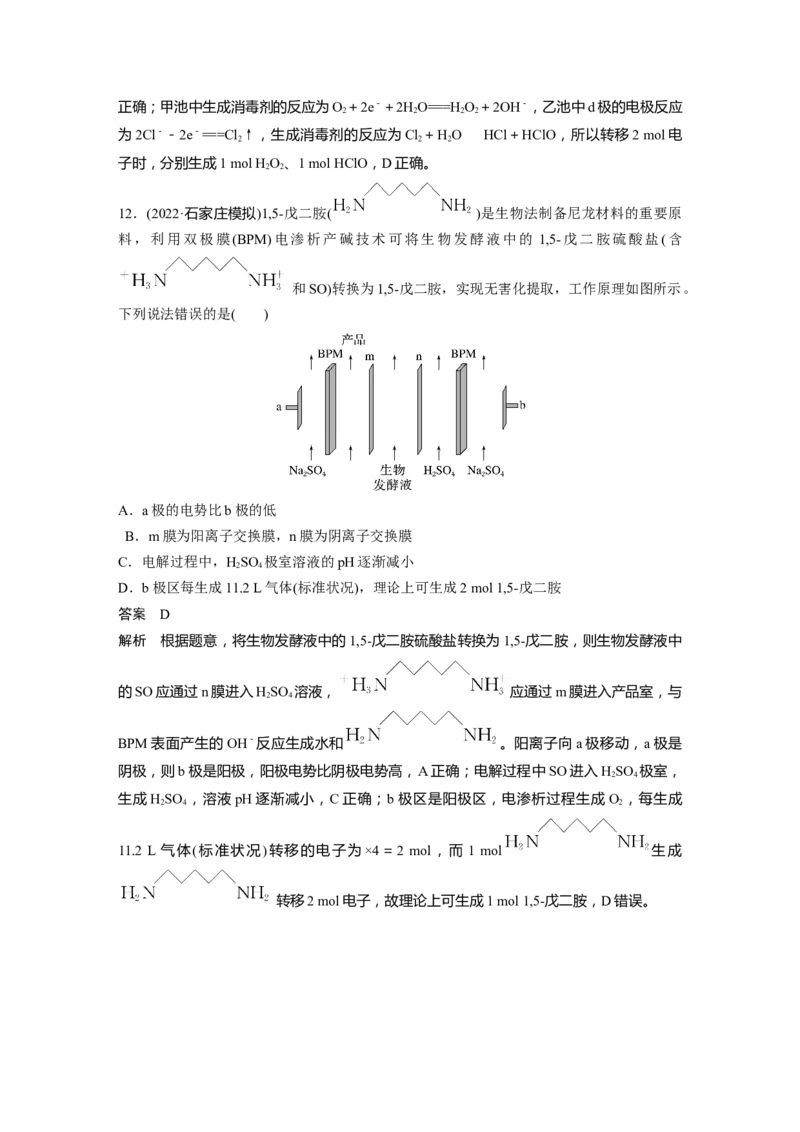
文档内容
第 43 讲 多池、多室的电化学装置
[复习目标] 1.了解串联装置的连接特点,了解离子交换膜的特点及作用。2.掌握多池、多
室问题分析的一般方法。3.能熟练用电子守恒、关系式法等进行有关电化学计算。
考点一 多池串联的两大模型及原理分析
1.常见多池串联装置图
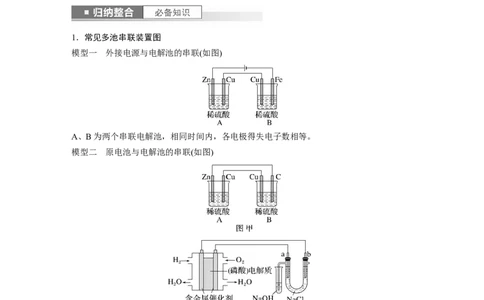
模型一 外接电源与电解池的串联(如图)
A、B为两个串联电解池,相同时间内,各电极得失电子数相等。
模型二 原电池与电解池的串联(如图)
甲、乙两图中,A均为原电池,B均为电解池。2.二次电池的充电
(1)可充电电池原理示意图
充电时,原电池负极与外接电源负极相连,原电池正极与外接电源正极相连,记作“正接正,
负接负”。
(2)可充电电池有充电和放电两个过程,放电时是原电池反应,充电时是电解池反应。充电、
放电不是可逆反应。
(3)放电时的负极反应和充电时的阴极反应相反,放电时的正极反应和充电时的阳极反应相
反。将负(正)极反应式变换方向并将电子移项即可得出阴(阳)极反应式。
例:Fe+Ni O+3HOFe(OH)+2Ni(OH),放电时负极的电极反应式为Fe-2e-+2OH
2 3 2 2 2
-
===Fe(OH) ,则充电时阴极的电极反应式为Fe(OH) +2e-===Fe+2OH-。
2 2
3.电化学计算的三种方法
如以电路中通过4 mol e-为桥梁可构建以下关系式:
4e-~ ~
(式中M为金属,n为其离子的化合价数值)
该关系式具有总览电化学计算的作用和价值,熟记电极反应式,灵活运用关系式便能快速解
答常见的电化学计算问题。
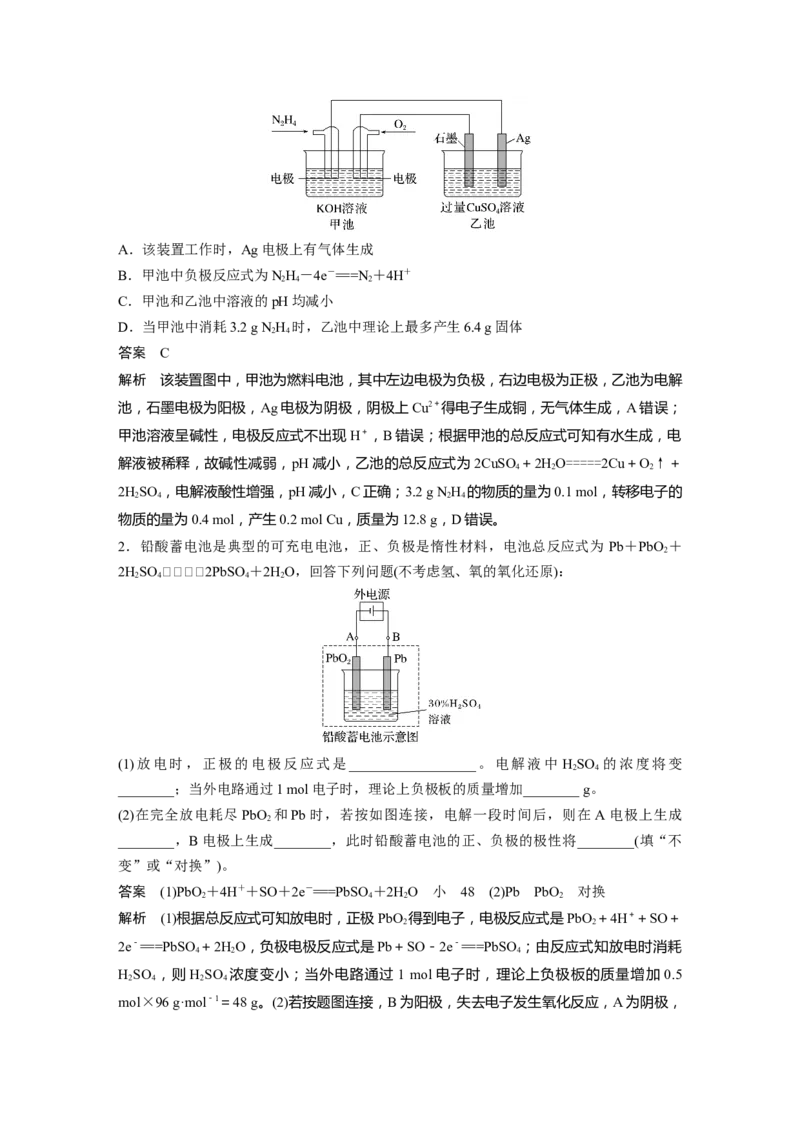
1.如图所示,甲池的总反应式为NH +O===N +2HO,下列关于该装置工作时的说法正
2 4 2 2 2
确的是( )A.该装置工作时,Ag电极上有气体生成
B.甲池中负极反应式为NH-4e-===N+4H+
2 4 2
C.甲池和乙池中溶液的pH均减小
D.当甲池中消耗3.2 g N H 时,乙池中理论上最多产生6.4 g固体
2 4
答案 C
解析 该装置图中,甲池为燃料电池,其中左边电极为负极,右边电极为正极,乙池为电解
池,石墨电极为阳极,Ag电极为阴极,阴极上Cu2+得电子生成铜,无气体生成,A错误;
甲池溶液呈碱性,电极反应式不出现H+,B错误;根据甲池的总反应式可知有水生成,电
解液被稀释,故碱性减弱,pH减小,乙池的总反应式为2CuSO +2HO=====2Cu+O↑+
4 2 2
2HSO ,电解液酸性增强,pH减小,C正确;3.2 g N H 的物质的量为0.1 mol,转移电子的
2 4 2 4
物质的量为0.4 mol,产生0.2 mol Cu,质量为12.8 g,D错误。
2.铅酸蓄电池是典型的可充电电池,正、负极是惰性材料,电池总反应式为 Pb+PbO +
2
2HSO 2PbSO +2HO,回答下列问题(不考虑氢、氧的氧化还原):
2 4 4 2
(1)放电时,正极的电极反应式是__________________。电解液中 HSO 的浓度将变
2 4
________;当外电路通过1 mol电子时,理论上负极板的质量增加________ g。
(2)在完全放电耗尽PbO 和Pb时,若按如图连接,电解一段时间后,则在 A电极上生成
2
________,B电极上生成________,此时铅酸蓄电池的正、负极的极性将________(填“不
变”或“对换”)。
答案 (1)PbO +4H++SO+2e-===PbSO +2HO 小 48 (2)Pb PbO 对换
2 4 2 2
解析 (1)根据总反应式可知放电时,正极PbO 得到电子,电极反应式是PbO +4H++SO+
2 2
2e-===PbSO +2HO,负极电极反应式是Pb+SO-2e-===PbSO ;由反应式知放电时消耗
4 2 4
H SO ,则H SO 浓度变小;当外电路通过1 mol电子时,理论上负极板的质量增加 0.5
2 4 2 4
mol×96 g·mol-1=48 g。(2)若按题图连接,B为阳极,失去电子发生氧化反应,A为阴极,得到电子发生还原反应,B电极上发生的反应为PbSO +2HO-2e-===PbO +4H++SO,A
4 2 2
电极发生的反应为PbSO +2e-===Pb+SO,所以A电极上生成Pb,B电极上生成PbO ,此
4 2
时铅酸蓄电池的正、负极的极性将对换。
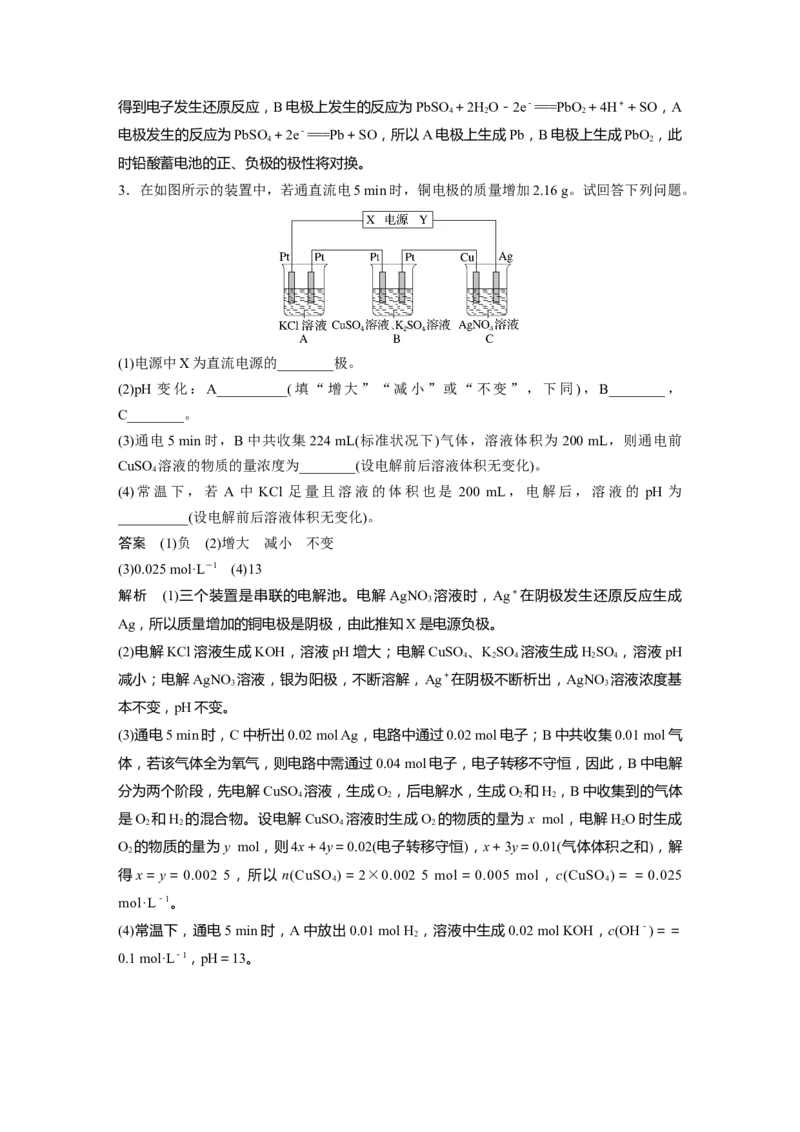
3.在如图所示的装置中,若通直流电5 min时,铜电极的质量增加2.16 g。试回答下列问题。
(1)电源中X为直流电源的________极。
(2)pH 变化:A__________(填“增大”“减小”或“不变”,下同),B________,
C________。
(3)通电5 min时,B中共收集224 mL(标准状况下)气体,溶液体积为 200 mL,则通电前
CuSO 溶液的物质的量浓度为________(设电解前后溶液体积无变化)。
4
(4)常温下,若 A 中 KCl 足量且溶液的体积也是 200 mL,电解后,溶液的 pH 为
__________(设电解前后溶液体积无变化)。
答案 (1)负 (2)增大 减小 不变
(3)0.025 mol·L-1 (4)13
解析 (1)三个装置是串联的电解池。电解 AgNO 溶液时,Ag+在阴极发生还原反应生成
3
Ag,所以质量增加的铜电极是阴极,由此推知X是电源负极。
(2)电解KCl溶液生成KOH,溶液pH增大;电解CuSO 、KSO 溶液生成HSO ,溶液pH
4 2 4 2 4
减小;电解AgNO 溶液,银为阳极,不断溶解,Ag+在阴极不断析出,AgNO 溶液浓度基
3 3
本不变,pH不变。
(3)通电5 min时,C中析出0.02 mol Ag,电路中通过0.02 mol电子;B中共收集0.01 mol气
体,若该气体全为氧气,则电路中需通过0.04 mol电子,电子转移不守恒,因此,B中电解
分为两个阶段,先电解CuSO 溶液,生成O ,后电解水,生成O 和H ,B中收集到的气体
4 2 2 2
是O 和H 的混合物。设电解CuSO 溶液时生成O 的物质的量为x mol,电解HO时生成
2 2 4 2 2
O 的物质的量为y mol,则4x+4y=0.02(电子转移守恒),x+3y=0.01(气体体积之和),解
2
得x=y=0.002 5,所以 n(CuSO )=2×0.002 5 mol=0.005 mol,c(CuSO )==0.025
4 4
mol·L-1。
(4)常温下,通电5 min时,A中放出0.01 mol H ,溶液中生成0.02 mol KOH,c(OH-)==
2
0.1 mol·L-1,pH=13。考点二 多室装置的分析
为实现特定功能需求,在电化学装置中增加离子交换膜,将原电池或电解池分隔成两个或多
个相对独立的室。
1.离子交换膜的分类和应用
2.分析某室质量变化的关键
分析某室质量的变化,既要考虑该区(或该电极)的化学反应,又要考虑通过“交换膜”的离
子带来的质量变化。
1.钠离子电池具有资源丰富、成本低、安全性好、转换效率高等特点,有望成为锂离子电
池之后的新型首选电池,如图是一种钠离子电池工作示意图:
下列说法不正确的是( )
A.放电时,Na+通过交换膜向N极移动
B.充电时,光照可促进电子的转移
C.充电时,TiO 光电极上发生的电极反应为3I--2e-===I
2
D.放电时,若负极室有2 mol阴离子发生反应,则电路中转移2 mol电子
答案 D解析 由图中信息知,放电时,电极N为正极,电极M为负极,Na+由M极移向N极,A
正确;根据题图:TiO 光电极能使电池在太阳光照下充电,所以充电时,光可以促进I-在
2
TiO 光电极上转移电子,B正确;充电时,阳极上发生失电子的氧化反应,根据图示,阳极
2
电极反应式为3I--2e-===I,C正确;充电时Na S 被还原为Na S,电极反应式为S+6e-
2 4 2
===4S2-,则放电时负极反应式为4S2--6e-===S,由此可知若负极室有2 mol阴离子发生
反应,则电路中转移3 mol电子,D错误。
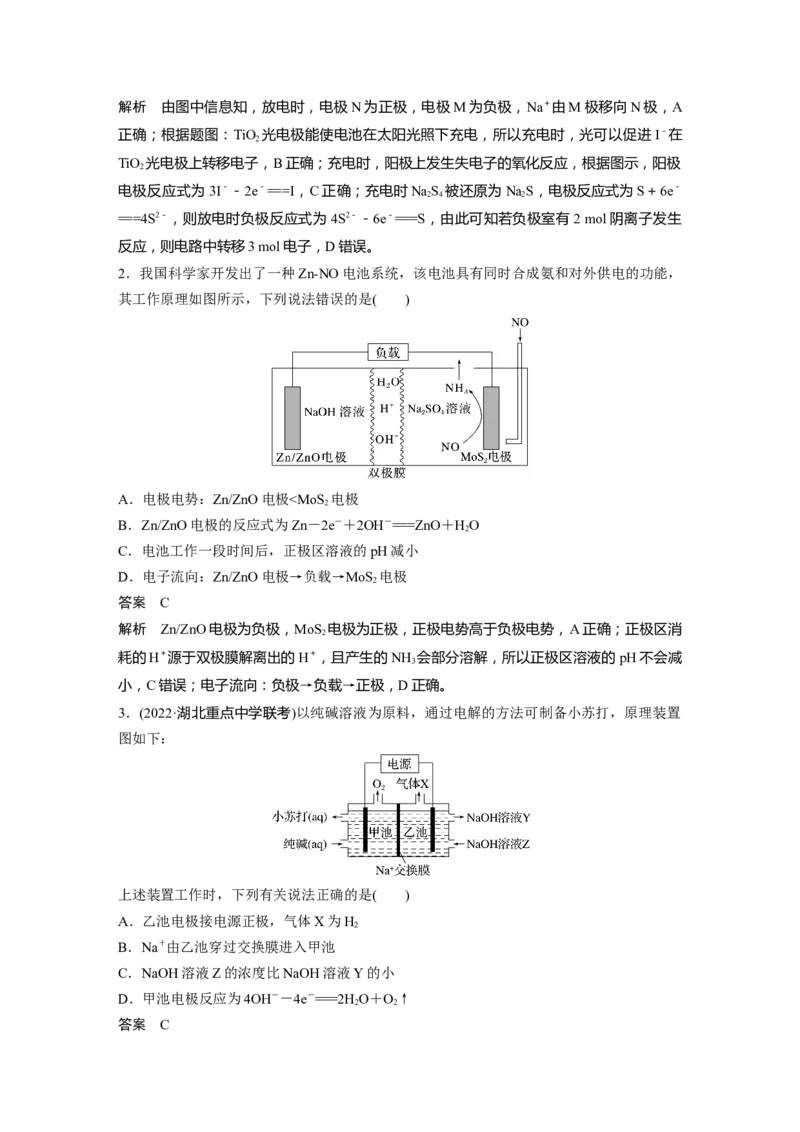
2.我国科学家开发出了一种Zn-NO电池系统,该电池具有同时合成氨和对外供电的功能,
其工作原理如图所示,下列说法错误的是( )
A.电极电势:Zn/ZnO电极