文档内容
热点强化 23 有关水溶液中平衡常数关系计算
1.水解常数与电离常数、水的离子积之间的关系
常温下,HS的电离常数为K 、K ,推导NaS溶液中S2-水解常数K 、K 与K 、K 的关
2 a1 a2 2 h1 h2 a1 a2
系。
答案 (1)S2-+HOHS-+OH-
2
K ===。
h1
(2)HS-+HOHS+OH-
2 2
K ===。
h2
2.水解常数与溶度积、水的离子积之间的关系
常温下推导Cu2+的水解常数与溶度积、水的离子积之间的关系。
答案 Cu2++2HOCu(OH) +2H+
2 2
K ===。
h
3.平衡常数与电离常数、溶度积之间的关系
(1)以反应CuS(s)+2Ag+(aq) Cu2+(aq)+Ag S(s)为例,推导沉淀转化的平衡常数K。
2
答案 K===。
(2)以反应ZnS(s)+2H+(aq)Zn2+(aq)+HS(aq)为例,推导该沉淀溶解的平衡常数K。
2
答案 K===。
1.已知pK =-lg K ,且常温下HCO :pK =6.4,pK =10.3。则常温下CO的pK 为
a a 2 3 a1 a2 h1
________。
答案 3.7
解析 CO的第一步水解常数K ===,而HCO 的pK =10.3,故K =10-10.3,则K =
h1 2 3 a2 a2 h1
==10-3.7。
2.常温下,K(HF)=4.0×10-4,25 ℃时,1.0 mol·L-1HF溶液的pH约等于____________(已
a
知lg 2≈0.3)。将浓度相等的 HF 与NaF 溶液等体积混合,判断溶液呈______(填“酸”
“ 碱 ” 或 “ 中 ” ) 性 , 并 结 合 有 关 数 据 解 释 原 因 :
_________________________________________。
答案 1.7 酸 HF和NaF的浓度相等,K=4.0×10-4,K ==2.5×10-11<K,故HF的电
a h a
离程度大于F-的水解程度,溶液呈酸性
解析 K(HF)=≈=4.0×10-4,则1.0 mol·L-1HF溶液中氢离子浓度为2.0×10-2 mol·L-1,
a
所以pH=-lg(2.0×10-2)=2-lg 2≈1.7。3.NaHS可用于污水处理的沉淀剂。已知:25 ℃时,反应Hg2+(aq)+HS-(aq)HgS(s)+
H+(aq)的平衡常数K=1.75×1038,HS的电离平衡常数K =1.0×10-7,K =7.0×10-15,计
2 a1 a2
算K (HgS)。
sp
答案 反应Hg2+(aq)+HS-(aq)HgS(s)+H+(aq)的平衡常数K=1.75×1038,即K====
1.75×1038,则K (HgS)===4.0×10-53。
sp
4.用40%的硫酸溶液吸收氨气获得(NH )SO 的稀溶液,测得常温下,该溶液的pH=5。
4 2 4
(1)计算的值[计算结果保留一位小数,已知K (NH ·H O)=1.7×10-5]。
b 3 2
(2)若将该溶液蒸发掉一部分水后恢复至室温,推理分析浓缩后溶液中的值如何变化。
答案 (1)===≈5.9×10-5。
(2)设(NH )SO 溶液的浓度为c,NH的水解程度为a,则==,蒸发掉一部分水后恢复室温,
4 2 4
溶液浓度增大,NH水解程度减小,即a减小,因而该比值减小。
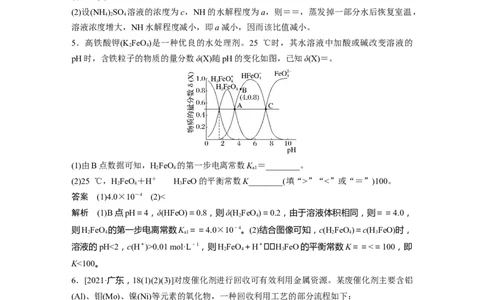
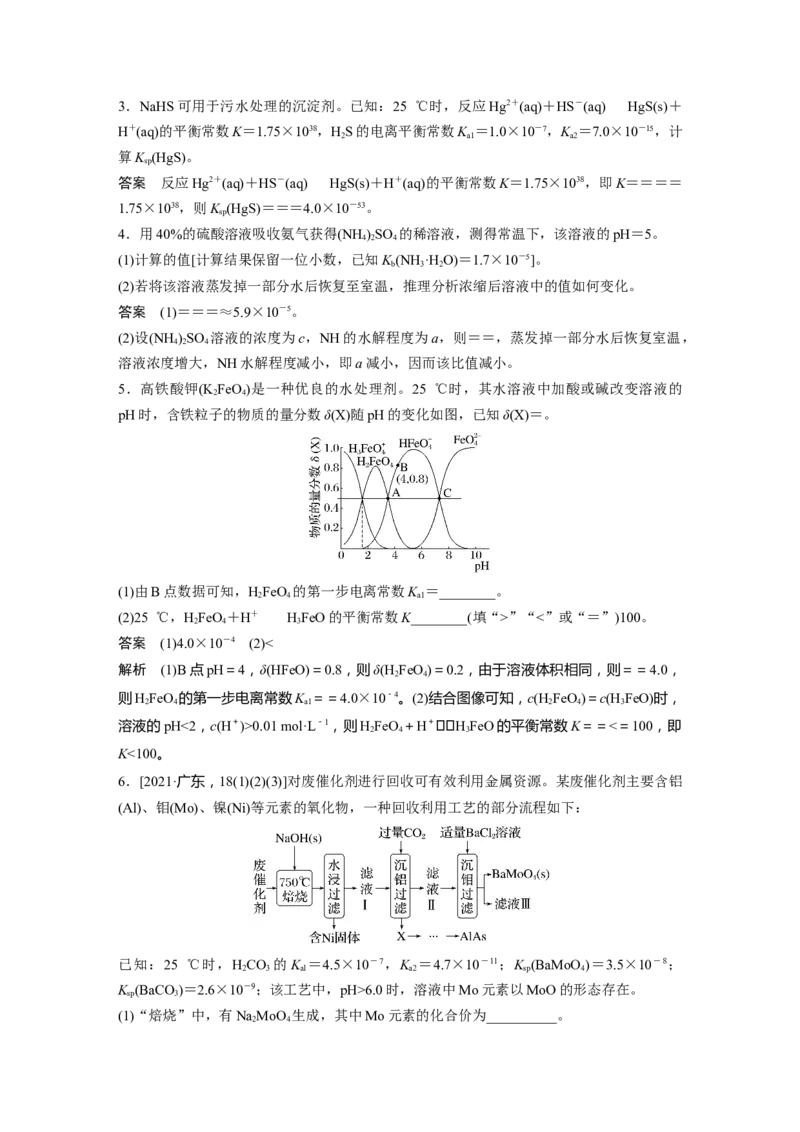
5.高铁酸钾(K FeO)是一种优良的水处理剂。25 ℃时,其水溶液中加酸或碱改变溶液的
2 4
pH时,含铁粒子的物质的量分数δ(X)随pH的变化如图,已知δ(X)=。
(1)由B点数据可知,HFeO 的第一步电离常数K =________。
2 4 a1
(2)25 ℃,HFeO+H+HFeO的平衡常数K________(填“>”“<”或“=”)100。
2 4 3
答案 (1)4.0×10-4 (2)<
解析 (1)B点pH=4,δ(HFeO)=0.8,则δ(H FeO)=0.2,由于溶液体积相同,则==4.0,
2 4
则HFeO 的第一步电离常数K ==4.0×10-4。(2)结合图像可知,c(H FeO)=c(H FeO)时,
2 4 a1 2 4 3
溶液的pH<2,c(H+)>0.01 mol·L-1,则HFeO +H+HFeO的平衡常数K==<=100,即
2 4 3
K<100。
6.[2021·广东,18(1)(2)(3)]对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝
(Al)、钼(Mo)、镍(Ni)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25 ℃时,HCO 的K =4.5×10-7,K =4.7×10-11;K (BaMoO )=3.5×10-8;
2 3 al a2 sp 4
K (BaCO)=2.6×10-9;该工艺中,pH>6.0时,溶液中Mo元素以MoO的形态存在。
sp 3
(1)“焙烧”中,有NaMoO 生成,其中Mo元素的化合价为__________。
2 4(2)“沉铝”中,生成的沉淀X为________。
(3)“沉钼”中,pH为7.0。
①生成 BaMoO 的离子方程式为_________________________________________。
4
②若条件控制不当,BaCO 也会沉淀。为避免 BaMoO 中混入 BaCO 沉淀,溶液中
3 4 3
c(HCO)∶c(MoO)=__________________________(列出算式)时,应停止加入BaCl 溶液。
2
答案 (1)+6 (2)Al(OH) (3)①MoO+Ba2+===BaMoO↓ ②
3 4
解析 (1)“焙烧”中,有NaMoO 生成,其中Na和O的化合价分别为+1和-2,根据化
2 4
合物中各元素化合价的代数和为0可知,Mo元素的化合价为+6。
(2)“沉铝”中,偏铝酸钠转化为氢氧化铝,因此,生成的沉淀X为Al(OH) 。
3
(3)①滤液Ⅱ中含有钼酸钠,加入氯化钡溶液后生成BaMoO 沉淀,该反应的离子方程式为
4
MoO+Ba2+===BaMoO↓。②若开始生成BaCO 沉淀,则体系中恰好建立如下平衡:HCO
4 3
+BaMoOBaCO +MoO+H+,该反应的化学平衡常数K===。为避免BaMoO 中混入
4 3 4
BaCO 沉淀,必须满足≤,由于“沉钼”中pH为7.0,c(H+)=1×10-7 mol·L-1,所以溶液
3
中=时,开始生成BaCO 沉淀, 因此,c(HCO)∶c(MoO)==时,应停止加入BaCl 溶液。
3 2
7.探究对氯苯甲酸(HA)在苯—水体系中的溶解状况。
已知:常温下,HA在水(W)和苯(B)两相间的分配系数:K ==1.00(只与温度有关)
D
在水中,HAH++A- ΔH>0,其K(HA)=1.00×10-4
a
在苯中,HA只发生二聚:2HA(HA)
2
实验测得:水中c(A-)=5.00×10-4 mol·L-1时,苯中的c=7.05×10-4 mol·L-1
试回答下列问题:
(1)水溶液的pH=________(lg 5≈0.7)。
(2)在苯中二聚反应的平衡常数K=________(结果保留三位有效数字)。
(3)若向萃取体系中滴入少量浓盐酸,则苯中 c将________(填“增大”“减小”或“不变”),
理由是___________________________________________________。
答案 (1)3.3 (2)1.13×102 (3)增大 浓盐酸只溶于水层,使水中c(H+)增大,电离平衡逆
向移动,c(HA) 增大,这促使更多的 HA 进入苯层[或 HA(W)HA(B)正向移动],使
W
c(HA) 增大,则苯中二聚平衡正向移动,最终c增大
W
解析 (1)水中c(A-)=5.00×10-4 mol·L-1时,c(H+)=5.00×10-4 mol·L-1,水溶液的pH=
-lg c(H+)=3.3。(2)K(HA)=1.00×10-4即==1×10-4,c(HA) =2.5×10-3 mol·L-1,K
a W D
==1.00,所以 c(HA) =2.5×10-3 mol·L-1,在苯中二聚反应的平衡常数 K==
B
≈1.13×102。