文档内容
一、选择题
1.(2019·洛阳第一次统考)能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的措施是(
)
A.向水中通入SO
2
B.将水加热煮沸
C.向纯水中投入一小块金属钠
D.向水中加入NaCl
解析:选A。在水中存在电离平衡:HOH++OH-。当向水中通入SO 时发生反应:
2 2
SO +HOHSO ,HSO H++HSO,HSO 电离产生的H+使溶液中的H+的浓度增大,
2 2 2 3 2 3 2 3
对水的电离起抑制作用,最终使水电离产生的H+(OH-)的浓度远远小于溶液中的H+浓度,
即溶液中的c(H+)>c(OH-),A项正确;水的电离是吸热过程,升高温度促进水的电离,所以将
水加热煮沸促进水的电离,但是水电离产生的H+和OH-的个数总是相同的,所以升温后水
中的H+和OH-的浓度仍然相等,B项错误;向纯水中投入一小块金属钠,钠与水发生反应:
2Na+2HO===2NaOH+H↑,促进水的电离,并使溶液中的c(OH-)>c(H+),C项错误;向水
2 2
中加入NaCl,NaCl是强酸强碱盐,对水的电离平衡无影响,所以溶液中的H+和OH-的浓度
仍然相等,D项错误。
2.(2019·福建质检)常温下,下列溶液的pH最大的是( )
A.0.02 mol·L-1氨水与水等体积混合后的溶液
B.pH=2的盐酸与pH=12的NaOH溶液等体积混合后的溶液
C.0.02 mol·L-1盐酸与0.02 mol·L-1氨水等体积混合后的溶液
D.0.01 mol·L-1盐酸与0.03 mol·L-1氨水等体积混合后的溶液
解析:选A。A项,混合后得到0.01 mol·L-1氨水,NH ·HO不能完全电离,则c(OH
3 2
-)<0.01 mol·L-1,70
2
C.向1 mol/L的HC O 溶液中加入等体积等浓度的NaOH溶液,完全反应后显酸性
2 2 4
D.向0.1 mol/L的HC O 溶液中加水稀释,的值将增大
2 2 4
解析:选B。根据图示,K (H C O)=
a1 2 2 4
=10-1×10-1=1×10-2,A正确;根据电荷守恒c(Na+)+c(H+)=c(HC O)+2c(C O)+
2 2
c(OH-),根据图示,K (H C O)==10-2×10-3=1×10-5,当pH=5时,c(HC O)=c(C O),所
a2 2 2 4 2 2
以c(Na+)-3c(HC O)=c(OH-)-c(H+)=10-9-10-5<0,B错误;向1 mol/L的HC O 溶液中
2 2 2 4
加入等体积等浓度的NaOH溶液,溶液中的溶质是NaHC O,HC O电离平衡常数是1×10-
2 4 2
5、水解平衡常数是=1×10-12,HC O的电离常数大于其水解常数,因此该溶液显酸性,C正
2
确;K (H C O)=,向0.1 mol/L的HC O 溶液中加水稀释,氢离子浓度减小,K (H C O)不
a1 2 2 4 2 2 4 a1 2 2 4
变,所以的值将增大,D正确。
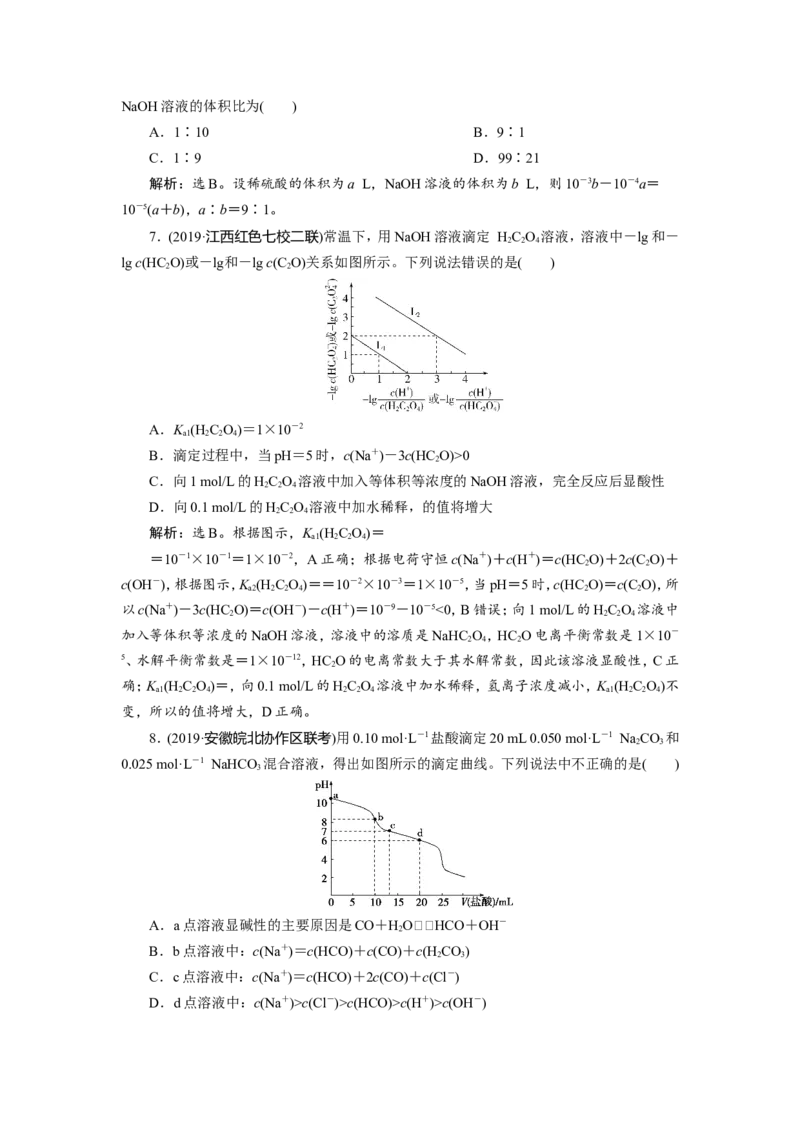
8.(2019·安徽皖北协作区联考)用0.10 mol·L-1盐酸滴定20 mL 0.050 mol·L-1 NaCO 和
2 3
0.025 mol·L-1 NaHCO 混合溶液,得出如图所示的滴定曲线。下列说法中不正确的是( )
3
A.a点溶液显碱性的主要原因是CO+HOHCO+OH-
2
B.b点溶液中:c(Na+)=c(HCO)+c(CO)+c(H CO)
2 3
C.c点溶液中:c(Na+)=c(HCO)+2c(CO)+c(Cl-)
D.d点溶液中:c(Na+)>c(Cl-)>c(HCO)>c(H+)>c(OH-)解析:选B。a点溶液为0.050 mol·L-1 NaCO 和0.025 mol·L-1 NaHCO 混合溶液,
2 3 3
NaCO 和NaHCO 均能水解使溶液呈碱性,但主要原因是CO的水解,A项正确;b点加入10
2 3 3
mL盐酸后,溶液中的溶质为NaHCO 和NaCl,由物料守恒得:c(Na+)=c(HCO)+c(CO)+
3
c(H CO)+c(Cl-),B项错误;根据电荷守恒可知,c(Na+)+c(H+)=c(HCO)+2c(CO)+c(Cl-)
2 3
+c(OH-),由于c点溶液显中性,c(H+)=c(OH-),所以c(Na+)=c(HCO)+2c(CO)+c(Cl-),C
项正确;d点加入20 mL 0.10 mol·L-1盐酸后,溶液中c(NaCl)=0.050 mol·L-1,c(NaHCO )=
3
0.012 5 mol·L-1,所以c(Na+)>c(Cl-)>c(HCO),又因为d点溶液pH<7,所以c(H+)>c(OH-),D
项正确。
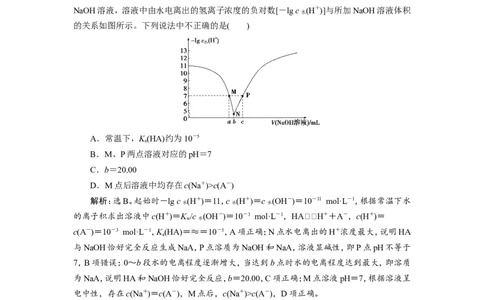
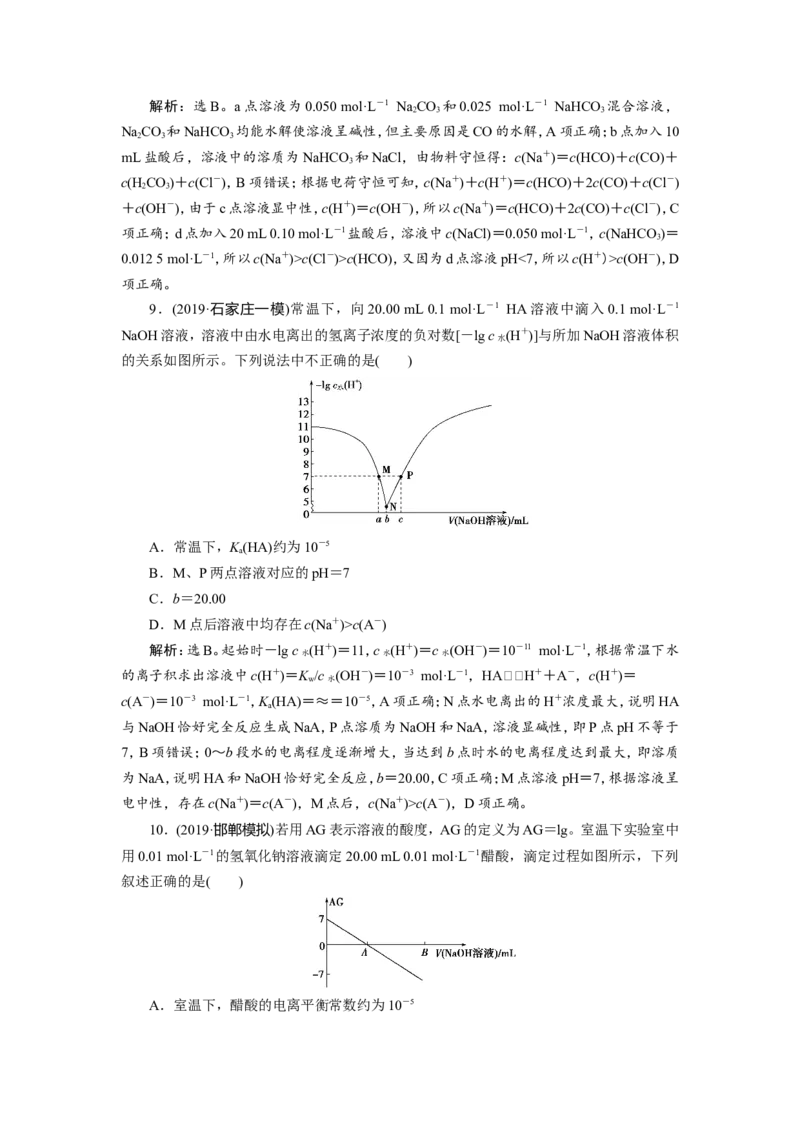
9.(2019·石家庄一模)常温下,向20.00 mL 0.1 mol·L-1 HA溶液中滴入0.1 mol·L-1
NaOH溶液,溶液中由水电离出的氢离子浓度的负对数[-lg c (H+)]与所加NaOH溶液体积
水
的关系如图所示。下列说法中不正确的是( )
A.常温下,K(HA)约为10-5
a
B.M、P两点溶液对应的pH=7
C.b=20.00
D.M点后溶液中均存在c(Na+)>c(A-)
解析:选B。起始时-lg c (H+)=11,c (H+)=c (OH-)=10-11 mol·L-1,根据常温下水
水 水 水
的离子积求出溶液中c(H+)=K /c (OH-)=10-3 mol·L-1,HAH++A-,c(H+)=
w 水
c(A-)=10-3 mol·L-1,K(HA)=≈=10-5,A项正确;N点水电离出的H+浓度最大,说明HA
a
与NaOH恰好完全反应生成NaA,P点溶质为NaOH和NaA,溶液显碱性,即P点pH不等于
7,B项错误;0~b段水的电离程度逐渐增大,当达到b点时水的电离程度达到最大,即溶质
为NaA,说明HA和NaOH恰好完全反应,b=20.00,C项正确;M点溶液pH=7,根据溶液呈
电中性,存在c(Na+)=c(A-),M点后,c(Na+)>c(A-),D项正确。
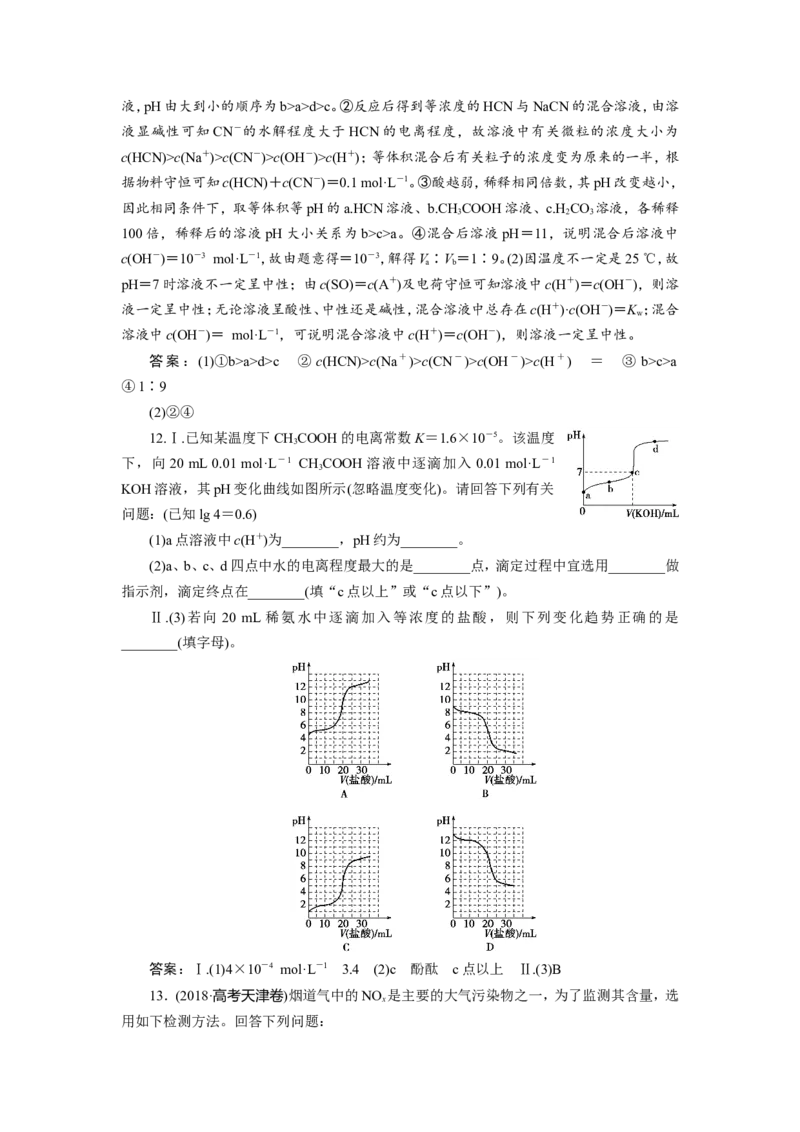
10.(2019·邯郸模拟)若用AG表示溶液的酸度,AG的定义为AG=lg。室温下实验室中
用0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定过程如图所示,下列
叙述正确的是( )
A.室温下,醋酸的电离平衡常数约为10-5B.A点时加入氢氧化钠溶液的体积为20.00 mL
C.若B点为40 mL,所得溶液中:c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
D.从A到B,水的电离程度逐渐变大
解析:选A。室温下,醋酸的AG=lg=7,即=107,而水的离子积K =c(H+)·c(OH-)=10
w
-14,两式联立可知:c(H+)=10-3.5 mol·L-1,而在醋酸溶液中,c(CHCOO-)≈c(H+)=10-3.5
3
mol·L-1,故电离平衡常数K=≈=10-5,故A正确;A点的AG=lg=0,即=1,即
a
c(H+)=c(OH-),溶液显中性,而当加入氢氧化钠溶液20.00 mL时,氢氧化钠和醋酸恰好完全
中和,得到醋酸钠溶液,溶液显碱性,故B错误;当B点加入NaOH溶液40 mL时,所得溶液
为等浓度的CHCOONa和NaOH的混合溶液,根据物料守恒可知,c(Na+)=2[c(CHCOO-)
3 3
+c(CHCOOH)],故C错误;A点之后,当V(NaOH)>20 mL时,水的电离受到抑制,电离程
3
度会逐渐变小,D项错误。
二、非选择题
11.(2019·呼和浩特高三检测)(1)已知下表数据:
化学式 电离平衡常数(25 ℃)
HCN K=5.0×10-10
a
CHCOOH K=1.8×10-5
3 a
HCO K =4.4×10-7,K =4.7×10-11
2 3 a1 a2
①25 ℃时,等浓度的四种溶液:a.NaCN 溶液;b.Na CO 溶液;c.CH COONa溶液;
2 3 3
d.NaHCO 溶液,pH由大到小的顺序为________________(填序号)。
3
②将0.2 mol·L-1 HCN溶液和0.1 mol·L-1的NaOH溶液等体积混合后,溶液显碱性,则
c(HCN)、c(H+)、c(OH-)、c(CN-)、c(Na+)大小排序为____________________________,
c(HCN)+c(CN-)________(填“>”“<”或“=”)0.1 mol·L-1。
③相同条件下,取等体积等pH的a.HCN溶液、b.CH COOH 溶液、c.H CO 溶液,各稀释
3 2 3
100倍,稀释后的溶液,其pH大小关系为____________(填序号)。
④25 ℃时,将体积为V、pH=13的某一元强碱与体积为V、pH=2的某二元强酸混合,
a b
若所得溶液的pH=11,则V∶V=________。
a b
(2)温度为T ℃时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的HSO 与b
w 2 4
mol·L-1的一元碱AOH等体积混合。则可判断溶液呈中性的是________(填序号)。
①混合溶液的pH=7
②c(SO)=c(A+)
③混合溶液中c(H+)·c(OH-)=K
w
④混合溶液中c(OH-)= mol·L-1
解析:(1)①由表中电离平衡常数可知酸性强弱:CHCOOH>H CO>HCN>HCO,相应的
3 2 3
酸根离子分别为CHCOO-、HCO、CN-、CO,酸的酸性越弱,其盐溶液中酸根离子水解程度
3
越大,故等浓度的四种溶液:a.NaCN溶液;b.Na CO 溶液;c.CH COONa溶液;d.NaHCO 溶
2 3 3 3液,pH由大到小的顺序为b>a>d>c。②反应后得到等浓度的HCN与NaCN的混合溶液,由溶
液显碱性可知CN-的水解程度大于HCN的电离程度,故溶液中有关微粒的浓度大小为
c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+);等体积混合后有关粒子的浓度变为原来的一半,根
据物料守恒可知c(HCN)+c(CN-)=0.1 mol·L-1。③酸越弱,稀释相同倍数,其pH改变越小,
因此相同条件下,取等体积等pH的a.HCN溶液、b.CH COOH溶液、c.H CO 溶液,各稀释
3 2 3
100倍,稀释后的溶液pH大小关系为b>c>a。④混合后溶液pH=11,说明混合后溶液中
c(OH-)=10-3 mol·L-1,故由题意得=10-3,解得V∶V=1∶9。(2)因温度不一定是25 ℃,故
a b
pH=7时溶液不一定呈中性;由c(SO)=c(A+)及电荷守恒可知溶液中c(H+)=c(OH-),则溶
液一定呈中性;无论溶液呈酸性、中性还是碱性,混合溶液中总存在c(H+)·c(OH-)=K ;混合
w
溶液中c(OH-)= mol·L-1,可说明混合溶液中c(H+)=c(OH-),则溶液一定呈中性。
答案:(1)①b>a>d>c ② c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+) = ③ b>c>a
④1∶9
(2)②④
12.Ⅰ.已知某温度下CHCOOH的电离常数K=1.6×10-5。该温度
3
下,向20 mL 0.01 mol·L-1 CHCOOH溶液中逐滴加入 0.01 mol·L-1
3
KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关
问题:(已知lg 4=0.6)
(1)a点溶液中c(H+)为________,pH约为________。
(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用________做
指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
Ⅱ.(3)若向 20 mL 稀氨水中逐滴加入等浓度的盐酸,则下列变化趋势正确的是
________(填字母)。
答案:Ⅰ.(1)4×10-4 mol·L-1 3.4 (2)c 酚酞 c点以上 Ⅱ.(3)B
13.(2018·高考天津卷)烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选
x
用如下检测方法。回答下列问题:将 v L气样通入适量酸化的H 2 O 2 溶液中,使NO x 完全被氧化成NO,加水稀释至100.00
mL。量取20.00 mL该溶液,加入 v1 mL c 1 mol·L-1 FeSO 4 标准溶液(过量),充分反应后,用
c 2 mol·L-1 K 2 Cr 2 O 7 标准溶液滴定剩余的Fe2+,终点时消耗 v2 mL。
(1)NO被HO 氧化为NO的离子方程式为____________________________________
2 2
________________________________________________________________________。
(2)滴定操作使用的玻璃仪器主要有____________________________________。
(3)滴定过程中发生下列反应:
3Fe2++NO+4H+===NO↑+3Fe3++2HO
2
Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
则气样中NO 折合成NO 的含量为________________mg·m-3。
x 2
(4)若FeSO 标准溶液部分变质,会使测定结果___________________________________
4
(填“偏高”“偏低”或“无影响”)。
解析:(1)NO被HO 氧化为NO,则HO 被还原为HO,配平离子方程式为2NO+
2 2 2 2 2
3HO===2NO+2H++2HO。(2)K Cr O 标准溶液具有强氧化性,能氧化碱式滴定管下端的
2 2 2 2 2 7
橡胶管,因此滴定操作使用的玻璃仪器主要有锥形瓶、酸式滴定管。(3)根据滴定原理,可得原
溶液中NO消耗的n(Fe2+)=(c
1
mol·L-1×
v1
×10-3 L-c
2
mol·L-1×
v2
×10-3 L×6)×=
5(c 1v1 -6c 2v2 )×10-3 mol,则n(NO)=n(Fe2+)=(c 1v1 -6c 2v2 )×10-3 mol,故气样中NO x 折合
成NO 2 的含量为(c 1v1 -6c 2v2 )×10-3 mol×46 000 mg·mol-1÷(v ×10-3) m3=×104 mg·m-
3。(4)若FeSO 标准溶液部分变质,则消耗的FeSO 标准溶液的体积偏大,测定结果偏高。
4 4
答案:(1)2NO+3HO===2H++2NO+2HO (2)锥形瓶、酸式滴定管
2 2 2
(3)×104 (4)偏高