文档内容
章末综合检测(三)
(时间:45分钟 分值:100分)
一、选择题(本题包括10小题,每小题6分,共60分)
1(. 2019·蚌埠高三第二次质检)化学与生活、社会发展息息相关,下列有关说法不正确的
是( )
A.将海水中的镁转化为氯化镁,再电解熔融氯化镁可制得金属镁
B.稻草秸秆和甘蔗渣中富含纤维素,可以用它来制造纸张
C.芯片制造中的“光刻技术”是利用光敏树脂在曝光条件下成像,该过程涉及化学变化
D.《新修本草》中有关“青矾”的描述为“本来绿色,新出窟未见风者,正如瑠璃……烧
之赤色……”这里的赤色是析出了Cu单质
解析:选D。海水中的Mg2+经一系列转化为MgCl ,然后电解熔融MgCl 得到Mg,A正确;
2 2
植物的叶茎的主要成分是纤维素,纸的主要成分也是纤维素,B正确;光敏树脂遇光会导致分
子结构发生变化,C正确;青矾是硫酸亚铁晶体,灼烧时生成的红棕色物质是Fe O,D错误。
2 3
2.(2019·哈尔滨模拟)化学已深入我们的生活。下列有关说法不正确的是( )
A.PM2.5含有的铅、镉、铬、钒等对人体有害的元素是金属元素
B.铝与Fe O 发生铝热反应,反应后固体物质增重
2 3
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,“剂钢”指的是铁的合金
解析:选B。铝与氧化铁发生铝热反应,由质量守恒定律知,反应前后固体质量不变(因为
反应物、产物均为固体)。
3.下列有关金属的工业制法中,正确的是( )
A.制钠:以海水为原料制得精盐,再电解纯净的NaCl溶液
B.制铁:以铁矿石为原料,CO还原得铁
C.制镁:以海水为原料,经一系列过程制得氧化镁固体,H 还原得镁
2
D.制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得铝
解析:选B。工业制钠是电解熔融NaCl:2NaCl(熔融)=====2Na+Cl↑,而电解NaCl溶液:
2
2NaCl+2HO=====2NaOH+H↑+Cl↑得不到钠,故A错误;工业制铁是用CO还原铁矿
2 2 2
石:3CO+Fe O=====2Fe+3CO ,故 B 正确;工业制镁是电解熔融 MgCl :MgCl (熔
2 3 2 2 2
融)=====Mg+Cl↑,故C错误;工业制铝是电解熔融Al O:2Al O(熔融)=====4Al+3O↑,
2 2 3 2 3 2
AlCl 是共价化合物,在熔融状态下不导电,故D错误。
3
4.(2019·佛山模拟)“类推”这种思维方法在化学学习与研究中有时会产生错误结论,因
此类推的结论最终要经过实践的检验才能确定其是否正确。下列几种类推结论中错误的是(
)
①钠与水反应生成NaOH和H;所有金属与水反应都生成碱和H
2 2
②铁露置在空气中一段时间后会生锈;性质更活泼的铝不能稳定存在于空气中
③Al(OH) 、Cu(OH) 受热易分解;Fe(OH) 受热也易分解
3 2 3
④不能用电解熔融的AlCl 来制取金属铝,也不能用电解熔融的MgCl 来制取金属镁
3 2
A.①④ B.②④
C.①②④ D.①②③④
解析:选C。①活泼金属钠与水反应生成NaOH和H,金属与水反应不一定生成碱,如Fe
2
与水蒸气在高温下反应生成Fe O 和H,错误;②铁露置在空气中一段时间后会生锈,是因为
3 4 2
发生了电化学腐蚀,金属铝在空气中和O 反应表面生成一层致密的氧化铝薄膜,阻止O 与内
2 2部铝反应,所以铝能稳定存在于空气中,错误;③难溶性碱受热易分解,所以Fe(OH) 受热也
3
易分解,正确;④AlCl 是共价化合物,熔融状态下不导电,故不能用电解熔融的AlCl 来制取
3 3
金属铝,MgCl 是离子化合物,熔融状态下导电,能用电解熔融的MgCl 来制取金属镁,错误。
2 2
5.(2019·北京海淀区模拟)元素及其化合物丰富了物质世界。下列说法正确的是( )
A.铜在冷的浓硫酸中会钝化,所以把铜放入冷的浓硫酸中无明显现象
B.NaOH溶液和AlCl 溶液相互滴加的现象不同
3
C.金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属
D.Al与热水反应困难,故活泼性不及Al的金属在任何条件下均不能与HO发生反应
2
解析:选B。 A.铜与冷的浓硫酸不反应,不是因为铜与浓硫酸发生钝化,错误;B.氢氧化
钠溶液滴入氯化铝溶液中开始有沉淀生成然后沉淀逐渐消失,而把氯化铝滴入氢氧化钠溶液
中,开始无沉淀生成然后逐渐产生沉淀,但不会消失,正确;C.金属比非金属易失电子,但非金
属可以置换金属,如C与CuO的反应,错误;D.Al与热水反应困难,但活泼性不如Al的Fe与
水蒸气在高温条件下能反应生成四氧化三铁和氢气,错误。
6.(2019·昆明模拟)下列实验现象与对应结论均正确的是( )
选项 操作 现象 结论
常温下将铁片放入浓硫酸 剧烈反应生成有刺激性气 常温下铁易与浓硫酸发生
A
中 味气体 反应
Al (SO ) 溶液中滴加过量 先生成白色沉淀,随后又溶
B 2 4 3 Al(OH) 能溶于氨水
稀氨水 解 3
向某溶液中滴加
C 析出蓝色沉淀 该溶液中含有Fe2+
K[Fe(CN) ]溶液
3 6
将表面氧化的铜丝从酒精 CuO被内焰中的乙醇蒸气
D 黑色的铜丝变红
灯的外焰慢慢移向内焰 氧化
解析:选C。A中现象错误,常温下铁遇浓HSO 会钝化,但无明显现象;B中现象和结论
2 4
均错误,Al(OH) 不溶于氨水中;D中结论错误,应是CuO被乙醇蒸气还原。
3
7.(2019·高考天津卷)下列有关金属及其化合物的应用不合理的是( )
A.将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
2 2
B.铝中添加适量锂,制得低密度、高强度的铝合金,可用于航空工业
C.盐碱地(含较多NaCO 等)不利于作物生长,可施加熟石灰进行改良
2 3
D.无水CoCl 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
2
解析:选C。将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl,发生反应2FeCl
2 2 2
+Cl===2FeCl 、2FeCl +Fe===3FeCl ,A项正确;铝中添加适量锂,制得的铝合金密度小、硬
2 3 3 2
度大,可用于航空工业,B项正确;盐碱地中施加熟石灰,发生反应NaCO +Ca(OH)
2 3
===CaCO +2NaOH,生成的NaOH为强碱,不利于作物生长,C项错误;无水CoCl 吸水后会
2 3 2
发生颜色变化,可用于判断变色硅胶是否吸水,D项正确。
8.利用废旧镀锌铁皮可制备磁性Fe O 胶体粒子及副产物ZnO。制备流程图如下:
3 4
已知:Zn及其化合物的性质与Al及其化合物的性质相似。下列相关说法错误的是( )
A.用NaOH溶液处理废旧镀锌铁皮的作用是去除油污、溶解镀锌层
B.调节溶液A的pH产生Zn(OH) 沉淀,经抽滤、洗涤、灼烧即可制得ZnO
2C.由溶液B制得Fe O 胶体粒子的过程中,须持续通N,其原因是防止Fe2+被氧化
3 4 2
D.Fe O 胶体粒子能用减压过滤法实现固液分离
3 4
解析:选D。NaOH能除油污、溶解镀锌层,A正确;调节溶液A的pH产生Zn(OH) 沉淀,
2
经抽滤、洗涤、灼烧Zn(OH) 分解制得ZnO,B正确;Fe2+容易被氧化,C正确;Fe O 胶体粒子
2 3 4
能透过滤纸,D错误。
9.下列实验过程中产生的现象与对应的图像不相符的是( )
解析:选C。NaOH溶液和AlCl 溶液按4∶1混合后完全转化为NaAlO ,继续加入AlCl
3 2 3
溶液,发生反应为Al3++3AlO+6HO===4Al(OH) ↓,A项正确;NaAlO 溶液中加入稀盐酸立
2 3 2
即有沉淀生成,继续加入盐酸,沉淀溶解,其反应为NaAlO +HCl+HO===Al(OH) ↓+
2 2 3
NaCl,Al(OH) +3HCl===AlCl +3HO,B 项正确;NaCO 溶液中加入稀盐酸先转化为
3 3 2 2 3
NaHCO 和NaCl,NaCO 完全转化为NaHCO 后,再加入稀盐酸才产生气体,C项错误;向含
3 2 3 3
Mg2+和Al3+的溶液中加入NaOH溶液得到Mg(OH) 和Al(OH) 两种沉淀,继续加入NaOH溶
2 3
液,Al(OH) 沉淀溶解,D项正确。
3
10.部分氧化的铁铜合金样品(氧化产物为Fe O、CuO)共5.76 g,经如下处理:
2 3
下列说法正确的是( )
A.滤液A中的阳离子为Fe3+、Fe2+、H+
B.样品中Fe元素的质量为2.24 g
C.样品中CuO的质量为4.0 g
D.V=896
解析:选B。因为硫酸足量,滤液A中不含Cu2+,且只有金属Cu不与HSO 反应,所以滤
2 4
渣3.2 g为金属铜,物质的量为0.05 mol,即合金样品中总共含有铜元素0.05 mol;滤液A中加
入足量NaOH溶液,所得滤渣灼烧得到的固体3.2 g为Fe O。生成的滤渣3.2 g是铜,金属铜
2 3
可以和Fe3+反应,所以滤液A中一定不含Fe3+,则滤液A中含有的阳离子为Fe2+、H+,A错误;
Fe元素的物质的量为×2=0.04 mol,其质量为0.04 mol×56 g·mol-1=2.24 g,B正确;根据B
项分析可知铁元素质量为2.24 g,而合金样品质量为5.76 g,所以CuO的质量不超过5.76 g-
2.24 g=3.52 g,C错误;最后滤液A中溶质为过量HSO 和FeSO ,而铁元素物质的量为0.04
2 4 4
mol,说明参加反应的硫酸的物质的量为0.04 mol,含H+ 0.08 mol,其中部分H+生成氢气,另
外的H+和合金中的O2-结合成水,由于合金中氧元素的物质的量为=0.02 mol,全转化为HO
2
需消耗H+ 0.04 mol,所以硫酸中生成H 的H+的物质的量为0.08 mol-0.04 mol=0.04 mol,
2
即生成0.02 mol H,标准状况下体积为448 mL,D错误。
2
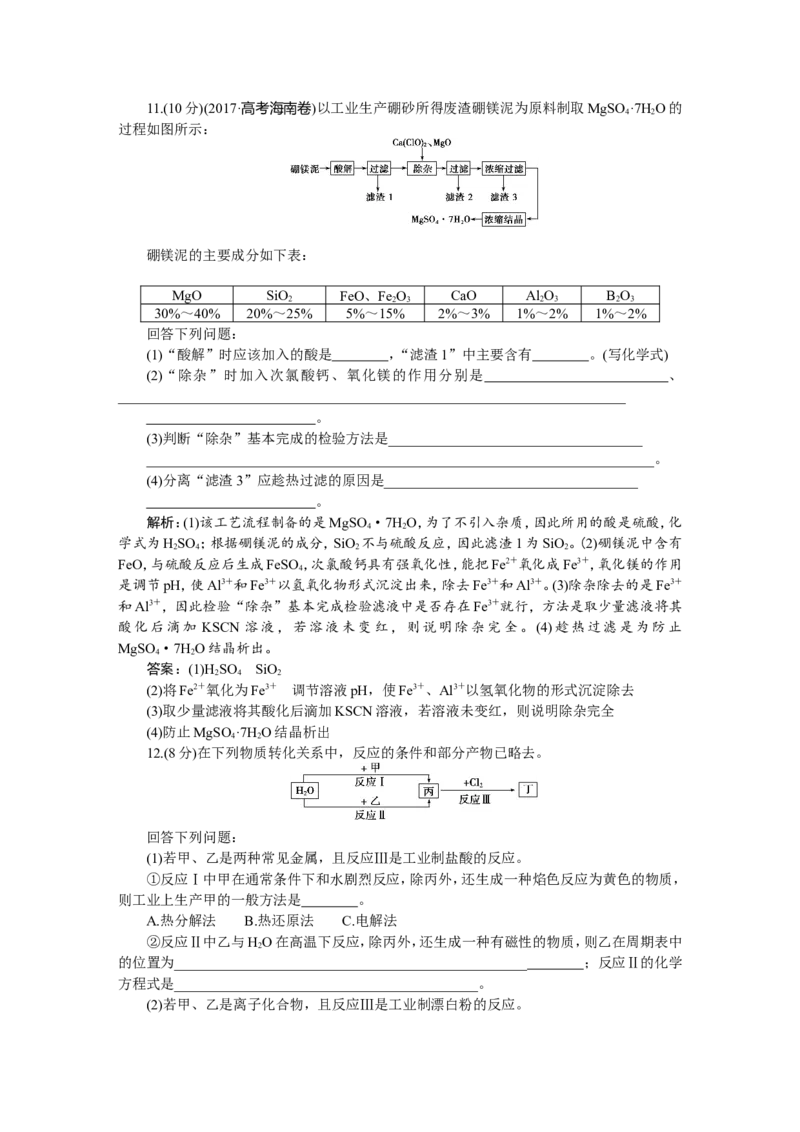
二、非选择题(本题包括4小题,共40分)11.(10分)(2017·高考海南卷)以工业生产硼砂所得废渣硼镁泥为原料制取MgSO ·7H O的
4 2
过程如图所示:
硼镁泥的主要成分如下表:
MgO SiO FeO、Fe O CaO Al O B O
2 2 3 2 3 2 3
30%~40% 20%~25% 5%~15% 2%~3% 1%~2% 1%~2%
回答下列问题:
(1)“酸解”时应该加入的酸是 ,“滤渣1”中主要含有 。(写化学式)
(2)“除杂”时加入次氯酸钙、氧化镁的作用分别是 、
________________________________________________________________________
。
(3)判断“除杂”基本完成的检验方法是____________________________________
________________________________________________________________________。
(4)分离“滤渣3”应趁热过滤的原因是____________________________________
。
解析:(1)该工艺流程制备的是MgSO ·7HO,为了不引入杂质,因此所用的酸是硫酸,化
4 2
学式为HSO ;根据硼镁泥的成分,SiO 不与硫酸反应,因此滤渣1为SiO。(2)硼镁泥中含有
2 4 2 2
FeO,与硫酸反应后生成FeSO ,次氯酸钙具有强氧化性,能把Fe2+氧化成Fe3+,氧化镁的作用
4
是调节pH,使Al3+和Fe3+以氢氧化物形式沉淀出来,除去Fe3+和Al3+。(3)除杂除去的是Fe3+
和Al3+,因此检验“除杂”基本完成检验滤液中是否存在Fe3+就行,方法是取少量滤液将其
酸化后滴加 KSCN 溶液,若溶液未变红,则说明除杂完全。(4)趁热过滤是为防止
MgSO ·7HO结晶析出。
4 2
答案:(1)H SO SiO
2 4 2
(2)将Fe2+氧化为Fe3+ 调节溶液pH,使Fe3+、Al3+以氢氧化物的形式沉淀除去
(3)取少量滤液将其酸化后滴加KSCN溶液,若溶液未变红,则说明除杂完全
(4)防止MgSO ·7H O结晶析出
4 2
12.(8分)在下列物质转化关系中,反应的条件和部分产物已略去。
回答下列问题:
(1)若甲、乙是两种常见金属,且反应Ⅲ是工业制盐酸的反应。
①反应Ⅰ中甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,
则工业上生产甲的一般方法是 。
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中乙与HO在高温下反应,除丙外,还生成一种有磁性的物质,则乙在周期表中
2
的位置为__________________________________________________ ;反应Ⅱ的化学
方程式是___________________________________________。
(2)若甲、乙是离子化合物,且反应Ⅲ是工业制漂白粉的反应。①反应Ⅲ的化学方程式是___________________________________________________。
②若反应Ⅰ是实验室制备某气体的反应,该气体分子为14电子结构。则反应Ⅰ的化学方
程式是 。
③在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体,其反应的离
子方程式是______________________________________________________
________________________________________________________________________;
写出HClO的结构式: 。
解析:(1)若甲、乙是两种常见金属,和水反应生成丙,且反应Ⅲ是工业制盐酸的反应,则
丙是氢气。
①甲和水反应生成的产物中除丙(氢气)外,还生成一种焰色反应为黄色的物质,则是氢氧
化钠,判断甲为钠,在工业生产中利用电解熔融氯化钠的方法得到金属钠。
②反应Ⅱ中乙与HO在高温下反应时,除丙外,还生成一种有磁性的物质,则乙为铁,铁
2
和水蒸气反应生成四氧化三铁和氢气,反应的化学方程式为3Fe+4HO(g)=====Fe O+4H。
2 3 4 2
(2)①若甲、乙是离子化合物,且反应Ⅲ是工业制漂白粉的反应,则丙是氢氧化钙,氢氧化
钙和氯气反应生成氯化钙、次氯酸钙和水。
②气体分子为14电子结构的物质是乙炔,故反应Ⅰ应为碳化钙和水的反应。
③氯水中含有HCl和HClO:Cl+HOHCl+HClO,在饱和氯水中加块状石灰石,碳酸
2 2
钙和盐酸反应生成氯化钙、二氧化碳和水,促进上述平衡右移,从而能制得较浓HClO溶液。
答案:(1)①C ②第四周期Ⅷ族 3Fe+4HO(g)=====Fe O+4H
2 3 4 2
(2)①2Cl+2Ca(OH) ===Ca(ClO)+CaCl +2HO
2 2 2 2 2
②CaC +2HO―→Ca(OH) +C H↑
2 2 2 2 2
③2Cl+HO+CaCO ===Ca2++2Cl-+2HClO+CO H—O—Cl
2 2 3 2
13.(10分)(2019·南京模拟)硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分
为ZnO,还含有Fe O、CuO、SiO 等杂质)制备ZnSO·7H O的流程如下:
2 3 2 4 2
相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计
算)如表所示:
金属离子 开始沉淀的pH 沉淀完全的pH
Fe3+ 1.1 3.2
Fe2+ 5.8 8.8
Zn2+ 6.4 8.0
(1)“滤渣1”的主要成分为 (填化学式)。“酸浸”过程中,提高锌元素浸出率的
措施有适当提高酸的浓度、 (填一种)。
(2)“置换”过程中,加入适量的锌粉,除与溶液中的Fe3+、H+反应外,另一主要反应的化
学方程式为_______________________________________________________
________________________________________________________________________。
(3)“氧化”一步中,发生反应的离子方程式为________________________________
________________________________________________________________________。
溶液pH控制在[3.2,6.4)之间的目的是____________________________________
。
(4)“母液”中含有的盐类物质有_______________________________________
(填化学式)。
答案:(1)SiO 粉碎锌白矿(或充分搅拌浆料、适当加热等)
2(2)Zn+CuSO ===Cu+ZnSO
4 4
(3)3Fe2++MnO+7ZnO+9H+===3Fe(OH) +MnO +7Zn2+ 使Fe3+沉淀完全,而Zn2+不
3 2
沉淀
(4)ZnSO 、KSO
4 2 4
14.(12分)(2019·潍坊模拟)铜及其化合物在生产生活中有广泛应用,铜在化合物中的常见
化合价有+1、+2。已知Cu O与稀硫酸反应,溶液呈蓝色。
2
(1)工业上可用Cu S+O=====2Cu+SO 反应制取粗铜,该反应中 元素被还原。
2 2 2
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50 ℃,加入HO 溶液,一段时间后,升
2 2
温到60 ℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为 。温
度控制在50~60 ℃的原因除了加快反应速率外,还有_______________________
。在CuSO 溶液中加入一定量的NaSO 和NaCl溶液加热,
4 2 3
生成CuCl沉淀,写出生成CuCl的离子方程式:________________________________
________________________________________________________________________。
(3)现向Cu、Cu O和CuO组成的混合物中,加入2 L 0.6 mol·L-1 HNO 溶液恰好使混合
2 3
物溶解,同时收集到4 480 mL NO气体(标准状况)。Cu O与稀硝酸反应的离子方程式为
2
________________________________________________________________________。
若将上述混合物用足量的H 加热还原,所得到固体的质量为 g。若混合物中含
2
0.2 mol Cu,将该混合物与稀硫酸充分反应,消耗HSO 的物质的量为 mol。
2 4
解析:(1)在该反应中铜、氧元素的化合价降低,得到电子,被还原。(3)Cu O与稀硝酸反应
2
的离子方程式是3Cu O+2NO+14H+===6Cu2++2NO↑+7HO。硝酸发生反应后氮元素的存
2 2
在形式是 Cu(NO ) 和 NO,由 2 L×0.6 mol·L-1=2n[Cu(NO )]+4.480 L÷22.4 L·mol-1得
3 2 3 2
n[Cu(NO )]=0.5 mol,n(Cu2+)=0.5 mol,所以若将上述混合物用足量的H 加热还原,所得到
3 2 2
固体的质量为0.5 mol×64 g·mol-1=32 g。若混合物中含0.2 mol Cu,则根据铜原子守恒可得:
2n(Cu O)+n(CuO)=0.3 mol;根据得失电子守恒可得:2n(Cu)+2n(Cu O)=3×(4.480 L÷22.4
2 2
L·mol-1),解得n(CuO)=0.1 mol,n(Cu O)=0.1 mol,消耗HSO 的物质的量为0.1 mol+0.1
2 2 4
mol=0.2 mol。
答案:(1)铜、氧
(2)Cu+HO +2H+===Cu2++2HO 防止 HO 分解 2Cu2++2Cl-+SO+
2 2 2 2 2
HO=====2CuCl↓+SO+2H+
2
(3)3Cu O+2NO+14H+===6Cu2++2NO↑+7HO 32 0.2
2 2