文档内容
2023年虹口区高考化学一模卷
相对原子质量:H-1 C-12 N-14 O-16 S-32
一、 选择题(本题共40分,每小题2分,每题只有一个正确选项)
1. 化学与生活密切相关,下列叙述正确的是
A. HB铅笔芯的成分为二氧化铅 B. 青铜与黄铜是不同结构的单质铜
C. 干冰可用在舞台上制造“云雾” D. 二氧化碳是形成酸雨的主要物质
2. 2022年3月神州十三号航天员在中国空间站进行了“天宫课堂”授课活动,其中太空“冰雪实验”展
现了过饱和醋酸钠溶液结晶现象。下列说法错误的是
A. 醋酸钠是强电解质 B. 醋酸钠是离子晶体
C. 醋酸钠是极性分子 D. 醋酸钠溶液呈碱性
3. 下列有关化学用语的说法正确的是
A. NaO 的电子式是 B. 二氧化硅的分子式是 SiO
2 2 2
C. Si原子的核外电子排布式是 3s23p2 D. 乙烯的结构式是 HC=CH
2 2
4. 下列试剂的实验室保存方法错误的是
A. 浓硝酸保存在棕色细口瓶中 B. 四氯化碳保存在广口塑料瓶中
C. 高锰酸钾固体保存在棕色广口瓶中 D. 氢氧化钠固体保存在广口塑料瓶中
5. 向某试剂中滴加少量溴水,振荡、静置后分层,上下层均无色,该试剂可能是
A. 苯 B. 四氯化碳 C.己烯 D. 溴乙烷
6. 同温同压同体积的16O 与18O,下列说法正确的是
2 2
A. 电子数相同 B. 沸点相同 C. 互为同位素 D. 分子量相同
7. 由键能数据大小,不能解释下列事实的是
A. 熔点:CO < SiO B. 活泼性:N < P
2 2 2 4
C. 热稳定性:CH > SiH D. 硬度:金刚石 > 晶体硅
4 4
8. 下列除杂所选试剂错误的是
A. 溴苯(Br ):NaOH 溶液 B. Cl(HCl):饱和食盐水
2 2
C. C H(HS):CuSO 溶液 D. FeCl (CuCl ):铁粉
2 2 2 4 3 2
9. 电解CuCl ,在阴极出现的现象是
2
A. 红色沉淀 B. 蓝色沉淀 C. 无色气体 D. 黄绿色气体
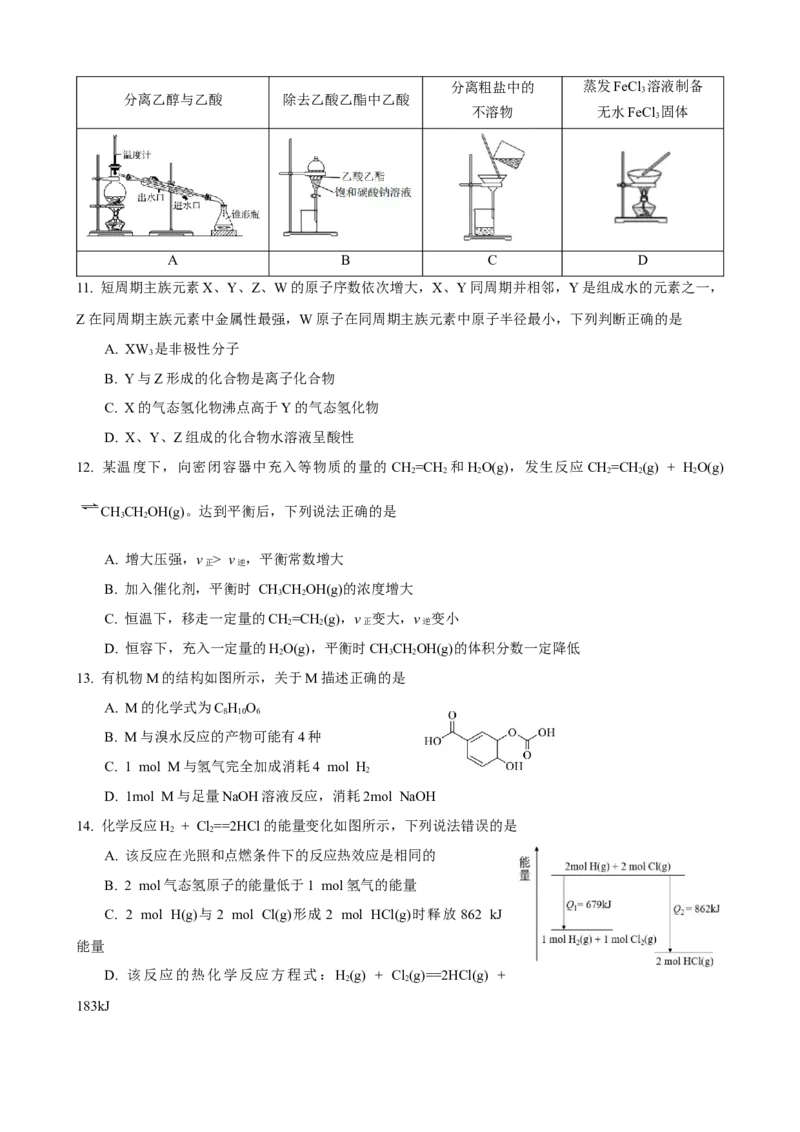
10. 下列实验中,不能达到实验目的的是分离粗盐中的 蒸发FeCl 溶液制备
3
分离乙醇与乙酸 除去乙酸乙酯中乙酸
不溶物 无水FeCl 固体
3
A B C D
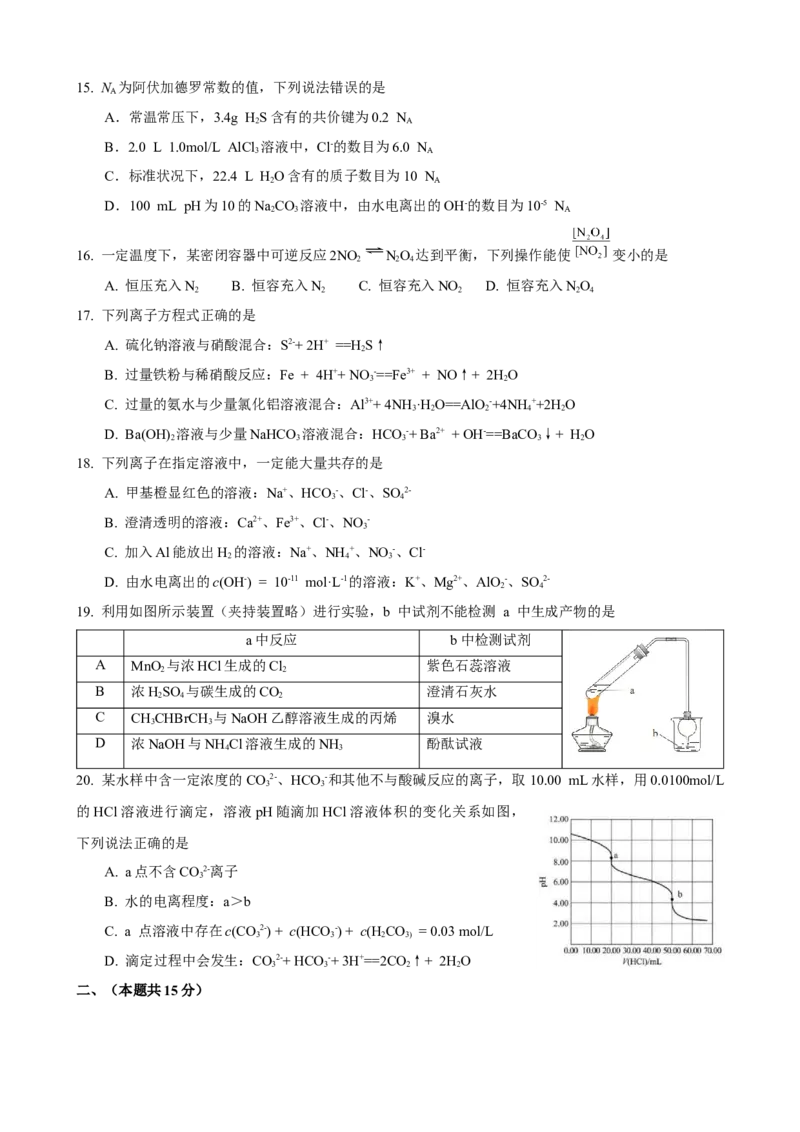
11. 短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y是组成水的元素之一,
Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列判断正确的是
A. XW 是非极性分子
3
B. Y与Z形成的化合物是离子化合物
C. X的气态氢化物沸点高于Y的气态氢化物
D. X、Y、Z组成的化合物水溶液呈酸性
12. 某温度下,向密闭容器中充入等物质的量的 CH=CH 和HO(g),发生反应 CH=CH (g) + HO(g)
2 2 2 2 2 2
CHCHOH(g)。达到平衡后,下列说法正确的是
3 2
A. 增大压强,v > v ,平衡常数增大
正 逆
B. 加入催化剂,平衡时 CHCHOH(g)的浓度增大
3 2
C. 恒温下,移走一定量的CH=CH (g),v 变大,v 变小
2 2 正 逆
D. 恒容下,充入一定量的HO(g),平衡时CHCHOH(g)的体积分数一定降低
2 3 2
13. 有机物M的结构如图所示,关于M描述正确的是
A. M的化学式为C H O
8 10 6
B. M与溴水反应的产物可能有4种
C. 1 mol M与氢气完全加成消耗4 mol H
2
D. 1mol M与足量NaOH溶液反应,消耗2mol NaOH
14. 化学反应H + Cl==2HCl的能量变化如图所示,下列说法错误的是
2 2
A. 该反应在光照和点燃条件下的反应热效应是相同的
B. 2 mol气态氢原子的能量低于1 mol氢气的能量
C. 2 mol H(g)与2 mol Cl(g)形成2 mol HCl(g)时释放862 kJ
能量
D. 该反应的热化学反应方程式:H(g) + Cl(g)==2HCl(g) +
2 2
183kJ15. N 为阿伏加德罗常数的值,下列说法错误的是
A
A.常温常压下,3.4g HS含有的共价键为0.2 N
2 A
B.2.0 L 1.0mol/L AlCl 溶液中,Cl-的数目为6.0 N
3 A
C.标准状况下,22.4 L HO含有的质子数目为10 N
2 A
D.100 mL pH为10的NaCO 溶液中,由水电离出的OH-的数目为10-5 N
2 3 A
16. 一定温度下,某密闭容器中可逆反应2NO NO 达到平衡,下列操作能使 变小的是
2 2 4
A. 恒压充入N B. 恒容充入N C. 恒容充入NO D. 恒容充入NO
2 2 2 2 4
17. 下列离子方程式正确的是
A. 硫化钠溶液与硝酸混合:S2-+ 2H+ ==HS↑
2
B. 过量铁粉与稀硝酸反应:Fe + 4H++ NO -==Fe3+ + NO↑+ 2HO
3 2
C. 过量的氨水与少量氯化铝溶液混合:Al3++ 4NH ·H O==AlO -+4NH++2H O
3 2 2 4 2
D. Ba(OH) 溶液与少量NaHCO 溶液混合:HCO -+ Ba2+ + OH-==BaCO ↓+ HO
2 3 3 3 2
18. 下列离子在指定溶液中,一定能大量共存的是
A. 甲基橙显红色的溶液:Na+、HCO -、Cl-、SO 2-
3 4
B. 澄清透明的溶液:Ca2+、Fe3+、Cl-、NO -
3
C. 加入Al能放出H 的溶液:Na+、NH +、NO -、Cl-
2 4 3
D. 由水电离出的c(OH-) = 10-11 mol·L-1的溶液:K+、Mg2+、AlO-、SO 2-
2 4
19. 利用如图所示装置(夹持装置略)进行实验,b 中试剂不能检测 a 中生成产物的是
a中反应 b中检测试剂
A MnO 与浓HCl生成的Cl 紫色石蕊溶液
2 2
B 浓HSO 与碳生成的CO 澄清石灰水
2 4 2
C CHCHBrCH 与NaOH乙醇溶液生成的丙烯 溴水
3 3
D 浓NaOH与NH Cl溶液生成的NH 酚酞试液
4 3
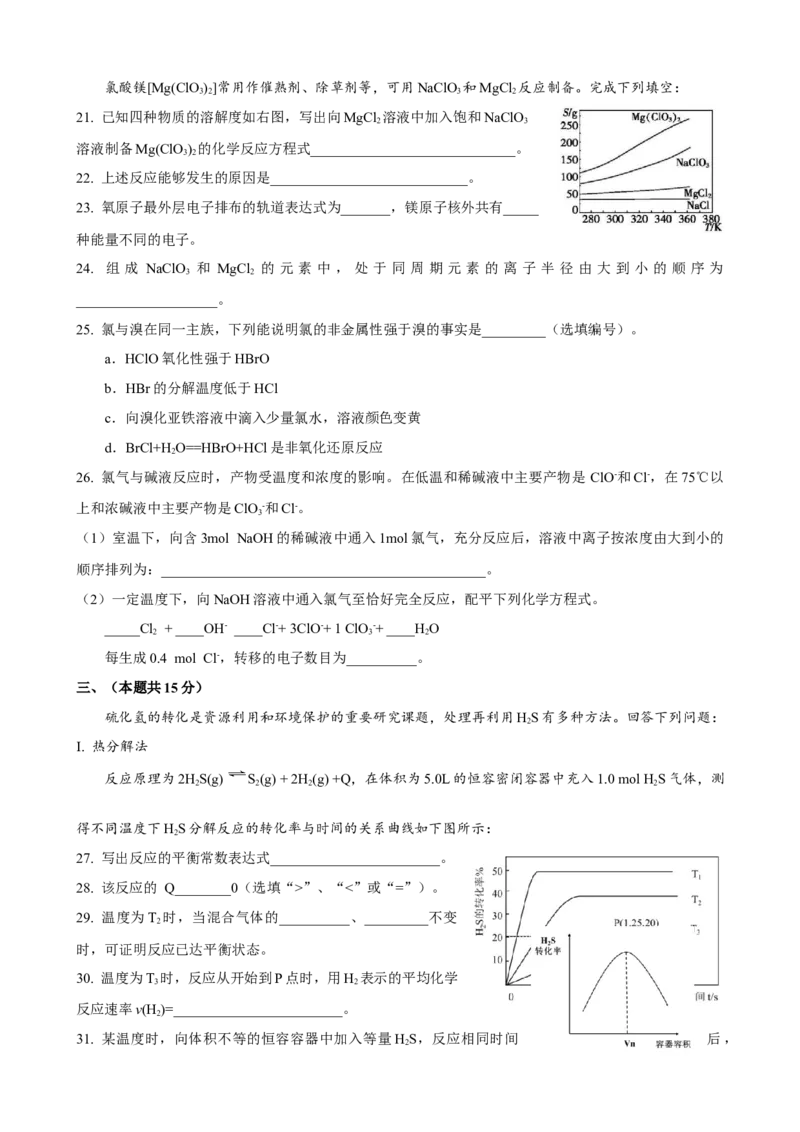
20. 某水样中含一定浓度的CO2-、HCO -和其他不与酸碱反应的离子,取10.00 mL水样,用0.0100mol/L
3 3
的HCl溶液进行滴定,溶液pH随滴加HCl溶液体积的变化关系如图,
下列说法正确的是
A. a点不含CO2-离子
3
B. 水的电离程度:a>b
C. a 点溶液中存在c(CO2-) + c(HCO -) + c(H CO = 0.03 mol/L
3 3 2 3)
D. 滴定过程中会发生:CO2-+ HCO -+ 3H+==2CO↑+ 2HO
3 3 2 2
二、(本题共15分)氯酸镁[Mg(ClO )]常用作催熟剂、除草剂等,可用NaClO 和MgCl 反应制备。完成下列填空:
3 2 3 2
21. 已知四种物质的溶解度如右图,写出向MgCl 溶液中加入饱和NaClO
2 3
溶液制备Mg(ClO) 的化学反应方程式_____________________________。
3 2
22. 上述反应能够发生的原因是____________________________。
23. 氧原子最外层电子排布的轨道表达式为_______,镁原子核外共有_____
种能量不同的电子。
24. 组 成 NaClO 和 MgCl 的 元 素 中 , 处 于 同 周 期 元 素 的 离 子 半 径 由 大 到 小 的 顺 序 为
3 2
____________________。
25. 氯与溴在同一主族,下列能说明氯的非金属性强于溴的事实是_________(选填编号)。
a.HClO氧化性强于HBrO
b.HBr的分解温度低于HCl
c.向溴化亚铁溶液中滴入少量氯水,溶液颜色变黄
d.BrCl+H O==HBrO+HCl是非氧化还原反应
2
26. 氯气与碱液反应时,产物受温度和浓度的影响。在低温和稀碱液中主要产物是 ClO-和Cl-,在75℃以
上和浓碱液中主要产物是ClO -和Cl-。
3
(1)室温下,向含3mol NaOH的稀碱液中通入1mol氯气,充分反应后,溶液中离子按浓度由大到小的
顺序排列为:______________________________________________。
(2)一定温度下,向NaOH溶液中通入氯气至恰好完全反应,配平下列化学方程式。
_____Cl + ____OH- ____Cl-+ 3ClO-+ 1 ClO -+ ____H O
2 3 2
每生成0.4 mol Cl-,转移的电子数目为__________。
三、(本题共15分)
硫化氢的转化是资源利用和环境保护的重要研究课题,处理再利用HS有多种方法。回答下列问题:
2
I. 热分解法
反应原理为2HS(g) S(g) + 2H(g) +Q,在体积为5.0L的恒容密闭容器中充入1.0 mol HS气体,测
2 2 2 2
得不同温度下HS分解反应的转化率与时间的关系曲线如下图所示:
2
27. 写出反应的平衡常数表达式________________________。
28. 该反应的 Q________0(选填“>”、“<”或“=”)。
29. 温度为T 时,当混合气体的__________、_________不变
2
时,可证明反应已达平衡状态。
30. 温度为T 时,反应从开始到P点时,用H 表示的平均化学
3 2
反应速率v(H )=________________________。
2
31. 某温度时,向体积不等的恒容容器中加入等量HS,反应相同时间 后,
2测得各容器中HS的转化率与容器体积关系如右图所示。V 之后,HS 的转化率下降的原因是_________。
2 n 2
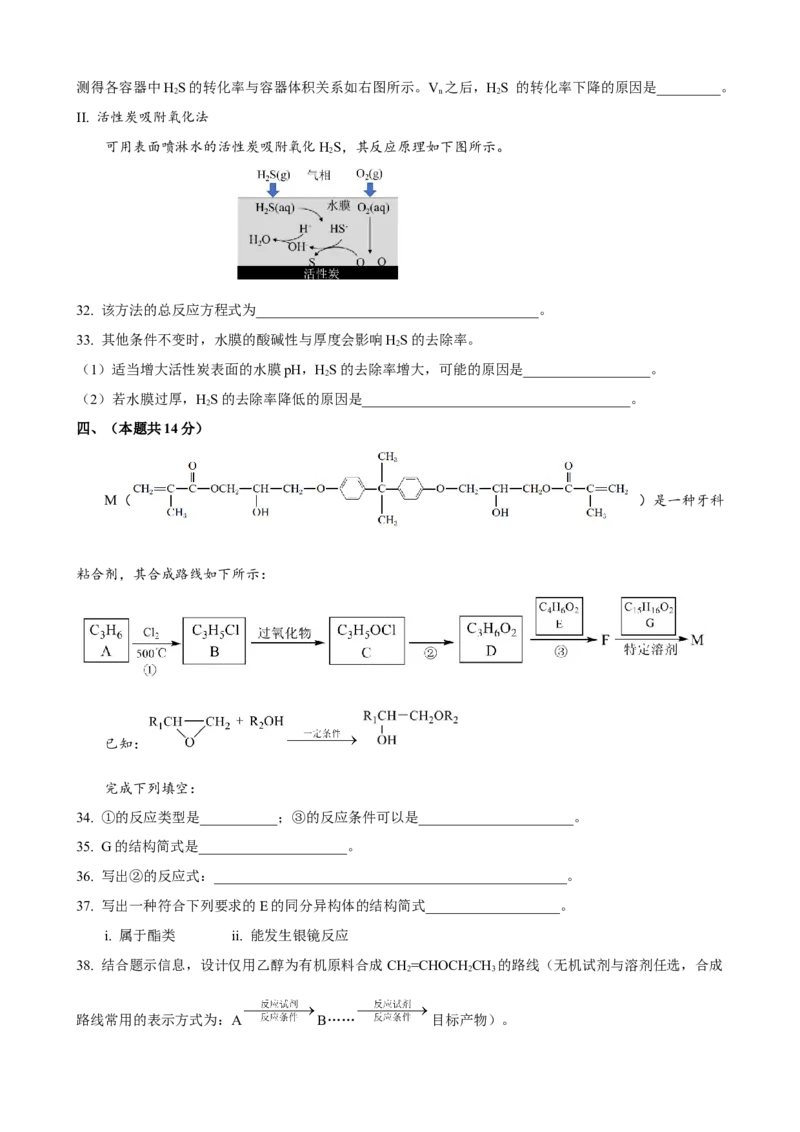
II. 活性炭吸附氧化法
可用表面喷淋水的活性炭吸附氧化HS,其反应原理如下图所示。
2
32. 该方法的总反应方程式为________________________________________。
33. 其他条件不变时,水膜的酸碱性与厚度会影响HS的去除率。
2
(1)适当增大活性炭表面的水膜pH,HS的去除率增大,可能的原因是__________________。
2
(2)若水膜过厚,HS的去除率降低的原因是______________________________________。
2
四、(本题共14分)
M( )是一种牙科
粘合剂,其合成路线如下所示:
已知:
完成下列填空:
34. ①的反应类型是___________;③的反应条件可以是______________________。
35. G的结构简式是_____________________。
36. 写出②的反应式:__________________________________________________。
37. 写出一种符合下列要求的E的同分异构体的结构简式___________________。
i. 属于酯类 ii. 能发生银镜反应
38. 结合题示信息,设计仅用乙醇为有机原料合成CH=CHOCH CH 的路线(无机试剂与溶剂任选,合成
2 2 3
路线常用的表示方式为:A B…… 目标产物)。五、(本题共16分)
硫化碱法是工业制备NaSO 的方法之一,某研究小组在实验室用硫化碱法制备NaSO·5H O。其原
2 2 3 2 2 3 2
理为:2NaS + Na CO + 4SO ==3Na SO + CO。
2 2 3 2 2 2 3 2
完成下列填空:
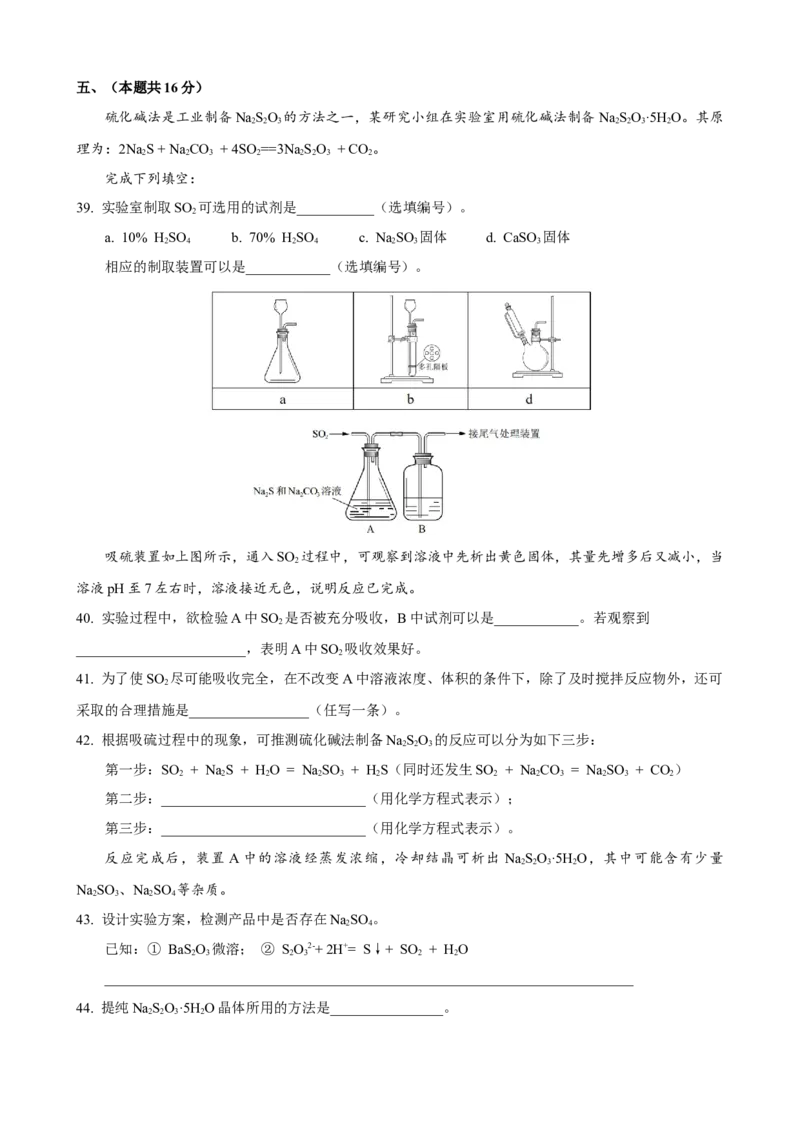
39. 实验室制取SO 可选用的试剂是___________(选填编号)。
2
a. 10% HSO b. 70% HSO c. NaSO 固体 d. CaSO 固体
2 4 2 4 2 3 3
相应的制取装置可以是____________(选填编号)。
吸硫装置如上图所示,通入SO 过程中,可观察到溶液中先析出黄色固体,其量先增多后又减小,当
2
溶液pH至7左右时,溶液接近无色,说明反应已完成。
40. 实验过程中,欲检验A中SO 是否被充分吸收,B中试剂可以是____________。若观察到
2
________________________,表明A中SO 吸收效果好。
2
41. 为了使SO 尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可
2
采取的合理措施是_________________(任写一条)。
42. 根据吸硫过程中的现象,可推测硫化碱法制备NaSO 的反应可以分为如下三步:
2 2 3
第一步:SO + NaS + HO = NaSO + HS(同时还发生SO + NaCO = NaSO + CO)
2 2 2 2 3 2 2 2 3 2 3 2
第二步:_____________________________(用化学方程式表示);
第三步:_____________________________(用化学方程式表示)。
反应完成后,装置 A中的溶液经蒸发浓缩,冷却结晶可析出 NaSO·5H O,其中可能含有少量
2 2 3 2
NaSO 、NaSO 等杂质。
2 3 2 4
43. 设计实验方案,检测产品中是否存在NaSO 。
2 4
已知:① BaS O 微溶; ② SO2-+ 2H+= S↓+ SO + HO
2 3 2 3 2 2
___________________________________________________________________________
44. 提纯NaSO·5HO晶体所用的方法是________________。
2 2 3 2高三化学试卷参考答案
一、(本题共 40 分)
1 2 3 4 5 6 7 8 9 10
C C A B C A A D A D
11 12 13 14 15 16 17 18 19 20
B D B B C A D B B B
二、(本题共 15 分)
21. MgCl + 2NaClO = 2NaCl↓+Mg(ClO ) (2分)
2 3 3 2
22. NaCl的溶解度最小,从溶液中析出,使反应得以发生(2分)
23. ;4 (每空1分)
24.Cl- > Na+ > Mg2+ (2分)
25.bd (2分)
26. (1)c(Na+)﹥c(OH-)﹥c(Cl-)﹥c(ClO-)﹥c(H+) (2分)
(2)6 、12 、8、 6 (1分) ; 0.4N (2分)
A
三、(本题共 15 分)
27. (1分)
28.<(2分)
29. 总压、总物质的量、总浓度、平均摩尔质量等(合理即可,每空1分)
30. 0.032 mol•L-1•s-1 (2分)
31.Vn之后的容器尚未达到平衡,随着容器容积增大,反应物浓度减小,反应速率减慢,相同时间内转化
率下降。(2分)
32. 2HS + O 2S↓+ 2H O(2分)
2 2 2
33.(1)c(H+)减小,使HS H+ + HS-电离平衡正向移动,c(HS-)增大(2分)
2
(2)水膜过厚,活性炭表面的溶解氧浓度减小,产生的O浓度减少(2分)
四、(本题共 14 分)34. 取代反应(2分);浓硫酸、加热(2分)
CH
3
35. HO C OH(2分)
CH
3
HO
CH CH CH Cl + NaOH 2 CH CH CH OH + NaCl
36. 2 2 2 2 (2分)
O O
CH COOCH
2
37. CH 3 、CH 3 CH=CHOOCH、CH 2 =CHCH 2 OOCH、 OOCH(2分,合理即可)
38. CH 3 CH 2 OH 浓 17 硫 0 酸 ℃ CH 2 CH 2 过氧化物 CH 2 CH 2 C 特 H 定 3C 溶 H 剂 2OH CH 2 CH 2 OCH 2 CH 3 浓硫 △ 酸 CH 2 CHOCH 2 CH 3(4分)
O OH
五、(本题共 16分)
39. bc(2分);c(2分)
40. 酸性高锰酸钾(或品红、或溴水)(1分);不褪色(1分)
41. 降低通入二氧化硫的速率(2分,合理即可)
42. 2H S + SO = 3S↓+ 2H O(2分);S + Na SO = Na S O (2分)
2 2 2 2 3 2 2 3
43. 取少量产品溶于足量稀盐酸,静置,取上层清液(或过滤,取滤液),滴加少量 BaCl 溶液,若
2
出现白色沉淀,则说明含有Na SO 杂质(3分)
2 4
44. 重结晶(1分)s