文档内容
杨浦区 2022-2023 学年高三上学期一模测试化学试题
相对原子质量:H-1 C-12 N-14 O-16 A1-27 S-32 Fe-56
一、选择题(每小题只有一个正确答案)
1. 发任意球时,足球裁判会在球场喷少量液体做标记,该液体迅速形成白色泡沫并很快消失。该液体的组
成:80%水、17%液态丁烷、2%植物油及1%表面活性剂,液体形成泡沫有表面活性剂的作用,还因为
A. 丁烷变成气体 B. 植物油变成固体 C. 水变成气体 D. 水变成固体
2. 等物质的量的A1、Fe分别与水完全反应,下列说法正确的是
A. 电子转移的数目相同 B. 均有碱生成 C. 生成等量的氢气 D. 反应条件不同
3. 甲烷和氯气1:4混合后,在光照下反应,生成的有机物都
A. 能发生消除反应 B. 溶于水 C. 只有一种结构 D. 是极性分子
4. 的结构片段为: , ,下列说法正确的是:
A. 是共价化合物 B. 为原子晶体 C. 为离子晶体 D. 原子最外层都是8电子
5. 下列事实不能从原子结构角度解释的是
A. 化合物 中 为 价 B. 沸点:
C. 非金属性: D. 热稳定性:
6. 不能由单质化合生成的物质是
A. B. C. D.
7. 实验室用a装置制备下列气体时,所选试剂及收集方法均正确的是
气体 试剂 收集
A b
B c
C 电石 饱和食盐水 dD 生石灰 浓氨水 d
A. A B. B C. C D. D
8. 如图,收集 后做喷泉实验。下列分析错误的是
A. 形成喷泉,说明烧瓶内的压强低于大气压
B. 烧瓶中剩余少量气体,说明 的溶解已达平衡
C. 烧瓶中溶液变红,说明 溶液显酸性
D. 烧瓶中溶液露置在空气中pH增大,说明 易挥发
9. 一种分子的结构如图所示,X、Y、Z、W为原子序数依次增大的短周期元素,W的原子序数等于X与
Y的原子序数之和,下列说法错误的是
A. 原子半径: B. X、Y、Z在同一周期
C. Y的氢化物在常温下是液态 D. 非金属性:
10. 用已知浓度的 溶液测定某 溶液的浓度,下表中正确的是
锥形瓶中溶液 滴定管中溶液 选用指示剂 滴定终点溶液颜色变化A 溶液 溶液 甲基橙 红色变为黄色
B 溶液 溶液 酚酞 浅红色变为无色
C 溶液 溶液 甲基橙 黄色变为橙色
D 溶液 溶液 石蕊 蓝色变 为紫色
A. A B. B C. C D. D
11. 下列生产中,不涉及勒夏特列原理的是
A. 合成氨 B. 饱和氨盐水中通 制碳酸氢钠
C. 和 制 D. 侯氏制碱法处理母液
12. 不能鉴别 和溴蒸汽的是
A. 湿润的淀粉碘化钾试纸 B. 水
C. 溶液 D.
13. 去掉表面氧化膜的等质量的两片铝箔,其一放入足量 溶液中,另一在空气中放置一段时间后再
放入足量 溶液中。下列说法错误的是
A. 均未得电子 B. 消耗等物质的量的
C. 生成等物质的量的 D. 生成等物质的量的气体
14. 配制新制 悬浊液、银氨溶液和检验醛基的过程中,叙述错误的是
A. 配制时均未发生氧化还原反应 B. 配制时碱均过量
C. 检验醛基时加热方式不同 D. 检验醛基时均发生氧化还原反应
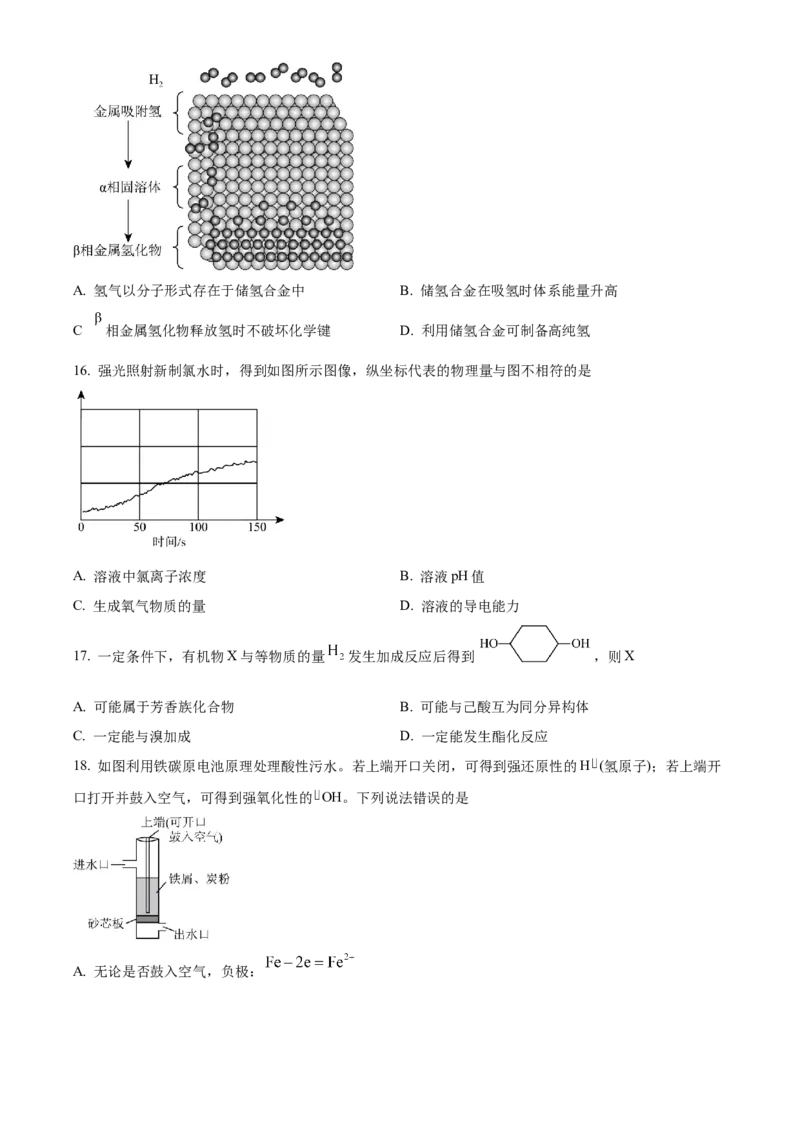
15. 图示为某储氢合金的吸氢过程,此过程放出大量热。下列说法正确的是A. 氢气以分子形式存在于储氢合金中 B. 储氢合金在吸氢时体系能量升高
.
C 相金属氢化物释放氢时不破坏化学键 D. 利用储氢合金可制备高纯氢
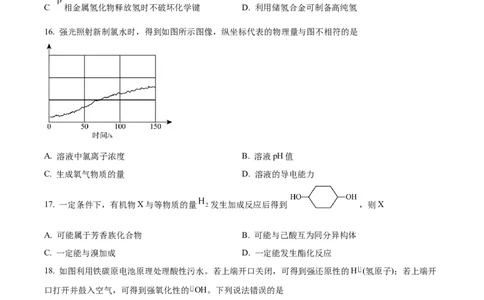
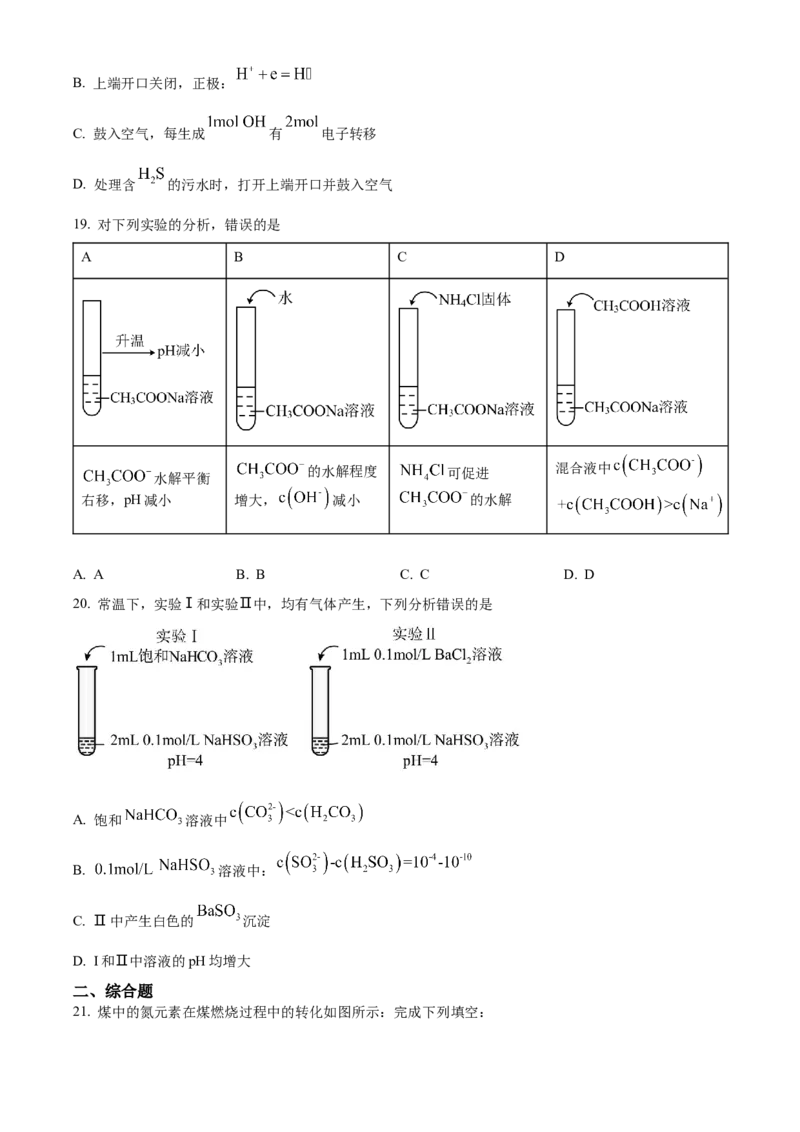
16. 强光照射新制氯水时,得到如图所示图像,纵坐标代表的物理量与图不相符的是
A. 溶液中氯离子浓度 B. 溶液pH值
C. 生成氧气物质的量 D. 溶液的导电能力
17. 一定条件下,有机物X与等物质的量 发生加成反应后得到 ,则X
A. 可能属于芳香族化合物 B. 可能与己酸互为同分异构体
C. 一定能与溴加成 D. 一定能发生酯化反应
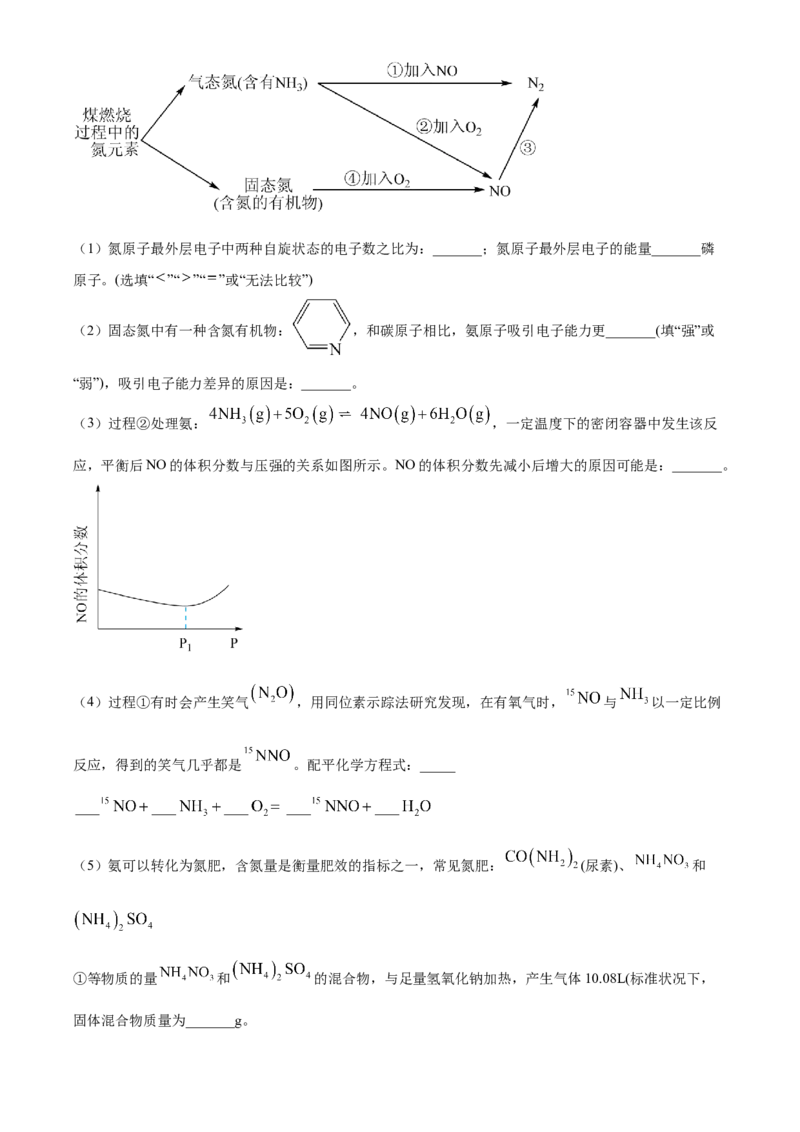
18. 如图利用铁碳原电池原理处理酸性污水。若上端开口关闭,可得到强还原性的H (氢原子);若上端开
口打开并鼓入空气,可得到强氧化性的 OH。下列说法错误的是
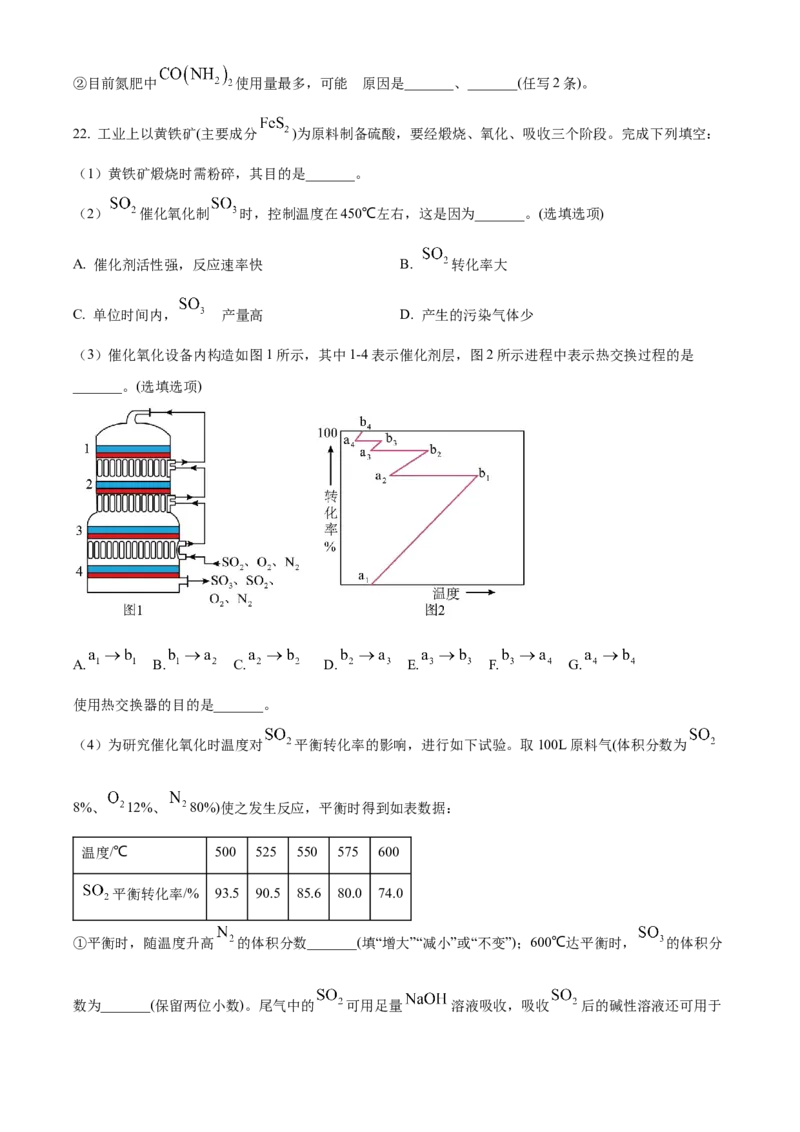
A. 无论是否鼓入空气,负极:B. 上端开口关闭,正极:
C. 鼓入空气,每生成 有 电子转移
D. 处理含 的污水时,打开上端开口并鼓入空气
19. 对下列实验的分析,错误的是
A B C D
的水解程度 可促进 混合液中
水解平衡
右移,pH减小 增大, 减小 的水解
A. A B. B C. C D. D
20. 常温下,实验Ⅰ和实验Ⅱ中,均有气体产生,下列分析错误的是
A. 饱和 溶液中
B. 溶液中:
C. Ⅱ中产生白色的 沉淀
D. I和Ⅱ中溶液的pH均增大
二、综合题
21. 煤中的氮元素在煤燃烧过程中的转化如图所示:完成下列填空:(1)氮原子最外层电子中两种自旋状态的电子数之比为:_______;氮原子最外层电子的能量_______磷
原子。(选填“ ”“ ”“ ”或“无法比较”)
(2)固态氮中有一种含氮有机物: ,和碳原子相比,氨原子吸引电子能力更_______(填“强”或
“弱”),吸引电子能力差异的原因是:_______。
(3)过程②处理氨: ,一定温度下的密闭容器中发生该反
应,平衡后NO的体积分数与压强的关系如图所示。NO的体积分数先减小后增大的原因可能是:_______。
(4)过程①有时会产生笑气 ,用同位素示踪法研究发现,在有氧气时, 与 以一定比例
反应,得到的笑气几乎都是 。配平化学方程式:_____
(5)氨可以转化为氮肥,含氮量是衡量肥效的指标之一,常见氮肥: (尿素)、 和
①等物质的量 和 的混合物,与足量氢氧化钠加热,产生气体10.08L(标准状况下,
固体混合物质量为_______g。②目前氮肥中 使用量最多,可能 的原因是_______、_______(任写2条)。
22. 工业上以黄铁矿(主要成分 )为原料制备硫酸,要经煅烧、氧化、吸收三个阶段。完成下列填空:
(1)黄铁矿煅烧时需粉碎,其目的是_______。
(2) 催化氧化制 时,控制温度在450℃左右,这是因为_______。(选填选项)
A. 催化剂活性强,反应速率快 B. 转化率大
的
C. 单位时间内, 产量高 D. 产生的污染气体少
(3)催化氧化设备内构造如图1所示,其中1-4表示催化剂层,图2所示进程中表示热交换过程的是
_______。(选填选项)
A. B. C. D. E. F. G.
使用热交换器的目的是_______。
(4)为研究催化氧化时温度对 平衡转化率的影响,进行如下试验。取100L原料气(体积分数为
8%、 12%、 80%)使之发生反应,平衡时得到如表数据:
温度/℃ 500 525 550 575 600
平衡转化率/% 93.5 90.5 85.6 80.0 74.0
①平衡时,随温度升高 的体积分数_______(填“增大”“减小”或“不变”);600℃达平衡时, 的体积分
数为_______(保留两位小数)。尾气中的 可用足量 溶液吸收,吸收 后的碱性溶液还可用于的尾气处理,吸收 后的溶液仍呈强碱性。
②吸收 后的溶液中一定存在的阴离子有 、_______,设计实验检验溶液中 :_______。
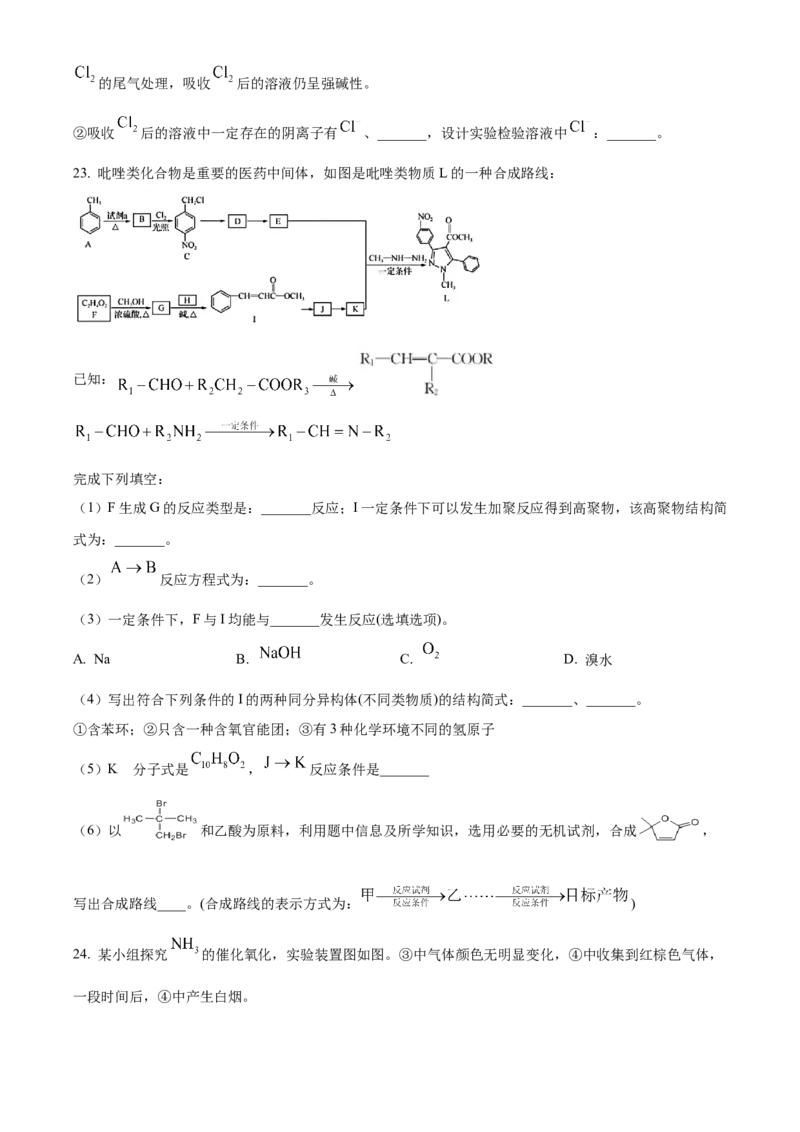
23. 吡唑类化合物是重要的医药中间体,如图是吡唑类物质L的一种合成路线:
已知:
完成下列填空:
(1)F生成G的反应类型是:_______反应;I一定条件下可以发生加聚反应得到高聚物,该高聚物结构简
式为:_______。
(2) 反应方程式为:_______。
(3)一定条件下,F与I均能与_______发生反应(选填选项)。
A. Na B. C. D. 溴水
(4)写出符合下列条件的I的两种同分异构体(不同类物质)的结构简式:_______、_______。
①含苯环;②只含一种含氧官能团;③有3种化学环境不同的氢原子
的
(5)K 分子式是 , 反应条件是_______
(6)以 和乙酸为原料,利用题中信息及所学知识,选用必要的无机试剂,合成 ,
写出合成路线____。(合成路线的表示方式为: )
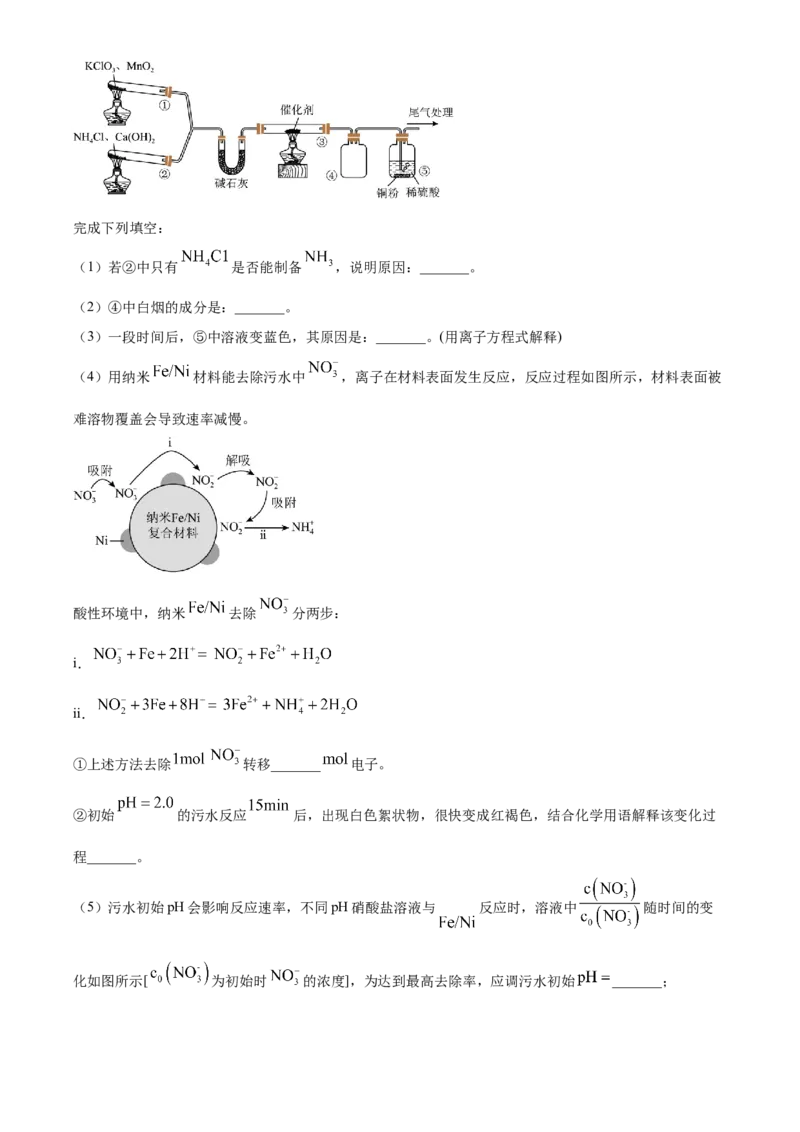
24. 某小组探究 的催化氧化,实验装置图如图。③中气体颜色无明显变化,④中收集到红棕色气体,
一段时间后,④中产生白烟。完成下列填空:
(1)若②中只有 是否能制备 ,说明原因:_______。
(2)④中白烟的成分是:_______。
(3)一段时间后,⑤中溶液变蓝色,其原因是:_______。(用离子方程式解释)
(4)用纳米 材料能去除污水中 ,离子在材料表面发生反应,反应过程如图所示,材料表面被
难溶物覆盖会导致速率减慢。
酸性环境中,纳米 去除 分两步:
i.
ii.
①上述方法去除 转移_______ 电子。
②初始 的污水反应 后,出现白色絮状物,很快变成红褐色,结合化学用语解释该变化过
程_______。
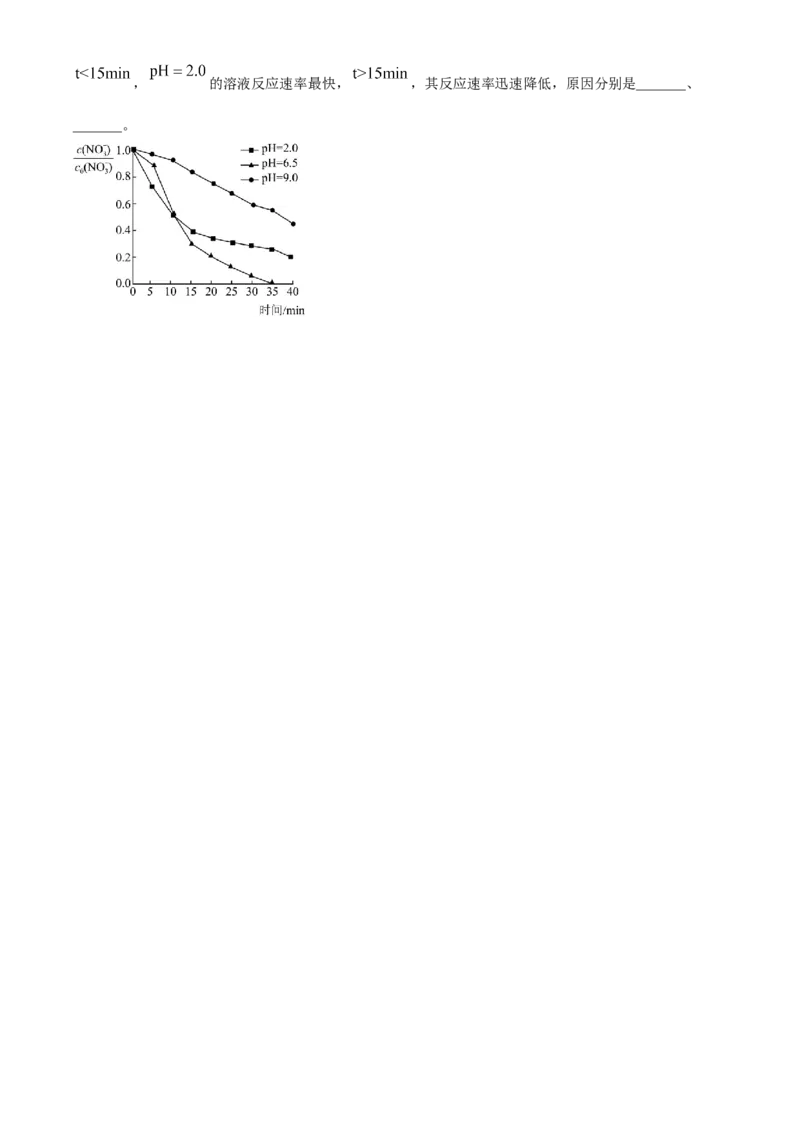
(5)污水初始pH会影响反应速率,不同pH硝酸盐溶液与 反应时,溶液中 随时间的变
化如图所示[ 为初始时 的浓度],为达到最高去除率,应调污水初始 _______;, 的溶液反应速率最快, ,其反应速率迅速降低,原因分别是_______、
_______。