文档内容
课时检测(三) 离子反应的基本知能评价
1.(2023·福建厦门统考二模)下列食品添加剂不属于电解质的是( )
A.二氧化硫 B.亚硝酸钠
C.葡萄糖酸 D.山梨酸钾
2.(2023·上海静安统考二模)能与硫酸铁溶液发生氧化还原反应的电解质是( )
A.氯化钡 B.铁
C.氢氧化钠 D.碘化氢
3.下列说法正确的是( )
A.CO 的水溶液能导电,所以CO 是电解质
2 2
B.BaSO 难溶于水,其水溶液的导电能力极弱,所以BaSO 的电离方程式为
4 4
BaSO Ba2++SO
4
C.液溴
⥫⥬
不导电,所以溴是非电解质
D.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
4.下列电离方程式书写正确的是( )
A.BaCl 溶于水:BaCl ===Ba2++Cl
2 2
B.Ba(OH) 溶于水:Ba(OH) ===Ba2++2OH-
2 2
C.Al (SO ) 的电离:Al (SO )===Al3++SO
2 4 3 2 4 3
D.NaHCO 溶于水:NaHCO ===Na++H++CO
3 3
5.下列反应中,不属于离子反应的是( )
A.Ba(OH) 溶液和NaHCO 溶液反应
2 3
B.固体Na O 和CO 反应
2 2 2
C.电解饱和食盐水
D.Na单质与HO混合
2
6.下列说法正确的是( )
A.Cl 溶于水得到的氯水能导电,所以Cl 是电解质
2 2
B.只有在电流作用下KHSO 才能电离成K+、H+和SO
4
C.强电解质溶液的导电能力不一定都强;弱电解质溶液的导电能力不一定都弱
D.BaSO 难溶于水,故BaSO 是弱电解质;醋酸铅易溶于水,故醋酸铅是强电解质
4 4
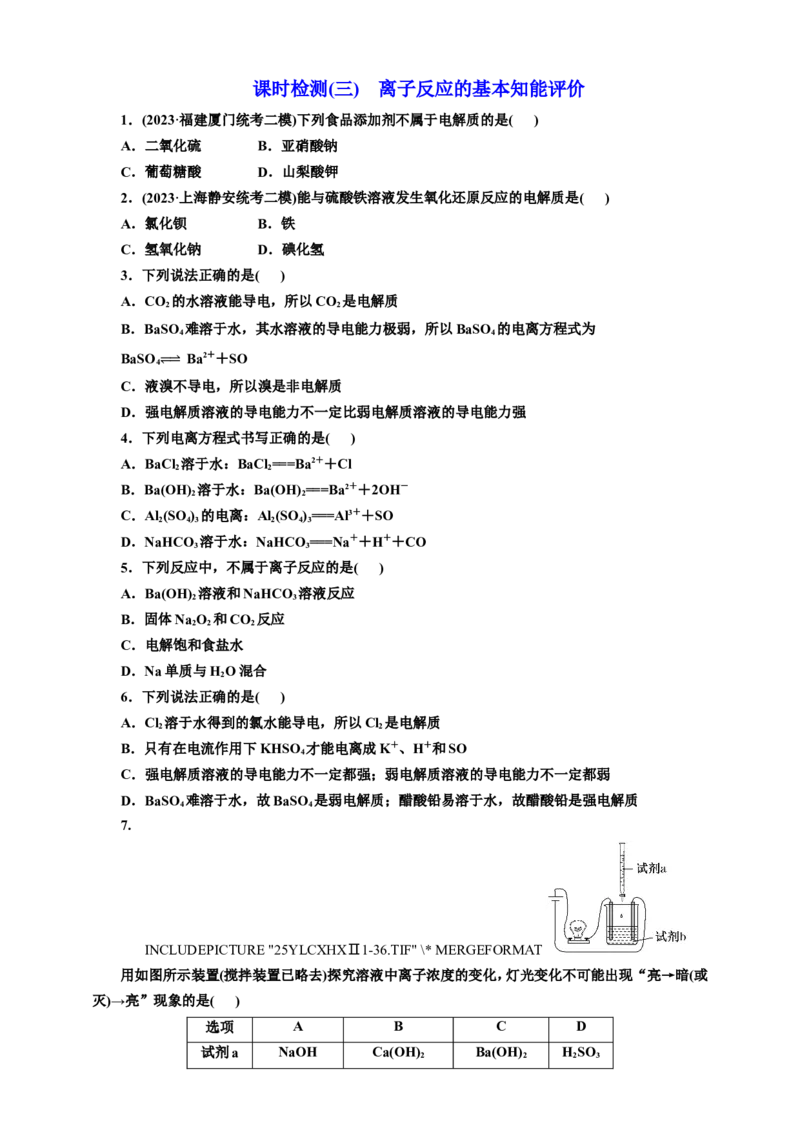
7.
INCLUDEPICTURE "25YLCXHXⅡ1-36.TIF" \* MERGEFORMAT
用如图所示装置(搅拌装置已略去)探究溶液中离子浓度的变化,灯光变化不可能出现“亮→暗(或
灭)→亮”现象的是( )
选项 A B C D
试剂a NaOH Ca(OH) Ba(OH) HSO
2 2 2 3试剂b CH COOH Ca(HCO ) HSO HS
3 3 2 2 4 2
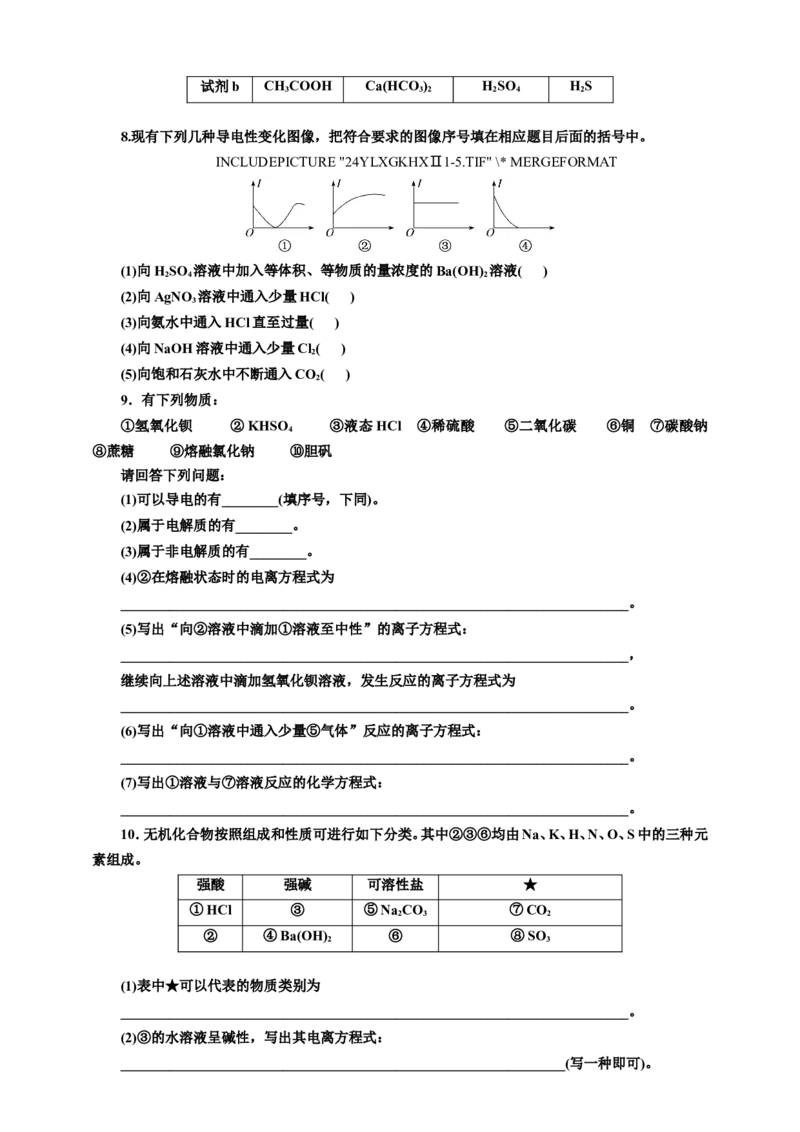
8.现有下列几种导电性变化图像,把符合要求的图像序号填在相应题目后面的括号中。
INCLUDEPICTURE "24YLXGKHXⅡ1-5.TIF" \* MERGEFORMAT
(1)向HSO 溶液中加入等体积、等物质的量浓度的Ba(OH) 溶液( )
2 4 2
(2)向AgNO 溶液中通入少量HCl( )
3
(3)向氨水中通入HCl直至过量( )
(4)向NaOH溶液中通入少量Cl ( )
2
(5)向饱和石灰水中不断通入CO ( )
2
9.有下列物质:
①氢氧化钡 ②KHSO ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦碳酸钠
4
⑧蔗糖 ⑨熔融氯化钠 ⑩胆矾
请回答下列问题:
(1)可以导电的有________(填序号,下同)。
(2)属于电解质的有________。
(3)属于非电解质的有________。
(4)②在熔融状态时的电离方程式为
________________________________________________________________________。
(5)写出“向②溶液中滴加①溶液至中性”的离子方程式:
________________________________________________________________________,
继续向上述溶液中滴加氢氧化钡溶液,发生反应的离子方程式为
________________________________________________________________________。
(6)写出“向①溶液中通入少量⑤气体”反应的离子方程式:
________________________________________________________________________。
(7)写出①溶液与⑦溶液反应的化学方程式:
________________________________________________________________________。
10.无机化合物按照组成和性质可进行如下分类。其中②③⑥均由Na、K、H、N、O、S中的三种元
素组成。
强酸 强碱 可溶性盐 ★
①HCl ③ ⑤Na CO ⑦CO
2 3 2
② ④Ba(OH) ⑥ ⑧SO
2 3
(1)表中★可以代表的物质类别为
________________________________________________________________________。
(2)③的水溶液呈碱性,写出其电离方程式:
_______________________________________________________________(写一种即可)。(3)②与④在水溶液中发生反应(无沉淀生成)的离子方程式为
________________________________________________________________________。
(4)④与少量的⑦在水溶液中发生反应的离子方程式为
________________________________________________________________________。
(5)④与⑥在水溶液中发生反应的离子方程式为
________________________________________________________________________。
课时检测(三)
1.A 二氧化硫为非电解质,A符合题意;亚硝酸钠属于盐,葡萄糖酸属于有机酸,山梨酸钾属于
盐,酸、碱、盐均为电解质。
2.D 氯化钡与硫酸铁反应生成硫酸钡和氯化铁,是非氧化还原反应,A错误;铁与硫酸铁反应生
成硫酸亚铁,是氧化还原反应,但铁是单质,不是电解质,B错误;氢氧化钠与硫酸铁反应生成氢氧化
铁和硫酸钠,是非氧化还原反应,C错误;碘化氢与硫酸铁反应生成硫酸亚铁、硫酸和单质碘,是氧化
还原反应,且碘化氢是电解质,D正确。
3.D CO 溶于水生成的HCO 能电离出自由移动的离子而使溶液导电,CO 自身不电离,因此
2 2 3 2
HCO 是电解质,CO 是非电解质,A错误;BaSO 溶解度很小,但溶于水的BaSO 完全电离,所以
2 3 2 4 4
BaSO 是强电解质,不能用“⥫⥬ ”,B错误;电解质和非电解质都是化合物,溴是单质,C错误;电解
4
质导电能力的强弱与溶液中自由移动的离子的浓度大小以及所带的电荷多少有关,所以强电解质溶液
的导电能力不一定比弱电解质溶液的导电能力强,D正确。
4.B BaCl 是可溶性盐,溶于水完全电离,电离方程式为BaCl ===Ba2++2Cl-,A错误;Ba(OH)
2 2 2
是可溶性碱,溶于水完全电离,电离方程式为Ba(OH) ===Ba2++2OH-,B正确;Al (SO ) 是可溶性盐,
2 2 4 3
溶于水完全电离,电离方程式为Al (SO )===2Al3++3SO,C错误;NaHCO 是可溶性盐,溶于水完全
2 4 3 3
电离,电离方程式为NaHCO ===Na++HCO,D错误。
3
5.B Ba(OH) 溶液和NaHCO 溶液的反应实质上是氢氧根离子、碳酸氢根离子和钡离子的反应,
2 3
生成碳酸钡和水,属于离子反应,故A不符合题意;固体Na O 和CO 反应生成碳酸钠和氧气,该反应
2 2 2
没有自由离子参加或生成,不属于离子反应,故B符合题意;电解饱和食盐水的反应为2Cl-+
2HO=====,H↑+Cl ↑+2OH-,属于离子反应,故C不符合题意;Na与HO反应的离子方程式为
2 2 2 2
2Na+2HO===2Na++2OH-+H↑,有自由离子生成,属于离子反应,故D不符合题意。
2 2
6.C Cl 是单质,既不属于电解质也不属于非电解质,故A错误;KHSO 溶于水电离成K+、H+
2 4
和SO,故B错误;溶液的导电能力与离子浓度、电荷数有关,强电解质溶液的导电能力不一定都强,弱
电解质溶液的导电能力不一定都弱,故C正确;电解质强弱与溶解性无关,BaSO 是强电解质,醋酸铅
4
是弱电解质,故D错误。
7.A 醋酸为弱电解质,加入氢氧化钠后二者反应生成强电解质醋酸钠,所以不会出现变暗的过
程,A符合题意;Ca(HCO ) 为强电解质,加入氢氧化钙后二者反应生成碳酸钙沉淀和水,溶液中的离
3 2
子浓度逐渐减小,直至接近于零,此时灯灭,之后随着氢氧化钙的加入,溶液中的离子浓度逐渐增大,
灯泡变亮,B不符合题意;硫酸为强电解质,加入氢氧化钡后二者反应生成硫酸钡沉淀和水,溶液中的
离子浓度逐渐减小,直至接近于零,此时灯灭,之后随着氢氧化钡的加入,溶液中的离子浓度逐渐增大灯泡变亮,C不符合题意;HS为弱电解质,加入亚硫酸后二者反应生成硫单质和水,硫难溶于水,溶
2
液中的离子浓度逐渐减小,直至接近于零,此时灯灭,之后随着亚硫酸的加入,溶液中的离子浓度逐渐
增大,灯泡变亮,D不符合题意。
8.(1)④ (2)③ (3)② (4)③ (5)①
9.(1)④⑥⑨ (2)①②③⑦⑨⑩ (3)⑤⑧
(4)KHSO (熔融)===K++HSO
4
(5)2OH-+Ba2++2H++SO===BaSO ↓+2HO Ba2++SO===BaSO ↓
4 2 4
(6)CO+2OH-+Ba2+===BaCO ↓+HO
2 3 2
(7)Ba(OH) +Na CO ===BaCO ↓+2NaOH
2 2 3 3
10.解析:(1)无机化合物分为酸、碱、盐、氧化物,表中★可以代表的物质类别为氧化物或酸性氧
化物。(3)②是强酸,可以是硝酸或硫酸,④是氢氧化钡,②与④在水溶液中发生反应且无沉淀生成,则
②是硝酸,硝酸与氢氧化钡反应生成硝酸钡和水,即OH-+H+===H O。(5)④是氢氧化钡,⑥是可溶
2
性盐,则⑥可以是NaNO 、KNO 、Na SO 、KSO 、Na SO 、KSO 、NaHS或KHS,其中参与发生复分
3 3 2 3 2 3 2 4 2 4
解反应的离子方程式有Ba2++SO===BaSO ↓、Ba2++SO===BaSO ↓、HS-+OH-===H O+S2-。
3 4 2
答案:(1)氧化物(或酸性氧化物)
(2)NaOH===Na++OH-(或KOH===K++OH-)
(3)OH-+H+===H O
2
(4)Ba2++2OH-+CO ===BaCO ↓+HO
2 3 2
(5)Ba2++SO===BaSO ↓、Ba2++SO===BaSO ↓、HS-+OH-===H O+S2-(合理即可)
3 4 2