文档内容
专练 14 铁、铜及其化合物
一、单项选择题
1.[2021·河北卷]“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景
在其《本草经集注》中提到“钢铁是杂炼生 作刀镰者”。“灌钢法”主要是将生铁和熟
铁(含碳量约0.1%)混合加热,生铁熔化灌入熟铁,再锻打成钢。下列说法错误的是(
)
A.钢是以铁为主的含碳合金
B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比熟铁高
D.冶炼铁的原料之一赤铁矿的主要成分为Fe O
2 3
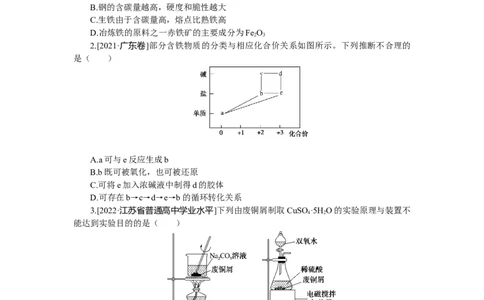
2.[2021·广东卷]部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的
是( )
A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b的循环转化关系
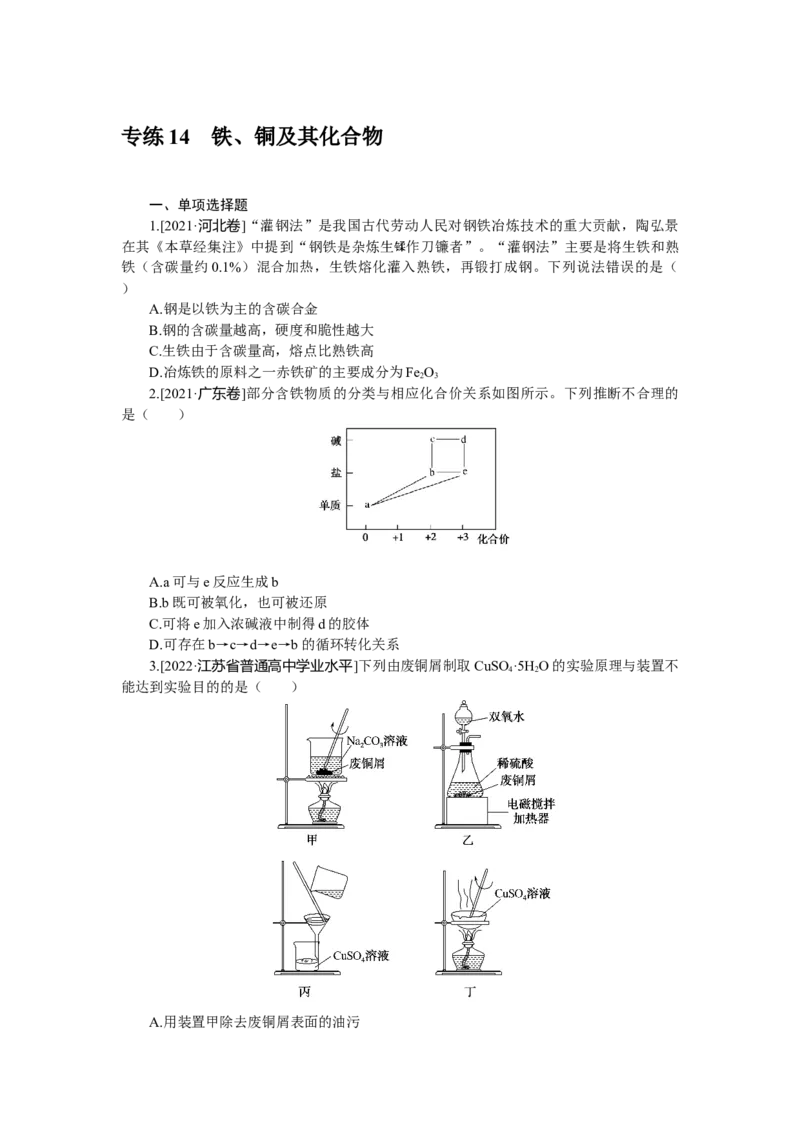
3.[2022·江苏省普通高中学业水平]下列由废铜屑制取CuSO ·5H O的实验原理与装置不
4 2
能达到实验目的的是( )
A.用装置甲除去废铜屑表面的油污B.用装置乙溶解废铜屑
C.用装置丙过滤得到CuSO 溶液
4
D.用装置丁蒸干溶液获得CuSO ·5H O
4 2
4.下列有关物质的性质与用途不具有对应关系的是( )
A.铁粉能与O 反应,可用作食品保存的吸氧剂
2
B.纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
C.FeCl 具有氧化性,可用于腐蚀印刷电路板上的Cu
3
D.聚合硫酸铁能水解并形成胶体,可用于净水
5.[2022·山东淄博调研]硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图
所示)。下列说法错误的是( )
A.碱式硫酸铁水解能产生Fe(OH) 胶体,可用作净水剂
3
B.为防止NH HCO 分解,生产FeCO 需在较低温度下进行
4 3 3
C.可用KSCN溶液检验(NH )Fe(SO ) 是否被氧化
4 2 4 2
D.常温下,(NH )Fe(SO )·6H O在水中的溶解度比FeSO 的大
4 2 4 2 2 4
6.[2022·经典习题选萃]下列说法正确的是( )
①FeO投入稀HSO 和稀HNO 中均得到浅绿色溶液;
2 4 3
②向红砖粉末中加入盐酸,充分振荡反应后取上层清液于试管中,滴加 KSCN溶液2
~3滴,溶液呈红色,但不一定说明红砖中含有氧化铁;
③Fe O――→FeCl (aq)――→无水FeCl ;
2 3 3 3
④制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可得到
白色的氢氧化亚铁;
⑤向一定量的Cu、Fe O 的混合物中加入300 mL 1 mol·L-1的盐酸,恰好使混合物完全
2 3
溶解,所得溶液中不含有Fe3+。若用过量的CO在高温下还原相同质量的此混合物,固体
减少的质量为2.4 g;
⑥磁性氧化铁溶于稀硝酸的离子方程式为
3Fe2++NO+4H+===2Fe3++NO↑+3HO;
2
⑦Fe(OH) 与HI溶液反应的离子方程式为Fe(OH)+3H+===Fe3++3HO;
3 3 2
⑧Fe O 不可与水反应得到Fe(OH),但能通过化合反应制取Fe(OH);
2 3 3 3
⑨赤铁矿的主要成分是Fe O,Fe O 为红棕色晶体;
3 4 3 4
⑩如图所示装置能较长时间观察到Fe(OH) 白色沉淀;
2A.①④⑦ B.⑤⑧
C.②③⑩ D.⑤⑥⑨
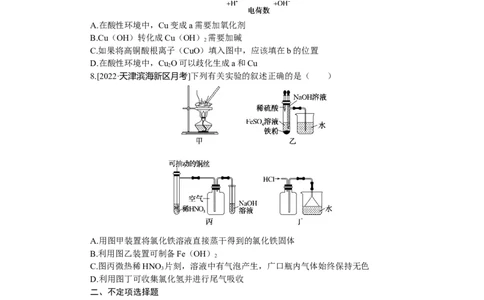
7.[2022·广东佛山顺德一模]如图是铜及部分含铜粒子的价荷图。下列推断不合理的是
( )
A.在酸性环境中,Cu变成a需要加氧化剂
B.Cu(OH)转化成Cu(OH) 需要加碱
2
C.如果将高铜酸根离子(CuO)填入图中,应该填在b的位置
D.在酸性环境中,Cu O可以歧化生成a和Cu
2
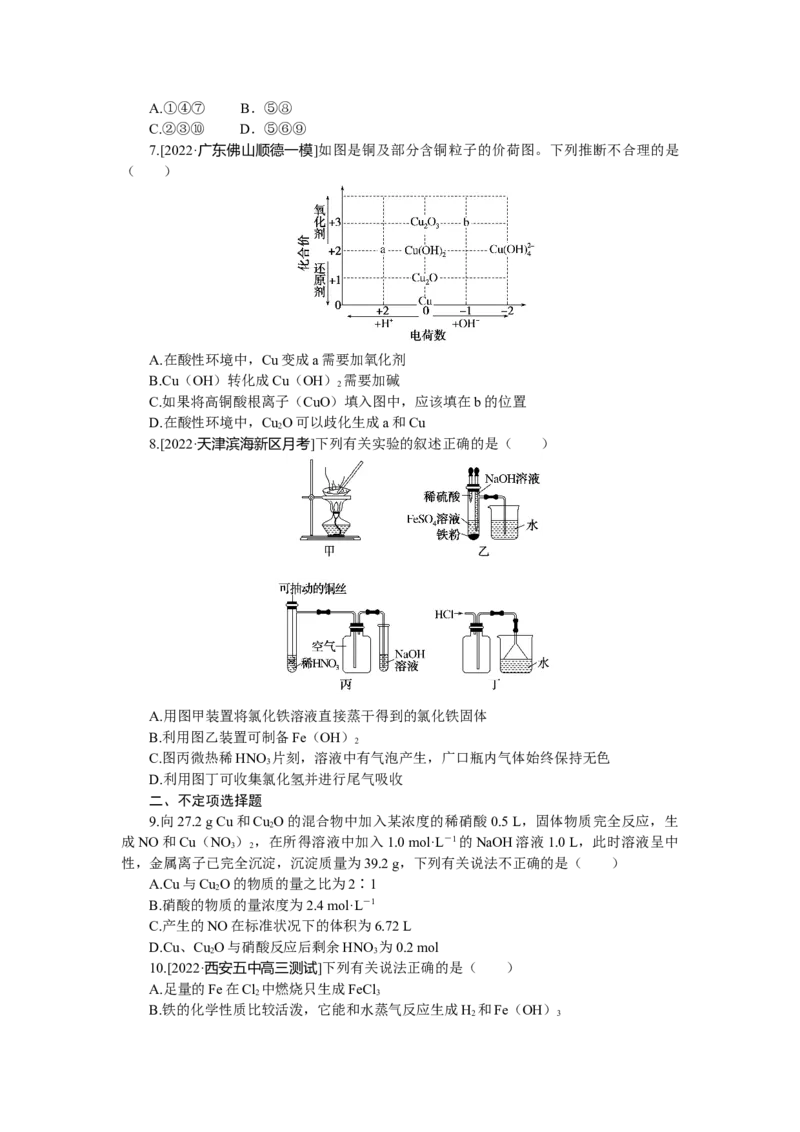
8.[2022·天津滨海新区月考]下列有关实验的叙述正确的是( )
A.用图甲装置将氯化铁溶液直接蒸干得到的氯化铁固体
B.利用图乙装置可制备Fe(OH)
2
C.图丙微热稀HNO 片刻,溶液中有气泡产生,广口瓶内气体始终保持无色
3
D.利用图丁可收集氯化氢并进行尾气吸收
二、不定项选择题
9.向27.2 g Cu和Cu O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,生
2
成NO和Cu(NO ) ,在所得溶液中加入1.0 mol·L-1的NaOH溶液1.0 L,此时溶液呈中
3 2
性,金属离子已完全沉淀,沉淀质量为39.2 g,下列有关说法不正确的是( )
A.Cu与Cu O的物质的量之比为2∶1
2
B.硝酸的物质的量浓度为2.4 mol·L-1
C.产生的NO在标准状况下的体积为6.72 L
D.Cu、Cu O与硝酸反应后剩余HNO 为0.2 mol
2 3
10.[2022·西安五中高三测试]下列有关说法正确的是( )
A.足量的Fe在Cl 中燃烧只生成FeCl
2 3
B.铁的化学性质比较活泼,它能和水蒸气反应生成H 和Fe(OH)
2 3C.用酸性KMnO 溶液检验FeCl 溶液中是否含有FeCl
4 3 2
D.向某溶液中加NaOH溶液得白色沉淀,且颜色逐渐变为红褐色,说明该溶液只含Fe2
+
11.[情境创新]从废水中回收硫酸亚铁固体和铜的流程如下:
下列说法正确的是( )
A.金属X为Fe
B.溶液Y为稀盐酸
C.硫酸亚铁可用作食品的抗氧化剂
D.无水硫酸铜常用于检验水或作干燥剂
12.[2022·上海交大附中月考]有4.8 g CuO、Fe O 混合物跟足量CO充分反应后固体质
2 3
量减少1.28 g,反应后气体用0.6 mol·L-1 Ba(OH) 溶液100 mL全部吸收。下列有关叙
2
述中正确的是( )
A.原混合物中CuO与Fe O 的物质的量之比为2∶1
2 3
B.原混合物中CuO与Fe O 的质量比为3∶1
2 3
C.反应中生成的CO 体积为1.792 L
2
D.吸收CO 后的溶液中一定有Ba(HCO )
2 3 2
三、非选择题
13.[2022·浙江1月选考]化合物X由4种元素组成。某兴趣小组按如下流程进行实验:
实验Ⅰ
实验Ⅱ
请回答:
(1)组成X的元素有
________________________________________________________________________;
X的化学式为 。
(2)溶液C中溶质的成分是 (用化学式表示);根据C→D→E的
现象,给出相应微粒与阳离子结合由弱到强的排序
________________________________________________________________________。(3)X与足量Na反应生成固体F的化学方程式是
________________________________________________________________________。
(4)设计实验确定溶液G中的阴离子
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
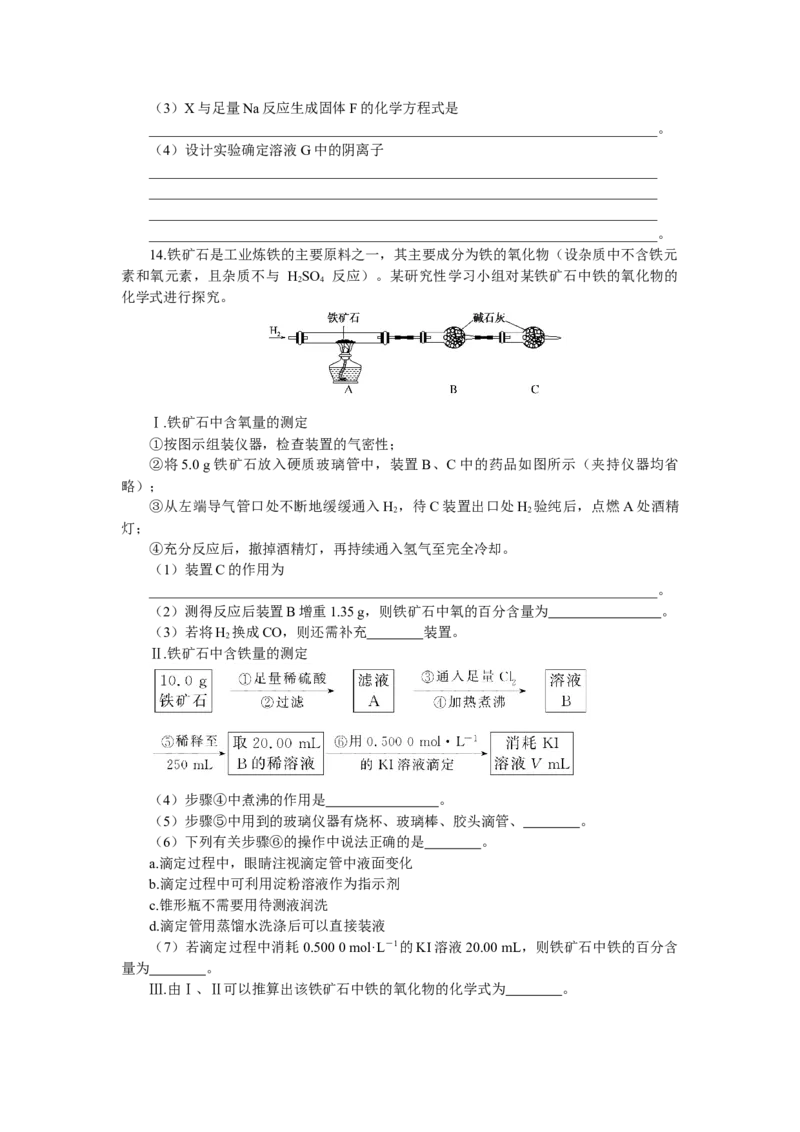
14.铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元
素和氧元素,且杂质不与 HSO 反应)。某研究性学习小组对某铁矿石中铁的氧化物的
2 4
化学式进行探究。
Ⅰ.铁矿石中含氧量的测定
①按图示组装仪器,检查装置的气密性;
②将5.0 g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省
略);
③从左端导气管口处不断地缓缓通入H ,待C装置出口处H 验纯后,点燃A处酒精
2 2
灯;
④充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)装置C的作用为
________________________________________________________________________。
(2)测得反应后装置B增重1.35 g,则铁矿石中氧的百分含量为 。
(3)若将H 换成CO,则还需补充 装置。
2
Ⅱ.铁矿石中含铁量的测定
(4)步骤④中煮沸的作用是 。
(5)步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、 。
(6)下列有关步骤⑥的操作中说法正确的是 。
a.滴定过程中,眼睛注视滴定管中液面变化
b.滴定过程中可利用淀粉溶液作为指示剂
c.锥形瓶不需要用待测液润洗
d.滴定管用蒸馏水洗涤后可以直接装液
(7)若滴定过程中消耗0.500 0 mol·L-1的KI溶液20.00 mL,则铁矿石中铁的百分含
量为 。
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为 。