文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练14 14道选择题+主观实验题
完卷时间:40分钟
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案
可能用到的相对原子质量:B 11 C 12 N 14 O 16 Mg 24 Si 28 S 32
一、选择题(共42分,只有1个正确选项)
1.科技兴国,中国科学家为国家的发展做出巨大的贡献,下列有关说法错误的是
A.科学家将镍钛系形状记忆合金用于航空领域,Ni和Ti均属于过渡金属元素
B.量子通信材料螺旋碳纳米管与石墨烯互为同位素
C.长征七号火箭发动机的碳化硅陶瓷是一种新型无机非金属材料
D.天和核心舱内以氙和氩为离子推进器气体,氙和氩均为稀有气体
2.下列化学用语表述正确的是
A.基态 原子的价层电子排布图为
B. 的化学名称为3-甲基-2-丁烯
C. 分子的 模型为
D.用电子式表示 的形成过程为
3.氮化硅( )是一种新型无机非金属材料,应用广泛,可由石英和焦炭在高温的氮气
中反应制备: ,设 为阿伏加德罗常数的值,下列说法
错误的是
A.标准状况下,2.24 L 中π键数为B.30 g 中 共价键的数目为
C.14 g由 和CO组成的混合气体含有的质子数为7N
A
D.上述反应中,当形成0.4 mol ,转移的电子数为
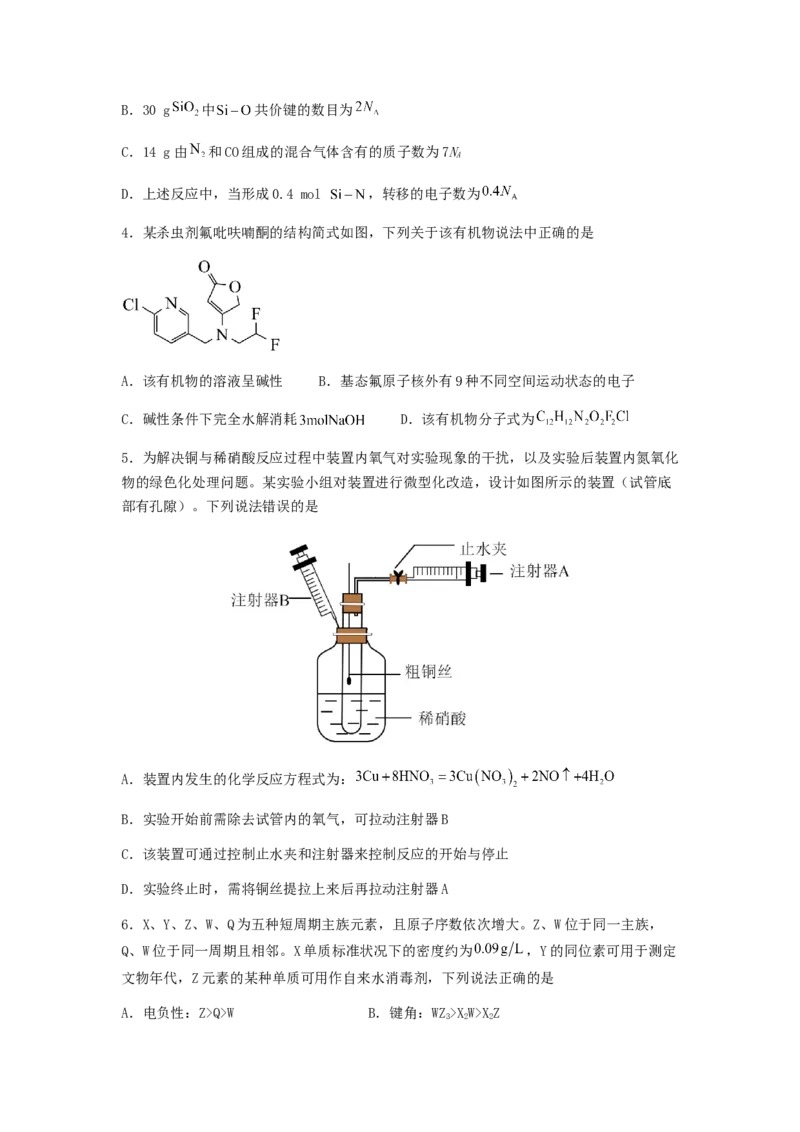
4.某杀虫剂氟吡呋喃酮的结构简式如图,下列关于该有机物说法中正确的是
A.该有机物的溶液呈碱性 B.基态氟原子核外有9种不同空间运动状态的电子
C.碱性条件下完全水解消耗 D.该有机物分子式为
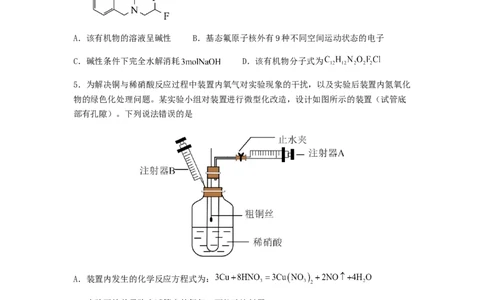
5.为解决铜与稀硝酸反应过程中装置内氧气对实验现象的干扰,以及实验后装置内氮氧化
物的绿色化处理问题。某实验小组对装置进行微型化改造,设计如图所示的装置(试管底
部有孔隙)。下列说法错误的是
A.装置内发生的化学反应方程式为:
B.实验开始前需除去试管内的氧气,可拉动注射器B
C.该装置可通过控制止水夹和注射器来控制反应的开始与停止
D.实验终止时,需将铜丝提拉上来后再拉动注射器A
6.X、Y、Z、W、Q为五种短周期主族元素,且原子序数依次增大。Z、W位于同一主族,
Q、W位于同一周期且相邻。X单质标准状况下的密度约为 ,Y的同位素可用于测定
文物年代,Z元素的某种单质可用作自来水消毒剂,下列说法正确的是
A.电负性:Z>Q>W B.键角:WZ>XW>XZ
3 2 2C.YW、XZ 均为非极性分子 D.Z形成的单质分子是非极性键形成的非极性分
2 2 2
子
7.能正确表示下列反应的离子方程式为
A.明矾溶液与过量氨水混合:
B.氯水久置颜色逐渐褪去:4Cl+4HO = HClO+7HCl
2 2 4
C.用NaSO 做碘量法实验时,pH过低溶液变浑浊:
2 2 3
D.苯酚钠溶液中通入少量CO,出现白色浑浊:2 2
2
8.化学处处呈现美。下列有关说法正确的是
A. 分子呈现完美对称,为V形结构
B.NaCl焰色试验为黄色,与氯原子的电子跃迁有关
C.冰雪融化时需要破坏氢键和范德华力
D.镁条燃烧发出耀眼的白光,只将化学能转化为光能
9.利用工业废液生产 CuSCN具有经济价值和社会效益。SCN⁻的测定方法如下:
①准确称取 CuSCN 样品 m g 置于 100 mL 烧杯中,加入 30 mL 水,再加入 20.00 mL
溶液充分反应,在不断搅拌下加热至微沸,保持5min;取下,趁热用中
速滤纸过滤于100 mL容量瓶中,用蒸馏水多次洗涤沉淀,至洗出液呈中性,并检查无
SCN⁻,用去离子水稀释滤液到刻度,混匀,作为含SCN⁻的待测试液。
②准确移取25.00mL SCN⁻待测试液于250mL锥形瓶中,加入8 mL硝酸酸化,摇匀后,加入
标准溶液和3~4滴指示剂溶液,充分摇匀,再用0.050 0
标准溶液滴定至终点,平行滴定3次,记录平均消耗NHSCN 标准溶液的
4
体积为`VmL。
2
已知:CuSCN+NaOH =NaSCN+CuOH↓,2CuOH =Cu
2
O+H
2
O;Ag⁺ +SCN⁻=AgSCN↓(白色)。
CuSCN 样品中SCN⁻含量(质量分数)计算正确的是
A. B.
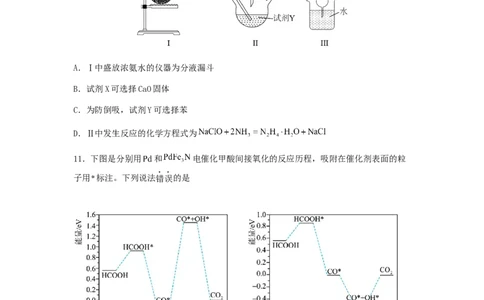
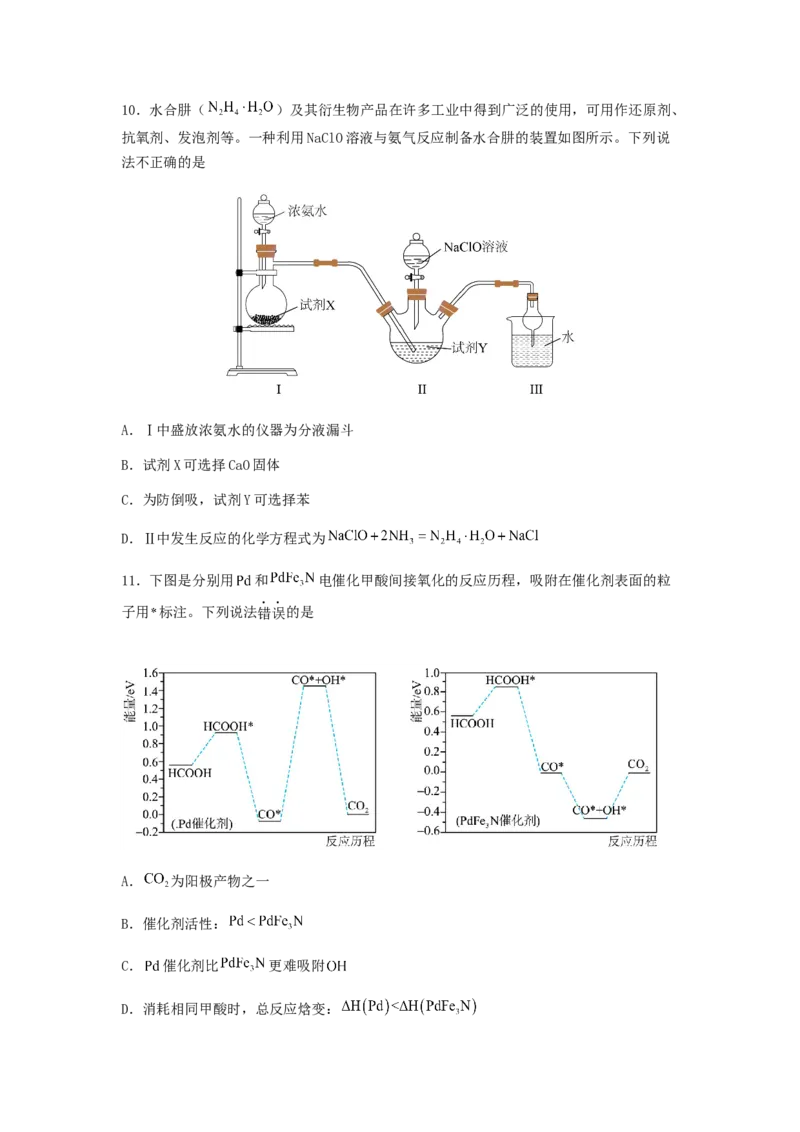
C. D.10.水合肼( )及其衍生物产品在许多工业中得到广泛的使用,可用作还原剂、
抗氧剂、发泡剂等。一种利用NaClO溶液与氨气反应制备水合肼的装置如图所示。下列说
法不正确的是
A.Ⅰ中盛放浓氨水的仪器为分液漏斗
B.试剂X可选择CaO固体
C.为防倒吸,试剂Y可选择苯
D.Ⅱ中发生反应的化学方程式为
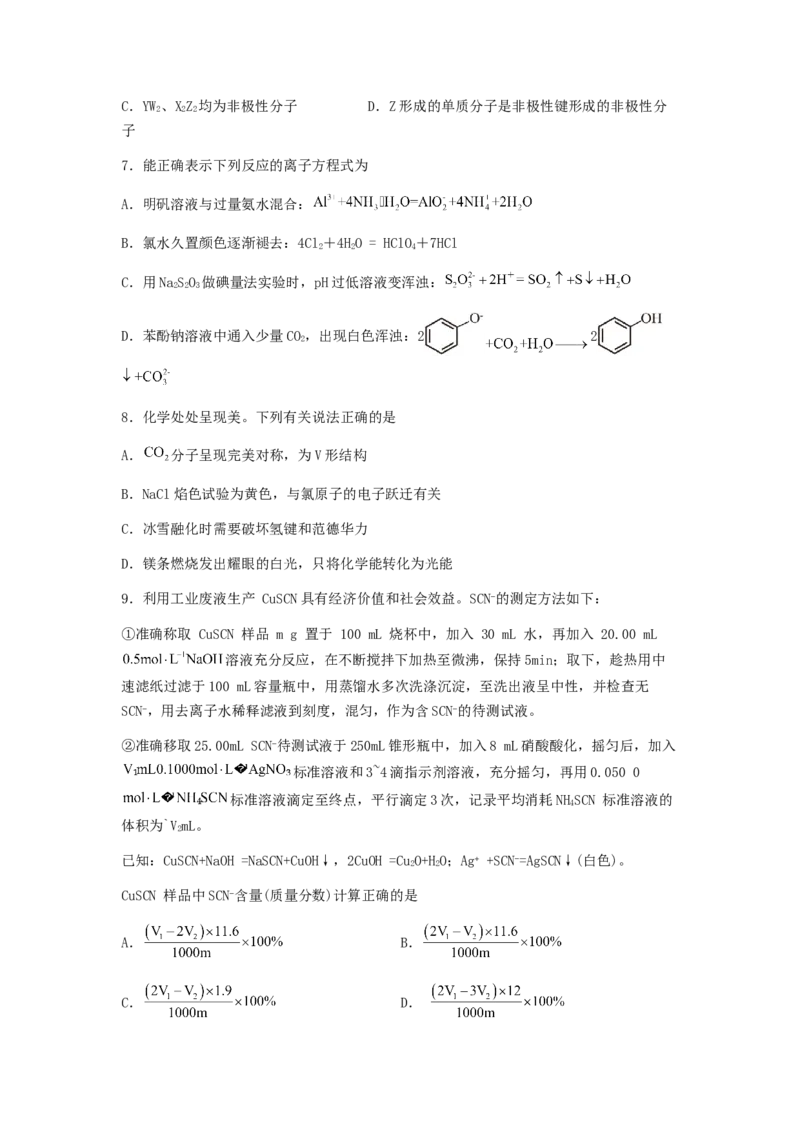
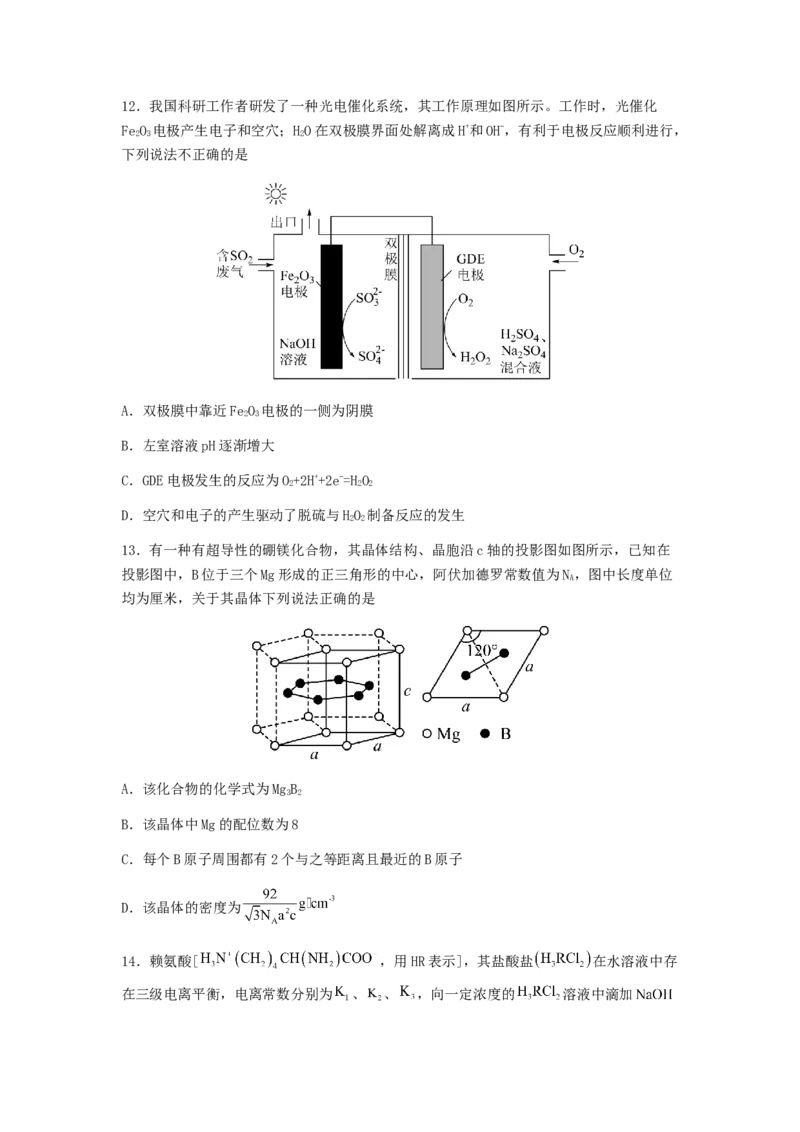
11.下图是分别用 和 电催化甲酸间接氧化的反应历程,吸附在催化剂表面的粒
子用 标注。下列说法错误的是
A. 为阳极产物之一
B.催化剂活性:
C. 催化剂比 更难吸附
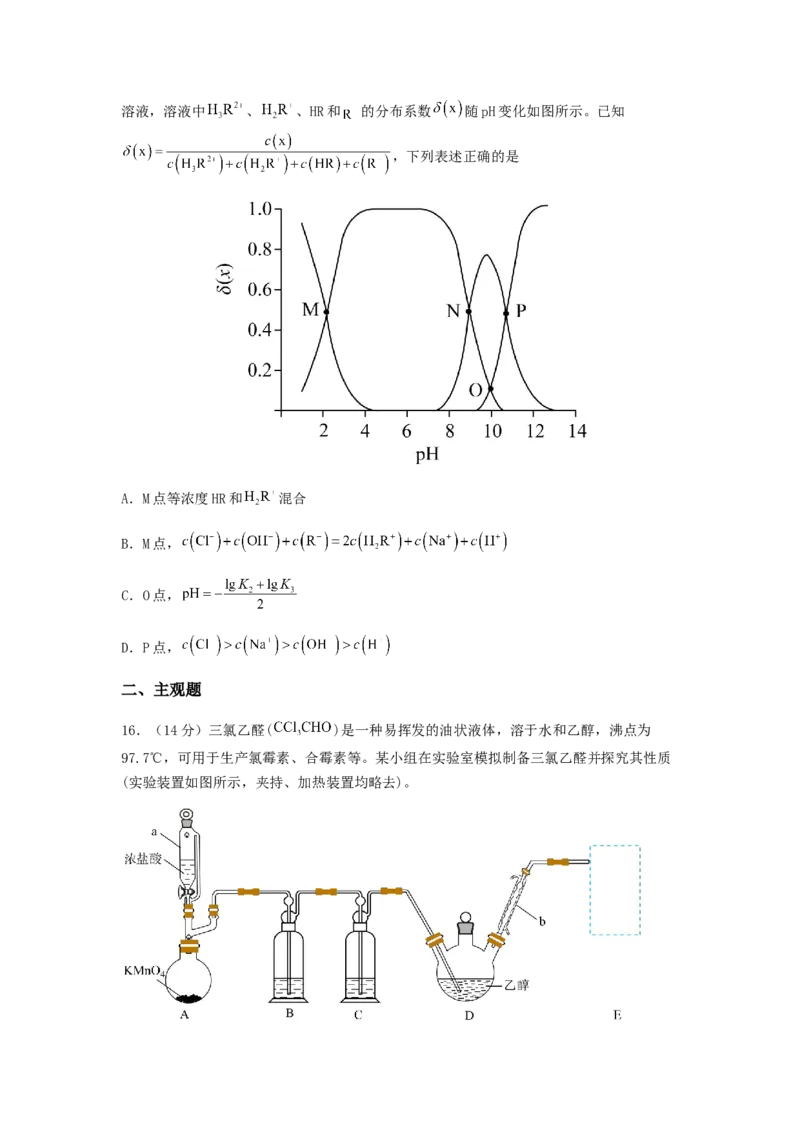
D.消耗相同甲酸时,总反应焓变:12.我国科研工作者研发了一种光电催化系统,其工作原理如图所示。工作时,光催化
FeO 电极产生电子和空穴;HO在双极膜界面处解离成H+和OH-,有利于电极反应顺利进行,
2 3 2
下列说法不正确的是
A.双极膜中靠近FeO 电极的一侧为阴膜
2 3
B.左室溶液pH逐渐增大
C.GDE电极发生的反应为O+2H++2e-=HO
2 2 2
D.空穴和电子的产生驱动了脱硫与HO 制备反应的发生
2 2
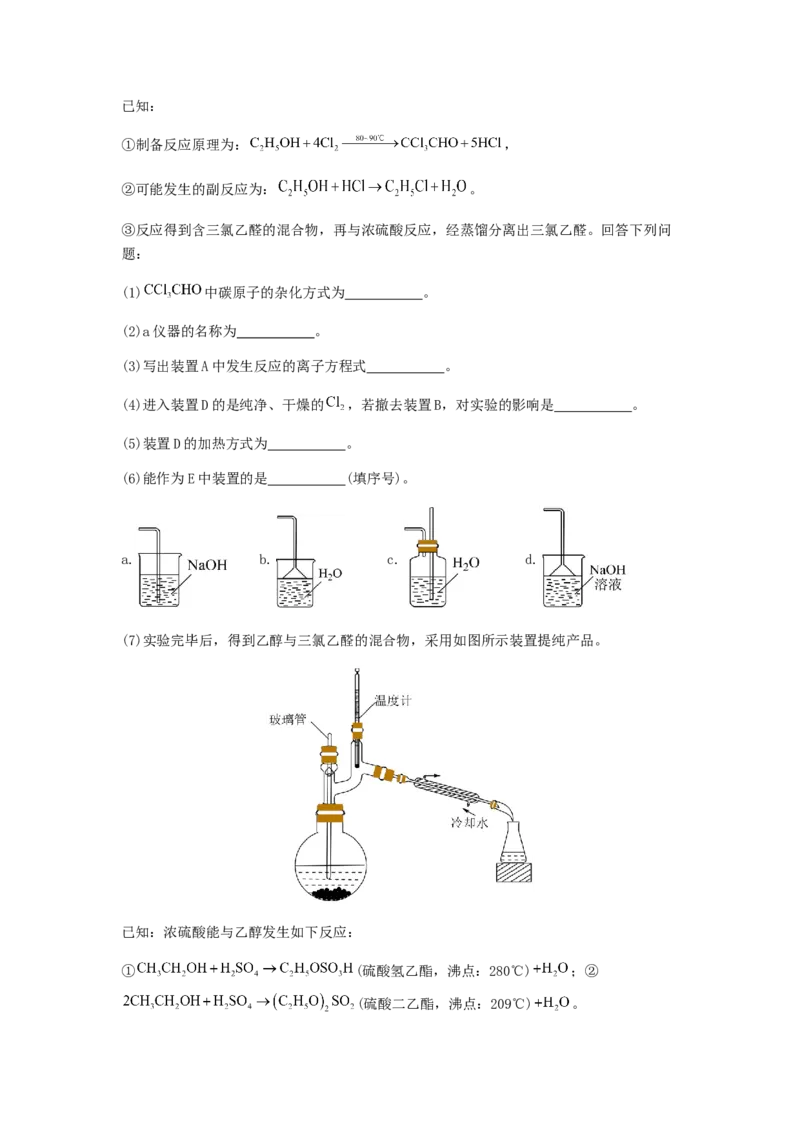
13.有一种有超导性的硼镁化合物,其晶体结构、晶胞沿c轴的投影图如图所示,已知在
投影图中,B位于三个Mg形成的正三角形的中心,阿伏加德罗常数值为N,图中长度单位
A
均为厘米,关于其晶体下列说法正确的是
A.该化合物的化学式为MgB
3 2
B.该晶体中Mg的配位数为8
C.每个B原子周围都有2个与之等距离且最近的B原子
D.该晶体的密度为
14.赖氨酸[ ,用HR表示],其盐酸盐 在水溶液中存
在三级电离平衡,电离常数分别为 、 、 ,向一定浓度的 溶液中滴加溶液,溶液中 、 、HR和 的分布系数 随pH变化如图所示。已知
,下列表述正确的是
A.M点等浓度HR和 混合
B.M点,
C.O点,
D.P点,
二、主观题
16.(14分)三氯乙醛( )是一种易挥发的油状液体,溶于水和乙醇,沸点为
97.7℃,可用于生产氯霉素、合霉素等。某小组在实验室模拟制备三氯乙醛并探究其性质
(实验装置如图所示,夹持、加热装置均略去)。已知:
①制备反应原理为: ,
②可能发生的副反应为: 。
③反应得到含三氯乙醛的混合物,再与浓硫酸反应,经蒸馏分离出三氯乙醛。回答下列问
题:
(1) 中碳原子的杂化方式为 。
(2)a仪器的名称为 。
(3)写出装置A中发生反应的离子方程式 。
(4)进入装置D的是纯净、干燥的 ,若撤去装置B,对实验的影响是 。
(5)装置D的加热方式为 。
(6)能作为E中装置的是 (填序号)。
a. b. c. d.
(7)实验完毕后,得到乙醇与三氯乙醛的混合物,采用如图所示装置提纯产品。
已知:浓硫酸能与乙醇发生如下反应:
① (硫酸氢乙酯,沸点:280℃) ;②
(硫酸二乙酯,沸点:209℃) 。(8)蒸馏时,在粗产品中加入浓硫酸的目的是 。
(9)探究 的性质:向溴水中滴加三氯乙醛,振荡,溶液褪色。经检验,反应后溶
液的 明显减小。写出三氯乙醛与溴水反应的化学方程式 。