文档内容
专练 41 盐类水解、离子浓度的比较
一、单项选择题
1.[2021·天津卷]常温下,下列有关电解质溶液的叙述正确的是( )
A.在0.1 mol·L-1HPO 溶液中c(H PO )>c(H PO)>c(HPO)>c(PO)
3 4 3 4 2
B.在0.1 mol·L-1NaC O 溶液中c(Na+)+c(H+)=c(OH-)+c(HC O)+c(C O)
2 2 4 2 2
C.在0.1 mol·L-1NaHCO 溶液中c(HCO)+c(HCO)=0.1 mol·L-1
3 2 3
D.氨水和NH Cl溶液混合,形成pH=9的溶液中c(Cl-)>c(NH)>c(OH-)>c(H+)
4
2.[2020·浙江7月]常温下,用0.1 mol·L-1氨水滴定10 mL浓度均为0.1 mol·L-1的
HCl和CHCOOH的混合液,下列说法不正确的是( )
3
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl-)>c(CHCOO-)
3 3
B.当滴入氨水10 mL时,c(NH)+c(NH ·H O)=c(CHCOO-)+c(CHCOOH)
3 2 3 3
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH ·H O)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(NH)c(H+)
3
D.4.76c(Na+)>c(H+)>c(OH-)
3
5.[2022·安徽省江南片高三摸底考试]常温下,下列有关溶液的说法正确的是( )
A.pH相等的①NH Cl ②NH Al(SO )
4 4 4 2
③NH HSO 溶液:浓度的大小顺序为①>②>③
4 4
B.HA 的电离常数 K =4.93×10-10,则等浓度的 NaA、HA 混合溶液中:c(Na+)
a
>c(HA)>c(A-)
C.NaHCO 溶液加水稀释,c(Na+)与c(HCO)的比值将减小
3
D.已知在相同条件下酸性HF>CH COOH,则物质的量浓度相等的NaF与CHCOOK
3 3
溶液中:c(Na+)-c(F-) >c(K+)-c(CHCOO-)
36.[2022·专题模块测试]常温下,将CO 通入2 L pH=12的KOH溶液中,溶液中水电
2
离出的OH-离子浓度(c)与通入的CO 的体积(V)的关系如图所示。下列叙述不正确的是(
2
)
A.a点溶液中:水电离出的c(H+)=1×10-12 mol·L-1
B.b点溶液中:c(H+)=1×10-7 mol·L-1
C.c点溶液中:c(K+)=2[c(CO)+c(HCO)+c(H CO)]
2 3
D.d点溶液中:c(K+)=2c(CO)+c(HCO)
7.[2022·长春实验中学高三开学考试]下列溶液中有关说法正确的是( )
A.室温下,0.1 mol·L-1 NaHA溶液中离子浓度的关系有:c(Na+)=c(HA-)+c(OH-)
+2c(A2-)
B.向0.1 mol·L-1 (NH )SO 溶液中滴加少量浓硫酸,不引起明显体积变化,则c(NH)
4 2 4
与c(SO)均增大
C.已知K (CuS)=1.3×10-36,则将足量CuSO 溶解在0.1 mol·L-1的HS溶液中,Cu2
sp 4 2
+能达到的最大浓度为1.3×10-35 mol·L-1
D.常温下,pH=5.6的CHCOOH与CHCOONa的混合溶液中,c(Na+)>c(CHCOO-)
3 3 3
8.[2022·江苏镇江期中]室温下,通过下列实验探究NaHCO 的性质。
3
实验 实验操作和现象
1 用pH试纸测得0.1 mol·L-1NaHCO 溶液的pH约为8
3
向10 mL 0.1 mol·L-1NaHCO 溶液中加入10 mL 0.1 mol·L-1NaOH溶液,测得溶液
2 3
pH约为11.3
3 向0.1 mol·L-1NaHCO 溶液中加入过量0.1 mol·L-1Ca(OH) 溶液,产生白色沉淀
3 2
4 向10 mL 0.1 mol·L-1NaHCO 溶液中加入10 mL 0.1 mol·L-1盐酸,产生无色气泡
3
下列有关说法正确的是( )
A.根据实验1,NaHCO 溶液中:
3
c(Na+)>c(HCO)>c(CO)>c(H CO)
2 3
B.实验2得到的溶液中有
c(OH-)=c(H+)+c(HCO)+2c(H CO)
2 3
C.实验3反应静置后的上层清液中有
c(Ca2+)·c(CO)>K (CaCO)
sp 3
D.实验4中反应的离子方程式:
CO+2H+===CO ↑+HO
2 2
二、不定项选择题
9.[2022·湖南卷]为探究FeCl 的性质,进行了如下实验(FeCl 和NaSO 溶液浓度均为
3 3 2 3
0.1 mol·L-1)。
实验 操作与现象
① 在5 mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5 mL FeCl 溶液中滴加2滴NaSO 溶液,变红褐色;再滴加K[Fe(CN) ]溶
② 3 2 3 3 6
液,产生蓝色沉淀。在5 mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;将上述混合液分成两
2 3 3
③ 份,一份滴加K[Fe(CN) ]溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色沉
3 6
淀。
依据上述实验现象,结论不合理的是( )
A.实验①说明加热促进Fe3+水解反应
B.实验②说明Fe3+既发生了水解反应,又发生了还原反应
C.实验③说明Fe3+发生了水解反应,但没有发生还原反应
D.整个实验说明SO对Fe3+的水解反应无影响,但对还原反应有影响
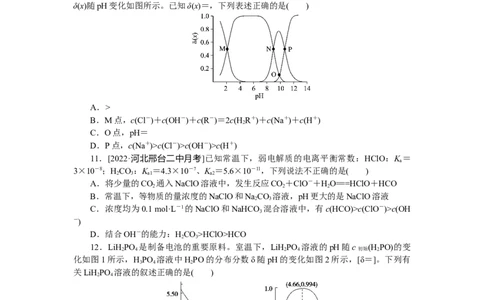
10.[2021·山东卷]赖氨酸[H N+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,
3 2 4 2
其盐酸盐(HRCl )在水溶液中存在如下平衡:HR2+HR+ HR R-。向
3 2 3 2
一定浓度的HRCl 溶液中滴加NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数
3 2 3 2
δ(x)随pH变化如图所示。已知δ(x)=,下列表述正确的是( )
A.>
B.M点,c(Cl-)+c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
11.[2022·河北邢台二中月考]已知常温下,弱电解质的电离平衡常数:HClO:K =
a
3×10-8;HCO:K =4.3×10-7、K =5.6×10-11,下列说法不正确的是( )
2 3 a1 a2
A.将少量的CO 通入NaClO溶液中,发生反应CO+ClO-+HO===HClO+HCO
2 2 2
B.常温下,等物质的量浓度的NaClO和NaCO 溶液,pH更大的是NaClO溶液
2 3
C.浓度均为0.1 mol·L-1的NaClO和NaHCO 混合溶液中,有c(HCO)>c(ClO-)>c(OH
3
-)
D.结合OH-的能力:HCO>HClO>HCO
2 3
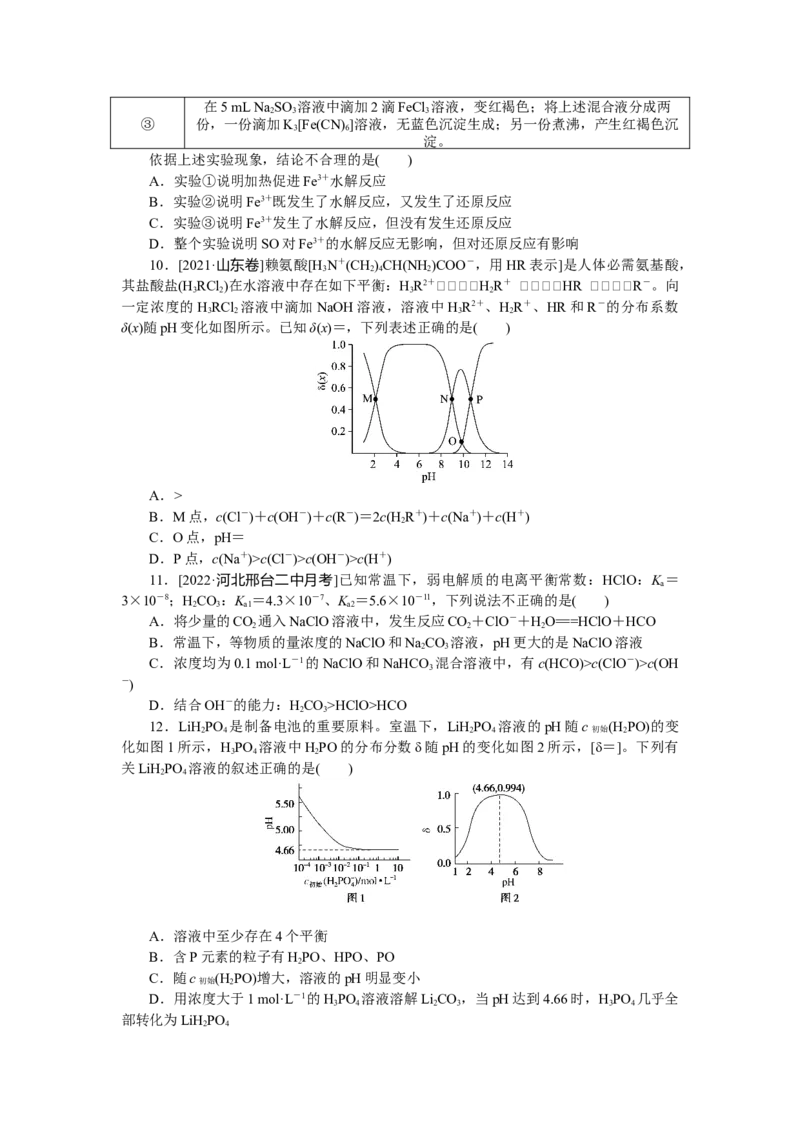
12.LiH PO 是制备电池的重要原料。室温下,LiH PO 溶液的pH随c (H PO)的变
2 4 2 4 初始 2
化如图1所示,HPO 溶液中HPO的分布分数δ随pH的变化如图2所示,[δ=]。下列有
3 4 2
关LiH PO 溶液的叙述正确的是( )
2 4
A.溶液中至少存在4个平衡
B.含P元素的粒子有HPO、HPO、PO
2
C.随c (H PO)增大,溶液的pH明显变小
初始 2
D.用浓度大于1 mol·L-1的HPO 溶液溶解LiCO,当pH达到4.66时,HPO 几乎全
3 4 2 3 3 4
部转化为LiH PO
2 413.[2022·四川成都一诊]25 ℃时,向一定浓度的NaC O 溶液中滴加盐酸,混合溶液
2 2 4
的pH与离子浓度变化关系如图所示。已知HC O 是二元弱酸,X表示或,下列叙述错误
2 2 4
的是( )
A.从M点到N点的过程中,c(H C O)逐渐增大
2 2 4
B.直线n表示pH与-lg的关系
C.由N点可知K (H C O)的数量级为10-2
a1 2 2 4
D.pH=4.18的混合溶液中:c(Na+)>c(HC O)=c(C O)=c(Cl-)>c(H+)>c(OH-)
2 2
14.[2022·全国百强校江苏扬州中学月考]常温下,下列有关叙述正确的是( )
A.向0.1 mol·L-1 Na CO 溶液中通入适量CO 气体后:c(Na+)=2[c(HCO)+c(CO)+
2 3 2
c(H CO)]
2 3
B.常温下,pH=6的NaHSO 溶液中:c(SO)-c(H SO )=9.9×10-7 mol·L-1
3 2 3
C.等物质的量浓度、等体积的NaCO 和NaHCO 混合:<
2 3 3
D.0.1 mol·L-1 Na C O 溶液与0.1 mol·L-1 HCl溶液等体积混合(H C O 为二元弱酸):
2 2 4 2 2 4
2c(C O)+c(HC O)+c(OH-)=c(Na+)+c(H+)
2 2
15.[情境创新]已知NaCN溶液中CN-的水解常数K =≈[c(NaCN)是NaCN溶液的起
h 0
始浓度]。25 ℃时,不断加水稀释1 mol·L-1的NaCN溶液,测得NaCN溶液浓度的对数值
lg c(NaCN)与2pOH[pOH=-lg c(OH-)]的关系如图所示,下列说法错误的是( )
A.25 ℃时,NaCN的K 的数量级为10-5
h
B.其他条件不变,升高温度,可使曲线上a点变到b点
C.25 ℃时,向a点对应溶液中加入固体NaCN,CN-水解程度减小
D.水的电离程度:a点小于c点